MUC19突变对派姆单抗治疗老年非小细胞肺癌的临床疗效及对预后的影响
刘华 蒋详德 张华鹏 程刚 杨培 陈方
(亳州市人民医院肿瘤科,安徽 亳州 236800)
随着社会发展及医疗技术手段进步,肺癌检出率逐年升高,且发病年龄日趋年轻化,而非小细胞肺癌(NSCLC)是最为常见的类型之一,但绝大部分患由于错过最佳治疗时机往往预后不佳,化疗及分子靶向治疗虽然能延长患者生命,但均存在一定局限性〔1,2〕。目前程序性死亡受体1(PD-1)/程序性死亡配体1(PD-L1)改变了NSCLC患者治疗模式,也显著改善患者预后〔3〕,但研究仅有部分患者对免疫检查点抑制剂(ICB)产生应答,因此需针对肺癌患者探索评估疗效的标志物,从而筛选出对于ICB产生应答的患者提高疗效进而改善预后的关键〔4〕。肿瘤突变负荷(TMB)作为免疫治疗的疗效预测标志物是目前研究的前沿,有研究表明TMB表达水平与肿瘤对ICB应答有效率呈正相关关系〔5〕。黏蛋白(MUC)19作为编码大分子量糖化蛋白,可构成有效的物理屏障以保护上皮细胞,使其不受应激诱导的损伤。MUC19可广泛在角膜和结膜等处进行高表达,同时在肺、骨髓等组织中也有相应表达〔6〕。相关研究证实干燥综合征和乳腺癌的发病和MUC19异常表达关系密切,其中乳腺癌患者预后差的指标之一即为MUC19基因突变〔7〕,先前研究也通过全外显子测序对生物信息学分析及筛选潜在突变,结果发现MUC19突变与NSCLC发生显著相关〔8〕,但肺癌患者预后与MUC19突变间的关联性还有待进一步研究。本研究旨在探讨MUC19突变对PD-1抑制剂派姆单抗治疗NSCLC的临床疗效及对预后的影响。
1 对象和方法
1.1研究对象 选择2018年3月至2019年12月于亳州市人民医院住院治疗的36例MUC19突变老年NSCLC患者。纳入标准:(1)术后病理结果诊断为NSCLC,且证实存在MUC19基因敏感突变;(2)预计生存期≥12个月;(3)免疫治疗前可接受放化疗治疗,包括术后放疗或化疗,但第1次免疫治疗前2 w需停止放化疗治疗;(4)年龄≥65岁。排除标准:(1)合并其他类型肿瘤;(2)合并严重感染和免疫系统疾病;(3)肝、肾及其他严重疾病者;(4)既往予以免疫药物治疗。同时选取同期在医院住院治疗的38例MUC19 基因野生型(MUC19基因未突变) NSCLC患者为对照组。采用蝎形探针扩增阻滞突变系统测定癌组织MUC19基因突变情况,检查结果显示观察组均为MUC19基因12染色体上外显子点突变。本研究经医院伦理委员会批准通过。两组一般资料差异无统计学意义(P>0.05),见表1。
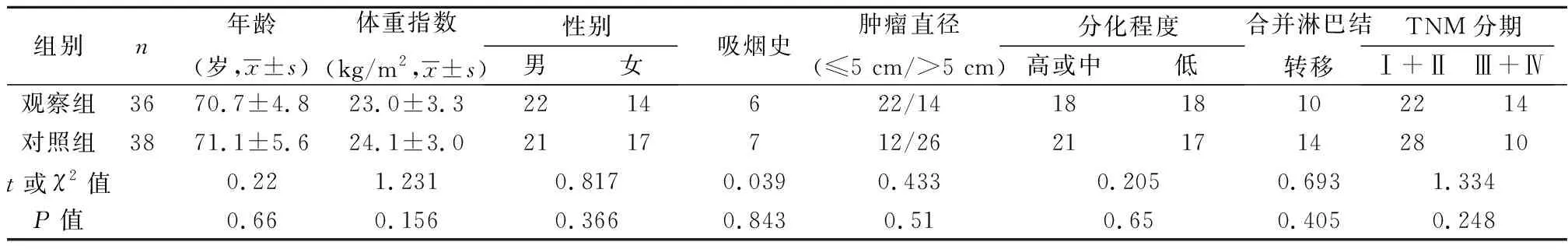
表1 两组基线数据(n)
1.2干预方法 研究对象入院后完善相关检查,排除禁忌后予以 PD-1抑制剂派姆单抗2 mg/kg静脉滴注,2 w为1个周期,治疗6个周期,共计12 w。
1.3评估指标 6个周期治疗结束后按照世界卫生组织(WHO)实体瘤疗效标准,分为完全缓解(CR)、不完全缓解(PR)、疾病稳定(SD)和疾病进展(PD)共4个等级。其中CR指肿瘤病灶完全消失,且维持时间>4 w;PR为肿瘤病灶体积缩小>50%,且维持时间>4 w;SD为NSCLC病灶缩小25%~50%;PD为NSCLC病灶增大超过25%或发现转移。总有效率=CR+PR。所有患者出院后通过门诊至少随访12个月,比较两组治疗前及治疗12个月时血清肿瘤标志物〔癌胚抗原(CEA)、糖类抗原(CA)125与神经元特异性烯醇化酶(NSE)〕水平。观察并比较两组肿瘤无进展生存期(PFS)及总生存期(OS)。在治疗过程中记录两组不良反应,包括恶心呕吐、过敏反应、皮疹、肝肾功能异常和凝血功能异常。
1.4肿瘤组织CD8+T细胞浸润 术后肿瘤组织均经4%甲醛固定,用石蜡包埋后连续组织切片(厚4 μm),后续应用 C单克隆抗CD8抗体进行免疫组织化学染色,严格按照说明书进行操作。 其中膜染色的淋巴细胞被认为是CD8阳性。 所有免疫组化切片由两名病理学家独立评估并记录CD8+细胞数,其中每个免疫组化切片选择4~6个视野进行统计。
1.5统计学分析 采用SPSS22.0统计软件进行t检验、χ2检验。
2 结 果
2.1两组治疗后疗效及生存指标比较 观察组总有效率(83.33%,CR 10例、PR 20例、SD 2例、PD 4例)明显高于对照组(57.89%,CR 6例、PR 16例、SD 10例、PD 6例;χ2=5.726,P=0.017);观察组PFS及OS〔(18.20±1.32)、(30.26±5.62)个月〕明显长于对照组〔(13.22±1.10)、(22.55±4.89)个月〕,差异有统计学意义(t=5.22、12.22,P=0.015、<0.001)。
2.2两组治疗前后血清CEA、CA125与NSE水平比较 治疗前两组CEA、CA125与NSE水平差异无统计学意义(P>0.05),治疗后两组均明显降低(P<0.05),且观察组明显低于对照组(P<0.001),见表2。

表2 两组治疗前后血清CEA、CA125与NSE水平比较
2.3两组不良反应发生率比较 观察组不良反应总发生率(13.89%,过敏反应2例、恶心呕吐1例、皮疹1例、肝肾功能异常1例)与对照组(15.79%,过敏反应3例、恶心呕吐2例、肝肾功能异常1例)差异无统计学意义(χ2=0.053,P=0.818)。
2.4两组肿瘤组织CD8+T细胞浸润结果 与观察组〔(26.32±3.10)HPF〕相比,对照组肿瘤组织CD8+T细胞数目〔(42.11±2.68)/HPF〕明显更多(P<0.05),见图1。

图1 两组肿瘤组织中CD8T细胞浸润(免疫荧光,×200)
3 讨 论
NSCLC的发病率逐年增高,严重影响患者的身心健康,且由于NSCLC早期症状不典型,超过50%的患者就诊时已错过手术时间窗,因此NSCLC 5年生存率相对较低〔9~12〕。化疗在疾病早期能取得一定疗效,但长期用药会产生耐药,远期来看并不能显著延长患者的生存周期〔13,14〕。免疫疗法为NSCLC的治疗提供了新方式,但研究指出只有部分患者能够从免疫疗法中获益〔15~17〕。此外,免疫疗法合并有一定的免疫毒性,且治疗成本较高〔18〕,因此通过特定的生物标志物对患者进行疗效评估很有必要。
实际上PD-1是表达在T细胞表面的跨膜蛋白,通过与配体PD-L1结合,发挥负向调控作用。在肿瘤组织的微环境中,肿瘤细胞表面通过表达PD-L1与PD-1结合,可有效抑制TCR传导信号通路中转导分子的磷酸化,进而抑制其通路下游信号的激活及炎性细胞的激活和炎性因子的表达,因此用抑制PD-1信号通路可改善机体的免疫反应,增强免疫能力〔19〕。也有研究指出高肿瘤突变负荷且PD-L1阳性的肿瘤组织对免疫治疗的应答率明显高于其他类型肿瘤组织〔20〕,与本研究结果基本一致。虽然目前研究普遍认为肿瘤组织PD-L1的表达是抗PD-1/PD-L1治疗前选择优势人群比较合理的标志物,但由于肿瘤异质性及标志物表达水平的动态变化等因素导致PD-L1的应用受到限制〔21〕。而MUC19基因突变作为肿瘤突变负荷的一部分,研究指出肿瘤突变负荷越大,机体的免疫原性增强,进而使得肿瘤特异性T 细胞能够对新抗原进行识别并最终产生免疫应答〔22〕,而肿瘤突变负荷可作为免疫疗效预测标志物之一,包括膀胱癌、肝癌及消化道肿瘤等恶性癌症对PD-1 抑制剂的有效率与肿瘤突变负荷的表达呈明显正相关〔22~25〕。本研究结果也发现,采用PD-1抑制剂派姆单抗MUC19突变的NSCLC患者不仅总有效率较高,治疗结束后肿瘤标志物水平明显降低,且PFS及OS均明显长于MUC19 基因野生型患者。说明MUC19 基因突变与其他分子之间存在一定关联,但其中的机制尚未阐明,需要大样本量的基因分析进一步研究。但也有研究指出应用免疫治疗联合化疗在治疗鳞状和非鳞状NSCLC患者中发现,其疗效与肿瘤突变无明显相关性〔26,27〕。虽然本研究结果发现不论是MUC19 基因野生型患者还是MUC19突变老年NSCLC患者,两组随访过程中的不良反应发生率无明显统计学差异,但因免疫治疗带来的免疫相关不良反应及药物的毒副作用仍有报道〔28,29〕。也有研究指出PD-1/PD-L1 抑制剂甚至会引发免疫相关的肝炎、肺部感染、皮肤过敏反应及内分泌代谢功能障碍等并发症等〔30,31〕。免疫治疗的禁忌证包括合并自身免疫性疾病及高龄体弱者等〔32〕,这是因为PD-1抗体通过发挥免疫调控作用,可有效激活免疫系统发挥抗癌作用,但其本身对肿瘤细胞无明显杀伤作用〔33~35〕,因此对于MUC19突变NSCLC患者予以免疫治疗时,需综合评估患者基本身体情况及病史,将风险降到最低。本研究也存在一些局限性,样本量相对较小,且均为老年患者,也需要多中心、大样本的研究进一步验证MUC19基因突变对PD-1抑制剂在NSCLC患者治疗中的临床效果。实际上人体对肿瘤疾病的免疫应答十分复杂且机制尚未完全明确〔36,37〕,仅依靠 MUC19基因突变预测PD-1抑制剂对NSCLC患者治疗可靠性有待商榷,需要与肿瘤突变负荷联合共同评估。
综上,MUC19突变可改善派姆单抗治疗老年NSCLC患者的临床效果,还可延长生存时间。

