胃镜下高频电切联合氩等离子体凝固术对消化道息肉患者术后疼痛及胃肠功能的影响
潘菲
消化道息肉是指消化道局部黏膜受慢性炎症影响,出现增生肥厚进而形成的黏膜隆起样病变,是消化道常见疾病之一[1]。其多数为良性病变,然而有学者研究认为,若不及时处理,则息肉存在恶性病变风险,从而威胁患者生命健康[2]。因此,安全有效的治疗方式具有重要意义。目前临床中对于消化道息肉主要以内镜下手术治疗为主,包括胃镜下高频电切术、氩等离子体凝固术、黏膜剥离术等多种治疗方式[3]。其中,胃镜下高频电切术具有良好的临床效果,可有效切除消化道息肉且可保证治愈率,但存在损伤大、术后创面愈合缓慢、影响胃肠功能等副作用,导致部分患者术后易出现不良事件[4-5]。氩等离子体凝固术是一种新型凝固技术,由于其是非接触式,对机体损伤小、术后预后较好,具备一定优势[6]。然而,临床较少见胃镜下高频电切术与氩等离子体凝固术联合应用相关报道。基于此,本研究应用胃镜下高频电切联合氩等离子体凝固术,探讨其对消化道息肉患者术后疼痛及胃肠功能的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2019 年6 月-2022 年6 月乐平市人民医院收治的消化道息肉患者72 例。纳入标准:符合文献[7]中关于消化道息肉相关诊断标准;符合文献[8]中胃镜下高频电切术相关适应证;息肉直径0.5~2.0 cm;息肉类型为广基无蒂型、扁平型、亚蒂型。排除标准:合并恶性病变;凝血功能障碍;心肺功能障碍。按照随机数字表法将所有患者分为试验组(n=36,59 枚息肉)、对照组(n=36,62 枚息肉)。本研究经医院医学伦理委员会批准,患者及家属均知情,且签署知情同意书。
1.2 方法 两组患者手术操作均由同一术者团队完成,术前进行心电图、凝血功能等常规检查,术前1 d 常规禁饮禁食,常规无痛胃镜探查,并静脉注射丙泊酚麻醉。(1)对照组给予胃镜下高频电切术治疗。具体包括:①吸除息肉周围水及分泌物,充分暴露息肉;②高频电切输出功率35~80 W,对于直径1.0 cm 以上息肉,先以钢丝圈套住息肉蒂部,收紧套圈并多次通电进行切除,直径为0.5~1.0 cm的息肉则直接灼除,切除后常规止血。(2)试验组在胃镜下高频电切除术切除息肉后给予氩等离子体凝固术治疗。具体包括:①打开电源并设置氩等离子体凝固术模式,选择高频电发生器参数,调节氩等离子体凝固治疗输出功率35~45 W,氩气流量1.0 L/s;②以胃镜观察病灶部位并伸出氩等离子体凝固器导管,将其置于病灶上方并踩踏凝固档,进行氩等离子体凝固治疗;治疗过程中及时抽吸管腔内烟雾,确保手术操作视野。(3)两组术后均禁食1 d,进流质饮食1 d,进半流质饮食或软食3 d,并根据患者具体情况常规给予保护胃黏膜药物、质子泵抑制剂等促进创面愈合,保持静卧休息。
1.3 观察指标及判定标准 (1)比较两组手术指标(手术时间、术中出血量、住院时间、术后排气时间)。(2)通过视觉模拟评分法(VAS),对比两组术后1 d 疼痛程度。评分标准:评分为0~10 分,其中0 分表示无痛,10 分表示难以忍受的剧烈疼痛,分值越高则疼痛程度越强烈[9]。(3)出院时,通过I-FEED 评分系统,比较两组住院期间胃肠功能。评分标准:系统通过患者临床症状、体征等对其胃肠功能进行评估,共包括正常、术后胃肠道耐受不良(POGI)及术后胃肠功能障碍(POGD),其中I-FEED 评分为0~2 分表示正常,I-FEED 评分 为3~5 分表示POGI,I-FEED 评分≥6 分表示POGD[10]。(4)比较两组一次手术成功率差异。术毕胃镜下观察,所有病灶均完全消失,且基底部完全凝固变白为手术成功。(5)通过观察患者术后临床症状,统计并比较两组术后并发症发生情况。
1.4 统计学处理 应用SPSS 20.0 统计学软件对所得数据进行分析。计量资料经方差齐性及正态性检验,确认具备方差齐性且近似服从正态分布,以()表示,行t检验;计数资料以率(%)表示,行χ2检验,等级资料行秩和检验。以P<0.05 表示差异有统计学意义。
2 结果
2.1 两组一般资料比较 试验组男7 例,女29 例;年龄34~85 岁,平均(46.75±4.32)岁;息肉类型:亚蒂型20 例,扁平型9 例,广基无蒂型7 例;息肉部位:贲门息肉18 例,胃大弯息肉6 例,胃窦息肉7 例,胃底息肉5 例;息肉直径(0.96±0.22)cm;息肉个数1~3 个,平均(1.63±0.68)个。对照组男7 例,女29 例;年龄34~85 岁,平均(47.12±4.45)岁;息肉类型:亚蒂型21 例,扁平型10 例,广基无蒂型5 例;息肉部位:贲门息肉16 例,胃大弯息肉7 例,胃窦息肉5 例,胃底息肉8 例;息肉直径(0.92±0.24)cm;息肉个数1~3 个,平均(1.75±0.65)个。两组患者年龄、性别、息肉类型、息肉部位、息肉直径等一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组手术指标及术后1 d 疼痛程度比较 试验组手术时间、术中出血量、住院时间及术后1 d VAS 评分均优于对照组(P<0.05);两组术后排气时间比较,差异无统计学意义(P>0.05)。见表1。
表1 两组手术指标及术后1 d疼痛程度比较()

表1 两组手术指标及术后1 d疼痛程度比较()
2.3 两组胃肠功能比较 两组I-FEED 评分构成比比较,差异有统计学意义(P<0.05),见表2。
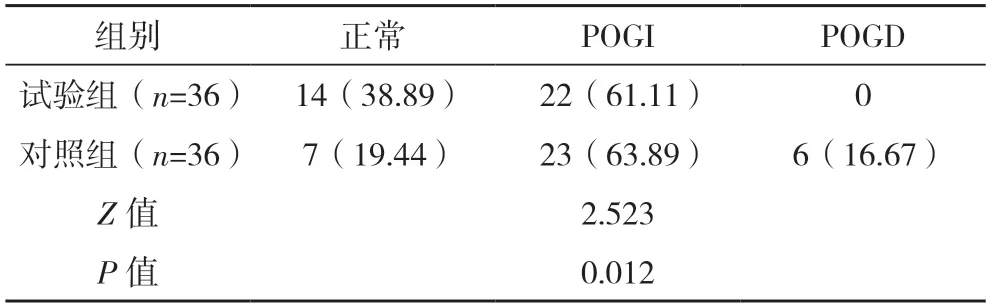
表2 两组胃肠功能比较[例(%)]
2.4 两组一次手术成功率比较 试验组一次手术成功率为96.61%(57/59),对照组一次手术成功率为85.48%(53/62),两组一次手术成功率比较,差异无统计学意义(χ2=0.216,P=0.642)。
2.5 两组术后并发症发生情况比较 两组术后各并发症发生率比较,差异均无统计学意义(P>0.05),见表3。

表3 两组术后并发症发生率比较[例(%)]
3 讨论
消化道息肉多数起病隐匿,无明显临床症状,然而上消化道息肉患者发病后若长期不进行处理,易出现恶性病变,对患者生命健康造成严重威胁[11]。在目前临床治疗中,胃镜下高频电切术利用电灼热效应产生高温,息肉在局部高温影响下其内部水分出现汽化[12],并引发息肉蛋白质变性,进而切除息肉。本研究观察到两组患者一次手术成功率比较差异无统计学意义(P>0.05),提示两种手术方案治疗效果均较好。然而有学者指出,高频电切在切除部分直径较小息肉时,易导致切除创面扩大或加深,从而术后愈合缓慢[13]。在本研究中,试验组手术时间、术中出血量、住院时间及术后1 d VAS 评分均优于对照组(P<0.05),这说明相较单纯胃镜下高频电切术,胃镜下高频电切联合氩等离子体凝固术可有效缩短手术操作时间、减少术中出血量,并加快术后愈合。究其原因,胃镜下高频电切术易导致创面加深或扩大,使术中损伤大、出血量增加,导致止血难度加大,常规止血所需时间延长。同时术中出血量增加易导致视野模糊,从而延长手术操作时间;而术中创面扩大或加深,导致术后疼痛感受强烈且创面愈合缓慢,住院时间延长。氩等离子体凝固术是借助氩等离子束的电传导将高频电能量传递至病灶部位,促使病灶组织脱水凝固,从而达到止血目的,是一种非电极接触式治疗[14]。其中氩气为保护性惰性气体,利用氩等离子束可降低创面温度[15],避免创面在治疗过程中出现碳化或氧化,且可选择性作用于组织,有利于减小术中损伤,减轻术后疼痛,对创面术后愈合起到积极作用。同时,治疗过程中烟雾较少且可及时抽吸管腔内烟雾,保持术中视野清晰[16],从而有利于手术操作顺利进行,避免操作时间延长。
有研究表明,手术创伤、应激反应等多种因素均可影响患者术后胃肠功能,导致胃肠功能恢复减缓[17]。在本研究中,两组I-FEED 评分构成比比较,差异有统计学意义(P<0.05),说明相较单纯应用胃镜下高频电切术,胃镜下高频电切联合氩等离子体凝固术可减少术后胃肠功能不良影响。究其原因,胃镜下高频电切术术中操作时间更长,创伤更大,从而术中肠道损伤风险更大。同时,更长的手术时间不利于患者体温调节,有学者认为,体温调节异常易引发胃肠耐受不良[18]。胃镜下高频电切联合氩等离子体凝固术则通过有效缩短手术操作时间、减少术中损伤而避免肠道损伤,保护胃肠功能。且氩等离子体凝固术治疗过程中通过避免创面因高温导致的碳化现象,利于创面愈合的同时,也有助于保护肠道[19],从而减轻对胃肠功能的影响,促进术后胃肠功能恢复。
理论上讲,氩等离子体凝固术治疗过程中,可于创面处形成一层绝缘层以避免深层组织进一步受到高温灼伤,从而有效降低术后并发症发生风险[20]。但本研究中,两组术后排气时间及术后并发症发生率比较,差异均无统计学意义(P>0.05),说明单纯应用胃镜下高频电切术与胃镜下高频电切联合氩等离子体凝固术在缩短术后排气时间、减少术后并发症发生方面无明显差异,这可能与本研究纳入研究对象过少有关。本研究需进一步扩大样本量以完善研究,对研究结果做进一步探讨。
综上所述,胃镜下高频电切联合氩等离子体凝固术应用于消化道息肉患者,有助于缩短手术时间,减轻术中损伤及术后疼痛,促进术后胃肠功能恢复,具备一定临床参考价值。

