硫氯含量对TC4渗铝涂层高温腐蚀性能的影响
董天乐,郑家银,陈淑娴,钱荟如,吴多利
(扬州大学机械工程学院,江苏 扬州 225127)
能源是全世界持续关注的核心问题之一,社会的发展程度越高,能源供求不平衡的矛盾就越严重。过多的垃圾滋生出各式各类急需解决的环境污染难题,为此人们从无害化、减量化、资源化的原则出发,构思发明了与之相对应的合理的科学措施。垃圾发电是一种垃圾处理方式,垃圾经过焚烧发电后,可达到最大程度减小垃圾的容积,并且烟气经过处理后也能达到国家制定的环保标准,以免造成二次污染。但是,大量的金属、皮革、橡胶、塑料包含在城市垃圾中,在燃烧过程中会释放出大量的腐蚀性气体,如Cl2、HCl、SO2等酸性气体及NaCl、KCl、Na2SO4等盐类蒸汽,使发电厂维护成本增加和发电效率下降,限制了垃圾焚烧发电的进一步发展。S离子的存在对腐蚀过程具有两面效应。一方面,S会导致局部的还原性环境,产生硫化腐蚀[6-8];另一方面,S对腐蚀过程也有积极作用,可合理增加烟气中的SO2含量,使硫/氯发生协同作用[9-12]。一定量的SO2与HCl共存,能够将烟气中腐蚀性较强的NaCl转化为Na2SO4以降低腐蚀的影响[13-15]。目前,对于硫和氯对腐蚀过程的协同作用机理尚不清楚。本文致力于阐明硫和氯的协同作用对于涂层的腐蚀性能的影响,以期为未来涂层服役性能的提升提供理论指导。
1 实验部分
1.1 试样
实验采用TC4合金作为基体材料,名义化学成分列于表1。首先将试样用线切割机切割成尺寸为10.0 mm×10.0 mm×1.5 mm,然后用碳化硅砂纸将试样打磨至6.5 μm,再用去离子水和乙醇在超声波清洗机中清洗15 min,干燥,以保证试样表面干净无污。

表1 TC4合金的名义化学成分Table 1 Nominal chemical composition of TC4 alloy
在TC4合金试样表面制备渗铝涂层。首先配制12AlCl3-10Al-78Al2O3(质量分数)粉末并置于刚玉坩埚中,然后将TC4合金试样埋在所制备的粉末中,最后将刚玉坩埚放入管式炉中,在700℃、氩气保护环境下对基体进行6 h的渗铝处理。
1.2 模拟垃圾焚烧受热面高温腐蚀实验
模拟实验在自主搭建的实验装置中进行,环境气氛为N2+O2(体积分数分别为95%和5%)。使用两个流量计将N2和O2气体通入管式炉中,在600℃下进行高温腐蚀实验。图1为高温腐蚀设备的示意图。

图1 高温腐蚀的设备示意图Figure 1 Schematic diagram of high temperature corrosion equipment
在腐蚀实验之前,在电子天平上测量每个样品的初始质量,每种涂盐条件下的实验样品各为3个。首 先 准 备3个 烧 杯,将NaCl、Na2SO4和NaCl+Na2SO4溶于水中制备成饱和腐蚀盐溶液。将所制备 的Na2SO4溶 液、NaCl溶 液 和NaCl+Na2SO4混 合溶液用喷枪分别涂在每个对应样品的表面上,使得表面分别沉积2 mg·cm-2的NaCl、Na2SO4和NaCl+Na2SO4,然后将样品放置在管式炉的坩埚中,在600℃下腐蚀24 h,取出样品冷却至室温,用去离子水洗涤以除去表面上残留的盐,干燥、称重。整个腐蚀试验需循环重复上述步骤7次,总腐蚀实验时间共计168 h。根据样品的质量变化,绘制出腐蚀增重曲线[24]。
1.3 微观结构表征
采用冷镶嵌法将样品镶嵌在环氧树脂中,目的是防止表面形成的腐蚀产物层的剥落。首先将腐蚀试样置于模具内,再将环氧树脂和固化剂溶液按3∶1(质量比)的比例混合均匀后倒入模具中,待容器中的溶液凝固后,将镶嵌后的样品研磨至5 μm,再用2.5 μm的金刚石抛光膏抛光。运用X射线衍射仪(D8 Advance Bruker)、扫描电子显微镜(GeminiSEM 300)及能量色散光谱仪(Oxford X-max),表征腐蚀后的相组成、元素分布、表面腐蚀形貌和截面腐蚀形貌。
2 结果及分析
2.1 宏观腐蚀形貌
图2为TC4涂层样品在600℃下腐蚀168 h后的宏观表面腐蚀形貌。从图2可见,在单独喷涂Na2SO4溶液时,试样表面宏观形貌无明显变化,仅能观察到少许白色氧化层;在喷涂NaCl+Na2SO4混合盐溶液时,样品表面出现比较明显的白色网状氧化层,随着氧化层逐渐增厚出现局部氧化层剥落的现象;在单独喷涂NaCl溶液时,样品腐蚀更为严重,表面氧化层大面积剥落,并且脱落发生的时间更早;样品表面残留着黄色的腐蚀产物,这可能是腐蚀产生的氯化物。

图2不同腐蚀条件下TC4涂层样品的宏观腐蚀形貌图Figure 2 Macroscopic corrosion morphologies of TC4 coating samples under different corrosion conditions
2.2 腐蚀动力学曲线
图3为TC4涂层样品模拟垃圾焚烧受热面高温腐蚀实验后的重量变化曲线。从图3可见:在单独喷涂Na2SO4溶液时,整个腐蚀过程中样品的质量变化很小;在喷涂NaCl+Na2SO4混合盐溶液时,在腐蚀前期样品质量变化平稳,随着腐蚀时间的延长增重量逐步降低,当腐蚀120 h后却出现负增重现象,表明表面的腐蚀产物发生了剥落;在喷涂NaCl溶液时,样品的腐蚀增重明显提升,在腐蚀24 h后就达到了2 mg·cm-2,随后样品的腐蚀增重显著降低,这也表明样品表面的腐蚀产物存在明显的剥落。对比3种涂盐的腐蚀动力学曲线可以看出,随着溶液氯离子浓度的增加,TC4涂层样品耐腐蚀性能显著降低。

图3 3种涂盐条件下TC4涂层样品的腐蚀动力学曲线Figure 3 Corrosion kinetic curves of TC4 coating samples under three salt coating conditions
2.3 表面相结构
图4为TC4涂层样品在600℃下腐蚀168 h后的表面XRD谱图。从图4可见,涂层的相主要为Al3Ti,而样品表面腐蚀产物主要为TiO2、Al2O3及少量的Al2S3,并且在样品表面检测到残留的Na2SO4和NaCl。
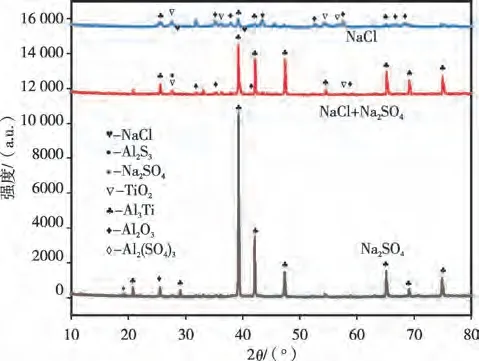
图4 TC4涂层样品在600℃下腐蚀168h后的表面XRD谱图Figure 4 Surface XRD patterns of TC4 coating samples after corrosion at 600℃for 168 h
2.4 表面腐蚀形貌
图5为TC4涂层样品在600℃下腐蚀168 h后的SEM图像。从图5可见:在只喷涂Na2SO4溶液的情况下,合金样品表面形貌较为平整,没有发生明显的缺陷和裂纹,表面生成了较为连续且致密的氧化膜,而且在大多数区域内腐蚀产物与基材结合良好;在喷涂NaCl+Na2SO4混合盐溶液的情况下,样品表面的腐蚀产物多为颗粒状和絮状,并且形成了粗糙、多孔的卷曲状和堆积状结构,在局部区域内腐蚀产物已经从样品表面脱落;在单独喷涂NaCl溶液的情况下,样品腐蚀更为严重,腐蚀产物变得更加松散,呈现针状结构,表明随着腐蚀溶液中氯离子浓度 的提升,表面氧化物发生了明显的腐蚀。

图5 600℃下腐蚀168 h后TC4涂层样品的表面SEM形貌图Figure 5 SEM images of the surface of the TC4 coating sample after etching at 600 °C for 168 h
2.5 截面腐蚀形貌
图6为600℃下经Na2SO4溶液腐蚀168 h后样品的截面SEM图和EDS元素分布图。从图6可以看出:样品的腐蚀氧化层较浅只有5 μm左右,并且其与基体结合良好;氧化层主要为Al和Ti的氧化物。
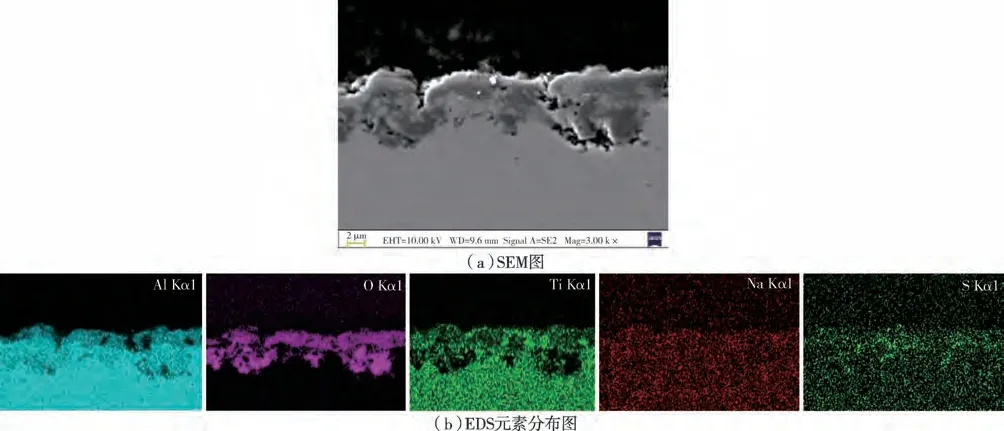
图6喷涂Na2SO4溶液腐蚀后TC4涂层样品的截面SEM图及EDS元素分布图Figure 6 Cross-sectional SEM image and EDS element distribution of TC4 coating sample after spraying Na2SO4 solution corrosion
图7为600℃下经NaCl+Na2SO4混合盐溶液腐蚀168 h后样品的截面SEM图和EDS元素分布图。从图7中可以看出:经NaCl+Na2SO4混合盐溶液腐蚀后,TC4涂层样品的表面生成了多层结构的氧化层;多层结构的外层氧化层的成分主要为Al的氧化物、内层主要为Ti的氧化物;在外层只检测到S元素的亮点,而在内层已存在Cl元素的零星亮点,说明少部分Cl元素侵蚀到涂层内部。
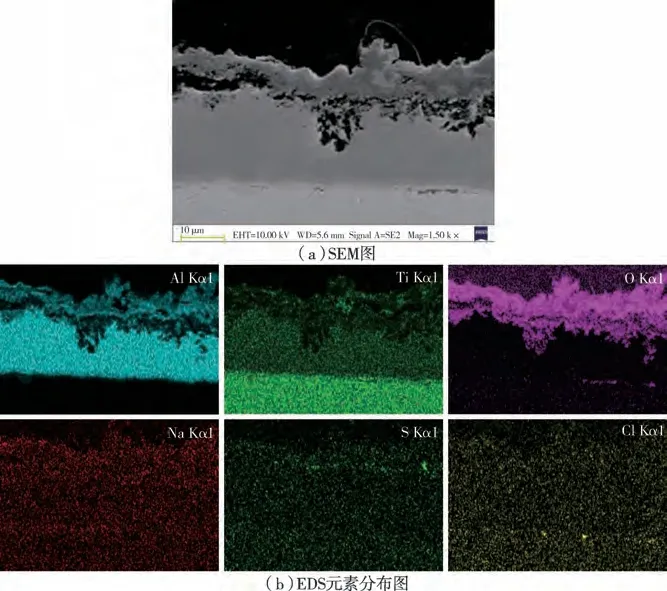
图7 在喷涂NaCl+Na2SO4溶液腐蚀后TC4涂层样品的截面SEM图及EDS元素分布图Figure 7 Cross-sectional SEM image and EDS element distribution of TC4 coating sample after spraying NaCl+Na2SO4 solution corrosion
从图8可以看出:当涂盐类型为NaCl溶液时,样品表面出现了严重的腐蚀破坏,在表面出现大量的腐蚀产物,并且最外层的腐蚀产物已经与基体分离,表面出现了明显的多孔剥落被腐蚀的形貌;腐蚀产物主要是富含Al、Ti的氧化物和氯化物。

图8 在喷涂NaCl溶液腐蚀后TC4涂层样品的截面SEM图及EDS元素分布图Figure 8 Cross-sectional SEM image and EDS element distribution of TC4 coating sample after spraying NaCl solution corrosion
3 分析与讨论
结合宏观腐蚀形貌、腐蚀前后相结构、腐蚀增重动力学曲线、表面形貌、截面微观结构和元素分布等实验结果分析,在不同涂盐种类条件下涂层样品的抗腐蚀性能差异明显,表明S和Cl协同作用对涂层样品抗腐蚀性能有影响。
在氯化腐蚀方面,被广泛接受的机理是“活性氧化”[16-20]。在腐蚀过程中,碱金属氯化物首先溶解氧化膜并生成氯气[21-22]。然后,氯气扩散到涂层表面并与涂层元素反应形成挥发性金属氯化物。当金属氯化物逐渐挥发时,氧分压逐渐升高,它们被氧化成非保护性的氧化物和氯气[23-24]。随后,一部分新生成的氯气再次返回到涂层表面并重复进行氯化物反应,最后在氯气的催化下涂层逐渐被腐蚀[25]。对于硫腐蚀而言,公认的机理是“碱性助溶腐蚀”[26-27]。在腐蚀过程中,硫酸盐首先分解为碱金属氧化物。然后,这些碱金属氧化物溶解保护性氧化物膜以而形成碱金属盐。最后,在浓度梯度的驱动下,这些碱金属盐逐渐向外扩散并分解形成不受保护的氧化物层,从而进一步降低了材料的耐高温腐蚀性[28-29]。
TC4涂层的热腐蚀过程包括以下几个步骤,其反应式如下。

在热腐蚀开始阶段(阶段1),由于Ti、Al与O具有高度相似的亲和力(见反应式(1)和(2)),在涂层表面迅速形成由Al2O3和TiO2组成的氧化物层。由于TiO2相对于Al2O3的生长速度较高,涂层表面的氧化层具有典型的多层微观结构,其中表层由TiO2组成、内层则由TiO2和Al2O3的异质相混合物组成。混合盐中的Na2SO4在高温下(见反应式(3))分解为Na2O和SO3,Na2SO4的分解增加了混合盐的碱度,加速了Al2O3两性氧化物和TiO2酸性氧化物的溶解;当涂层氧化到一定程度时,涂层表面被氧化层完全覆盖,从而减缓了氧的内部扩散,因此腐蚀反应在随后的腐蚀过程中起主导作用;TiO2鳞片结构疏松、氧空位浓度高、间隙多,成为腐蚀介质的有效输运通道。
腐蚀过程进入第2阶段(阶段2)。在这一阶段,表层的TiO2与NaCl和Na2O反应(见反应式(4)和(6)),导致TiO2发生酸性溶解并形成钛酸钠NaTiO2和Na2TiO3,而氯气(见反应式(5)和(6))重新释放。由于TiO2表层疏松多孔,混合盐和氯的腐蚀产物通过缝隙和孔隙向内部的氧化层渗透;由于Al2O3的形成,氧化鳞片的内层比上层密度大,因此内层对混合盐和氯的快速向内传输有较好的阻隔作用。
混合盐在表层和内层界面与TiO2和Al2O3发生反应,腐蚀过程进入第3阶段(阶段3),在这一阶段,界面沿横向和纵向溶解,TiO2(见反应式(4)—(6))溶解形成钛酸钠和氯。根据XRD结果,氯化钠和氧化钠可能与Al2O3发生反应生成铝酸钠(见反应式(7)和反应式(8)),表面TiO2的溶解和界面的侧向损伤导致腐蚀产物的剥落;随着腐蚀过程的进行TiO2和Al2O3不断溶解,混合盐和氯通过松散的TiO2氧化物进一步向内扩散,到达氧化层和涂层之间的界面。
腐蚀过程进入第4阶段(阶段4)(见反应式(5)和(6)),界面处发生了自续反应。氯气与Ti、Al反应(见反应式(9)—(11))生成挥发性氯化物TiCl2、TiCl4和AlCl3,而Ti、Al与O2和NaCl反 应(见 反应式(12)和反应式(13))生成钛酸钠和铝酸钠,氯化物与O2反应(见反应式(14)—(16))生成氧化物和氯气,氧化物TiO2和Al2O3与氯化钠反应(见反应式(4)—(8))引起氧化物溶解并释放氯气。自续反应加速了涂层的腐蚀溶解,当涂层与氧化层之间的界面被破坏时氧化层整体脱落。在热腐蚀过程中,混合盐覆盖在氧化层的表面,氯的生成降低了氧的溶解度和扩散率,这两方面的综合作用导致氧化层的形成速率小于腐蚀溶解速率。因此,氧化层不再是防止热腐蚀的保护层,涂层被盐和氯直接腐蚀并破坏。
4 结论
(1)研究了表面喷涂Na2SO4溶液、NaCl溶液及NaCl+Na2SO4混合盐溶液的TC4涂层样品,在模拟垃圾焚烧炉受热面高温腐蚀环境下的抗高温腐蚀性能。当单独喷涂Na2SO4溶液时,涂层表面发生微弱的腐蚀;当喷涂NaCl+Na2SO4混合盐溶液时,在涂层表面生成了多层结构的腐蚀氧化层;当单独喷涂NaCl溶液时,涂层表面出现了严重的腐蚀破坏,腐蚀产物主要是富含Al、Ti的氧化物和氯化物。
(2)在腐蚀过程中,NaCl在高温下形成Cl-1,穿透初期形成的氧化膜。随后,生成的金属氯化物在高温下汽化,向外扩散到达表面氧分压较高的区域时,又被氧化为金属氧化物。此过程连续循环,使表面的多层氧化膜不断被腐蚀破坏,最终导致氧化膜的剥落,而S和Cl的协同作用可以降低腐蚀速率。

