液下阳极放电等离子体的放电特性和光谱诊断
陆泉芳,马晓娟,冯 妍,李娟龙,王 波
(1.西北师范大学 化学化工学院,甘肃 兰州 730070;2.西北师范大学 学报编辑部,甘肃 兰州 730070)

发射光谱法(OES)作为一种简便的采集等离子体光学特征的诊断手段,在等离子体研究中得到了广泛应用[16-18].如Sun等[17]用发射光谱法证明脉冲流光电晕放电中有OH,H和O产生,并提出了活性物种产生的初步机理.郑培超等[18]建立了一种基于液体阴极放电的大气压等离子体发生装置,测量了200~900 nm内的发射光谱,观察到了强度较高的H,OH和O谱线,并对这些物种的激发过程进行了探讨.另外,利用发射光谱可以估算电子密度(Ne)、OH转动温度(Trot)、电子激发温度(Te),这些物理参数对深入理解等离子体形成过程中的激发、解离、电离等具有举足轻重的作用,是解释放电产生的机理和推广等离子体的应用所要解决的关键科学问题[19-20].如Mukasa等[21]用发射光谱法计算了射频等离子体中的温度分布,得到的Te在3 300~4 800 K,OH的Trot在1 500~3 700 K.Liu等[22]用发射光谱诊断了接触辉光放电等离子体的光谱特性和物理参数,发现当放电电压从450 V升高到500 V时,Te由1.09×104增大到1.59×104K,而Ne存在先逐渐减小而后有轻微增大的趋势,估算得到的Ne约为7.49 ×1023m-3.
通常情况下,气相和气-液界面产生的等离子体用光谱诊断报道较多[16-22],由于溶液对液下放电产生的光有吸收,导致光谱仪检测到的光非常有限,这给液下放电等离子体光谱诊断和等离子体参数估算带来了极大困难.最近,Nomura等[23]虽然用光谱诊断技术得到液下放电的Te约为3 200~3 700 K,Trot为3 500~5 000 K,Ne为(0.5~5.8)×1021m-3,但是光谱诊断装置结构复杂,且对放电机理的研究深入不够.
为了深入研究液下阳极放电的物理化学反应机理,文中构建了一种新颖的液下阳极放电的光谱诊断装置.利用该装置,测量了200~1 070 nm范围内不同放电电压下H,O,OH等的发射光谱,用酸度计测定了阴阳极周围溶液的pH和总体溶液的pH,用H的二谱线法估算了等离子体的电子激发温度Te,Lifbase软件模拟估算了OH的转动温度Trot,H原子谱线的Stark展宽估算了电子密度Ne,同时考查了放电电压对等离子体光谱特性和物理参数的影响规律.本研究结果为进一步推广液下阳极放电的应用提供理论依据.
1 实验部分
1.1 仪器与试剂
增强电荷耦合器件(ICCD)相机(MN:DH 334 T-18U-03,英国Andor公司);八通道高分辨光纤光谱仪(荷兰AvaSpec公司),波长200~1 070 nm,电荷耦合器件(CCD)探测器;直流稳压稳流电源(LW100J2,中国上海力友公司),电压0~1 000 V,电流0~500 mA.高精密分析天平、超纯水仪、酸度计及恒温磁力搅拌器等.Na2SO4、甲基橙、酚酞均为市售分析纯试剂.
1.2 实验装置及方法
图1a为液下阳极放电的产生装置和光谱检测系统.
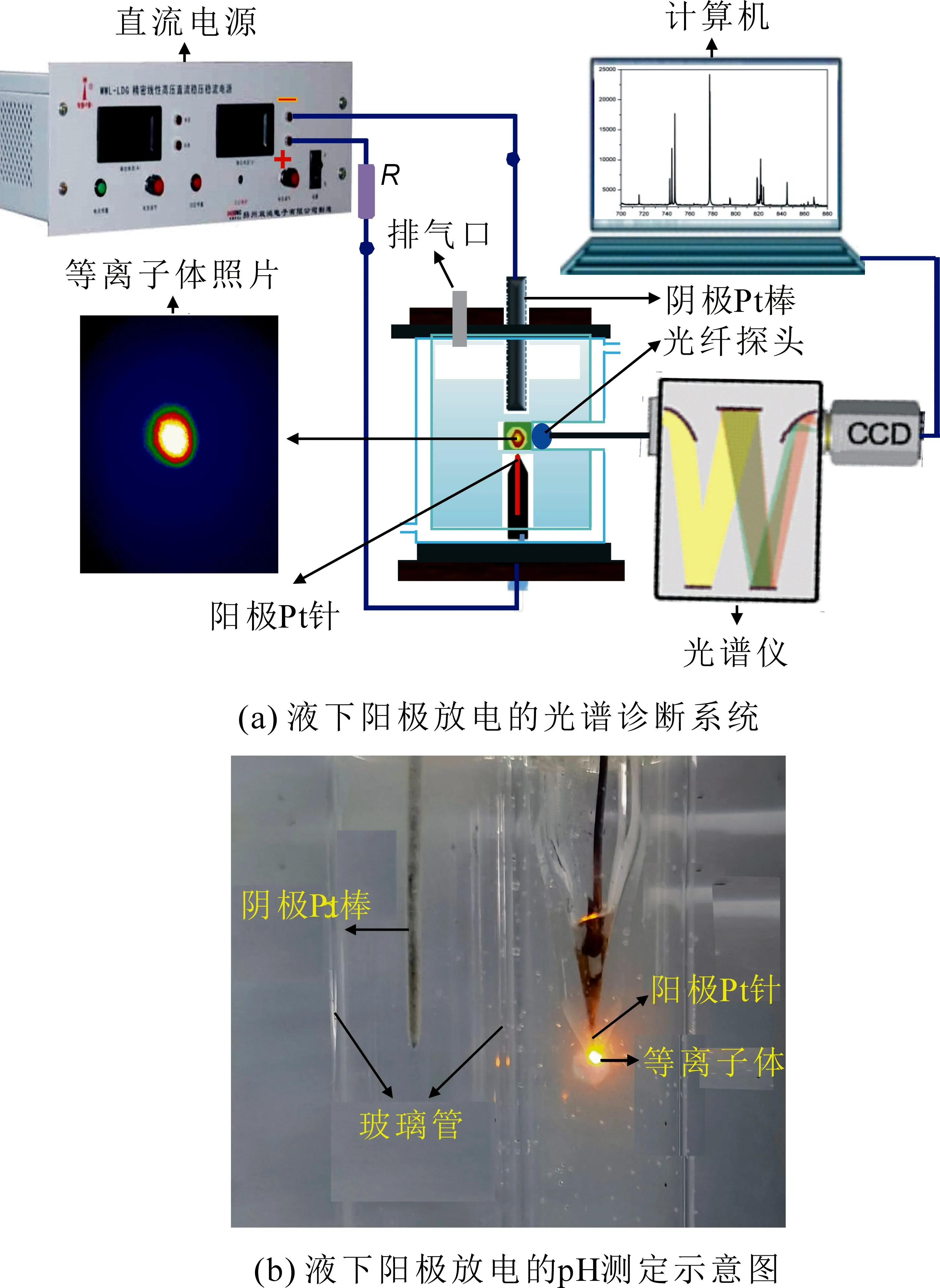
图1 液下阳极放电的光谱诊断(a)和阴阳两电极周围溶液pH的测定装置(b)
放电装置(图1a)由石英放电器皿、直流电源、阴极铂棒(直径2 mm)和自制阳极铂针(直径为0.5 mm、针尖长为0.5 mm)构成.在放电器皿侧面凹进开一个直径15 mm的窗口,是为了缩短光在液体内部的光程,从而减小溶液对光的吸收[24].用pH计测定不同放电时间下溶液的pH.
验证和测定电极周围溶液酸碱性的装置见图1 b,将阳极铂针和阴极铂棒分别放入两支玻璃管中,两玻璃管的间隙约5 mm.在放电过程中,将甲基橙和酚酞指示剂滴入玻璃管,观察溶液颜色变化.同时,用酸度计测定阴阳极周围溶液的pH.
2 结果与讨论
2.1 液下阳极放电的电流-电压曲线
图2为2 g·L-1Na2SO4电解液中液下阳极放电的电流随电压变化的特性曲线.AB段(0~190 V),遵循欧姆定律,电流随电压的升高而增大[24];BC段(190~340 V),欧姆加热导致Pt阳极周围的水局部气化,随后在阳极铂丝周围形成连续、脉动的蒸汽泡,使阳极表面与电解液之间被气泡隔离,间歇性地阻止电流通过,从而使电流出现波动.同时,随着外加电压的增加,电流开始减小.这是因为气泡的导电性低于电解液的导电性,而气泡的等效电阻远高于电解液的等效电阻,导致电流突然下降.CD段(340~480 V),Pt针表面的气泡被击穿,产生蒸汽鞘,并发出微弱的辉光,也称为部分辉光放电;DE段(480~600 V),蒸汽鞘被完全击穿,电流随电压升高而基本保持不变,但辉光逐渐增强,为正常放电区.在该区域,蒸汽鞘形成辉光放电等离子体,并通过辉光放电等离子体传输电流.在高能电子作用下气态原子的外层电子激发至高能态然后跃迁到较低的能态,这时原子将发射出特征谱线.EF段(>600 V),随电压增大,电流逐渐增大,这是由于等离子体为导电气体,回路的电阻变小,电流变大,这一区域为异常放电区[25].当电压低于480 V时产生的光弱,未能检测到活性物种的谱线,而放电电压高于600 V时,较高能量使阳极铂针高温融化损坏,因此光谱测量所需电压范围为500~600 V.

图2 液下阳极放电的电流-电压曲线
2.2 液下阳极放电过程中两电极周围溶液和总溶液的酸碱性检测
将阴阳两极放入2个玻璃管中,分别用甲基橙和酚酞指示剂对放电过程中电极周围的溶液酸碱性进行测试,结果见图3.可以看出,在放电过程中阳极铂针周围的溶液中滴加甲基橙后,溶液变红色,说明溶液显酸性,证明液下阳极放电过程中产生H+;在阴极铂棒周围的溶液中滴加酚酞后,溶液变紫色,说明溶液显碱性,证明阴极铂棒周围产生OH-.

(a)放电前 (b)放电过程中
为了进一步确定阳极和阴极周围溶液的酸碱性,用pH计测定了阴极电解液和阳极电解液在不同放电时间内的pH值变化.由图4可知,放电前溶液基本为中性,初始pH约为6.8;放电3 min后,阳极电解液溶液的pH值从6.8下降到2.3,阴极溶液的pH从6.8上升到11.7.放电5 min后,阳极和阴极溶液的pH分别保持在2.5和11.8左右,这些结果进一步说明放电过程中,阳极有H+产生,阴极有OH-产生.
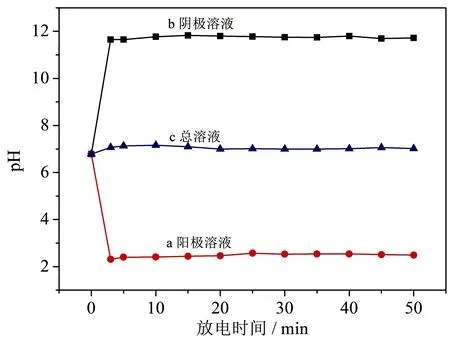
图4 不同放电时间内阳极溶液(a)、阴极溶液(b)和总溶液(c)pH的变化
去除阴阳极玻璃管后,测定了总体溶液的pH值,发现放电过程中溶液总体pH基本保持在7左右,说明溶液呈现中性.基于以上分析,可以将液下放电产生的H+和OH-进行调控,使其应用于一些有益的化学反应中.
2.3 液下阳极放电的发射光谱
图5为2 g·L-1Na2SO4溶液在570 V、波长为200~1 070 nm的发射光谱.283.0~309.0 nm的谱线为OH的分子谱带;656.3和486.1 nm处为Hα和Hβ的原子发射线[24];777.4和844.6 nm处为激发态OⅠ 原子的谱线;459.6和463.7 nm处为OⅡ 的离子线[22].588.6处为NaⅠ的原子发射谱线[10],证明放电溶液中有Na+存在,据此可以将液体阳极放电用于溶液中金属元素的发射光谱诊断.另外,放电过程中阳极发出明亮的黄光,这是因为钠的焰色反应为黄色.此外,由图6可以看出,随放电电压从500 V升高到600 V,以上各谱线的发射强度逐渐升高,这是因为随电压增大,功率增大,轰击水分子的高能电子的能量增加,导致单位时间内H2O被碰撞电离产生的等离子体数目增多,因而发射光谱强度增大[26].

图5 570 V放电电压下的发射光谱

图6 不同放电电压下溶液的发射光谱
研究表明,等离子体鞘层内的水蒸汽在高能电子轰击下,被激发分解生成H,O,OH等高活性物种,主要反应和解离能如下[22,26-282]:
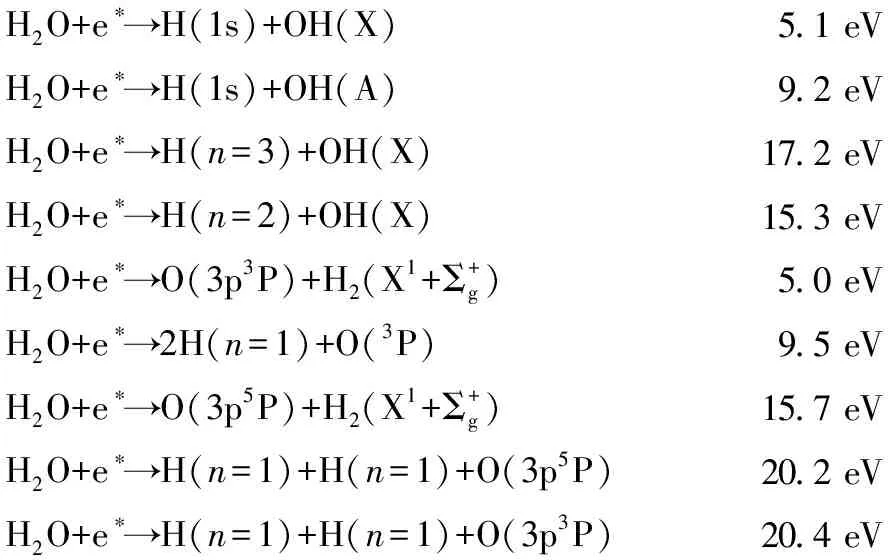
H2O+e∗→H(1s)+OH(X)5.1 eVH2O+e∗→H(1s)+OH(A)9.2 eVH2O+e∗→H(n=3)+OH(X)17.2 eVH2O+e∗→H(n=2)+OH(X)15.3 eVH2O+e∗→O(3p3P)+H2(X1+Σ+g)5.0 eVH2O+e∗→2H(n=1)+O(3P)9.5 eVH2O+e∗→O(3p5P)+H2(X1+Σ+g)15.7 eVH2O+e∗→H(n=1)+H(n=1)+O(3p5P)20.2 eVH2O+e∗→H(n=1)+H(n=1)+O(3p3P)20.4 eV
表1列出了活性物种的特征波长和跃迁能态,基于表1和上述分解反应,说明液下阳极放电过程中,等离子体的解离能可能超过20.4 eV.

表1 活性物种的特征波长和跃迁能态
另外,水分子被激发产生的各种活性物种之间也会发生如下反应[29]:
基于以上分析,液下阳极放电过程中,阳极周围的水分子在高能电子轰击下产生的活性物种为:
表2列出了活性物种的标准电极电势[9,12].利用液下阳极放电产生的H,e-等的强还原性,HO,O,H2O2等的强氧化性,以及紫外光、热辐射,通过控制反应条件,使溶液中难以发生的还原反应、氧化反应、消除反应、加成反应等得以顺利进行,从而使液下阳极放电等离子体在废水处理、纳米材料制备、有机合成、光谱分析、杀菌消毒、医药卫生等方面具有广阔的应用前景.

表2 放电产生的活性物种和标准(氢标还原)电极电势
2.4 等离子体参数的测量
激发温度(Te)的高低对等离子体形成过程中的电离和激发以及激发效率有重要影响[30-31].液下放电过程中,等离子体自身的辐射相对较弱,光激发和光电离截面小,原子发光的主要机制是通过电子碰撞电离和激发,激发态的原子通过退激辐射发射光子,因此可通过发射光谱的谱线强度的比值方法测量得到激发温度[32].一般情况下,假设等离子体处于局部热力学平衡,即电子的速率符合麦克斯韦分布,原子在不同能级上的布居满足玻尔兹曼分布,此时激发温度可以用二谱线法求得[23,33-35]:
(1)
(1)式取对数,可变为:
(2)
其中,k为玻尔兹曼常数,k=1.38×10-23J·K-1;下标1和2分别代表H原子的Hα(656.3 nm)和Hβ(486.1 nm)谱线;E1,E2,λ1,λ2,I1,I2,g1,g2A1,A2分别为谱线1和谱线2的激发能量、波长、辐射强度、上能级统计权重和跃迁几率.电子在不同能级之间跃迁时,统计权重(总简并度)g=2n2[36].表3列出了H原子2条谱线的参数,将谱线参数和谱线发射强度代入(2)式,得到激发温度.

表3 氢原子谱线的特征参数
转动温度(Trot)反映了分子中转动能级的能量.利用LIFBASE软件拟合,对OH(A2∑+→X2∏)在305~320 nm范围内不同温度OH的实验光谱进行拟合,从而得到OH的Trot[22,37].图7a为570 V放电电压下实验光谱与理论光谱的拟合曲线,得到570 V下的Trot为2 630 K.
等离子体的电子密度(Ne)表示等离子体内粒子之间的碰撞程度,Ne越大,粒子间的碰撞几率越大,等离子体光谱信号强度越高.在局部热力学平衡条件下,Balmer线系的Stark展宽被用于估算等离子体中的Ne.Hα的Stark展宽半高全宽(FWHM)用(3)式计算[22,38]:
(3)
其中,FWHMHHα为Hα谱线的半高全宽.利用origin 8.5对光谱测量的Hα谱线进行高斯拟合,就可得到FWHMHHα值,然后代入(3),最终得到电子密度.图7b为570 V下Hα的FWHM拟合曲线,得到FWHMHHα为0.234 nm,将其代入(3)式,获得Ne为2.860×1022m-3.

图7 570 V下Trot(a)和Ne(b)的实验和理论拟合曲线
放电电压对激发温度和转动温度的影响见图8.可以看出,激发温度和转动温度均随放电电压的增大而升高.即,当电压从500 V升高到600 V时,激发温度从3 051 K升高到3 628 K,转动温度从2 100 K升高到2 800 K.这是由于增大放电电压,会使电子能量增大,等离子体电子激发温度升高,导致更多的原子跃迁到激发态,从而使得高能级向低能级跃迁的电子数增加,谱线强度增加.由于液下阳极放电的电子激发温度范围为3 051~3 628 K,低于104K,说明液下阳极放电属于低温等离子体中的辉光放电范畴[36].
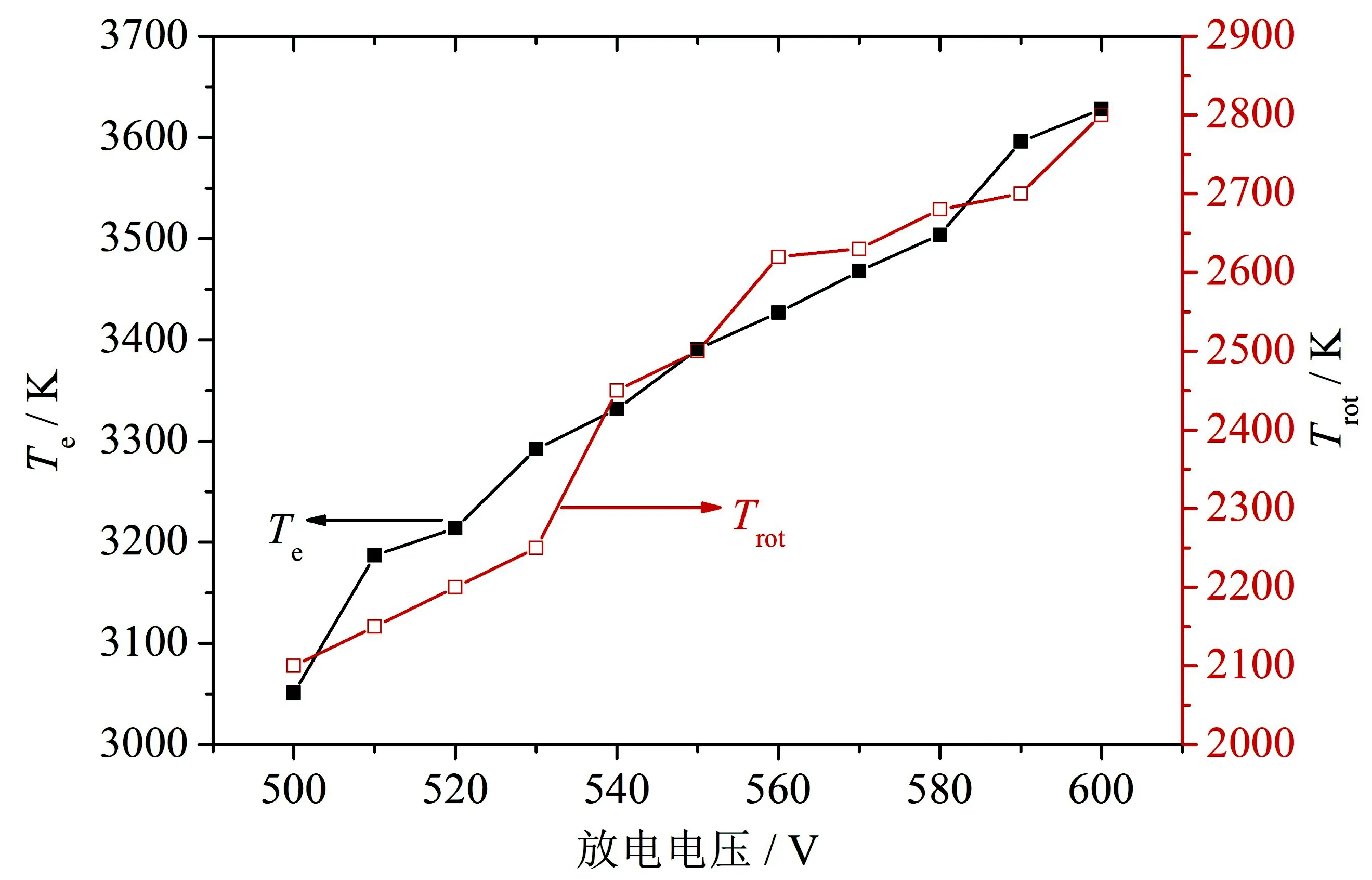
图8 Te和Trot随放电电压的变化
不同放电电压下电子密度的变化见图9.可以看出,电子密度随放电电压的增大而逐渐增大.即,当放电电压从500 V升高到600 V时,Ne从2.680×1022m-3升高到2.894×1022m-3.这是由于放电电压增大,导致功率增大,激发等离子体的能力增大,加剧了水分子的激发和电离,从而产生更多的电子.

图9 电子密度随放电电压的变化
图10展示了不同放电电压下ICCD拍摄的等离子体图斑变化.可以看出,液下放电的发光强度随放电电压的升高而增强,这是因为电子获得的能量增加,激发效率提高.另外,从图10还可以看出,电压越高,产生的辉光放电等离子体的图斑体积越大.由于单位体积内的电子数远比等离子体的体积增大的快,因此电子数密度升高.ICCD照片进一步证明理论计算的准确性,暗示放电电压对等离子体空间分布和激发温度有强烈的相关性.
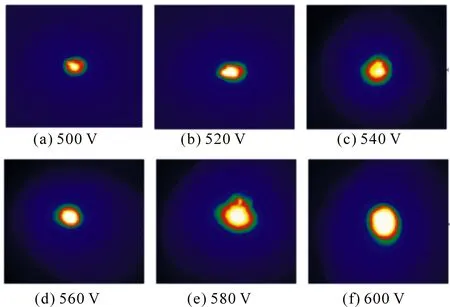
图10 不同放电电压下液下阳极放电等离子体的图像
3 结论
通过发射光谱诊断法对液下阳极放电的特性进行了研究,得出结论如下:

2)H,O和OH的谱线发射强度随放电电压从500 V升高到600 V而逐渐增大.
3)当放电电压从500 V升高到600 V时,激发温度从3 051 K升高到3 628 K,OH的转动温度从2 100 K升高到2 800 K;Hα计算得到的电子密度从2.680×1022m-3升高到2.894×1022m-3.


