用C272从粗硫酸镍溶液中分离锌试验研究
葛素志
(1.紫金铜业有限公司,福建 龙岩 364204;2.福建省通绿色生产及伴生资源综合利用重点实验室,福建 龙岩 364204)
铜电解液中,镍离子随电解进行而逐渐富集,需定期开路。目前,大部分企业采用冷冻结晶、蒸发浓缩工艺脱除电解液中部分镍离子,制成粗硫酸镍。这种粗硫酸镍中镍质量分数一般为18%~20%,也含铜、铁、锌、铅、钴、钙、镁等杂质[1-3]。硫酸镍中的大部分杂质可以通过化学沉淀、溶剂萃取、氟化沉淀等方法脱除[3-7],而锌一般采用溶剂萃取法脱除。主要的萃取剂有P204、P507。这2种萃取剂对于铁、镍的分离效果较好,而对锌、镍分离效果稍差,且萃取条件苛刻,使用前需进行皂化,分离效果与皂化效果有关,如进行钠碱皂化,则容易引入钠离子,导致硫酸镍中钠离子超标[8-9]。
C272成分稳定,选择性高,萃取和反萃取平衡水相酸度较低,多用于钴离子萃取、稀土离子之间的分离[10-19]。在硫酸盐溶液中分离钴、镍,分离系数是P507的24.6倍[11];对稀土的萃取选择性优于P507和P204[14-16]。但其用于萃取分离锌的研究较少。
C272是一种有机膦萃取剂,在酸性介质中对金属离子的萃取顺序为Fe3+>Zn2+>Cu2+>Pb2+>Co2+>Mg2+>Ca2+>Ni2+,因此,合理控制pH可以实现Zn2+与Ni2+的有效分离[20-23]。试验研究了以C272从电解液中萃取分离锌离子。
1 试验部分
1.1 试验原料、试剂与设备
粗硫酸镍:取自某铜冶炼企业电解厂冷冻蒸发结晶工序,其中镍质量分数约21%,含铜、铁、铅、锌、钙、镁等杂质元素。水溶解后,脱除铜、铁等杂质元素,除杂后溶液主要化学成分见表1。

表1 除杂后粗硫酸镍溶液的主要化学成分 mg/L
主要试剂:氢氧化钠、硫酸,分析纯,均大于95%;C272,工业级,大于99%。
主要设备:1 000 mL分液漏斗,pHB-4型便携式pH计。
1.2 试验原理
C272是一种弱酸类萃取剂,主要成分二(2,4,4-三甲基戊基)次膦酸,可以完全稳定存在于芳香族和脂肪族稀释剂中[23-25]。C272的结构式为
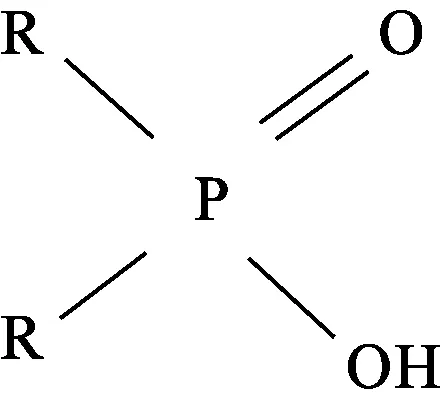
其中,R为

锌、镍均属于第4周期过渡金属元素,锌电负性为1.6,镍电负性为1.9。一般认为,电负性大于1.8非金属性较强,小于1.8金属性较强,因此锌的金属性更强,更容易取代—OH上的氢而发生萃取反应。
若不考虑缔合离解等因素,C272萃取金属离子的反应为

(1)
热力学平衡常数为
(2)
萃取分配比为
(3)
将式(3)带入式(2)中,转换后取对数可得
lgD=lgKa+npH+nlg[HA]。
(4)
由此表明C272对金属离子的萃取受溶液pH影响很大。在相同pH溶液中,C272对某些金属离子的萃取次序为Fe3+>Zn2+>Cu2+>Pb2+>Co2+>Mg2+>Ca2+>Ni2+。所以,控制溶液pH,可实现镍与锌的较好分离[20-23]。溶液中Fe3+质量浓度较高,萃取Zn2+之前,需先除Fe3+。
1.3 试验方法
萃取试验:有机相为20%C272+80%磺化煤油混合摇匀,与调好pH且已去除Fe3+的硫酸镍溶液按一定相比加入到分液漏斗中,充分振荡并静置分层,分离萃余液,测定其中锌、镍离子质量浓度,计算萃取率。
反萃取试验:负载有机相与质量浓度180 g/L的硫酸溶液按体积比1/1在分液漏斗中混合充分,振荡2 min,静置分层,分离水相,测定水相中锌、镍离子浓度,计算反萃取率。
2 试验结果与讨论
2.1 Vo/Va对Zn2+、Ni2+萃取分离的影响
萃原液体积300 mL,pH=3.0,与不同体积有机相混合,振荡5 min后静置分层,如此6级循环萃取,Vo/Va对Zn2+、Ni2+萃取率的影响试验结果如图1所示。

图1 Vo/Va对Zn2+、Ni2+萃取率的影响
由图1看出:随Vo/Va增大,Zn2+、Ni2+萃取率均有所下降;Vo/Va=1/1时,Zn2+萃取率为99.74%,Ni2+损失率为6.84%;继续增大Vo/Va,Zn2+萃取率降低,与Ni2+难以有效分离。另外,Vo/Va越大,处理成本越高。综合考虑,确定Vo/Va以1/1为宜。
2.2 溶液pH对Zn2+、Ni2+萃取分离的影响
萃原液体积300 mL,Vo/Va=1/1,振荡5 min后静置分层,6级循环萃取,溶液pH对Zn2+、Ni2+萃取率的影响试验结果如图2所示。

图2 溶液pH对Zn2+、Ni2+萃取率的影响
由图2看出:随溶液pH增大,Zn2+萃取率有所下降,而Ni2+萃取率反而升高;pH=3.0时,Zn2+萃取率为98.58%,Ni2+萃取率仅为0.11%。随溶液pH升高,溶液中H+浓度下降,化学反应式(1)向右移动,使得金属离子易与萃取剂结合,而溶液中Ni2+浓度较高,约为Zn2+浓度的30倍,单位体积内活化分子数更大,从而使Ni2+与萃取剂之间的有效碰撞概率更大,更易促进萃取反应发生。因此,随溶液pH增大,Ni2+反而更易被萃取至有机相中。综合锌、镍的萃取效果,确定溶液pH以3.0为宜。
2.3 振荡时间对Zn2+、Ni2+萃取分离的影响
萃原液体积300 mL,pH=3.0,Vo/Va=1/1,振荡后静置分层,6级循环萃取,振荡时间对Zn2+、Ni2+萃取率的影响试验结果如图3所示。

图3 振荡时间对Zn2+、Ni2+萃取率的影响
由图3看出:振荡5 min时,Zn2+、Ni2+分离效果最好;振荡时间大于5 min,Ni2+损失率增大。振荡时间越长,越易导致乳化,影响分层;另外,萃取剂与金属离子之间的结合都是可逆的,平衡后,继续反应可能会影响金属离子的萃取。综合考虑,确定振荡时间以5 min为宜。
2.4 萃取级数对Zn2+、Ni2+萃取分离的影响
萃原液体积300 mL,pH=3.0,Vo/Va=1/1,振荡5 min后静置分层,分别进行4、5、6、7、8级萃取。萃取级数对Zn2+、Ni2+萃取率的影响试验结果如图4所示。

图4 萃取级数对Zn2+、Ni2+萃取率的影响
由图4看出:随萃取级数增加,Zn2+、Ni2+萃取率提高;萃取级数为6级时,Zn2+萃取率大于99%,Ni2+萃取率很低。萃取级数的变化不仅会影响萃取效果而且也涉及萃取成本,一般级数越多,萃取剂夹带损失及运行成本也越高,综合考虑,确定萃取以6级为宜。
2.5 综合萃取
根据上述单因素试验结果,在Vo/Va=1/1、萃原液pH=3.0条件下混合振荡5 min,之后静置分层,循环6级萃取。萃余液的组成见表2。

表2 萃余液的组成 mg/L
对负载有机相用180 g/L硫酸溶液反萃取,Vo/Va=1/1,反应2 min,静置分层,反萃取液的组成见表3。

表3 反萃取液的组成 mg/L
由表2、3看出:在最佳试验条件下萃取,Zn2+与Ni2+得到较好萃取分离,锌萃取率为99.86%,而镍萃取率仅为2.38%;用硫酸对负载有机相进行反萃取,Zn2+、Ni2+易于被反萃取,有机相再生后可重复使用。
3 结论
用C272萃取剂可以从粗硫酸镍溶液中有效分离去除杂质Zn2+,而Ni2+损失率较低。C272为一元弱酸类萃取剂,由于—OH的氢被金属离子取代而发生萃取反应,所以溶液pH对萃取过程有很大影响。根据不同pH条件下,C272对Zn2+、Ni2+的萃取效果不同而实现有效分离。在Vo/Va=1/1、萃原液pH=3.0条件下混合振荡5 min,之后静置分层,经6级循环萃取,锌萃取率大于99%,而镍萃取率仅为2.38%,二者分离效果较好。

