正交实验优化高浓玉米燃料乙醇发酵条件
惠继星,金香梅,宁艳春,杨艳妮,伊 凤,陈希海,范 锐
(1.中国石油吉林石化公司研究院,吉林 吉林 132021;2.中国石油吉林石化公司质量检验中心,吉林 吉林 132021;3.吉林燃料乙醇有限责任公司,吉林 吉林 132101)
国家“十四五”规划提到要构建现代能源体系,推进能源革命,建设清洁低碳、安全高效的能源体系,提高能源供给保障能力,加快发展非化石能源。燃料乙醇作为一种清洁、可再生能源,能有效缓解对化石燃料的依赖、提高能源安全性,对缓解石油短缺、降低环境污染、节能减排具有重要意义[1]。
目前,世界超过95%乙醇以农副产品为原料生产,在中国燃料乙醇主要以不宜食用的陈化玉米为原料[2],近年来,随着能源危机、环境危机日益加重以及玉米价格的持续上涨,更多的燃料乙醇企业都纷纷关注如何最大限度地降低燃料乙醇生产成本和提高原料出酒率[3]。利用高浓乙醇发酵技术生产燃料乙醇,可降低物料输送、精馏及烘干等工序的能耗,减少污水排放,符合国家清洁生产的要求,是今后燃料乙醇行业的发展趋势[4]。
高浓乙醇发酵强度一方面取决于酵母菌自身的繁殖力、发酵力以及对发酵环境的耐受性,另一方面主要取决于对发酵工艺的控制[5]。发酵液pH值、糖化酶添加量及外加氮源等因素都直接影响酵母菌发酵产乙醇的效果,有关发酵工艺优化方面的报道较多,但是利用正交实验方法优化高浓玉米燃料乙醇发酵方面的报道相对较少。实验以玉米粉为原料,采用同步糖化发酵工艺,在单因素实验的基础上,利用正交实验优化发酵过程中酸性蛋白酶添加量、糖化酶添加量、尿素添加量及发酵液初始pH对高浓玉米燃料乙醇发酵效果的影响,以期为高浓玉米燃料乙醇的工业化生产提供参考。
1 实验部分
1.1 原料、试剂与仪器
市售玉米粉;酸性蛋白酶:市售,酶活力5万U/mL;糖化酶:市售,10万U/mL;耐高温α-淀粉酶:市售,24万U/mL;浓醪酵母:湖北安琪酵母股份有限公司。
硫酸:分析纯,辽宁新兴试剂有限公司;氢氧化钠:分析纯,北京化工厂;尿素:分析纯,天津市风船化学试剂科技有限公司。
立式全温振荡培养箱:ZQPL-200,天津市莱玻特瑞仪器设备有限公司;洁净工作台:SW-CJ-1FD;高压灭菌锅:MJ-78A,施都凯仪器设备(上海)有限公司;离心机:A14,Sartorius公司;液相色谱:LC-20A,岛津公司;数字酸度计:PP-25-P11,Sartorius公司;快速水分测定仪:MS-70,AND公司;恒温水浴锅:BWS-10,上海一恒科学仪器有限公司;数显电动搅拌器:WB3000-D,维根技术(北京)有限公司。
1.2 实验方法
1.2.1 液化
以料水质量比1∶2将玉米与水混合,调节pH=5.0~5.5,加入30 U/g玉米粉的液化酶,90℃液化120 min,期间不断搅拌,制备得到玉米液化醪。
1.3.2 酵母活化
称量0.3 g安琪超级酿酒高活性干酵母,加入装有100 mL无菌水的三角瓶中,在32 ℃,180 r/min的摇床中活化60 min。
1.3.3 同步糖化发酵
将玉米液化醪快速降温至33 ℃,加入适量的糖化酶、酸性蛋白酶、尿素、1%的酵母活化液,在转速180 r/min,温度33 ℃的条件下开始发酵。
1.3 分析方法
1.3.1ρ(乙醇)和ρ(葡萄糖)测定
取发酵液样品1.5 mL加入2.0 mL离心管中,在12 000 r/min下离心3 min,取上清液稀释10倍,然后用0.22 μm的水系滤膜过滤,用液相色谱仪(检测器:示差折光检测器;流速:0.6 mL/min;流动相:0.005 mol/L硫酸;柱温:55 ℃)测定发酵液中乙醇浓度和葡萄糖浓度,按公式(1)计算样品中乙醇体积分数,按公式(2)计算样品中葡萄糖的浓度。
ρ(乙醇)=测定值×稀释倍数/100
(1)
ρ(葡萄糖)=测定值×稀释倍数/100
(2)
1.3.2 固含量测定
糖化醪固含量的测定参照GB/T2793—1995,干燥温度为105 ℃。
1.4 实验设计
该实验以发酵成熟醪ρ(乙醇)为参考指标,主要对玉米乙醇发酵的4个重要外部因素,即糖化酶添加量、尿素添加量、酸性蛋白酶添加量、发酵液初始pH值进行研究。利用正交表L9(34),设计4因素3水平的正交实验(见表1),根据正交实验结果确定最佳发酵工艺条件。
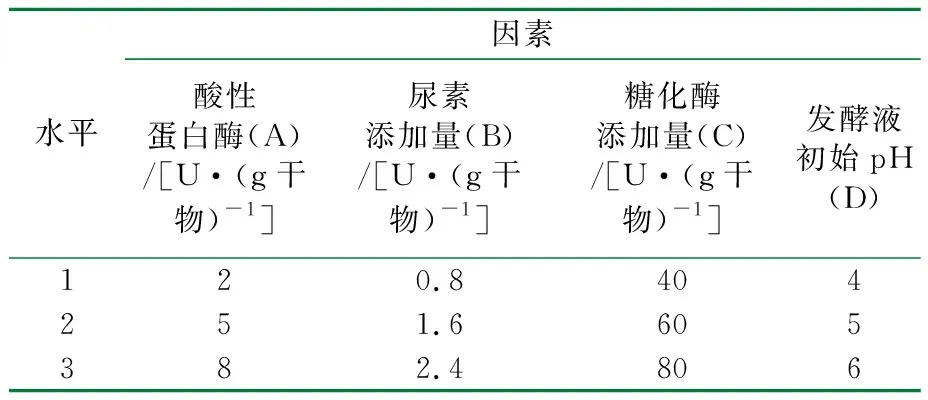
表1 正交实验设计
2 结果与讨论
2.1 酸性蛋白酶添加量的确定
在通常发酵中,酵母菌不能直接利用淀粉质原料中的蛋白质,加入酸性蛋白酶后,其水解作用可增加发酵醪液中可被酵母利用的有机氮的浓度,促进酵母生长繁殖,提高酒精产率[6]。在尿素添加量为1.0 g/kg干物、糖化酶添加量为50 U/g干物、发酵液初始pH=5.5(自然)的条件下,对不同酸性蛋白酶添加量进行研究。结果见图1。
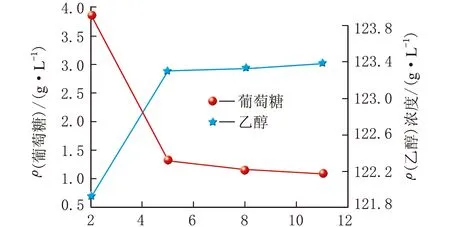
酸性蛋白酶添加量/(U/g干物)图1 蛋白酶加量对成熟醪ρ(乙醇)和ρ(葡萄糖)的影响
由图1可知,发酵成熟醪中ρ(乙醇)随着酸性蛋白酶添加量的增大而增大,残余ρ(葡萄糖)随着酸性蛋白酶添加量的增大逐渐下降,当酸性蛋白酶添加量大于5 U/g干物时,ρ(乙醇)增长缓慢,考虑到酸性蛋白酶的价格及经济因素,确定最佳的酸性蛋白酶添加量为5 U/g干物。
2.2 尿素添加量的确定
在酒精生产中,氮源是构成菌体物质和一些代谢产物的必需营养元素,一般氮源分为无机氮源和有机氮源两类[7]。尿素作为最常用的一种无机氮源,具有高效、廉价易得等优点而广泛应用于燃料乙醇生产中,成为酒精发酵生产中补充氮源的首选[8]。在酸性蛋白酶添加量为5 U/g干物、糖化酶添加量为50 U/g干物、发酵液初始pH=5.5(自然)的条件下,对不同尿素添加量进行研究。结果见图2。
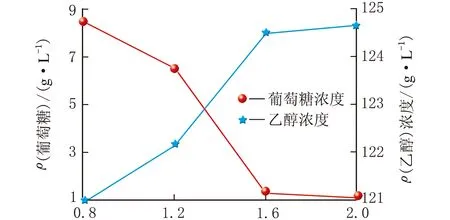
尿素添加量/[g·(kg干物)-1]图2 尿素添加量对成熟醪乙醇浓度和葡萄糖浓度的影响
由图2可知,发酵成熟醪中ρ(乙醇)随着尿素添加量的增大而增大,残余ρ(葡萄糖)随着尿素添加量的增大而逐渐下降,当尿素添加量为1.6 g/kg干物时,ρ(乙醇)达到最大,相应的残余ρ(葡萄糖)达到最低,继续增加尿素的添加量,发酵成熟醪中ρ(乙醇)上升不明显,因此确定最佳的尿素添加量为1.6 g/kg干物。
2.3 糖化酶添加量的确定
在淀粉质原料燃料乙醇生产过程中,淀粉通过蒸煮后,逐步从颗粒状态的淀粉变成溶解状态的糊精,该糊精不能被酵母菌直接利用,必须添加糖化酶,把液化后的短链淀粉和糊精彻底水解为葡萄糖,因此糖化酶添加量是影响高浓乙醇发酵的一个重要因素[9]。在酸性蛋白酶添加量为5 U/g干物、尿素添加量为1.6 g/kg干物、发酵液初始pH=5.5(自然)的条件下,对不同糖化酶添加量进行研究。结果见图3。

糖化酶添加量//[g·(kg干物)-1]图3 糖化酶添加量对成熟醪乙醇浓度和葡萄糖浓度的影响
由图3可知,发酵成熟醪中ρ(乙醇)随着糖化酶添加量的增大而增大,相应残余ρ(葡萄糖)随着糖化酶添加量的增大逐渐下降,当糖化酶添加量大于60 U/g干物时,发酵成熟醪中ρ(乙醇)增长趋缓,因此确定最佳的糖化酶添加量为60 U/g干物。
2.4 发酵液初始pH值的确定
发酵液pH值是酵母菌生长最重要的外部条件之一,其对酵母的生长有显著影响,发酵液pH值主要通过抑制或激活细胞中某些酶的活性,使酵母细胞的代谢途径及细胞膜的渗透性发生改变,从而影响酵母营养吸收及代谢产物的分泌[10]。在酸性蛋白酶加量为5 U/g干物、糖化酶加量为60 U/g干物、尿素加量为1.6 g/kg干物的条件下,对不同发酵液初始pH进行研究。结果见图4。
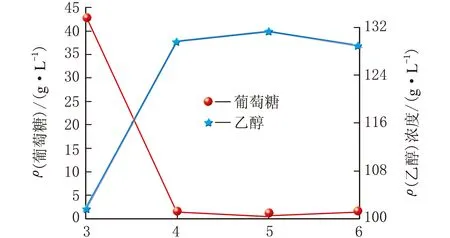
pH图4 发酵液初始pH对成熟醪ρ(乙醇)和ρ(葡萄糖)的影响
由图4可知,发酵成熟醪中ρ(乙醇)随着发酵液初始pH值的增大而增大,相应的残余ρ(葡萄糖)逐渐下降,当发酵液初始pH=5时,乙醇浓度达到最大,相应残余葡萄糖浓度达到最低值,继续增大发酵液初始pH,发酵成熟醪中乙醇浓度有所下降,因此确定较佳的发酵液初始pH为5。
2.5 正交优化玉米乙醇发酵工艺结果与分析
根据正交实验设计对9种条件下发酵成熟醪进行测定,结果见表2。
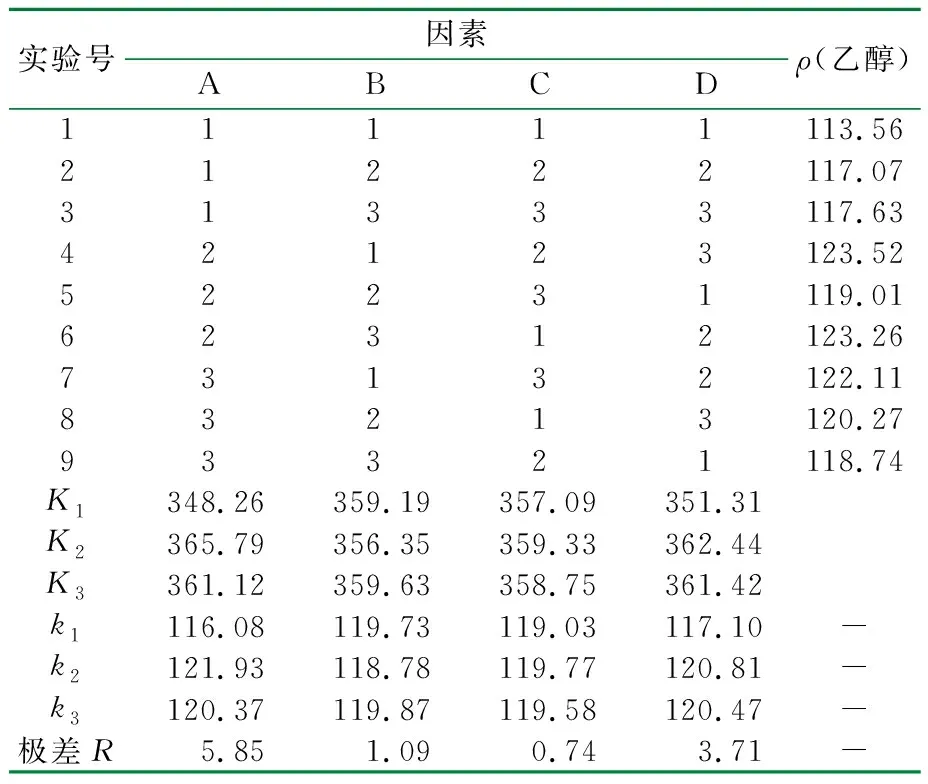
表2 正交实验结果及分析
从发酵成熟醪乙醇浓度和各因素极差(R)值可知,实验因素A(酸性蛋白酶添加量)的R值最大,为5.85,说明酸性蛋白酶添加量对发酵成熟醪ρ(乙醇)的影响最大;其次是D(发酵液初始pH),为3.71;再次是B(尿素添加量),为1.09;最后是B(糖化酶添加量),为0.74;即各因素对发酵成熟醪乙醇浓度的影响程度从高到低依次为酸性蛋白酶添加量>发酵液初始pH值>尿素添加量>糖化酶添加量。
2.2 验证性实验
为验证高浓玉米燃料乙醇发酵的稳定性,按最佳工艺条件A2B3C2D2,即酸性蛋白酶添加量为5 U/g干物,尿素添加量为2.4 g/kg干物,糖化酶添加量为60 U/g干物,发酵液初始pH=5.0,于33 ℃发酵72 h,得到发酵成熟醪,实验重复3次取平均。由表3可知,在该工艺条件下,发酵成熟醪ρ(乙醇)=136.34 g/L,残余ρ(葡萄糖)=0.35 g/L,在此条件下高浓玉米燃料乙醇发酵具有较好的稳定性。
3 结 论
正交实验结果表明,影响高浓玉米燃料乙醇发酵因素的顺序为酸性蛋白酶添加量>发酵液初始pH值>尿素添加量>糖化酶添加量,最佳发酵工艺条件为酸性蛋白酶添加量为5 U/g干物,尿素添加量为2.4 g/kg干物,糖化酶添加量为60 U/g干物,发酵液初始pH=5。在以上最佳工艺条件下,72 h发酵成熟醪中ρ(乙醇)=136.34 g/L,ρ(葡萄糖)=0.35 g/L。

