甜菜碱三元复配乳化降黏实验研究
孟令治,吴玉国,李小玲
(辽宁石油化工大学 石油天然气工程学院,辽宁 抚顺 113001)
石油是工业发展不可或缺的能源和材料[1],我国稠油储量高,但稠油黏度高,开采运输利用难度大,稠油乳化降黏得到了广泛关注[2-6]。目前由于两性表面活性剂种类较多,亲水端结构复杂,对两性表面活性剂和不同表面活性剂的协同作用和不同亲水亲油端的协同作用机理研究较少。基于此,本文筛选出两性表面活性剂LAB-35作为主剂,从降黏率和稳定性的角度,研究具有不同亲水或亲油结构的表面活性剂与LAB-35复配对乳化效果的影响,分析协同机理,并研究二元体系与有机碱的协同作用,确定最优三元复配方案。
1 实验部分
1.1 材料与仪器
实验用油,取自辽河某区块稠油,25 ℃表观黏度2 908.44 mPa·a;表面活性剂见表1。
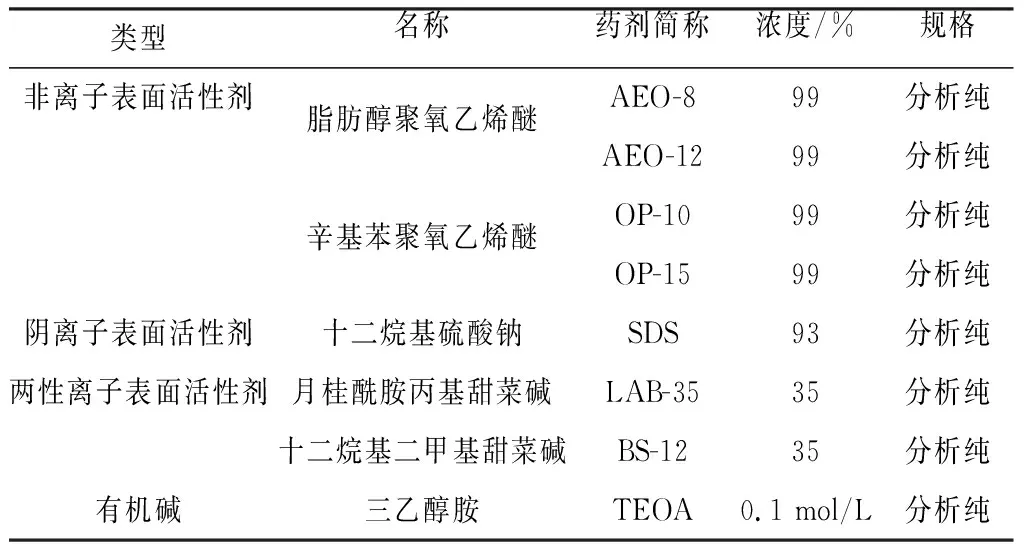
表1 实验用试剂Table 1 Experimental reagent
HH-S2数显恒温水浴锅;DV-T2型数字黏度仪;HJ-5数显恒温多功能搅拌器;HDR流变仪。
1.2 实验方法
1.2.1 稠油乳状液配制 将稠油与不同质量分数及复配比例的表面活性剂溶液按油水比7∶3的质量比混合,在25 ℃的水浴温度下恒温30 min,将油水混合物以400 r/min的转速搅拌乳化10 min。
1.2.2 稳定性 将乳状液倒入50 mL的比色管中,设置水浴温度为25 ℃,每30 min测量一次分离出的水柱高度,测量直到3 h。乳状液静置24 h后,测量分出的水柱高度,最后计算乳状液的分水率。
Ψ=(V1/V2)×100%=(h1/h2)×100%
(1)
式中Ψ——分水率,%;
V1、V2——分别为析出水体积、总体积,mL;
h1、h2——分别为析出水高度、全部水高度,cm。
1.2.3 黏度测量 将乳状液加入数字黏度仪套筒,设置好水浴温度和黏度计的转子和转速,使扭矩维持在50%,开始测量黏度。
δ=[(η0-ηe)/η0]×100%
(2)
式中δ——降黏率,%;
η0——稠油的黏度,mPa·s;
ηe——乳状液的黏度,mPa·s。
2 结果与讨论
2.1 表面活性剂类型对乳化效果的影响
选取8种表面活性剂,分别配制质量分数为1%的水溶液,对油样进行乳化,生成的乳状液黏度和降黏率见表2。

表2 不同表面活性剂对乳状液黏度和降黏率的影响Table 2 Effects of different surfactants on viscosity and viscosity reduction of emulsion
由表2可知,AEO-8、AEO-12、BS-12、SDBS无法生成水包油乳液,OP-10和OP-15形成的乳状液的黏度为107.5 mPa·s和102.5 mPa·s,SDS和LAB-35形成的乳状液的黏度分别为100.4 mPa·s和96 mPa·s。在非离子表面活性剂中,OP系列的表面活性剂,亲油端较短,且含有苯环结构,AEO和OP具有不同的亲油基团,导致不同的亲水亲油平衡值,使乳化效果不同[7]。阴离子表面活性剂SDS在油水界面结合时,亲水端的硫酸盐与水结合,生成氢键,同时使界面带负电荷,界面内的SDS分子因为电荷排斥导致界面膜强度变低。两性离子表面活性剂LAB-35聚结在油水界面上,亲水端带有正电荷和负电荷,界面内相邻分子间产生静电引力,表面活性剂分子在油水界面上排列更为紧密。
月桂酰胺丙基甜菜碱LAB-35分子中的亲油基团是十二烷基,亲水基团中有酰胺基、带正电荷的季胺基、带负电荷的羧基,其中羧基和季胺基亲水性能较强,易溶解在水中。酰胺基团能通过分子间氢键的相互作用,使界面上的表面活性剂分子排布更紧密,增强界面膜的稳定性,因此,在几种表面活性剂中选择LAB-35作为实验的表面活性剂主剂。
2.2 LAB-35质量分数对乳化效果影响
将LAB-35质量分数设置为1%~4%,分析LAB-35浓度对稠油乳化效果的影响,实验结果见图1、图2。
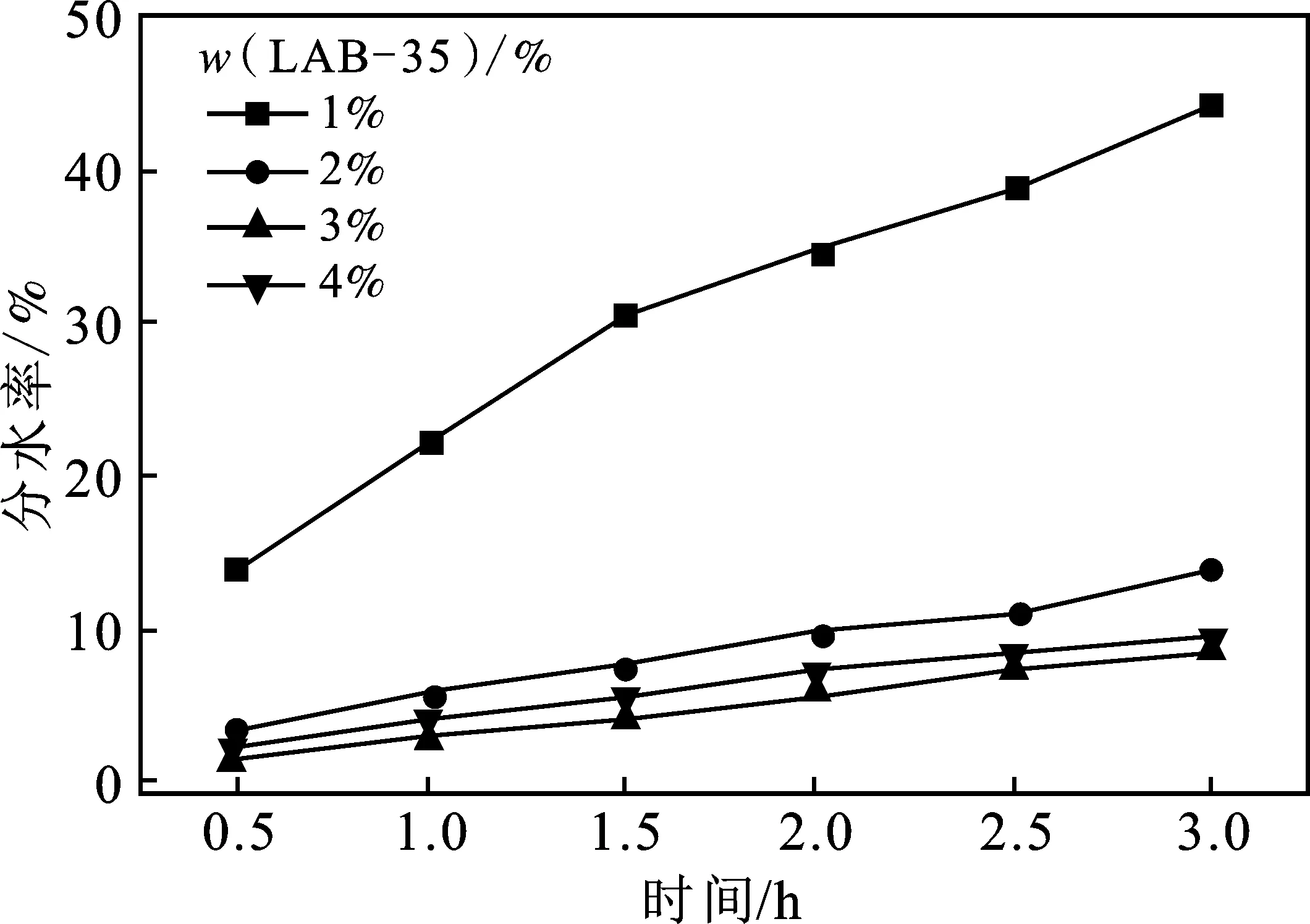
图1 LAB-35质量分数对乳状液分水率的影响Fig.1 Effect of LAB-35 mass fraction on water separationrate viscosity of emulsion
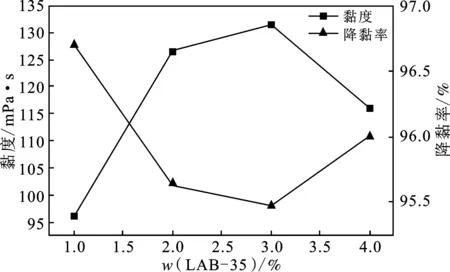
图2 LAB-35质量分数对乳状液黏度、降黏率的影响Fig.2 Effects of LAB-35 mass fraction on viscosityand viscosity reduction of emulsion
由图1、图2可知,随着表面活性剂LAB-35浓度的提升,乳状液黏度先快速升高后逐渐升高,浓度>3%后,黏度有所降低。乳状液黏度最低为 96 mPa·s,最高达到131.6 mPa·s。乳状液3 h的分水率随LAB-35的浓度提高先快速降低后逐渐趋于稳定,LAB-35浓度为1%时乳状液的3 h分水率为44.4%。LAB-35浓度达到3%时,分水率降低至8.3%,进一步提高浓度,乳状液分水率略微提高,但相差不大。
LAB-35表面活性剂浓度为1%时,活性物质浓度较低,降低界面张力的能力较弱,乳化效果较差,生成的乳状液油滴粒径较大且分布不均匀,油滴间距离较大,聚结在油水界面的活性分子较少,不足以稳定油水界面,因此乳化后黏度较低,分水率较高。随LAB-35浓度增加,降低界面张力的效果加强,液滴粒径变小,且分布更均匀,因此黏度稍有升高[8],同时聚结在油水界面的LAB-35分子增多,能够稳定更大的油水界面,稳定性大幅度提升。继续增加LAB-35浓度,会促使更多的LAB-35分子在疏水作用下形成胶束,不利于LAB-35的吸附[9],因此降低界面张力效果较差,液滴粒径变大,且分布不均匀,油滴间距离较大,因此黏度较低;与此同时,胶束对连续水相有增稠作用,导致乳状液的分水率略微增高,黏度降低。
2.3 不同表面活性剂与LAB-35协同作用
LAB-35单剂乳化效果有限,且表面活性剂乳化形成的油水界面膜,主要由其亲水亲油基团排列组成。为增强乳化效果和探究具有不同亲水亲油结构的表面活性剂与LAB-35的复配效果和机理,在保持亲油基团相同的基础上,选择非离子表面活性剂,亲水基团聚氧乙烯醚数量不同的AEO-8、AEO-12、阴离子表面活性剂亲水基团为磺酸钠的SDS和两性离子表面活性剂,亲水基团为季胺基和羧基的BS-12和选择与AEO系列表面活性剂具有相似亲水基团,但亲油端不同的OP系列表面活性剂进行实验。
保持表面活性剂3%的总质量浓度,将质量分数2.5%的LAB-35与质量分数0.5%的其余类型表面活性剂复配乳化,将乳状液放入黏度计转筒持续剪切,每隔2 min记录1次黏度。
2.3.1 AEO-8、AEO-12与LAB-35复配 由图3、图4可知,AEO-8、AEO-12与LAB-35复配形成的乳状液的3 h的分水率分别为33.9%,45.3%,初始黏度分别为120.9,111.2 mPa·s,随时间变化,逐渐增加到200.5,235 mPa·s,AEO-8、AEO-12与LAB-35复配乳化的乳状液的分水率高于LAB-35单剂乳化的乳状液,其中AEO-8的稳定性高于AEO-12的。

图3 AEO表面活性剂与LAB-35复配对乳状液分水率的影响Fig.3 Effects of AEO surfactant and LAB-35 on waterfraction of emulsion
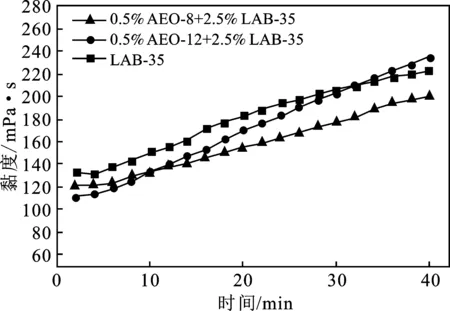
图4 AEO表面活性剂与LAB-35复配对乳状液黏度的影响Fig.4 Effects of AEO surfactant and LAB-35 onviscosity of emulsion
原因是:①AEO系列非离子表面活性剂由脂肪醇和环氧乙烷合成[10],其亲水端聚氧乙烯醚与水分子结合生成氢键,结合在油水界面,降低界面张力,构成油水界面膜稳定乳状液;②因为油水界面的面积有限,局部缺少用于与表面活性剂分子结合形成氢键的结合水,且几种非离子表面活性剂亲水聚氧乙烯基数量相比LAB-35较多,亲水基团较宽,会占据更大的油水界面,LAB-35分子穿插在非离子表面活性剂中。在油水界面结合的LAB-35分子数量大幅降低,同时作为助剂的AEO表面活性剂浓度较低,导致形成界面膜的活性分子较少,分水率较高[11];③在两种AEO类型的表面活性剂中,AEO-8到AEO-12亲水基团由少到多。两种复配体系的亲油基团均是十二烷基的基础下,聚氧乙烯基多的复配体系分水率更高。因为聚氧乙烯基更多的非离子表面活性剂与LAB-35复配时占据的界面空间更多,在与水分子形成氢键时,与主剂的竞争更大,导致聚结在界面上的活性分子更少,因而乳化效果更差,分水率更高。
以上因素导致,AEO-12与LAB-35复配乳化的乳状液,在持续剪切的过程中,界面膜逐渐破裂,黏度随时间升高,最终黏度超过LAB-35单剂配制的乳状液。AEO-8与LAB-35复配体系乳化机理相同,但因为其亲水端聚氧乙烯基数目更小,稳定性相对较好,因此黏度随时间虽然不断升高但最终低于AEO-12与LAB-35二元体系的乳状液。
2.3.2 OP-10、OP-15与LAB-35复配 由图5、图6可知,OP-10、OP-15与LAB-35复配形成的乳状液的3 h分水率分别为18.7%,30.6%,初始黏度分别为145.8,96.2 mPa·s,随时间变化逐渐增加到195,202.5 mPa·s。非离子表面活性剂OP-10、OP-15复配体系形成的乳状液的分水率高于LAB-35单剂配制的乳状液,其中OP-10复配体系形成的乳状液的稳定性高于OP-15的。
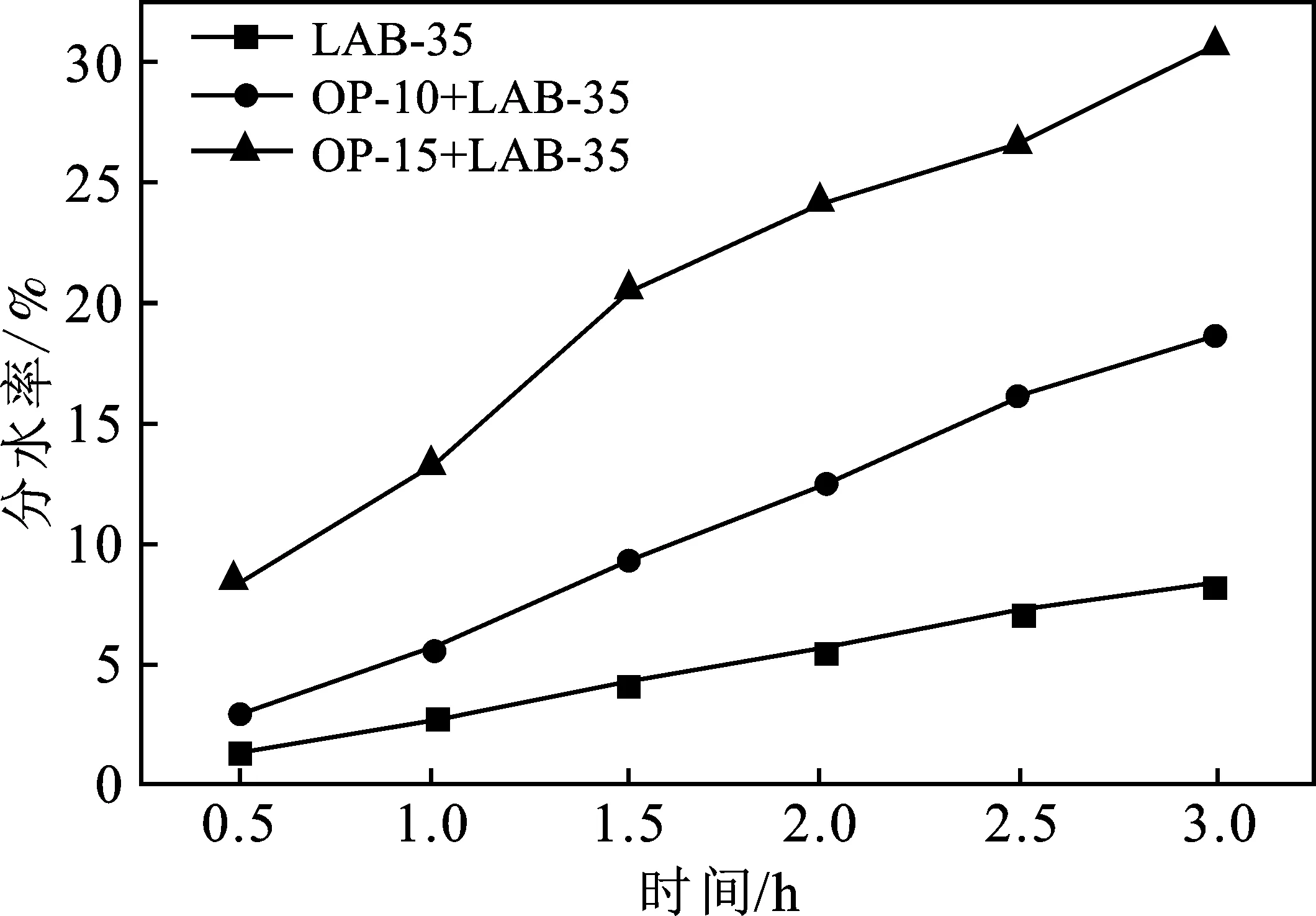
图5 OP表面活性剂与LAB-35复配对乳状液分水率的影响Fig.5 Effect of the compound of OP surfactant and LAB-35on water fraction of emulsion
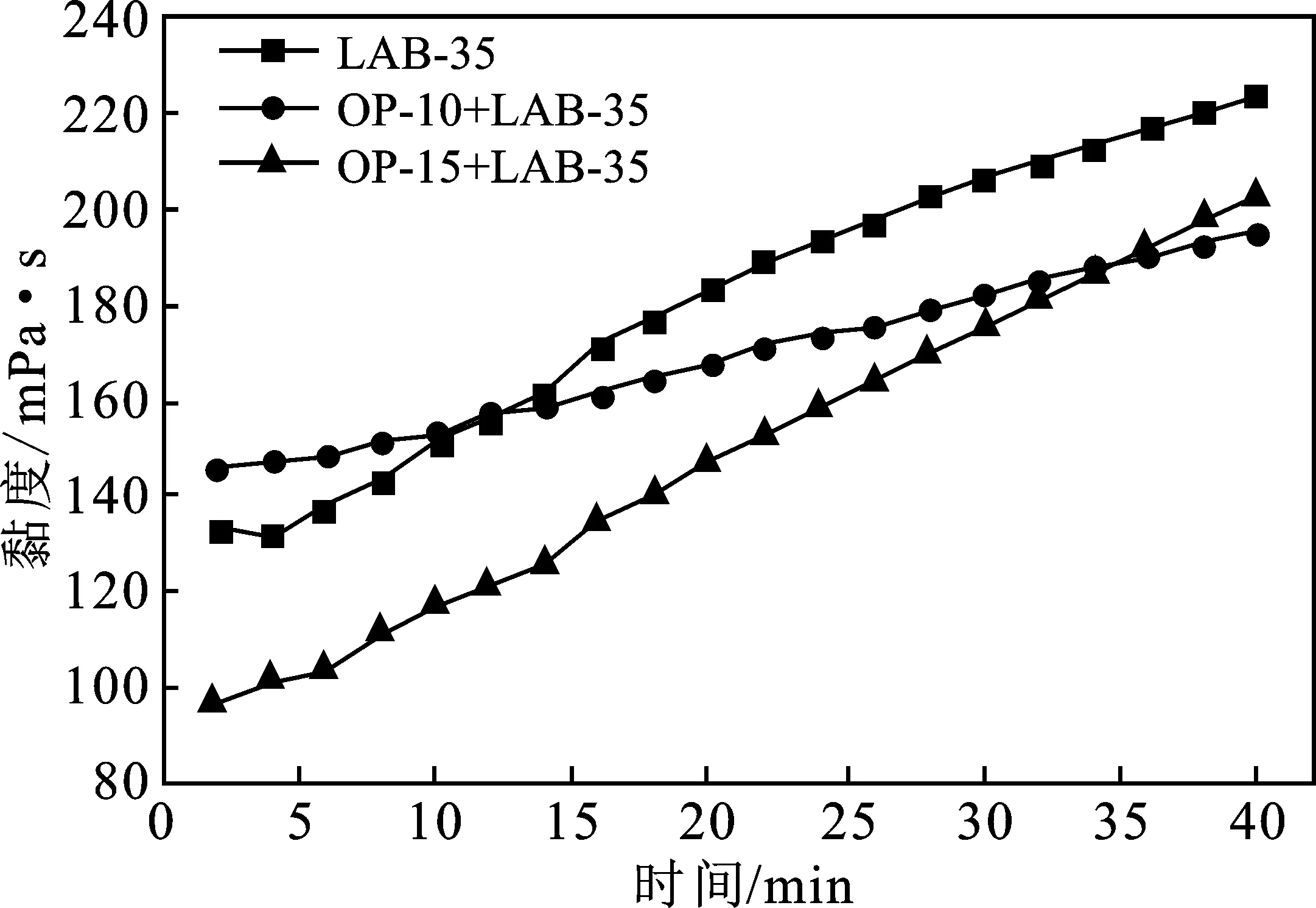
图6 OP表面活性剂与LAB-35复配对乳状液黏度的影响Fig.6 Influence of the compound of OP surfactantand LAB-35 on viscosity of emulsion
相比于AEO系列,OP系列的非离子表面活性剂对实验油样适配更好,但由于同样具有数目较多的亲水端,与LAB-35在油水界面产生竞争,在OP-10和OP-15用量较小的情况下,导致在油水界面上吸附的表面活性剂分子较少,因此相比于LAB-35单剂配制的乳状液稳定性较低,且亲水端数目少的OP-10与LAB-35复配乳化的乳状液的稳定性要大幅度强于OP-15与LAB-35复配体系形成的乳状液。
以上因素导致,OP-10、OP-15与LAB-35复配体系形成的乳状液稳定性较差,在持续剪切下,油水界面膜不断破碎,黏度随时间不断升高,但OP-10的亲水端与OP-15的相比较小,与LAB-35的竞争吸附更小,因此尽管OP-10二元体系形成的乳状液初始黏度高于OP-15的,但最终OP-15与LAB-35二元体系形成的乳状液黏度超过OP-10与LAB-35二元体系的乳状液。
2.3.3 SDS、BS-12与LAB-35复配 由图7、图8可知,SDS、BS-12与LAB-35复配形成的乳状液的 3 h 分水率分别为4.8%,10.1%,初始黏度分别为173.3,135.8 mPa·s,随时间变化逐渐增加到 190.0,182.0 mPa·s。SDS与LAB-35复配形成的乳状液分水率有一定降低,BS-12的与LAB-35的相比稍微提高,SDS、BS-12复配乳化形成的乳状液,初始黏度均高于LAB-35单剂的。随时间变化,SDS复配形成的乳状液黏度稍有提高,较为稳定,BS-12和LAB-35的黏度均有升高。最终,SDS与BS-12复配形成的乳状液黏度均低于LAB-35单剂的。
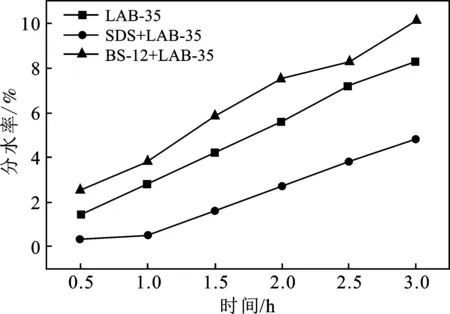
图7 SDS、BS-12表面活性剂与LAB-35复配对乳状液分水率的影响Fig.7 Effects of SDS,BS-12 surfactant and LAB-35 onwater fraction of emulsion
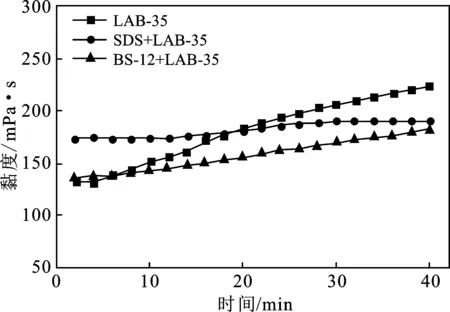
图8 SDS、BS-12表面活性剂与LAB-35复配对乳状液黏度的影响Fig.8 Effects of SDS,BS-12 surfactant and LAB-35on viscosity of emulsion
由上可知,在几种复配体系中阴离子表面活性剂SDS作为助剂效果最佳,SDS的亲水基团为单一的硫酸钠,SDS的金属钠阳离子溶于水后,亲水基团硫酸根离子与游离水结合生成氢键,与LAB的酰胺基和季胺基相互吸引,羧基排斥,季胺基与羧基相比更为靠近水相,一方面与LAB-35分子结合紧密,增大界面膜强度,聚集在油水界面的活性分子变多[12]。一方面阴离子与阳离子结合降低油滴界面间电势差,减弱油滴间的静电排斥力。以上原因导致乳状液的分水率降低。
BS-12作为两性离子表面活性剂,亲水基团为阳离子季胺基和阴离子羧基,整体结构与LAB-35结构相近,保持总表面活性浓度不变复配后,分水率略有提高,但总体变化不大。
以上因素导致SDS和LAB-35二元复配体系形成的乳状液稳定性较强,在持续剪切下黏度表现稳定,BS-12二元复配体系黏度变化与LAB-35相似。
2.4 SDS质量分数对乳化效果的影响
经过对二元复配体系的研究,SDS与LAB-35协同作用最强,将SDS与LAB-35复配并研究最优配比。实验保持表面活性剂质量分数为3%的总浓度不变,将SDS的质量分数设置为0.1%~0.9%,与LAB-35复配,并测量黏度、计算分水率,结果见 图9、图10。
由图9、图10可知,乳状液黏度随SDS的加量提高而提高,直到浓度为0.7%,此时黏度为 178.7 mPa·s,而后黏度随浓度提高略有降低。分水率随SDS浓度提高而降低,在SDS浓度为0.7%时达到最小值2.9%,随后分水率提高。
随SDS浓度提高,在界面膜中阴离子表面活性剂占比逐渐提高,SDS的阴离子亲水基团与LAB-35的阳离子基团相互吸引结合,形成排列更紧密的界面膜,同时界面膜间的静电斥力减弱,两种作用下分水率逐渐降低。当SDS浓度达到0.7%时,两种表面活性剂协同作用最强,形成的界面膜最紧密,界面张力值也最低[13]。继续增加SDS,此时阴离子表面活性剂浓度较高,由于SDS分子间存在静电排斥,使SDS分子间距变大,且阴离子表面活性剂相较于两性离子表面活性剂亲水基团较短,稳定界面能力较低[14],导致随SDS继续增加分水率提高。
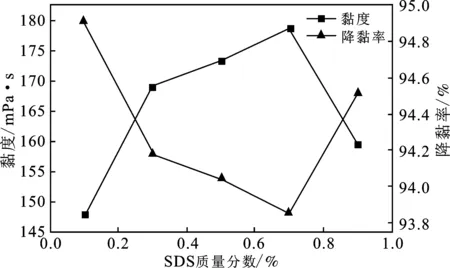
图9 SDS浓度对乳状液黏度和降黏率的影响Fig.9 Effect of SDS concentration on viscosity andviscosity reduction of emulsion
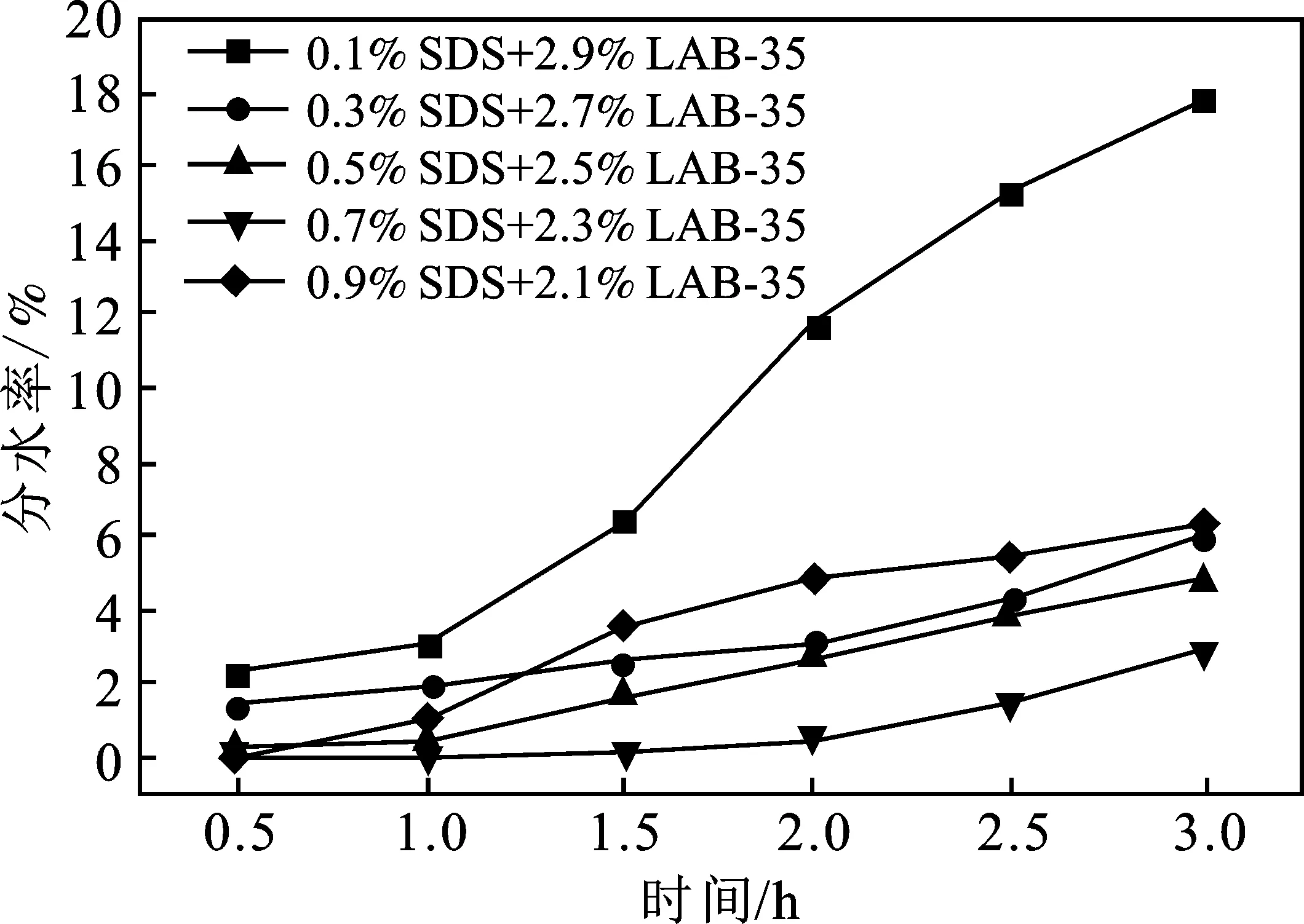
图10 SDS浓度对乳状液分水率的影响Fig.10 Influence of SDS concentration onwater fraction of emulsion
随SDS浓度的提高,阴离子表面活性剂穿插在LAB-35分子之间,降低界面张力效果增加,乳化后的溶液,油滴粒径更小,分布更均匀,油滴界面膜增厚,同时连续水相黏度增高,导致在这一阶段乳状液黏度升高。浓度达到0.7%后,随SDS浓度进一步增大,作为主剂的LAB-35数量减少,降低界面张力效果变差,同时界面间静电斥力增加,表现为乳状液的黏度降低。
2.5 TEOA质量分数对乳化效果的影响
表面活性剂与碱协同使用能提高乳化效果。相比于无机碱,有机碱具有一定的油溶性,能结合在油水界面,并且对管道腐蚀作用较小。因此,选取小分子的有机碱三乙醇胺(TEOA)与二元体系复配。向二元体系中加入质量分数为0.1%~0.4%的TEOA,配制乳状液,并测量黏度,计算分水率,结果见表3。

表3 TEOA质量分数对乳状液黏度、降黏率和分水率的影响Table 3 Effects of TEOA mass fraction on viscosity,viscosity reduction and water fraction of emulsion
由表3可知,乳状液黏度先随乙醇胺的加量提高而降低,直到浓度为0.2%,此时黏度为 157.5 mPa·s,而后黏度随浓度提高略有增高。分水率随乙醇胺浓度提高而逐渐降低,24 h分水率最低达到13.7%。
TEOA质量分数较低时,与稠油中的酸性物质反应生成的石油酸盐较少,使得乳状液黏度较高。TEOA质量分数提高到0.2%时,TEOA基本与稠油中的石油酸反应完全,乳状液黏度降到最低。随TEOA质量分数继续提高,没有过多的石油酸与其反应,多余的TEOA分子结合在油水界面,增大连续水相的黏度。有机碱TEOA能与石油中的酸性物质反应,生成阴离子表面活性物质石油酸盐[15],吸附在油水界面上,使界面膜加厚,分水率逐渐降低。其次,三乙醇胺作为小分子有机碱,同样能够吸附在油水界面上,降低界面张力[16],提高乳状液稳定性。以上两种作用结合,导致随着TEOA质量分数提高,乳状液稳定性逐渐提高。
综上所述,对辽河稠油最优复配体系为:2.3%LAB-35+0.7%SDS+0.2%TEOA,最优复配体系降黏率为94.6%,3 h分水率1.9%,24 h分水率16.7%。
3 结论
(1)LAB-35单剂使用浓度为3%时,稳定性最好,黏度131.6 mPa·s,降黏率达到95.47%,3 h的分水率8.3%,继续提高浓度,效果不明显,且分水率提高。
(2)浓度较低的聚氧乙烯醚非离子表面活性剂与LAB-35复配时,聚氧乙烯基数量多的表面活性剂与LAB-35存在竞争吸附,聚氧乙烯基数量较低的稳定性更高,可以选用聚氧乙烯基数量更少的非离子表面活性剂复配。LAB-35与SDS亲水端有互补作用,SDS的阴离子硫酸根与LAB-35的季胺基结合,形成致密的界面膜,稳定性大幅度提高,SDS浓度为0.7%时,降黏率达到93.85%,3 h的分水率2.9%。
(3)LAB-35与SDS二元体系与有机碱TEOA具有一定协同作用,随TEOA浓度提高,分水率进一步降低。
(4)辽河稠油降黏剂最优方案为2.3%LAB-35+0.7%SDS+0.2%TEOA,最优浓度下降黏率达到 94.6%,3 h分水率1.9%,24 h分水率16.7%。

