类风湿血管炎性周围神经病3例临床特点分析并文献复习
文春蓓,杨 洁,罗利俊,魏东生
类风湿血管炎(rheumatoid vasculitis,RV)是类风湿关节炎(rheumatoid arthritis,RA)的一种关节外表现,主要影响中小型血管,临床具有高度异质性,可表现为广泛的器官受累,预后不良[1]。其中,以累及周围神经为主的类风湿血管炎性周围神经病,为临床主要表型之一,部分患者病程可能很严重,并伴有其他关节外表现,包括皮肤溃疡和肢端坏疽等[2]。由于临床医生对此病认识不足,致其诊断不明。现报道我科于2020年10月-2021年10月收治的3例类风湿血管炎性周围神经病患者的病史资料、实验室检查及肌电图结果,并进行临床特点分析。
1 资料与方法
1.1 临床资料 例1,女,64岁,因“双下肢酸胀麻木15 m,无力1 w”于2020年10月4日入院。入院15 m前,患者无明显诱因出现双下肢小腿酸胀不适,入院1 w前出现左侧臀部及左下肢酸胀麻木,次日出现右侧臀部及右下肢酸胀麻木,伴双足疼痛无力,足下垂,不能行走。2 m前因腹痛于外院就诊,未明确诊断。既往有类风湿性关节炎病史近10 y,仅间断应用洛索洛芬对症治疗。有高血压、糖尿病史2 y。查体:双腕及膝关节肿胀变形,双小腿中下1/3及双足痛觉过敏,膝关节以下关节震动觉减弱或消失,双下肢肌力近端4级,远端1级,背屈、跖屈不能,踝反射消失,双侧Lasegue(+)。辅助检查:Rf 1680 KIU/L,A-CCP<7.00 U/ml。抗ANA抗体:阳性(1∶320~1∶1000)。WBC、NE%↑,ESR 77 mm/H↑。CRP正常,TP、ALB稍↓,补体C3、C4正常,大便OB(+)。四肢肌电图:下肢运动及感觉神经(左右腓浅、腓肠神经、左侧隐神经)CMAP/SNAP波幅未引出,右侧隐神经波幅降低,多发性单神经病变可考虑。
例2,女,56岁,因“右上肢疼痛伴右手无力1 m,加重3 d”于2021年6月29日入院。患者1 m前无明显诱因出现右侧颈肩胛部、上臂外侧三角肌处疼痛不适,右手小指活动不灵活,伸指无力。3 d前右手无名指、小指活动受限加重,不能背伸。既往有类风湿性关节炎病史20 y,长期口服甲氨蝶呤10 mg qw、来氟米特10 mg qn、甲泼尼龙2/4 mg交替及辅助予以白芍总苷、骨化三醇治疗。查体:双手近端指间关节肿胀,四肢肌力5级,右手小指、无名指背伸力弱,分指、并指不能,右小指尺侧及以下浅感觉减退,余感觉、运动功能均正常。辅助检查:Rf 42.10 KIU/L↑,A-CCP 255 U/ml↑。抗ANA抗体:阳性(1∶100),TP、ALB、GLO稍↓,SAA 15.5 mg/L↑,CRP、ESR正常范围,补体C3 0.52 g/L↓,C4正常范围,血常规提示三系减低,双侧臂丛神经及颈椎MRI未见异常(见图1)。四肢肌电图:右侧桡神经、左侧隐神经损害肌电改变,多发性单神经损害可考虑。
例3,女,55岁,因“右足麻木不适4 m,左足疼痛12 d”于2021年9月24日入院。患者4 m前无明显诱因出现右足底麻木不适,12 d前突发左足底麻木,后出现左足底疼痛,不能耐受。既往有类风湿性关节炎病史30 y,长期口服中药治疗,1 y前改为口服甲氨蝶呤10 mg qw、强地松10 mg qd以及双氯芬酸钠片1片Bid。查体:双手梭形改变,四肢肌力5级,右足底痛觉减退,左足底痛觉过敏,共济、深浅反射均正常。辅助检查:Rf 1350.10 KIU/L↑,A-CCP 166 U/ml↑。抗ANA抗体:阳性(1∶1000~1∶320),TP、ALB↓,补体C3、C4稍↓,ESR 58 mm/H↑、CRP 15.8 U/ml↑。四肢肌电图:多发性周围神经损害(左右胫、腓总神经CMAP/SNAP波幅均降低,双侧足底内侧神经SNAP波幅未引出)肌电改变,下肢运动和感觉神经轴索损害可考虑。
1.2 实验室检查 3例患者均行血常规、ESR、CRP、VitB6、B12、糖化血红蛋白、肝肾功能、甲状腺功能、血免疫固定电泳、尿常规、尿蛋白电泳、尿游离轻链k、λ值、肿瘤标志物、抗自身抗体、ANCA、RF、A-CCP、补体C3、C4、传染病全套、心电图、心脏彩超、头部MRI+MRA、胸部CT、肝胆脾胰双肾、颈部及双下肢血管彩超检查。3例均行脑脊液穿刺,送检常规、生化、结核、免疫全套检测。
1.3 肌电图检查 3例患者均行针极肌电图及神经传导检查,全面检查包括四肢感觉、运动神经在内的多根神经。在运动传导方面,评估了远端潜伏期、传导速度、波幅、F波和H波;在感觉传导方面,评估了远端潜伏期、传导速度和波幅。
2 结 果
2.1 临床特点 本组3例患者均为女性,年龄55~64岁,平均60岁,3例均有较长的类风湿性关节炎病史,确诊至发病的平均时间间隔为20 y;例1首发症状为足下垂,痛觉过敏,例2为小指背伸无力、感觉减退,例3为足底麻木及疼痛,查体发现:病变肢体肌张力减退,肌力Ⅲ~Ⅳ级,膝腱反射、肱二头肌肌腱反射减退或消失,痛温觉减退或过敏,3例均出现不同程度多根周围神经损害表现,主要以肢体麻木、疼痛、肌无力等原因就诊,查体可见下运动神经元损害体征;例1,12 m前起病,1 w内加重,例2,1 m前起病,3 d内加重,例3,4 m前起病,1 w内加重,3例患者均有隐匿性起病,短期内快速进展的发病特点。
2.2 辅助检查 2例患者均有高RF、A-CCP滴度,1例仅RF滴度升高,A-CCP正常范围,3例均有高RF和(或)A-CCP滴度特点。1例患者仅ESR高,1例ESR及CRP均高,1例ESR及CRP正常,但SAA高,3例均有不同的急性时相炎性反应物升高。1例补体C3、C4均减低,1例仅C3减低,1例正常范围;3例均有TP及ALB减低及ANA阳性特点。余检查包括电解质、甲状腺功能、肿瘤标志物、ANCA、抗心磷脂抗体、结核抗体、狼疮抗凝物质、血免疫固定电泳、尿本-周氏蛋白均未见明显异常。1例血常规提示三系减低,可能与长期服用甲氨蝶呤有关。
2.3 肌电图 3例均显示有慢性神经源性损害,并发现更多亚临床的周围神经病变。1例显示左右腓浅、腓肠神经、左侧隐神经CMAP/SNAP波幅未引出,右侧隐神经SNAP波幅降低,1例右侧桡神经CMAP、左侧隐神经SNAP损害,均为典型多发性单神经病变。1例左右胫、腓总神经CMAP/SNAP波幅降低,双侧足底内侧神经SNAP波幅未引出,表现为多发性周围神经损害肌电改变。
2.4 脑脊液检测 3例行腰椎穿刺检查,仅1例示ALB稍低,余无异常。
2.5 其他检查 心电图异常1例,表现为部分导联ST改变。心脏彩超异常3例,均有左室舒张功能减退,分别伴二尖瓣、三尖瓣及二、三尖瓣轻度反流。颈部血管彩超异常3例,2例表现为右侧锁骨下动脉及左侧颈动脉粥样斑块形成;1例仅右侧锁骨下动脉粥样斑块形成。胸部CT异常者2例,1例表现为慢性炎症及少许纤维灶伴小结节,主动脉及冠脉钙化,1例为双肺炎性病变,纵膈淋巴结钙化,心影稍大及冠脉钙化。头部MRI+MRA异常者2例,1例表现为多发腔隙性脑梗死伴急性期梗死,轻度深部脑白质缺血及脑萎缩,部分颅内动脉硬化(见图2);1例仅表现为多发腔隙性脑梗死及颅内动脉硬化(见图3)。双下肢血管彩超异常者2例,1例表现为动脉粥样斑块形成,1例为动脉粥样斑块伴右侧腘静脉血栓形成(见图3)。肝胆脾胰及双肾彩超3例均无异常。
2.6 确诊时间及手段 3例从发病至确诊时间1 m~15 m。1例因双下肢酸胀在外院误诊为腰椎间盘突出症,1例因右手无力,1例因足底麻木,入住神经内科。3例患者均经自身抗体检测、肌电图检查,并排除其他可能的原因后明确诊断。
2.7 治疗及预后 例1、例3转风湿科行TNF-α抑制剂皮下注射,规范治疗;例2因费用问题坚持出院,口服抗风湿药物甲氨蝶呤10/12.5 mg qw、甲泼尼龙 4 mg qd、托法替布1 片 bid,随访时例1、例3患者均有不同程度好转,例2症状加重。
3 讨 论
3.1 病因及发病机制 RA是一种自身免疫性疾病,以累及多个大、小关节为特征,并伴有多系统关节外表现[3]。周围神经病变(peripheral neuropathy,PN)是已知的RA的关节外表现,根据既往研究,其发病率约为39.19%。RA患者周围神经病变的类型有单纯感觉型、单纯运动型、远端轴突感觉运动型、多发性单神经炎和神经压迫型[4]。以往的研究认为神经卡压、药物毒性、血管炎、淀粉样变性可能是RA患者周围神经病变的原因,而根据对其的了解,血管炎是最可能的发病机制[5]。
RV是RA的一种关节外表现,可累及任何大小的血管,引起血管壁炎症、损伤、坏死、血栓形成和组织缺血,最常出现皮肤损害(如孤立性甲襞梗死、小腿溃疡、紫癜)及伴有远端感觉和运动神经的周围神经系统受累(如多发性单神经炎)[6,7]。常见于长期、严重、血清学阳性且经常不受控制的类风湿性关节炎患者[7]。当小血管炎症的发生影响其供应区域的神经血供时,可出现肢体麻木、足下垂等周围神经损害。
3.2 临床表现和实验室检查 急性或亚急性起病的多发性、疼痛性感觉或感觉运动性单神经病变是RV的特征性表现。症状在数周内逐渐加重,最终可能重叠,出现远端对称或不对称的多发性神经病变[8]。本组中例1、例3早期均有肢端感觉异常,以单侧为主,后期逐渐进展至对侧,并有急性加重出现,符合经典神经受累模式。
RV患者常有很高的心血管和周围血管疾病的共病负担,这与脑血管炎症和高凝状态都有关系[1]。例3下肢血管彩超提示右侧腘静脉血栓,可能因炎症增加了促凝血因子,也抑制了天然的抗凝途径和纤溶活性,导致血栓形成[9]。本组中3例患者均有多发腔隙性脑梗死及颅内动脉硬化,并且例1头部MRI提示急性期梗死,不排除与这种可能的机制有关。Tanemoto等[10]也曾报道1例类似的RV患者。
RV患者肠道受累相对少见,但也可影响高达38%的RV患者。胃肠道的任何一段都可能受累,导致食道和胃溃疡、肠道出血、穿孔等,胃肠镜下活检是其确诊的主要手段[11]。本组中例1入院前因腹痛于当地医院就诊,未明确诊断,后出现便血、体重减轻等,症状可能与血管炎累及肠道有关。
电生理最常见多发性单神经病,其次是不对称或对称性感觉运动轴索损伤为主的多发性周围神经病,并能发现较多亚临床的周围神经损害[8]。本组中3例患者均在肌电图中发现早期的神经损伤,同时例3为对称性多发性周围神经损害肌电改变,这与病程较长后血管炎症最终的重合有关。
RA患者常有较高的RF、A-CCP、ESR、CRP滴度[3]。但RF及A-CCP是否为RA并发PN的危险因素尚存在争论[4,5,12,13]。丁允琪等[12]对46例RA并发PN患者行回顾性分析发现RF滴度>178.4 IU/ml可能是RA发生PN的危险因素之一,而与RA病程、ESR、CRP、A-CCP、关节破坏、畸形、间质性肺炎及既往治疗无关。Kaeley等[4]的一项研究认为年龄、病程、疾病活动度、疾病修饰类药物的使用与其发生有关,RF在两组之间有差异,但缺少统计学意义。Kumar等[13]的横断面研究发现周围神经病变占血清阳性RA患者的34.04%,只占血清阴性患者的15.38%,提示与可能的疾病进展有关。Li[5]等的研究发现,多神经受累者WBC、PLT、ESR、CRP、RF水平较高,白蛋白水平较低,认为严重炎症状态是多神经受累者的危险因素。本组中3例患者均有高RF和(或)A-CCP滴度、不同的急性时相炎性反应物升高、TP及ALB减低,伴或不伴有补体的下降,这种变化与Li等人在2021年的研究相一致,提示血管炎症是其可能的病理机制。血清白蛋白具有强大的抗氧化特性,抑制了自由基的产生,并具有清除过氧化自由基的能力[5],其血清水平与体重、身高、营养状况等都有关系,但参与炎症反应后被消耗是最可能的原因,这也可以解释补体水平为何下降。
3.3 诊断标准和防范误诊的措施 类风湿血管炎的明确诊断需要受影响器官中小血管炎症的组织学证据。病理特征包括血管壁的单核或中性粒细胞浸润与血管壁破坏(坏死,白细胞沉着和弹性层破裂)[1]。此3例患者缺少神经活组织的病理检查,故只能临床诊断。但满足Scott和Bacon[14]在1984年提出的诊断标准,并排除其他可能导致血管炎的原因,如HCV相关冷球蛋白血症、HBV相关结节性多动脉炎(PAN)、ANCA相关性血管炎、药物诱导血管炎、HIV和感染相关血管炎等[15],可以考虑用药治疗。
类风湿血管炎性周围神经病常因临床表现多样、肌电图检查不规范、缺乏特异性实验室指标及医生对该病的认识不足而误诊。全身性血管炎性周围神经病通常伴有多个器官系统受累,神经病变可能被肺部,胃肠道,皮肤病或泌尿系统症状所掩盖[8]。患者常因其他脏器受累辗转于消化、呼吸、皮肤等科室,因未能窥见疾病全貌而耽误诊断。提醒我们要强调对RV患者的早期识别及治疗,在患者存有高危因素时尤其如此[16]。
3.4 治疗 治疗往往是经验性的,并且需要长久的免疫抑制。血管炎性周围神经病的初始诱导治疗通常是皮质类固醇与环磷酰胺,利妥昔单抗,或甲氨蝶呤等的联合治疗,待患者的临床症状缓解后,再用硫唑嘌呤或甲氨蝶呤维持治疗18~24 m。对于难治性症状或疾病进展可以选择血浆置换和IVIG输注[8,17]。TNF-a抑制剂和Rituximab也被认为是难治性RV的有效治疗手段[18,19]。
托法替尼(Tofacitinib,也称托法替布)和巴瑞克替尼(Baricitinib)是一种参与JAK/STAT信号转导的JAK抑制剂,与传统DMARDs(Disease-modifying antirheumatic drugs,DMARDs)联合使用,用于其他生物DMARD无效或无法接受输液或注射的患者[3]。生物DMARD可延缓疾病进展,有效改善预后,但其广泛使用常受到高成本和副作用的阻碍[20]。大多数指南对这些二线药物的选择都是平行推荐,常结合患者主观意愿、是否合并禁忌证而定,其疗效大致类似,但可能存在个体差异。本组中例1、例3规范使用TNF-a抑制剂后症状好转,而例2因费用原因选择直接加用托法替布,随访时症状更加严重。由于RV可导致严重的残疾和死亡,远期预后差,因此提倡积极治疗,在疾病早期应用生物制剂,患者可能获益更多。
类风湿血管炎性周围神经病并不罕见,但因大部分神经内科临床医生对其认识不足,早期易被漏诊。这3例患者以分别以肢体麻木、足下垂、小指背伸不能以及足底疼痛为理由就诊,并无RV特征的瘀点、紫癜、下肢缺血性溃疡等,因此应扩大对类风湿关节炎并发症的认识。本组3例患者同样提示,当出现长病程、血清RF和(或)A-CCP阳性、高CRP、ESR、低补体、低蛋白的RA患者时,需及时完善肌电图检查及其他影像学检查,明确炎症累及的范围。同时应早期予以积极治疗,以改善远期预后。
致谢:感谢武汉市卫生健康委员会科研项目基金对本项目的资助。
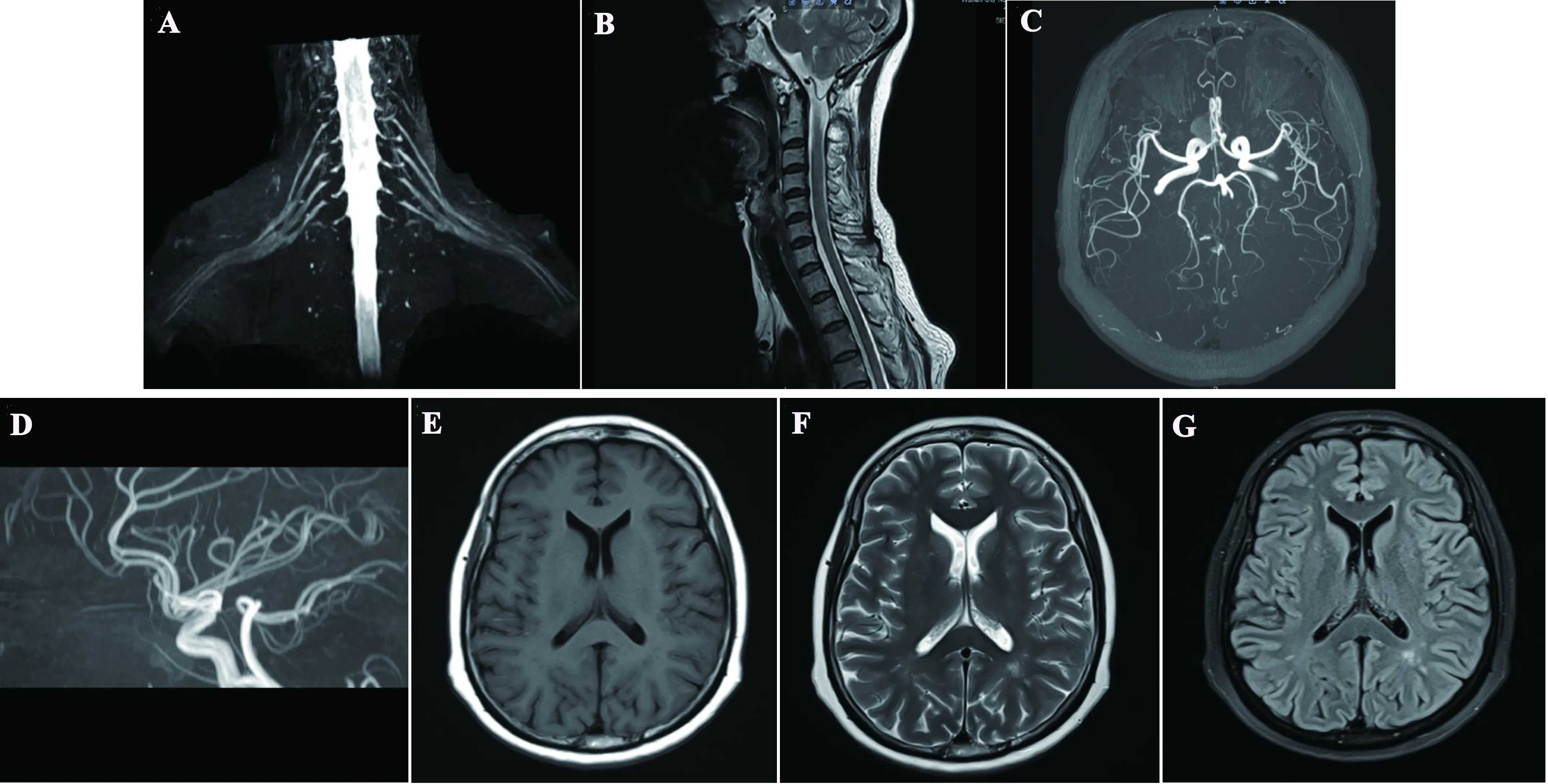
图1 例2,A:双侧臂丛神经显示对称,走行自然,未见明显增粗及异常信号影;B:颈椎MRI提示C5/6,C6/7腰椎间盘突出;C~D:MRA检查未见明显异常;E~G:T1、T2及T2 Flair相未见明显异常信号影

图2 例1,A~B:头部MRA示部分颅内动脉硬化;C:T2 Flair示颅内多发斑片状信号影,腔隙性脑梗死可能;D:DWI示右侧基底节区、胼胝体膝部高信号影,可能为急性期梗死

图3 例3,A~B:双下肢动静脉彩超示动脉粥样斑块形成,右侧腘静脉血栓形成;C~D:头部MRA示颅内动脉硬化(轻度);E~G:头部MRI示双侧基底节区、半卵圆中心、双侧额顶叶散在分布点状、斑片状长T1长T2及T2 Flair高信号影,腔隙性脑梗死可能

