柱前甲基衍生化GC-MS法测定人粪便短链脂肪酸
常满,李晓飞,何芍莹,贺炳凯,范辉
(广东省代谢病中西医结合研究中心/糖脂代谢病教育部重点实验室/国家中医药管理局高脂血症调肝降脂重点研究室/广东药科大学中医药研究院/广东省代谢性疾病中医药防治重点实验室,广东 广州 510006)
短链脂肪酸(SCFAs)是由肠道微生物代谢产生、少于7个碳原子的一类有机脂肪酸,主要包括乙酸、丙酸、丁酸、异丁酸、戊酸、异戊酸[1]。人体粪便样品中的SCFAs 以乙酸、丙酸和丁酸为主[2-3]。研究表明,SCFAs是一种重要的信号分子,可与其特异性受体相互作用[4],对肠道有氧化、维持水电解质平衡、调节肠道菌群平衡、改善肠道功能、抗炎、抗肿瘤和调控基因表达等重要作用;在多个水平上影响糖脂质代谢,既参与脂肪的合成又有一定程度抑制作用;作为肠道菌群重要的代谢物,SCFAs可通过对多个系统的影响,协同发挥其广泛生理作用,提高机体抗病力,维护机体健康[5-10]。
SCFAs为挥发性脂肪酸,易逸失,直接测定难度大,测定方法多采用高效液相色谱法、气相色谱法等[11]。现有文献报道粪便类样本的SCFAs 测定方法,样品前处理复杂,干扰峰多,灵敏度不高[12]。本研究收集人的粪便样品,建立一种新颖的柱前甲基衍生化GC-MS 技术对粪便样本中的SCFAs 进行定性定量分析,拟为肠道菌群功能的相关研究提供依据。
1 实验部分
1.1 仪器与试剂
7890B-5977B GC-MS 气相色谱质谱仪(安捷伦科技有限公司);DB-23 色谱柱(安捷伦科技有限公司);5180R 低温高速离心机(Eppendorf 公司);Vortex-3 漩涡混合器(德国IKA 公司);BT2245 电子天平(德国sartorius);BCD-266CM -80 ℃冰箱(美的集团有限公司)。
对照品乙酸、丙酸、异丁酸、异戊酸均购于德国DR 公司(批号分别为CDCT-C10015500、CDCTC16493000、CDCT-C14395500、CDCT-C14479470);丁酸(批号CDDE-N-4-A-1GM,NU-CHEK 公司);戊酸(批号CDAE-75054-1ML,Sigma 公司);4-甲基戊酸(批号M813962,麦克林Macklin 公司);甲醇(色谱纯,批号M813962,德国Merck 公司);3-(三氟甲基)苯基三甲基氢氧化铵5% 甲醇溶液(批号IH0096-0,TCI 公司);三氯甲烷(分析纯,麦克林公司);浓硫酸(分析纯,广州化学试剂厂);超纯水(生物级,屈臣氏蒸馏水公司)。
1.2 溶液的制备
1.2.1 粪便收集 招募健康志愿者,受试者在开展受试前签署书面通知书并完成伦理审批。采样前备好干冰及冰盒,无菌杯采集新鲜粪便,粪样收集后,迅速放入干冰盒中冷冻。完成采样后,将样本立即冻存于-80 ℃冰箱中。
1.2.2 混合对照品溶液的制备 精密量取4-甲基戊酸内标物适量置于5 mL容量瓶中,加甲醇溶解并定量稀释,配制成内标溶液(4-甲基戊酸0.42 mmoL/L)。精密量取乙酸、丙酸、异丁酸、丁酸、异戊酸、戊酸短链脂肪酸对照品,置5 mL 容量瓶中,加甲醇溶解并定量稀释制成短链脂肪酸对照品混合储备液(乙酸、丙酸、异丁酸、丁酸、异戊酸、戊酸浓度分别为36.00、14.40、14.40、14.40、12.00、12.00 mmoL/L)。再精密量取各混合储备液1.0 mL 于2.0 mL 或5.0 mL 容量瓶,加甲醇溶解并稀释至刻度,依次制备成不同浓度的混合对照品溶液,见表1。

表1 混合对照品溶液的浓度Table 1 Concentration of mixed reference substancec/(mmoL·L-1)
精密量取各混合对照品溶液100 μL 于EP 管中,精密加入内标溶液100 μL,再精密加入100 μL衍生化试剂3-(三氟甲基)苯基三甲基氢氧化铵(5%甲醇溶液),用封口膜封口,充分混匀后,常温下静置反应60 min,完成后即可上样检测(甲基化反应)。
1.2.3 粪便供试品溶液的制备 精密称取150 mg粪便样本,加入500 μL 三氯甲烷浓硫酸溶液(取适量的三氯甲烷于50 mL离心管中,缓慢加入浓硫酸,调节其pH 值至2.0~3.0),涡旋10 min,充分混匀,冰上静置5 min,12 000 r/min 下离心10 min,取下清液于1 mL EP 管中,再次12 000 r/min 下离心5 min。取上述两次离心后的下清液100 μL,精密加入内标溶液100 μL,最后精密加入3-(三氟甲基)苯基三甲基氢氧化铵(5%甲醇溶液)试剂100 μL,用封口膜封口,常温静置反应60 min,即为粪便供试品溶液。
1.3 测定条件
色谱条件:色谱柱DB-23 石英毛细管柱(60 m×0.25 mm×0.25 μm);进样口温度250 ℃,分流比10∶1,进样量1.0 μL,载气为高纯氦气,流速1.0 mL/min。升温程序:初始温度40 ℃保持0.5 min,58 ℃保持3 min,70 ℃保持2 min,120 ℃保持1 min,最后240 ℃保持10 min,总运行36.5 min,见表2。
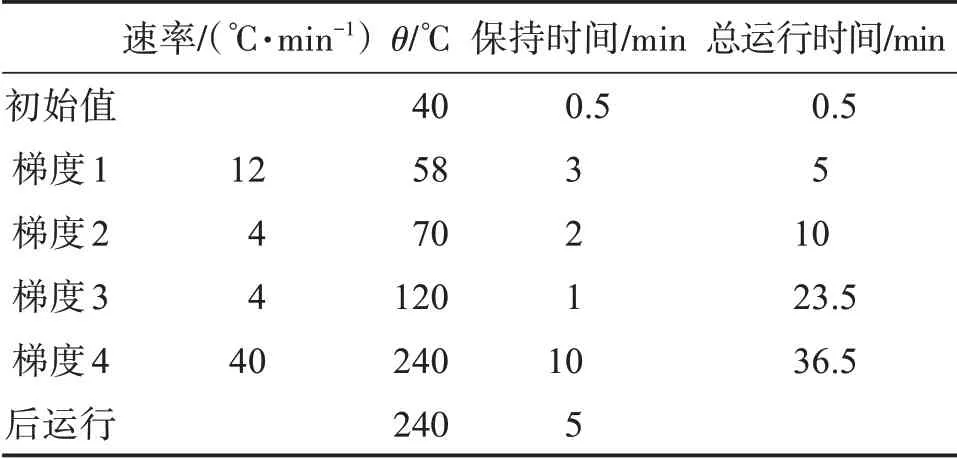
表2 气相色谱升温条件Table 2 Gas chromatography heating conditions
质谱条件:EI离子源;离子源温度:230 ℃;电子轰击能量:70 eV;四极杆温度:150 ℃;溶剂延迟时间4.5 min;采用选择离子扫描方式(扫描范围m/z:40~500)。
2 结果
2.1 系统适应性试验
在上述色谱质谱条件下,混合对照品溶液、粪便样品溶液的6 种短链脂肪酸、内标物实现完全分离,根据总离子流图(图1)和成分质谱图(图2)可以确定衍生化短链脂肪酸的各组分定性、定量离子(表3)。

表3 7种化合物的定性、定量离子Table 3 Qualitative and quantitative ions of seven compounds

图1 混合对照品溶液(a)和粪便供试品溶液(b)的总离子流图Figure 1 Total ion chromatograms of the mixed standard solution(a)and the fecal sample solution(b)

图2 供试品中主要成分质谱图Figure 2 Mass spectrograms of main components in the sample
2.2 线性关系
取配置好的混合对照品溶液,按“1.2.2”项下方法发生甲基化反应后,按“1.3”项下色谱质谱条件进样测定,用加权最小二乘法作线性回归,得回归方程。进样分析得到6 种化合物相应的标准方程,以待测物峰面积与内标物峰面积的比值为纵坐标(Y),待测物浓度(mmoL/L)为横坐标(X),进行加权最小二乘法作线性回归,得各化合物线性方程,结果显示相关系数均r>0.999,各化合物线性范围内线性关系均良好,见表4。以信噪比10∶1 确定各化合物的方法结果定量下限均达到0.1 μmoL/L,灵敏度高。
2.3 精密度、重复性及稳定性试验
取中间浓度(乙酸、丙酸、异丁酸、丁酸、异戊酸、戊酸浓度分别为1.5、0.6、0.6、0.6、0.5、0.5 mmoL/L)混合对照品溶液浓度连续进样6 次分析,结果显示各短链脂肪酸的峰面积RSD值均小于3.0%,表明仪器精密度良好。
取同一粪便样品6份按“1.2.3”项下方法制备供试品溶液,进样分析平行6份相同粪便样品中,结果显示各短链脂肪酸的含量RSD值均小于5.0%,表明方法重复性好。
取同一粪便样品按“1.2.3”项下方法制备供试品溶液后,于0、2、4、6、8、12、24 h 进样测定,结果显示样本中24 h内6种短链脂肪酸的含量RSD值均小于8.0%,表明供试品溶在室温下24 h稳定性良好。
以上结果均符合生物样本检测的基本要求,见表4。

表4 线性关系、精密度、重复性及稳定性考察结果Table 4 Results of linear relationship,precision,repeat ability and stability
2.4 加样回收率试验
取已知浓度的同一粪便样品75 mg,分别加入约相当于样品质量的混合对照品溶液,各对照品加入量按80%、100%、120%的低、中、高3 种浓度组配置,每组平行制备3份样品,按“1.2.3”项方法处理样本后,按“1.3”项色谱、质谱条件检测各样品中SC‐FAs 的含量,计算回收率及RSD 值,见表5。结果显示,样本中各个SCFAs 测得的RSD 大部分小于10.0%,表明方法的提取回收率良好,符合生物样本检测的要求。

表5 粪便中SCFAs提取回收率Table 5 Recovery rate of SCFAs extraction from feces(n=3)
2.5 样品中短链脂肪酸的含量测定
收集粪便后,按“1.2.3”项下方法制备供试品溶液,按“1.3”项色谱、质谱条件进样测定各个化合物的峰面积后,代入表4的回归方程进行计算,得出各脂肪酸的浓度见表6。

表6 短链脂肪酸的测定Table 6 Determination of short-chain fatty acids(n=3)
3 讨论
目前,GC法、GC-MS法分析脂肪酸时采用的柱前衍生法多为甲酯化法[13]。甲酯化法使羧基与醇羟基酯化反应生成相应的脂肪酸甲酯,通常采用酸催化(浓硫酸)、碱催化(氢氧化钾)进行酯化反应。浓硫酸催化产物多,影响成分分离,且过量硫酸需要氮气吹干,步骤提取程序复杂。碱催化甲酯化法不适合游离型脂肪酸,适合甘油三酯型脂肪酸[13]。三氟化硼催化法[14-16],存在步骤繁琐,加标回收率低,溶液毒性较强,易于挥发,加热时易变成毒性更大的氟化氢等有害物质的缺点。
本研究对样品的前处理方法进行了考察,比较了乙酸乙酯、正己烷、乙醚、三氯甲烷与50%浓硫酸按1∶10的比例混合作为有机提取溶剂的效果,结果发现:使用乙酸乙酯提取时,溶剂会与组分乙酸出现共流出峰现象;使用正己烷提取时,提取率比三氯甲烷低,色谱峰峰形不理想;使用乙醚时,挥发性较强,导致样本定量结果不稳定;而使用三氯甲烷作提取溶剂时,提取效率较高,且处理后可得到比较澄清的样本,杂质较少,峰形较好。综合考虑,选用三氯甲烷加50%浓硫酸按照1∶10比例混合,作为粪便产物的提取试剂。
本研究采用的3-(三氟甲基)苯基三甲基氢氧化铵(TMTFTH)的成酯反应是一种热裂解的甲基化反应所生成的脂肪酸甲酯,反应原理见图3。该反应属于烷基化反应,TMTFTH 是季胺碱,化学反应包含两个连续的过程:第一步是在季胺碱的作用下,脂肪酸羧基去质子,与季胺碱形成相应的季胺盐,这一过程反应产物为有机酸有机碱盐,物质稳定,决定了方法的稳定;第二步是上述季胺盐在气相色谱进样口处进一步热分解成三甲基叔胺和相应的羧酸甲酯衍生物,该反应属于阴离子的亲核反应,这一步反应在气相色谱进样口温度250 ℃的条件下,瞬间分解为易挥发的羧基甲酯。热裂解的甲基化反应虽然生成的是羧基甲酯,但反应原理不同于酯化反应。热裂解的甲基化反应省去萃取、氮吹、蒸发等复杂步骤,加样反应后离心,取下清液即为待测液。该方法较好地解决了短链脂肪酸分析中存在的易逸失、衍生化反应不完全、提取步骤复杂等瓶颈问题。

图3 柱前甲基化反应原理Figure 3 Principle of pre-column methylation reaction
本研究建立了一种柱前甲基衍生化GC-MS 法测定人粪便短链脂肪酸的方法,利用GC-MS联用法对微量样品的检测优势,改进衍生化方法,以浓硫酸水解,减少离心次数,梯度洗脱增强灵敏性。该方法操作简便、快速、灵敏,且样品前处理简单、反应原理新颖、切实可行,适用于人粪便样本中短链脂肪酸含量的检测,为提升肠道菌群功能的科学研究奠定了基础。

