TiO2改性钒磷氧催化剂催化醋酸甲醛合成丙烯酸研究
黄博雅,郭荷芹,贾丽涛,肖 勇,李德宝,张建利
(1. 中国科学院山西煤炭化学研究所 煤转化国家重点实验室,山西 太原 030001;2. 中国科学院大学,北京 100049;3. 中国科学院洁净能源创新研究院,辽宁 大连 116023;4. 宁夏大学 省部共建煤炭高效利用与绿色化工国家重点实验室,宁夏 银川 750021)
丙烯酸是C3产业链的中间产品,可发生交联反应生成高吸水性树脂(Super Absorbent Polymer,SAP),也可以自身聚合用作洗涤助剂和水处理剂,并且可以与多种醇类反应生成丙烯酸酯,广泛应用于涂料、胶黏剂以及纺织等行业[1-5]。丙烯酸的主要生产工艺是丙烯两步氧化法[6-10],该工艺路线成熟,丙烯酸收率高,但原料丙烯对石油资源依赖性强。醋酸甲醛法合成丙烯酸,可将低值的醋酸和甲醛转化为高附加值的丙烯酸,工艺流程简单,原子利用率高,是一条极具前景的非石油路线的丙烯酸生产工艺[11-15]。
目前,应用于醋酸甲醛法合成丙烯酸反应的催化剂主要有Cs系催化剂和钒磷氧(VPO)催化剂[16-21]。其中,VPO催化剂兼具氧化还原性和酸碱性,有利于醋酸甲醛缩合反应进行,备受研究者青睐,但该催化剂上丙烯酸收率有待进一步提升。为此,研究者通过助剂掺杂对VPO催化剂进行改性。如Wang等[22]制备了Nb改性的VPO催化剂,发现当Nb/V=0.06时,V的平均价态由4.84降至4.77,同时强酸中心的相对含量明显提升,两者协同将丙烯酸收率由17.3%提升到18.5%(基于醋酸)。Yang等[23]制备了K、Fe、Co、Bi、Cu、Ni、Ce、Ba及Zr修饰的VPO催化剂,发现金属助剂的加入提升了V4+/V5+比值,促进了催化剂表面氧化还原循环,有利于丙烯酸的生成,其中,2%Zr-VPO催化剂具有最大V4+/V5+比值(0.76),因而具有最高的丙烯酸生成速率(18.6 μmol/(g·min))。Wang等[24]利用沉积法制备出了Cs、Ce及Nd等阳离子修饰的VPO/SiO2催化剂,发现阳离子的加入增加了催化剂表面V5+/V4+比值,并且失活后催化剂中V5+/V4+的比值明显降低,因此,认为V5+/V4+离子可能参与了催化反应。综上所述,尽管金属助剂能够提升VPO催化剂上丙烯酸收率,但对于其促进丙烯酸生成的机制,存在“与V价态改变相关的氧化还原促进机制”以及“与酸碱性改变相关的酸碱促进机制”的争议。因此,明确特定催化剂上丙烯酸的生成机制,对于高效醋酸甲醛合成丙烯酸催化剂设计具有重要的指导价值。
TiO2是一种两性的氧化物,表面同时具有弱酸、弱碱性位点,对VPO催化剂进行TiO2改性可能会调变VPO催化剂表面酸碱性;此外,TiO2中的Ti离子半径与V相近,且电负性低于V、P及O三种元素,对VPO催化剂进行TiO2改性也可能会调变VPO催化剂表面V5+与V4+的分布,这为TiO2改性VPO催化剂上丙烯酸收率的提升以及丙烯酸生成机制的研究提供了可能。
基于以上分析,本研究采用有机溶剂热法制备了系列TiO2改性的VPO催化剂,通过TEM、XRD、XPS、NH3-TPD及CO2-TPD表征手段对催化剂结构性质、V5+与V4+分布及表面酸碱性等进行表征,采用醋酸甲醛合成丙烯酸反应对催化剂进行评价,旨在提升VPO催化剂上丙烯酸收率的同时,阐明TiO2对丙烯酸生成的促进机制,为高效醋酸甲醛合成丙烯酸VPO催化剂的构建提供理论借鉴。
1 实验部分
1.1 催化剂的制备
以金红石相TiO2作为钛源制备了系列TiO2含量不同的VPO催化剂,制备过程如下:将一定量五氧化二钒(V2O5)和苯甲醇与异丁醇的混合溶剂(两种醇的体积比为1∶1)加入到500 mL三口烧瓶中,加热至140 ℃,并在此温度下回流4 h,得到溶液A。同时将一定量金红石相纳米TiO2(Rut)加入至一定量异丁醇溶液中,室温下搅拌4 h后,得到溶液B。将溶液B缓慢加入到溶液A中,140 ℃下继续反应1 h。然后将混合液冷却至70 ℃,缓慢滴加一定量85%的磷酸(物质的量比P/V = 5∶1),滴加完毕迅速升温至140 ℃,继续反应6 h至反应完全。将所得浊液冷却、抽滤、洗涤、干燥,然后在马弗炉中550 ℃下焙烧5 h,即得TiO2改性的VPO催化剂,记为VPO-Rut-x(x表示Ti与V的物质的量比)。
采用相同方法分别制备未改性VPO催化剂以及不同TiO2前驱体的VPO催化剂,TiO2前驱体分别选用钛酸四丁酯(TBOT)、锐钛相纳米TiO2(Ana)和金红石相纳米TiO2(Rut),Ti与V的物质的量比为2,所得催化剂分别记为VPO、VPO-TBOT-2、VPO-Ana-2和VPO-Rut-2。
1.2 催化剂的表征
催化剂TEM表征由日立JEM-2100F场发射透射电子显微镜测定,加速电压200 kV,放大倍数(4-50)万倍,催化剂表面元素分布由EDS mapping进行分析。催化剂XRD测试由PANalytical X’pert3 Powder衍射仪测定,使用CuKα辐射(波长λ=0.15406 nm),测试电压为40 kV,电流为40 mA,扫描10°-90°,扫描速率为5(°)/min。NH3/CO2-TPD测定在自组装置上进行,称取样品100 mg于石英管,在500℃用Ar(30 mL/min)吹扫30 min,基线稳定后降至室温,将气体切换为NH3/CO2吸附饱和,再用Ar进行吹扫至基线平稳,以10℃/min的速率由室温升温至650℃,在此过程中,通过TCD检测NH3/CO2脱附量,并记录TPD谱图。X射线光电子能谱由AXIS ULTRA DLDX型X射线光电子能谱仪测定,以AlKα射线为激发源,采用污染碳的C 1s峰(结合能为284.6 eV)作为定标标准。根据计算了(IV5+/V4+)/IV比值,其中,“|IV5+-IV4+|”是指未形成离子对的V离子的量,“IV”是指V离子的总量。因此,(IV5+/V4+)/IV比值是指“形成V5+和V4+离子对的V离子占V离子总量的比例”。
1.3 催化剂的评价
醋酸甲醛合成丙烯酸反应在固定床反应器上进行。称取6.0 g 20-40目催化剂装入固定床反应器恒温段,热电偶传感器置于加热炉和反应炉恒温段,通过程序升温控制仪控制预热炉和反应炉温度。催化剂在100 mL/min空气气氛下以10 ℃/min速率升温至400℃恒温4 h。随后降到室温,切换1%O2的氧氮混合气,标定气体流量为100 mL/min,升温到反应温度,然后,通入甲醛与醋酸的混合溶液(n甲醛∶n醋酸=1∶3,三聚甲醛作为甲醛源)。待反应稳定(1 h)后,开始收集液相产物(每1 h收集一次)。液相产物由配有TCD检测器的海欣GC950气相色谱仪分析测定,色谱柱类型为Porapak-T。气相产物通过三台海欣GC950色谱仪分析测定,其中,H2、N2、CO、CH4及CO2由碳分子筛柱和TCD检测器进行分析;C1-C7烯烷烃由Al2O3色谱柱进行分离,采用FID检测器分析;极少量未冷却完全的产物由Porapak-T色谱柱和TCD检测器进行分析,三种分析结果通过CH4关联归一得到气相产物组成。反应中原料转化率及产物选择性和收率具体计算过程如下:
醋酸的转化率:
丙烯酸的选择性:
丙烯酸的收率:
目标产物的收率通常与催化剂装填量、反应物浓度、液体空速(LHSV)等参数相关。为了消除这些参数的影响,采用目标产物的生成速率(STY,即单位质量催化剂在单位时间内生成目标产物的摩尔量,单位:mmol/(g·min))来表示催化剂的活性。
2 结果与讨论
2.1 催化剂的TEM-EDS表征
采用TEM-EDS对VPO和VPO-Rut-x催化剂的形貌及表面元素分布状况进行表征,结果如图1所示。图1(a)中TEM结果表明,未改性的VPO催化剂为块状结构,粒径2-4 μm。TiO2改性后的VPORut-x催化剂仍保持块状结构,但催化剂粒径随x增加呈减小趋势,当x= 12时,粒径减小至0.2-0.6 μm。
进一步通过EDS对催化剂表面元素分布进行分析,结果如图1(b)所示。可以看出,未改性的VPO催化剂表面V、P元素均匀分布。TiO2改性后的VPO-Rut-x催化剂,当x= 1时,催化剂表面TiO2出现团聚现象导致Ti元素分布不均匀;当x= 2时,团聚现象消失,催化剂表面V、P、Ti元素均匀分布,说明TiO2和VPO发生了较强的相互作用,可能有利于活性相的生成。随着x进一步增加,催化剂表面的Ti含量不断增加,V、P含量减少,这可能会导致催化剂表面VPO活性位相对含量降低。由上述分析可以得出,当x= 2时,催化剂中TiO2与VPO具有较强的相互作用并且可能会生成较多的活性相。
2.2 催化剂的物相表征
VPO和VPO-Rut-x催化剂的XRD谱图如图2所示。未改性的VPO催化剂在2θ为22.3°、22.9°、25.6°、27.7°、32.2°、36.2°、46.5°和60.5°处出现V4+的VOP2O6衍射峰(JCPDS,44-0066)。TiO2改性的VPO-Rut-x催化剂,在2θ为27.5°、36.1°、39.2°、41.3°、44.1°、54.4°、69.0°和69.8°处均出现金红石型TiO2的特征衍射峰,且峰强度随x的增大而增加。此外,当x≤6时,只检测到V4+的VOP2O6物相,但后续的XPS表征中检测到V以V4+和V5+两种价态形式存在,这可能是因为生成的V5+物相在催化剂表面高度分散或者晶粒尺寸太小(低于4 nm的XRD检测限);当x>6时催化剂物相发生改变,在2θ为22.0°和21.0°分别出现V5+的VOPO4(JCPDS,47-0951)和V4+的(VO)2P2O7(JCPDS,41-0696)的特征衍射峰,同时在2θ为24.3°和29.3°处出现Ti4P6O23(JCPDS,39-0004)的特征衍射峰,这可能是因为Ti的离子半径与V相近,取代V进入VPO物种的表面层状结构或体相中形成Ti4P6O23。
2.3 催化剂的XPS表征
进一步通过XPS对VPO和VPO-Rut-x催化剂表面元素分布及元素价态进行了表征(见图3、图4和表1)。对催化剂表面物相组成进行分析(见表1),结果表明,对于VPO-Rut-x催化剂,随着x的增加,Ti元素含量增加,V、P元素含量降低,这与EDS结果一致。此外,当x≤6时,催化剂表面Ti/V摩尔比接近理论值;当x= 12时,催化剂表面Ti/V以及P/V摩尔比都明显小于理论值,这可能是由于表面Ti、P元素进入催化剂体相形成Ti4P6O23的缘故,与XRD结果一致。
对催化剂中各个元素的结合能进行分析(见图3、图4和表1),未改性的VPO催化剂上V5+的结合能为518.5 eV,TiO2改性后,V5+结合能不断降低,当x= 12时降低到517.1 eV,同时V4+和P的结合能分别从517.5和134.9 eV降低到516.1和133.5 eV。这可能是因为Ti元素的电负性低于P、V元素,当Ti引入VPO体系后,P、V电子密度增加,导致P、V元素结合能下降。该现象表明,TiO2与VPO组分间存在较强的相互作用。
结合P、V元素结合能的偏移,对VPO和VPORut-x催化剂的V 2p3/2轨道进行分峰处理(见图3),并计算了VPO和VPO-Rut-x催化剂表面V5+和V4+的分布以及(IV5+/V4+)/IV比值(即形成V5+和V4+离子对的V占总V的比例)(见表1)。结果表明,随着x增加,(IV5+/V4+)/IV比值先增加后减小,当x= 2时,(IV5+/V4+)/IV比值最大(90.3%)。由于助剂促进VPO催化剂催化醋酸甲醛合成丙烯酸反应的机制有可能遵循“与V价态改变相关的氧化还原机制”[11,23],因此,VPO-Rut-x催化剂表面(IV5+/V4+)/IV比值的变化可能会对醋酸甲醛合成丙烯酸反应性能产生重要影响。
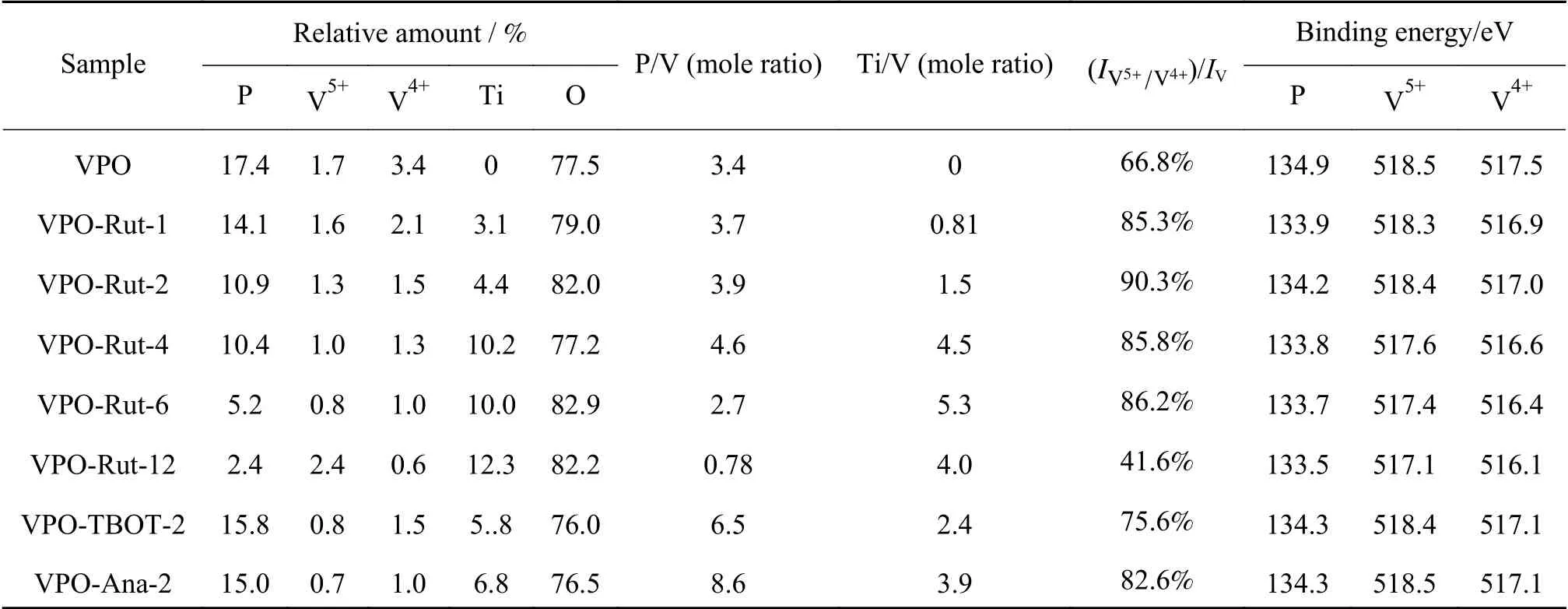
表1 催化剂的表面组成Table 1 Surface composition of catalysts
2.4 催化剂的表面酸碱性表征
采用NH3-TPD表征手段对VPO和VPO-Rutx催化剂的表面酸性进行了表征(见图5、图6和表2)。所有催化剂均在50-300和300-600 ℃出现NH3脱附峰,分别对应催化剂表面的弱酸性位点和强酸性位点。进一步对脱附峰进行了分峰拟合并对催化剂表面酸量进行了定量分析(见图6和表2)。结果表明,未改性的VPO催化剂表面酸性位点数量最少。TiO2改性后的VPO-Rut-x催化剂,随着x的增加,催化剂表面弱酸性位点数量增加,这与TiO2表面的弱酸性位点有关,而强酸性位点数量先增加后减小,在x= 2时达到最大(1910.9 μmol/g)。
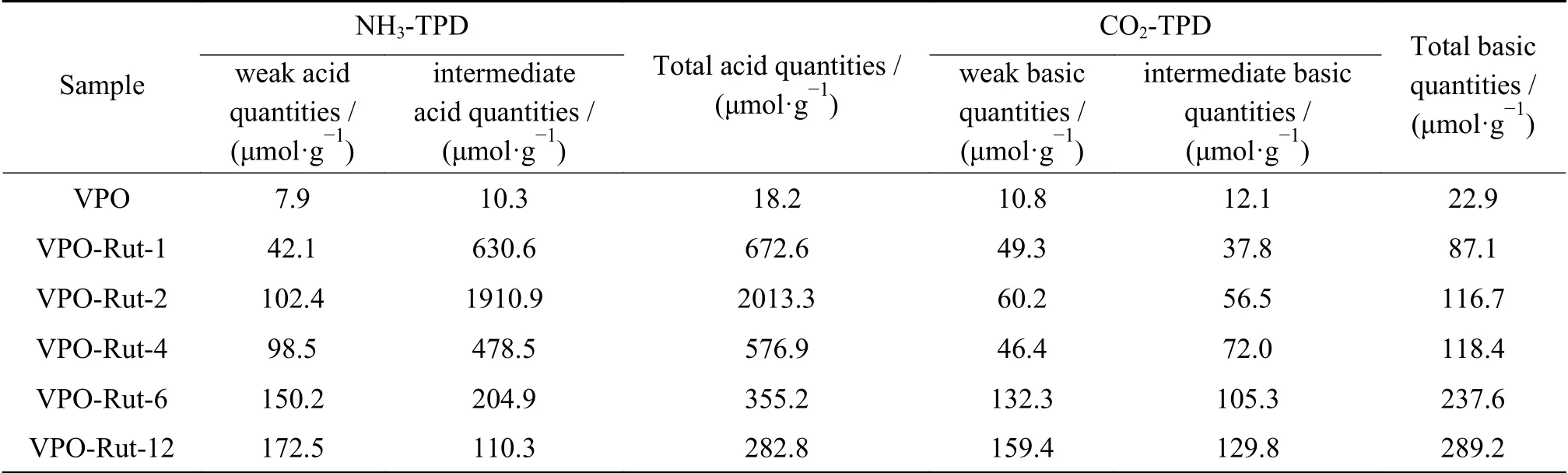
表2 催化剂的表面酸碱性Table 2 Surface acidity and basicity of catalysts
采用CO2-TPD表征手段对VPO-Rut-x催化剂的表面碱性进行了表征(见图7、图8和表2)。所有催化剂均在50-200和200-500 ℃出现CO2脱附峰,分别对应催化剂表面的弱碱性位点和强碱性位点。进一步对脱附峰进行了分峰拟合并对催化剂表面碱量进行了定量分析(见图8和表2)。结果表明,未改性的VPO催化剂表面碱性位点数量最少。TiO2改性后的VPO-Rut-x催化剂,随着x的增加,催化剂表面弱碱性位点和强碱性位点数量均增加,这可能与TiO2表面的弱碱性位点有关。
由于助剂促进VPO催化剂催化醋酸甲醛合成丙烯酸反应的机制有可能遵循“与酸碱性改变相关的酸碱促进机制”,并且鉴于该反应在较高的反应温度下进行(320-380 ℃),因此,催化剂表面强酸、强碱性位点数量的变化可能是导致醋酸甲醛合成丙烯酸反应性能的差异的重要因素。
2.5 催化剂的反应性能与构效关系分析
采用醋酸甲醛合成丙烯酸反应对VPO和VPORut-x催化剂进行了评价(见表3)。对于未改性的VPO催化剂,醋酸的转化率为15.1%,丙烯酸的选择性为83.0%,丙烯酸的收率为12.5%。TiO2改性后的VPO-Rut-x催化剂,随x的增加,醋酸转化率、丙烯酸选择性及收率均呈现先增加后减小的趋势,当x= 2时,丙烯酸的选择性和收率达到最大值,分别为85.4%和18.0%。
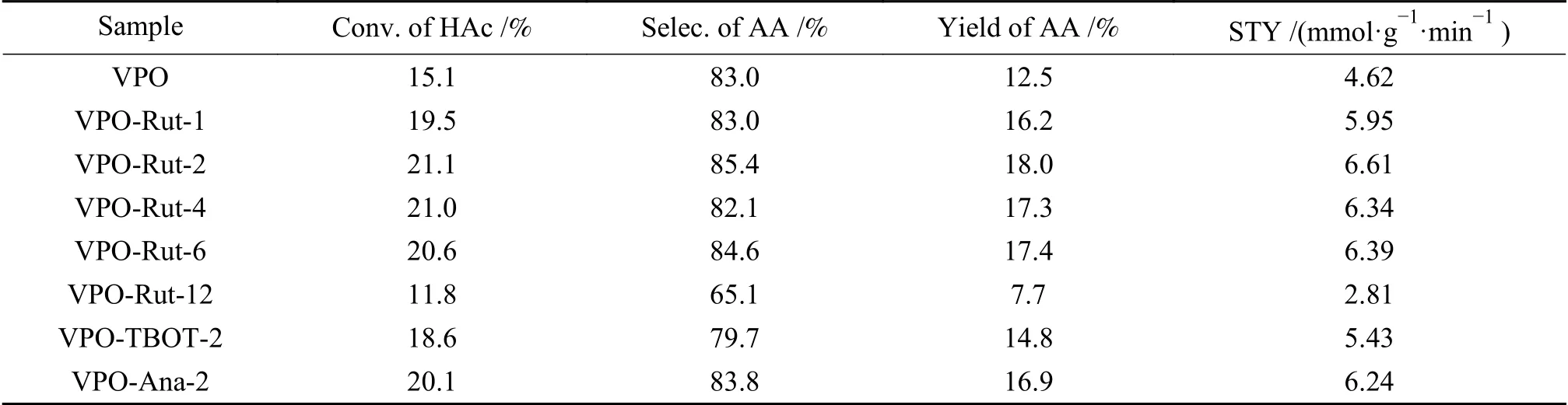
表3 催化剂的反应性能Table 3 Reaction performances of catalysts
结合催化剂表征结果,对催化剂构效关系进行了分析。文献报道[11,14,18,22-24],对于助剂改性的VPO催化剂,丙烯酸生成的机制可能遵循“与V价态改变相关的氧化还原促进机制”,也有可能遵循“与酸碱性改变相关的酸碱促进机制”。因此,本部分将丙烯酸生成速率(STY)分别与催化剂表面强酸性位点数量和表面强碱性位点数量进行了关联,发现并未出现相关性。由此推测,对于TiO2改性的VPO催化剂体系,催化剂表面酸碱性对醋酸甲醛合成丙烯酸反应的影响较小。进一步将丙烯酸收率与(IV5+/V4+)/IV比值进行关联(见图9(a)),发现丙烯酸收率与(IV5+/V4+)/IV比值有较好的线性关系,由此推测,对于VPO-Rut-x催化剂,V5+和V4+的氧化还原循环有可能是促进醋酸甲醛合成丙烯酸反应进行的主要因素,合适的(IV5+/V4+)/IV比值有利于丙烯酸的生成。
为了进一步验证上述推测,分别对不同TiO2前驱体制备的VPO-TBOT-2、VPO-Ana-2和VPORut-2催化剂的表面(IV5+/V4+)/IV比值进行分析(见图3和表1),发现TiO2的引入,均会促进V5+的形成,其中,VPO-Rut-2催化剂表面(IV5+/V4+)/IV比值最高,为90.3%,即该催化剂表面生成的V5+和V4+离子对的含量最高。对三种催化剂的反应性能进行分析(见表3),发现VPO-Rut-2催化剂的丙烯酸选择性和收率最高,分别达到85.4%和18.0%。进一步将三种催化剂以及未改性VPO催化剂的丙烯酸收率与其(IV5+/V4+)/IV比值进行关联(见图9(b)),发现丙烯酸收率与(IV5+/V4+)/IV比值存在较好的线性关系,进一步说明TiO2促进VPO催化剂催化醋酸甲醛合成丙烯酸反应的机制遵循“与V价态改变相关的氧化还原机制”,合适的(IV5+/V4+)/IV比值有利于丙烯酸的生成。
2.6 反应条件的优化
在固定床反应器中考察了反应温度对VPORut-2催化剂反应性能的影响(见表4)。反应温度由320 ℃升高至380 ℃,醋酸的转化率、丙烯酸选择性和收率以及丙烯酸形成速率均呈现先增加后减小的趋势。反应温度在365 ℃时,醋酸的转化率、丙烯酸选择性和收率最高,分别为21.1%、85.4%和18.0%,同时丙烯酸形成速率也达到最高6.61 mmol/(g·min)。因此,该催化剂催化醋酸甲醛合成丙烯酸反应适宜的反应温度为365 ℃。
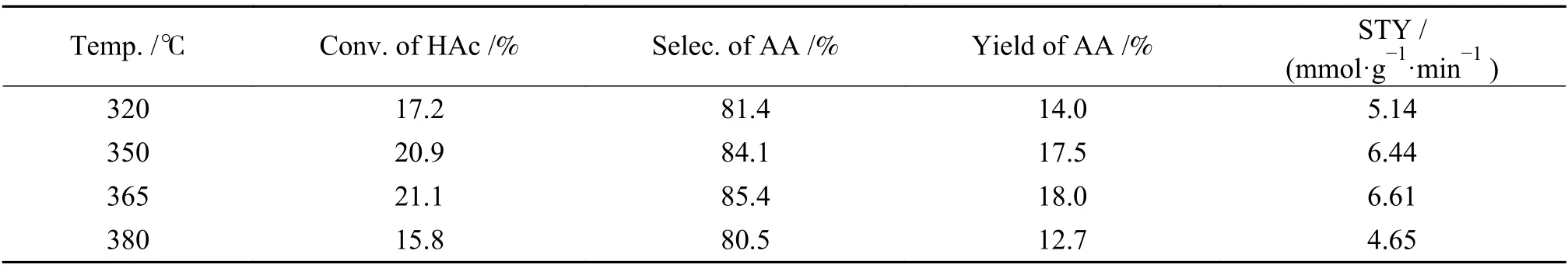
表4 温度对催化剂反应性能的影响Table 4 Effect of reaction temperature on the catalytic performance
进一步考察液空对VPO-Rut-2催化剂反应性能的影响(见表5)。结果表明,液空从1.0 h-1增加到4.0 h-1时,醋酸转化率持续降低,说明液空增大超出了催化剂的处理能力。但丙烯酸选择性及形成速率先增加后降低,在液空为2.5 h-1时,丙烯酸选择性及形成速率达到最高,分别为85.4%和6.61 mmol/(g·min)。综合考虑醋酸转化率,丙烯酸选择性以及形成速率,该催化剂催化醋酸甲醛合成丙烯酸反应适宜的液空为2.5 h-1。
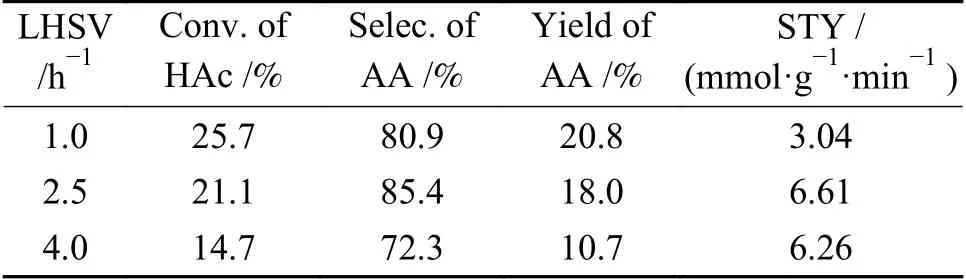
表5 液空对催化剂的反应性能的影响Table 5 Effect of LHSV on the catalytic performance
2.7 催化剂的稳定性能
图10为VPO-Rut-2催化剂上醋酸转化率、丙烯酸选择性以及丙烯酸收率随反应时间的变化趋势。反应2 h,醋酸转化率、丙烯酸选择性及收率分别为21.1%、85.4%和18.0%。随反应时间延长,醋酸转化率,丙烯酸选择性及收率均下降,反应5 h后分别降低至6.9%、71.0%和4.9%,说明催化剂稳定性较差。根据文献报道[25],催化剂失活可能是由于积炭对活性中心的覆盖导致的,因此,分别在6和10 h处对失活后催化剂进行空气气氛下的烧炭再生,并考察了再生后催化剂的性能。发现烧炭再生后催化剂基本能恢复与新鲜催化剂相当的性能,说明VPO-Rut-2催化剂能够循环利用,表现出较好的循环流化床应用潜力。
3 结 论
TiO2能够促进VPO催化剂催化醋酸甲醛合成丙烯酸反应的进行,当TiO2的前驱体为金红石相且Ti/V = 2时,丙烯酸收率最高(18.0%)。催化剂构效关系表明,TiO2促进VPO催化剂催化醋酸甲醛合成丙烯酸反应的机制遵循“与V价态改变相关的氧化还原机制”,合适的(IV5+/V4+)/IV比值有利于丙烯酸的生成。此外,催化剂稳定性结果表明,该催化剂具有较好的再生性能。
- 燃料化学学报的其它文章
- 混合胺溶液耦合CaO吸收-矿化CO2特性及矿化过程关键影响因素研究
- 循环流化床煤气化炉灰渣的组成结构特征与热转化性能
- Effect of Zn on performance of Ni/SiO2 for hydrodeoxygenation of anisole
- Oxidation treatment of carbon aerogels supports to modulate Ru/CA catalysts for Fischer-Tropsch synthesis
- O2、SO2对As2O3在W-Cu/γ-Al2O3催化剂表面吸附特性的影响:实验及理论模拟
- 双金属Cu-Ce/SAPO-34催化剂的制备及其NH3-SCR脱硝性能研究

