基于化学计量学结合UPLC评价白术药材质量
林 爽,王 杰,高珊珊,张志强,周永康,吉艳慧
(1. 北京康仁堂药业有限公司,北京 101301;2. 中药配方颗粒关键技术国家地方联合工程研究中心,北京 101301)
白术在我国具有悠久的应用和栽培历史,主要生长分布于浙江、江西、安徽、河南等地[1],其主要成分为挥发油[2-3]、多糖[4-6]、内酯类[7-9]等,药理学研究表明具有保肝、调节胃肠运动、抗炎性反应、调节免疫系统、降血糖等作用[10-11]。白术作为我国的大宗药材品种,在临床上亦有广泛应用。
在白术药材的质量控制方面,有指纹图谱研究[12-15]报道,提示白术质量与产地、不同炮制规格存在一定的相关性。含量测定方面多集中在内酯类[16-18]的成分,也有少部分有机酸类[19-20]成分研究,未见同时检测两大类成分含量的文献报道。本次试验采用超高效液相色谱法建立指纹图谱,结合化学计量学,分析研究影响白术质量的主要成分群,筛选出影响白术质量的两大类关键性成分,并对其中5种化合物定量分析,为白术的质量评价提供参考。
1 材料
1.1 仪器
ACQUITY UPLC H-Class型超高效液相色谱仪(搭载PDA检测器,配备Empower3工作站)、CORTECS UPLC Shield RP18色谱柱(2.1 mm×150 mm,1.6μm)(美国Waters公司);ML204T型分析天平 (d = 0.001 g)、MSA6.6S.0CE-DM型电子天平(d = 0.001mg)(德国Sartorius公司)。
1.2 试药
乙腈(色谱纯,德国Merck KGaA公司);磷酸(色谱纯,美国Fisher公司);蒸馏水(广州屈臣氏食品饮料有限公司);甲醇(分析纯,国药集团有限公司)。
绿原酸(批号:110753-202119,纯度:96.3%)、3, 5-O-二咖啡酰基奎宁酸(批号:111782-201807,纯度:94.3%)、4, 5-O-二咖啡酰基奎宁酸(批号:111894-202104,纯度:95.1%)、白术内酯Ⅲ(批号为111978-201501,纯度:99.9%)、白术内酯Ⅱ(批号:111976-201501,纯度:99.9%)以上5种对照品购于中国食品药品检定研究院;新绿原酸(批号:DSTDX001502,纯度:99.68%)、隐绿原酸(批号:DSTDY003502,纯度:98.77%)以上2种对照品购于成都德思特生物技术有限公司。
1.3 药材
收集的16批白术样品为北京康仁堂定点采购的菊科植物白术Atractylodis macrocephalaeKoidz一年至两年生的干燥根茎,经北京康仁堂药业有限公司“中药传承工作室”工程师于立伟鉴定为正品白术。其中,S1 ~ S6产地为安徽、S7 ~ S12产地为河南、S13 ~ S16产地为浙江,样品信息见表1。
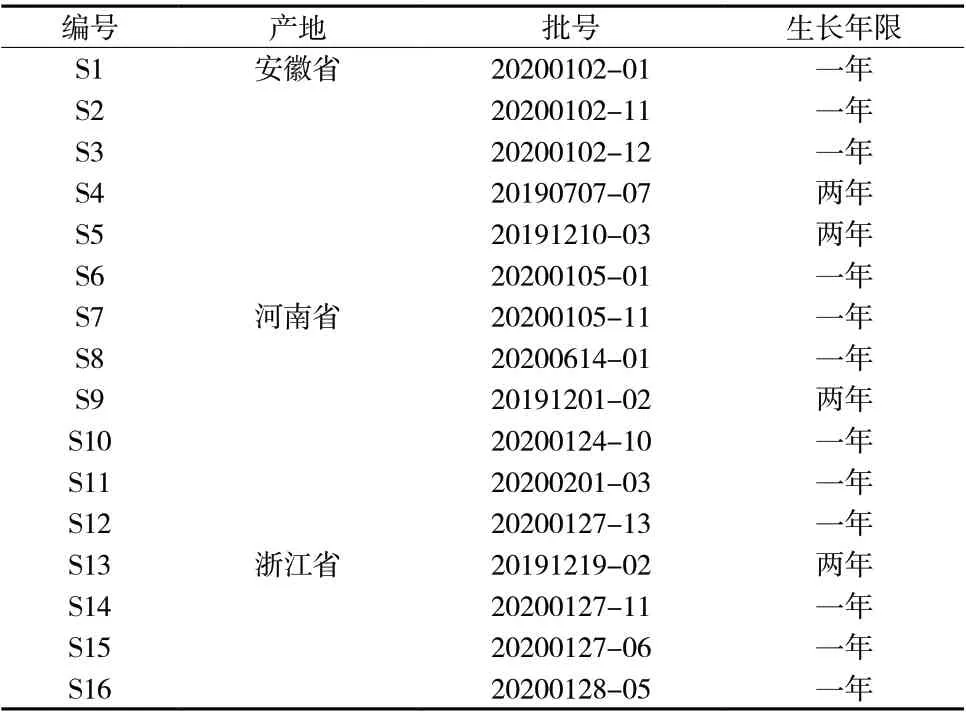
表1 白术样品信息表Tab. 1 Sample information table of AMR
2 方法与结果
2.1 指纹图谱研究
2.1.1 色谱条件 色谱柱为CORTECS UPLC Shield RP18(2.1 mm×150 mm,1.6μm),流动相为乙腈(A)-0.1%磷酸水溶液(B),梯度洗脱顺序为0 ~ 8 min,8% → 12%A;8 ~ 18 min,12% → 39%A;18 ~ 30 min,39% → 48%A;30 ~ 40 min,48% → 90%A。体积流量为0.3 mL/min,柱温为30℃,检测波长为221 nm,采样体积为3μL。
2.1.2 配制参照物对照品溶液 以50%甲醇为溶媒制成每1 mL含10µg的白术内酯Ⅲ溶液。
2.1.3 配制样品溶液 精密称取白术粉末1 g,于100 mL具塞锥形瓶中,精密加50%甲醇25 mL,密塞,称重,80℃加热回流提取30 min,冷却后补足失重,离心,过滤。
2.1.4 精密度试验 按“2.1.3”项配制白术样品(S1)溶液后,按“2.1.1”项连续进样检测6次,参考峰设定为白术内酯Ⅲ,并计算出21个共有峰与参考峰的相对保留时间和相对峰面积,RSD分别为0.01% ~ 0.04%、0.17% ~ 2.56%,表明仪器具有良好的精密度。
2.1.5 稳定性试验 按“2.1.3”项配制白术样品(S1)溶液后,按“2.1.1”项下分别在0、2、4、8、12、24 h进样检测,参考峰设定为白术内酯Ⅲ,并计算出21个共有峰与参考峰的相对保留时间和相对峰面积,RSD分别为0.01% ~ 0.06%、0.17% ~ 1.98%,表明在24 h内样品溶液具有良好的稳定性。
2.1.6 重复性试验 按“2.1.3”项配制6份白术样品(S1)溶液后,按“2.1.1”项进样检测,参考峰设定为白术内酯Ⅲ,并计算出21个共有峰与参考峰的相对保留时间和相对峰面积,RSD分别为0.01% ~0.08%、0.17% ~ 2.89%,表明该方法具有良好的重复性。
2.1.7 多批次样品色谱图 按“2.1.3”项配制16批白术样品溶液后,按“2.1.1”项进样检测,将色谱图导入“指纹图谱相似度评价系统(2012版)”,设置S1为参照图谱、时间窗宽度为0.1,采用中位数法结合全谱峰匹配方式,得到16批白术指纹图谱叠加图及对照指纹图谱,见图1,其相似度在0.972 ~0.995,表明各批次之间相似度良好。
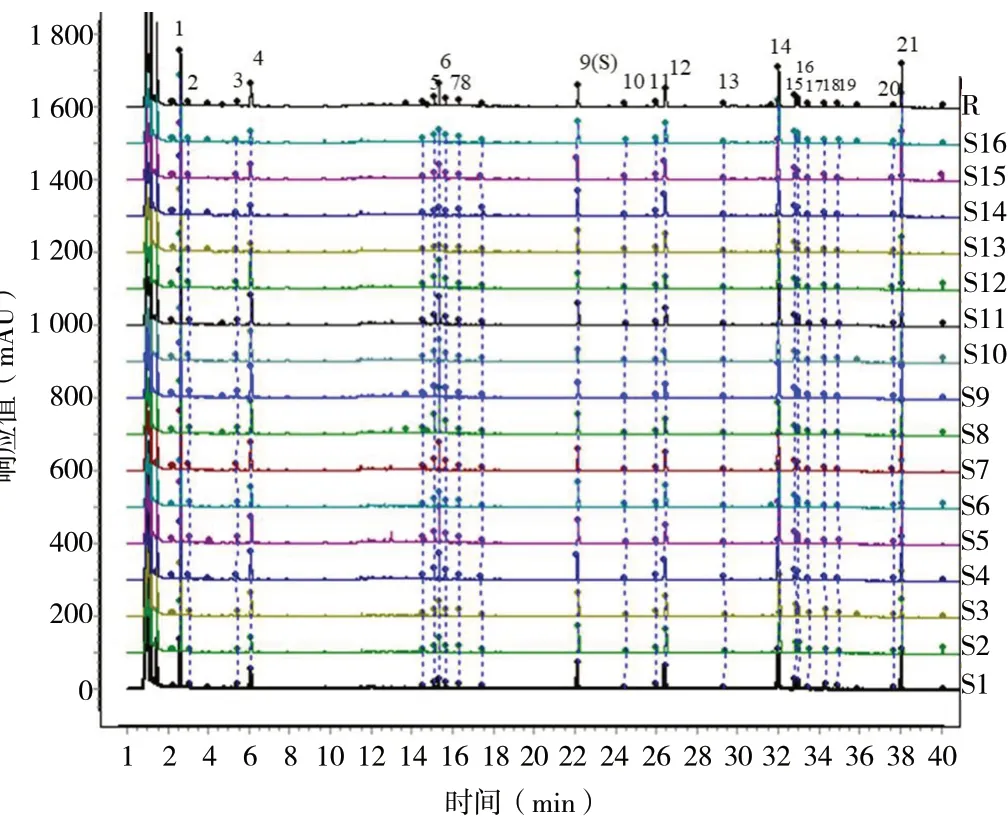
图1 16批白术药材的UPLC叠加图谱(S1 ~ S16)及对照图谱(R)Fig. 1 UPLC fingerprints of 16 batches of AMR(S1 ~ S16)and reference fingerprints(R)
2.1.8 共有峰的指认 经匹配后标定了16批白术中的21个共有峰,通过对照品比对,指认出7个色谱峰,分别为新绿原酸、隐绿原酸、绿原酸、3,5-O-二咖啡酰基奎宁酸、4, 5-O-二咖啡酰基奎宁酸、白术内酯Ⅲ、白术内酯Ⅱ,见图2。9号色谱峰(白术内酯Ⅲ)保留时间和峰面积适中,故以峰9为参照峰。
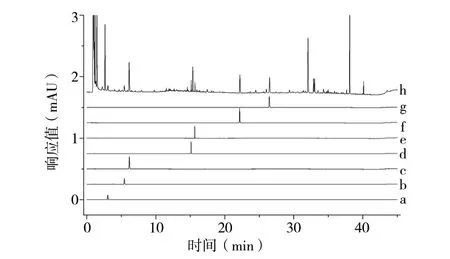
图2 7个共有峰在白术中的指认Fig. 2 Identification of seven common peaks in AMR referenc
2.2 化学计量学分析
2.2.1 聚类分析(CA) 以16批白术指纹图谱21个共有峰的峰面积为变量,应用SPSS 25.0软件进行CA分析,聚类方法为组间联接,应用平方欧式距离、标准化采用Z得分方法,聚类分析结果见图3,当类间距为15 ~ 20时,16批白术药材可以被分为3类,分别为S7 ~ S12、S13 ~ S16、S1 ~ S6,这三类白术样品的产地分别为安徽、河南和浙江,提示白术的质量与产地具有一定的相关性。
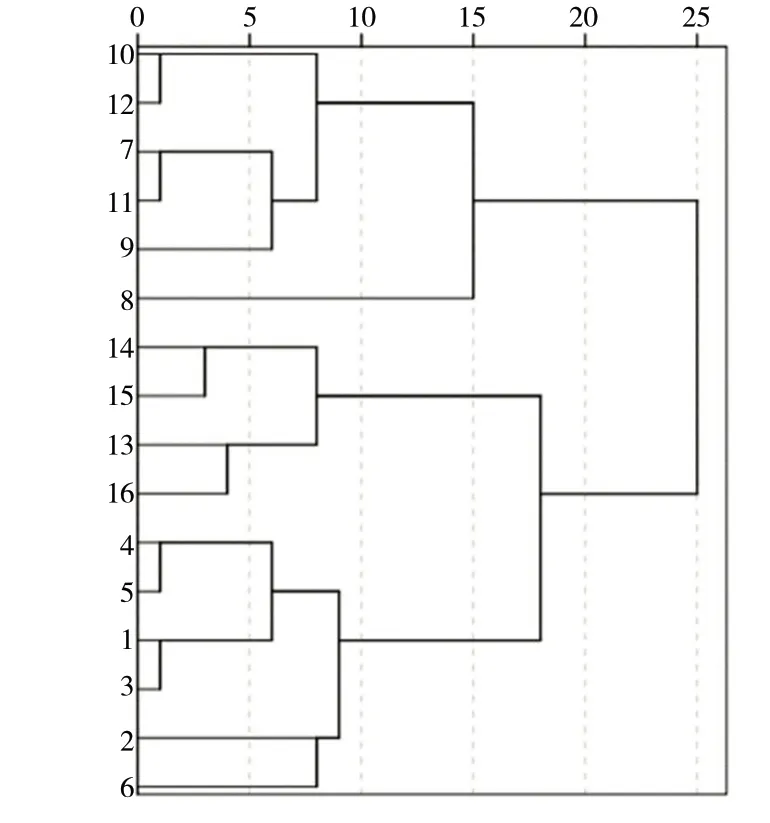
图 3 16批白术药材聚类分析树状图Fig. 3 Cluster analysis of 16 batches of AMR
2.2.2 主成分分析(PCA) 以16批白术指纹图谱21个共有峰的峰面积为变量,应用SPSS 25.0软件进PCA分析,特征值和方差贡献率结果见表2。提取出主成分特征值大于1的共有5个,累积贡献率为88.32%,大于50%,能够表征16批白术的质量特点。初始因子载荷矩阵结果见表3,其中,第1主成分包含的信息量最大,峰9、峰12、峰11(均大于0.9)有明显的载荷值;峰14、峰20、峰15(均大于0.8)在第2主成分中有明显的载荷值;峰7、峰5、峰6(均大于0.85)在第3主成分中有明显的载荷值,表明影响白术药材质量差异性的是多个成分。鉴于主成分1的贡献值最大,因此筛选峰9(白术内酯Ⅲ)、峰12(白术内酯Ⅱ)作为含量测定的指标性成分。用SIMCA 14.1绘图软件,对21个共有峰的峰面积进行主成分分析,结果见图4,其结果与聚类分析结果一致。
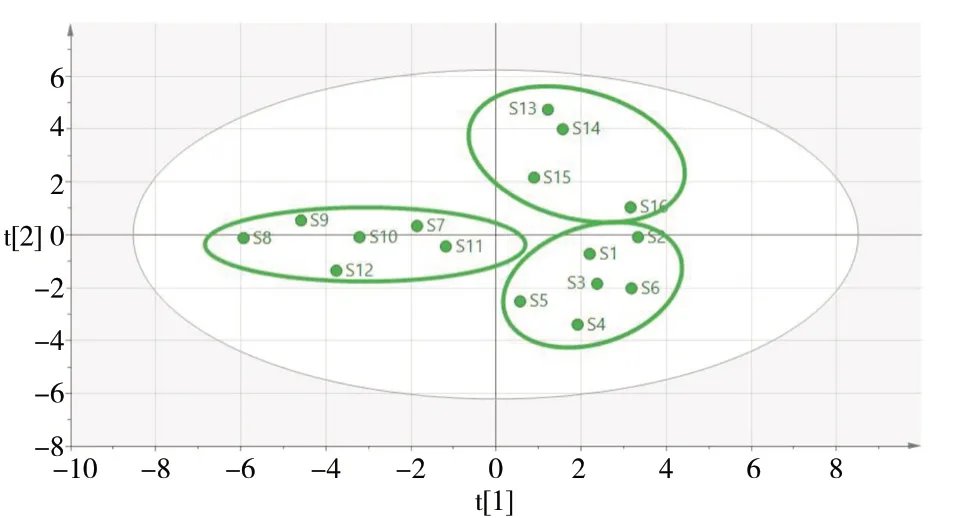
图4 白术PCA 图Fig. 4 PCA plots of 16 batches of AMR
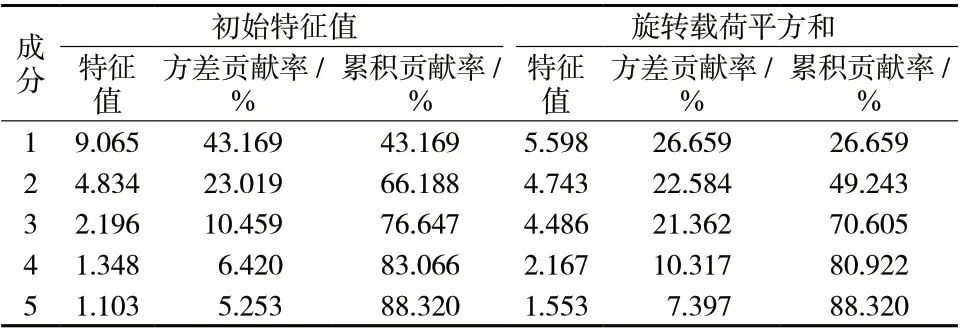
表2 特征值与方差贡献率Tab. 2 Eigenvalue and contribution rate
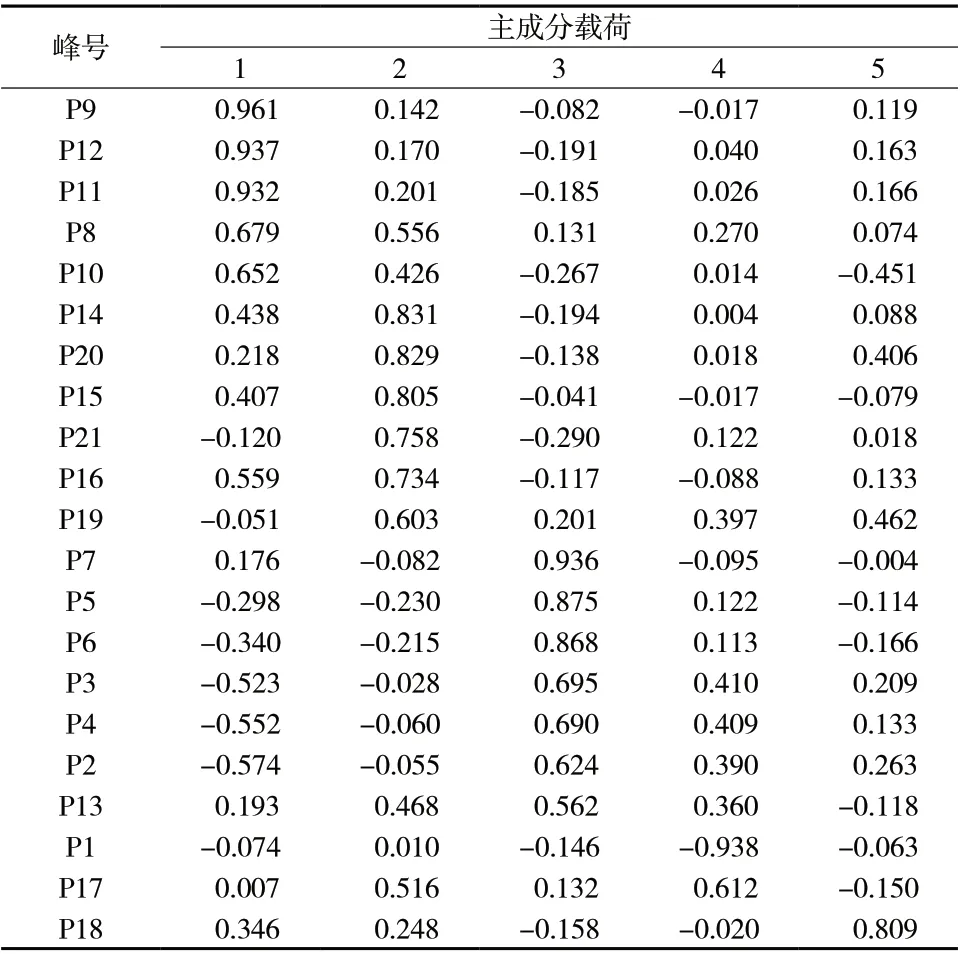
表 3 初始因子载荷矩阵Tab. 3 Initial factors loading matrix
2.2.3 偏最小二乘法判别分析(PLS-DA) 以16批白术的共有峰的峰面积为变量,使用SIMCA 14.1软件进行PLS-DA分析。建立的PLS-DA模型中,累积解释能力参数R2X和R2Y分别为0.659和0.841,预测能力参数Q2为0.774,均大于0.5,说明模型可靠。由PLS-DA得分图(图5)可知,16批白术样品被分为3类,根据模型中变量权重要性排序(VIP)预测值(见图6),筛选出具有统计学意义(VIP>1)的差异标志物,分别为峰13(VIP = 1.32)、峰4(VIP =1.27)、峰3 (VIP = 1.25)、峰1(VIP = 1.23)、峰8 (VIP =1.22)、峰2(VIP = 1.21)、峰16(VIP = 1.01)。因此,筛选峰4(绿原酸)、峰3(隐绿原酸)、峰2(新绿原酸)可作为鉴别和区分白术质量的标志物,选择为含量测定指标成分。
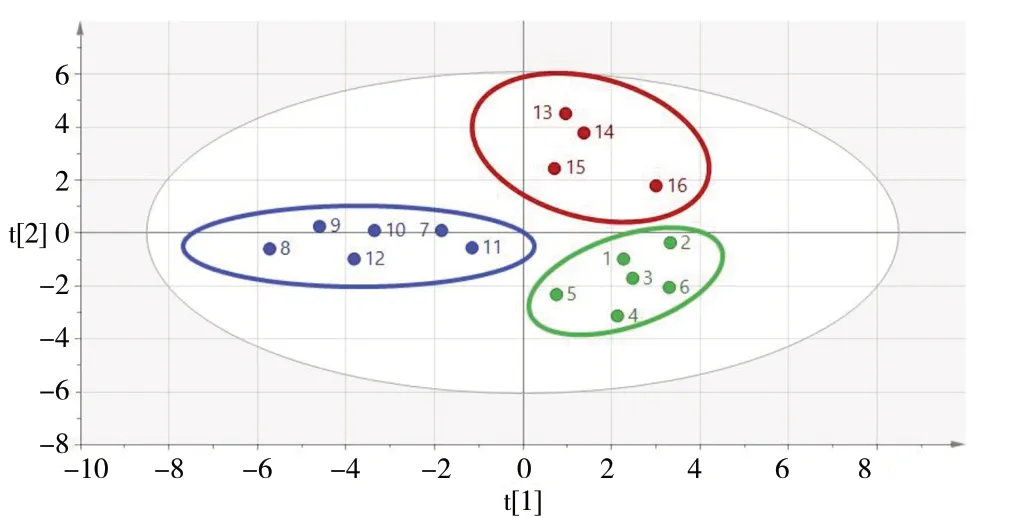
图 5 白术的 PLS-DA 得分图Fig. 5 PLS-DA scores plots of 16 batches of AMR
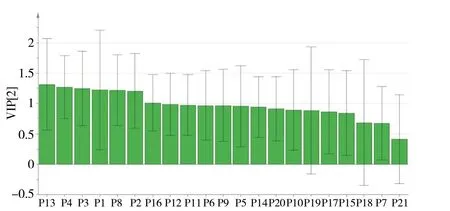
图6 VIP 值Fig. 6 VIP plot
2.3 含量测定
2.3.1 检测波长的选择 在白术指纹图谱中,新绿原酸、隐绿原酸和绿原酸3种有机酸类的响应值和分离度不佳,不能达到含量测定的检测要求,因此选择其它检测波长。提取三者的PDA光谱图,发现均在324 nm左右处有最大吸收,且基线平稳,分离度大于1.5,因此选择324 nm检测有机酸类成分。提取白术内酯Ⅲ和白术内酯Ⅱ的PDA光谱图,发现在紫外吸收末端处有最大吸收,因此选择221 nm检测内酯类成分。混合对照品和样品在324 nm和221 nm波长下的色谱图见图7。
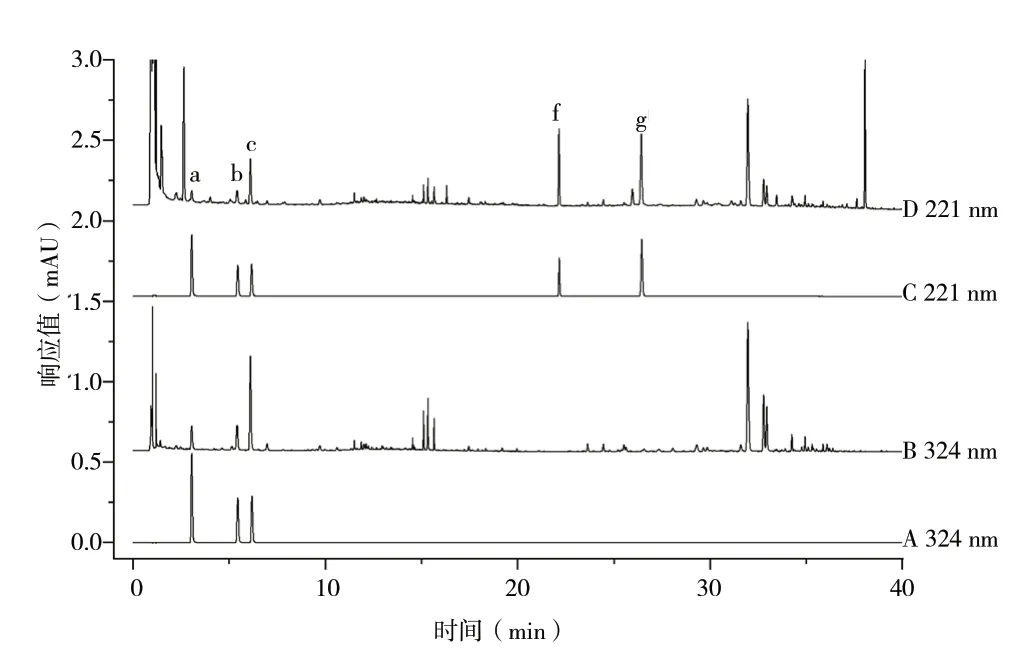
图7 混合对照品溶液(A、C)和供试品溶液(B、D)的UPLC色谱图Fig. 7 UPLC chromatograms of mixed control(A/C)and sample(B/D)
2.3.2 色谱条件 在324 nm测定新绿原酸、隐绿原酸和绿原酸;在221 nm测定白术内酯Ⅲ和白术内酯Ⅱ,余同“2.1.1”项指纹图谱色谱条件。
2.3.3 配制对照品溶液 以50%甲醇为溶媒制成每1 mL含3、6、10、10、8µg的新绿原酸、隐绿原酸、绿原酸、白术内酯Ⅲ和白术内酯Ⅱ的溶液。
2.3.4 配制样品溶液 同“2.1.3”项样品溶液配制方法。
2.3.5 线性关系考察 以50%甲醇为溶媒配制成每1 mL含14.562、2.602、30.153、32.012、25.392μg的新绿原酸、隐绿原酸、绿原酸、白术内酯Ⅲ和白术内酯Ⅱ的储备液。精密量取储备液15.0、10.0、5.0和1.0 mL,分别置20 mL容量瓶中,加50%甲醇定容至刻度,得系列浓度培养液后,按“2.3.2”项进样测定,以峰面积为纵坐标(Y),对照品浓度为横坐标(X,µg/mL),绘制标准曲线,考察结果见表4。
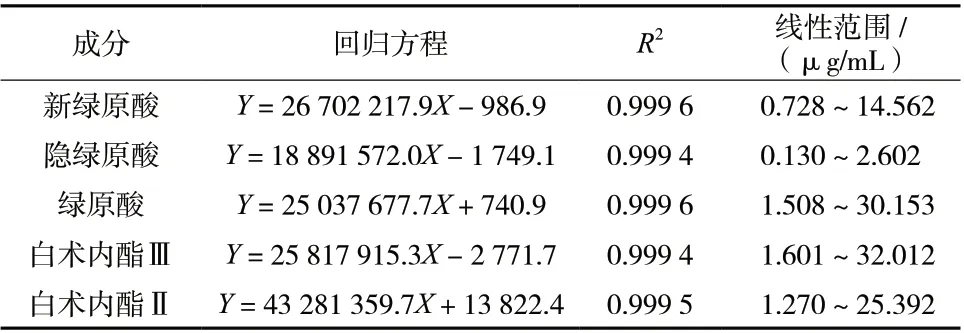
表4 白术中5种化学成分线性关系考察结果Tab. 4 Results of linear relation of constents of AMR
2.3.6 精密度试验 按“2.1.3”项配制白术样品(S1)溶液后,按“2.3.2”项连续进样测定6次,计算新绿原酸、隐绿原酸、绿原酸、白术内酯Ⅲ和白术内酯Ⅱ含量,RSD分别为0.59%、0.62%、0.48%、0.89%和0.57%,表明仪器具有良好的精密度。
2.3.7 稳定性试验 按“2.1.3”项配制白术样品(S1)溶液后,按“2.3.2”项在0、2、4、8、12、24 h进样测定,计算新绿原酸、隐绿原酸、绿原酸、白术内酯Ⅲ和白术内酯Ⅱ的含量,RSD分别为0.89%、0.76%、0.59%、0.63%和0.84%,表明在24 h内供试品溶液具有良好的稳定性。
2.3.8 重复性试验 按“2.1.3”项配制白术样品(S1)溶液后6份,按“2.3.2”项进样测定,计算新绿原酸、隐绿原酸、绿原酸、白术内酯Ⅲ和白术内酯Ⅱ的含量,RSD分别为1.58%、1.89%、1.26%、1.67%和1.98%,表明该方法具有良好的重复性。
2.3.9 加样回收率试验 取白术样品(S1)粉末6份,每份0.5 g,加入混合对照品溶液(以50%甲醇为溶媒制成每1 mL含1.728 µg、3.648 µg、7.009 µg、5.682 µg和4.082 µg的新绿原酸、隐绿原酸、绿原酸、白术内酯Ⅲ和白术内酯Ⅱ的溶液)25 mL,余同按“2.1.3”项配制回收率样品溶液,按“2.3.2”项进样测定,计算各成分的回收率和RSD,见表5,回收率平均值均大于90%,RSD均小于3%,说明该方法测得的结果准确。
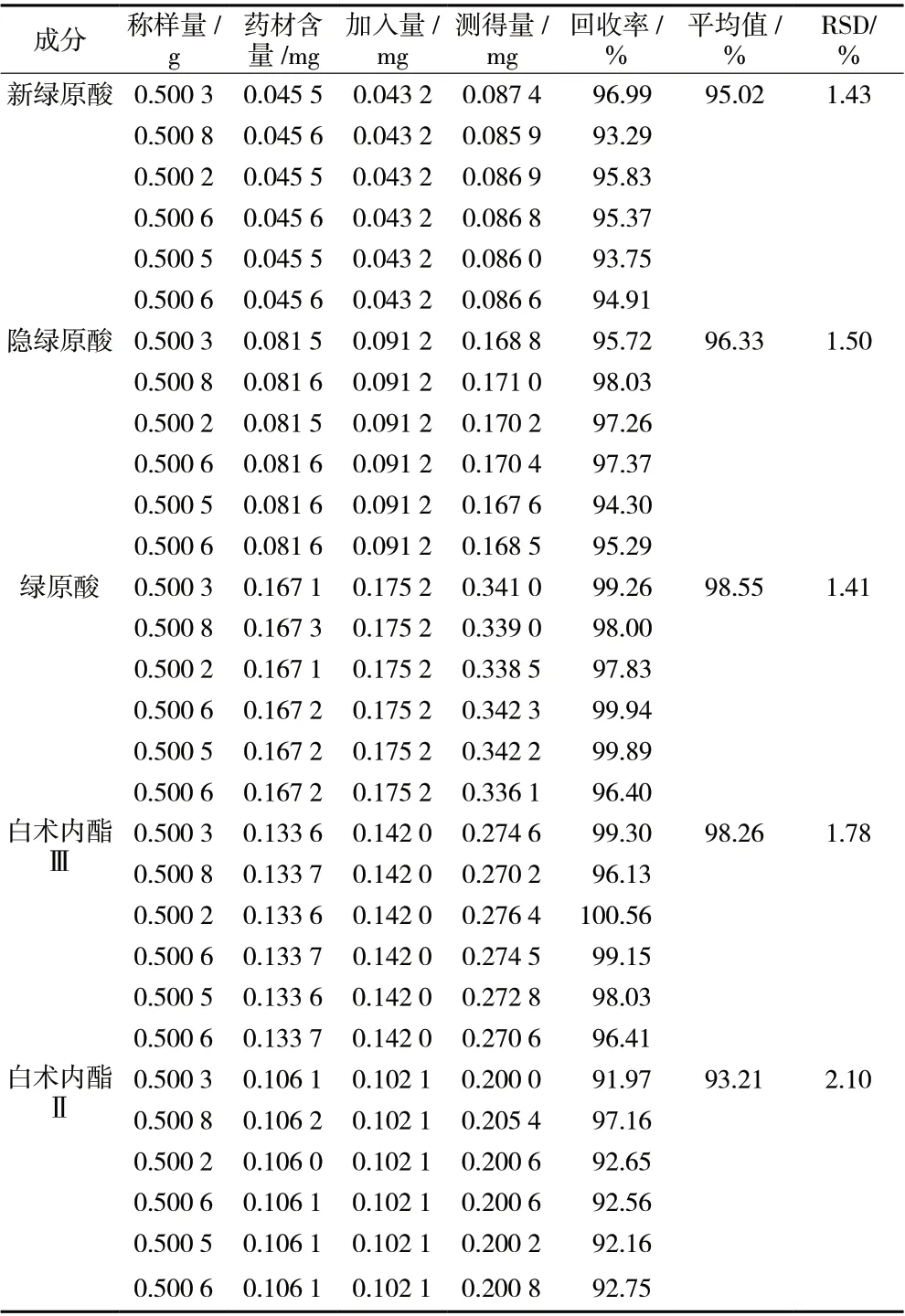
表5 加样回收率试验结果(n = 6)Tab. 5 Results of recovery standard addition(n = 6)
2.3.10 样品测定 按“2.1.3”项配制16批白术样品溶液后,按“2.3.2”项测定,计算其含量,见表6。
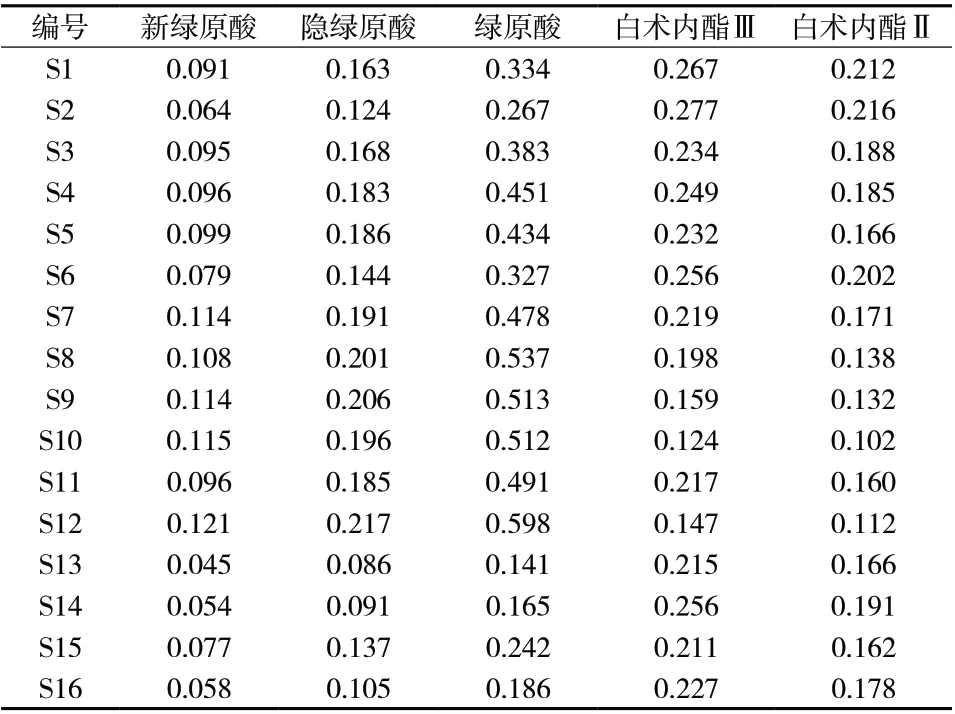
表6 16批白术中5种化学成分含量测定结果(mg/g,n = 2)Tab. 6 Determination of five chemicals of 16 batches of AMR(mg/g,n = 2)
3 讨论
本试验考察了不同提取溶剂、提取方式、提取时间和料液比对各成分提取效率的影响,最终确定供试品溶液的制备方法为以50%甲醇按料液比1.0 g∶25 mL回流提取30 min。在指纹图谱研究中,通过与对照品的保留时间及PDA光谱图对比,指认出新绿原酸、隐绿原酸、绿原酸、3,5-O-二咖啡酰基奎宁酸、4,5-O-二咖啡酰基奎宁酸、白术内酯Ⅲ、白术内酯Ⅱ共7个成分。通过比较不同波长条件下各峰的响应值、分离度、对称性及拖尾因子等参数,最终选择221 nm作为指纹图谱的检测波长。
采用UPLC法对16批白术进行分析检测后,通过SPSS 25.0聚类分析,结合SIMCA14.1绘图软件,对21个共有峰的峰面积进行主成分分析,结果均将16批白术聚为3类,分类符合产地规律。主成分分析提取得到的前5个主成分的累积贡献率达到88.32%,其中白术内酯Ⅲ和白术内酯Ⅱ在主成分1中有明显贡献值,鉴于白术内酯类成分为白术的主要活性成分,因此将其纳入含量测定指标中。偏最小二乘判别分析以VIP值为筛选标准得到5个差异性标志成分,其中有3个峰被指认出,分别为绿原酸、隐绿原酸和新绿原酸,为含量测定指标的选择提供参考。
4 结论
本研究通过化学计量学结合超高效液相色谱法的分析方式,对白术的质量控制提供了一种评价思路,该方法表明白术质量与产地之间具有一定的相关性。本次研究收集的白术药材有一年生和两年生区别,但通过以上试验分析并未发现不同生长年限的白术质量存在差异,对于白术生长年限的研究或可以通过增大样本量、收集更长生长时间的白术药材加以研究,以期为白术质量控制和临床应用提供参考依据。

