额日赫木-8散HPLC指纹图谱建立及秦皮乙素测定
徐 楠, 赵宇郁, 张 伟, 尚亚倩, 马桂芝*, 滕 亮
(1.新疆医科大学药学院,新疆 乌鲁木齐 830011;2.广东药科大学医药商学院,广东 广州 510006;3.新疆医科大学第一附属医院药学部,新疆 乌鲁木齐 830054)
额日赫木-8散为新疆维吾尔自治区博州蒙医医院制剂,出自《四部医典》,又称清热八味散,由红花、黄连、紫花地丁、麦冬、人工牛黄、檀香、瞿麦、石膏、冰糖组成[1],具有清热解毒之效,可增强正常小鼠免疫反应[2],联用三臣丸对小儿上呼吸道感染高热效果显著[3],还可作为SARS治疗的辅助用药[4]。
目前,额日赫木-8散质量标准仅有性状描述,无法全面反映其整体质量状况,也不能保证其临床应用安全性和有效性;相关质量控制文献也主要集中在TLC鉴别[5]和有效成分定量测定[6-9]方面,无法准确全面评价该制剂质量。中药指纹图谱能系统全面地反映中药品质的真实性、一致性、稳定性,结合化学模式识别可全面获得其质量信息,故在中药制剂的质量控制中被广泛应用[10-12]。
本实验建立了额日赫木-8散HPLC指纹图谱,并结合化学模式识别评价不同批次样品的一致性和稳定性,找出差异性成分。同时,采用2020年版《中国药典》中《药品质量标准分析方法验证指导原则》相关要求,建立主要药材紫花地丁中秦皮乙素含量的测定方法,以期为提高全方质量控制水平奠定基础。
1 材料
1.1 仪器 LC-20AD高效液相色谱仪,配置SPD-M20A 230 V光电二极管阵列紫外可见光检测器、πNAP COSMASIL C18色谱柱(4.6 mm×250 mm,5 μm)(日本岛津公司);New Classic MF分析天平(瑞士梅特勒-托利多公司,0.01 mg);KQ5200DE数控超声波清洗器(昆山市超声仪器有限公司,功率250 W,频率50 kHz);Milli-Q艾柯超纯水仪(美国密理博公司);Agilent SB C18色谱柱(4.6 mm×250 mm,5 μm)(美国安捷伦科技公司)。
1.2 试剂与药物 檀香(批号170805)、红花(批号170308)、黄连(批号170518)、紫花地丁(批号170618)、麦冬(批号160116)、人工牛黄(批号160101)、瞿麦(批号170716)、石膏(批号170718)、冰糖(批号141620)均由新疆博州蒙医医院提供,经新疆医科大学第一附属医院刘冰主任中药师鉴定为正品。羟基红花黄色素A对照品(批号MUST17082905,纯度≥98%)购自成都曼思特生物科技有限公司;秦皮乙素对照品(批号C25J7Y18390,纯度≥98%)、阿魏酸对照品(批号20130301,纯度≥98%)均购自上海源叶生物科技有限公司。额日赫木-8散(新疆博州蒙医医院,批号20170915、20171201、20180208、20180410,供含量测定用;批号20180822、20180917、20181024、20181119、20181213、20190104、20190225、20190318、20190423、20190526,编号S1~S10,供指纹图谱建立用)。甲醇为色谱纯(美国Sigma公司);其他试剂均为分析纯(天津永晟精细化工有限公司)。
2 方法与结果
2.1 HPLC指纹图谱建立
2.1.1 溶液制备
2.1.1.1 对照品溶液 精密称取秦皮乙素、羟基红花黄色素A、阿魏酸对照品适量,60%甲醇溶解,即得。
2.1.1.2 供试品溶液 精密称取本品适量,置于25 mL量瓶中,精密加入60%甲醇20 mL,超声处理20 min,取出,放冷,60%甲醇定容至刻度,摇匀,静置,取上清液,0.22 μm微孔滤膜过滤,取续滤液,即得。
2.1.1.3 阴性样品溶液 按处方比例及制备工艺,精密称取除紫花地丁外的其余药材,按“2.1.1.2”项下方法制备,即得。
2.1.2 色谱条件 Agilent SB C18色谱柱(4.6 mm×250 mm,5 μm);流动相0.1%磷酸(A)-甲醇(B),梯度洗脱(0~20 min,85%~75%A;20~25 min,75%~70%A;25~30 min,70%A;30~40 min,70%~80%A;40~45 min,80%~71%A;45~68 min,71%A;68~85 min,71%~72%A;85~100 min,72%~75%A;100~105 min,75%~85%A;105~110 min,85%A);体积流量1.0 mL/min;柱温30 ℃;检测波长345 nm;进样量10 μL。
2.1.3 方法学考察
2.1.3.1 精密度试验 精密称取本品1 g,按“2.1.1.2”项下方法制备供试品溶液,在“2.1.2”项色谱条件下进样测定6次,以4号峰(秦皮乙素)为参照,测得各共有峰相对保留时间、相对峰面积RSD均小于3%,表明仪器精密度良好。
2.1.3.2 重复性试验 精密称取本品1 g,共6份,按“2.1.1.2”项下方法制备供试品溶液,在“2.1.2”项色谱条件下进样测定,以4号峰(秦皮乙素)为参照,测得各共有峰相对保留时间、相对峰面积RSD均小于3%,表明该方法重复性良好。
2.1.3.3 稳定性试验 精密称取本品1 g,按“2.1.1.2”项下方法制备供试品溶液,于0、1.5、3、4.5、6、7.5、9 h在“2.1.2”项色谱条件下进样测定,以4号峰(秦皮乙素)为参照,测得各共有峰相对保留时间、相对峰面积RSD均小于3%,表明溶液在9 h内稳定性良好。
2.1.4 图谱生成 取10批样品,按“2.1.1.2”项下方法制备供试品溶液,在“2.1.2”项色谱条件下进样测定,采用“中药指纹图谱相似度评价软件”(2012.13723版本),以S1为参照图谱,采用中位数法,经多点校正后得到指纹图谱共有模式,选择分离度和重复性良好、特征明显的17个色谱峰作为共有峰,生成对照图谱,见图1~2,相似度见表1,发现均大于0.9,提示各批次之间成分一致性理想。

图1 10批样品HPLC指纹图谱
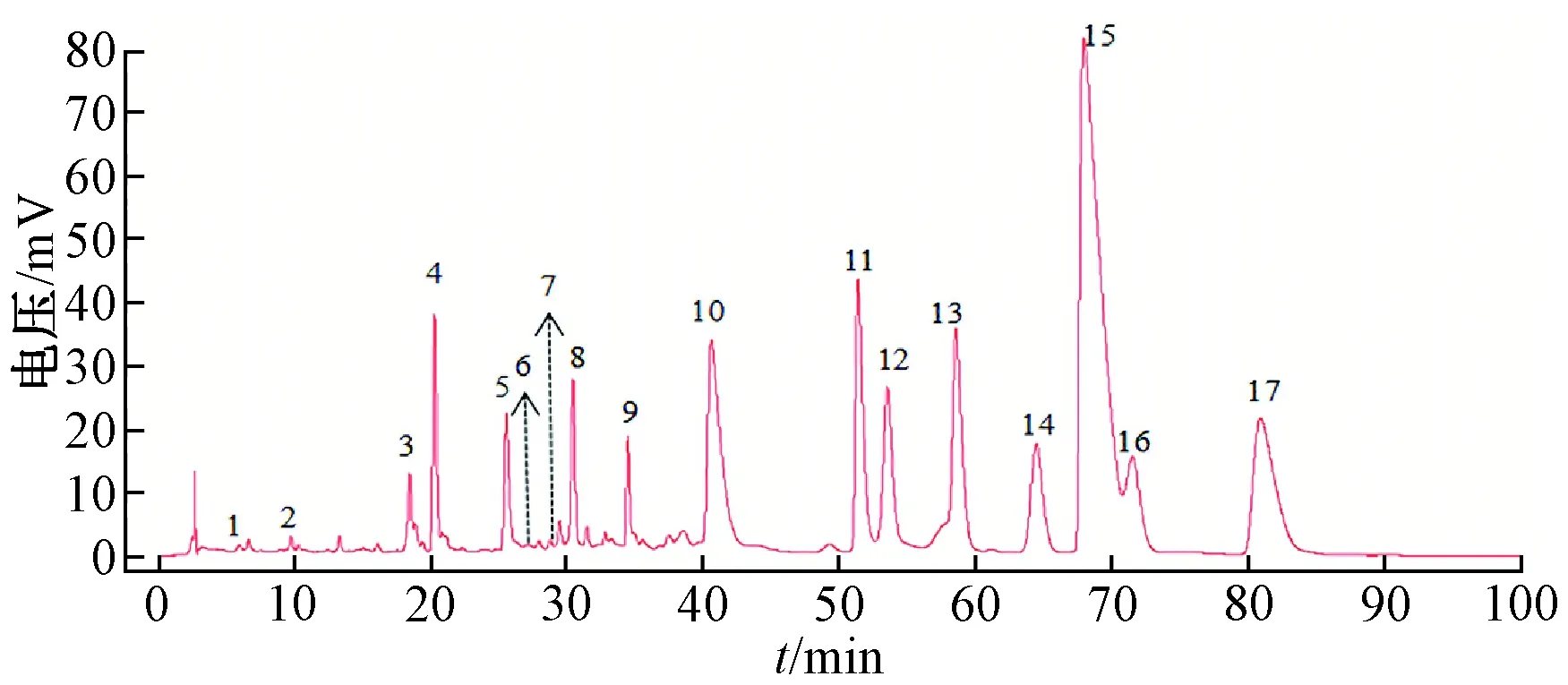
图2 共有峰对照图谱
选择保留时间稳定、峰面积适宜、分离度和对称性良好的4号峰(秦皮乙素峰)作为参照,测得各共有峰相对保留时间RSD均小于0.45%,表明其出峰时间较稳定,但其相对峰面积RSD相差较大,表明存在一定批间差异。
2.1.5 色谱峰归属 按“2.1.1.2”项下方法制备供试品溶液,在“2.1.2”项色谱条件下进样测定,通过与对照品色谱图保留时间和全波长紫外扫描图谱比对,发现4号峰为秦皮乙素,5号峰为羟基红花黄色素A,9号峰为阿魏酸,见图3。

1.秦皮乙素 2.羟基红花黄色素A 3.阿魏酸1. esculeyin 2. hydroxylaffin A 3. ferulic acid
2.2 化学模式识别
2.2.1 聚类分析 采用组间平均联接法,以平方Euclidean距离为测度,对10批样品共有峰峰面积进行聚类分析[13-16],结果见图4。由此可知,类间距为5时,各批样品聚为3类,S2~S9为一类,S1、S10各一类;不同批次样品之间各成分含量存在差异,可能是由于生产工艺及原材料采收、加工、产地所致[12-15]。

图4 10批样品聚类分析树状图
2.2.2 主成分分析 对10批样品共有峰峰面积进行因子分析,结果见表2。由此可知,3个主成分累积方差贡献率为91.677%,可代表样品大部分信息;以绝对值大于0.5为重要性标准,4号峰(秦皮乙素)、9号峰、7号峰对2个及2个以上主成分的贡献较大。
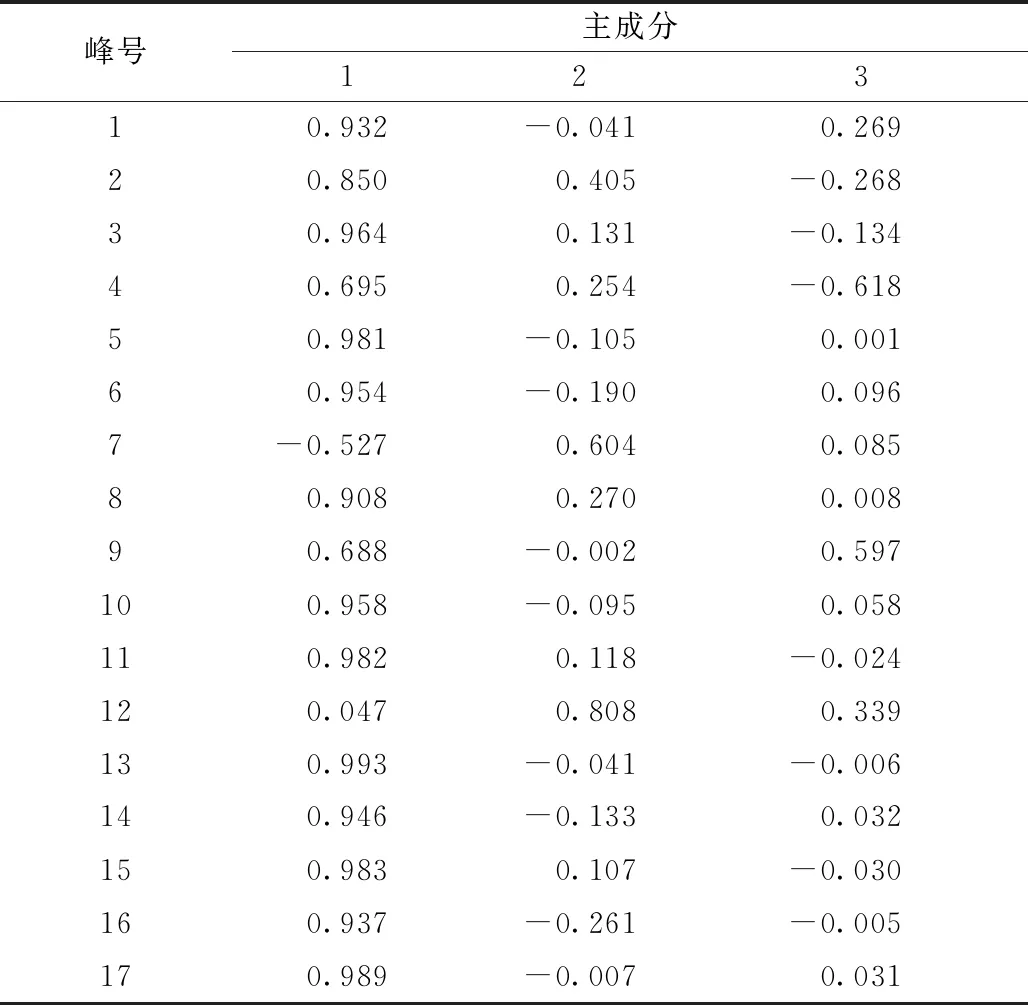
表2 主成分因子载荷矩阵
根据文献[16]报道计算10批样品综合得分F,公式为F=0.529F1+0.369F2+0.102F3,结果见表3。

表3 10批样品综合得分及排序
采用 SIMICA 14.1软件进行主成分分析,结果见图5~6。由此可知,质量参数(R2X)、预测度(Q2)均大于0.5,表明模型预测性较好[13-17];前2个主成分贡献率最大,累积贡献率达85.568%。另外,图6所得结果与表2一致。
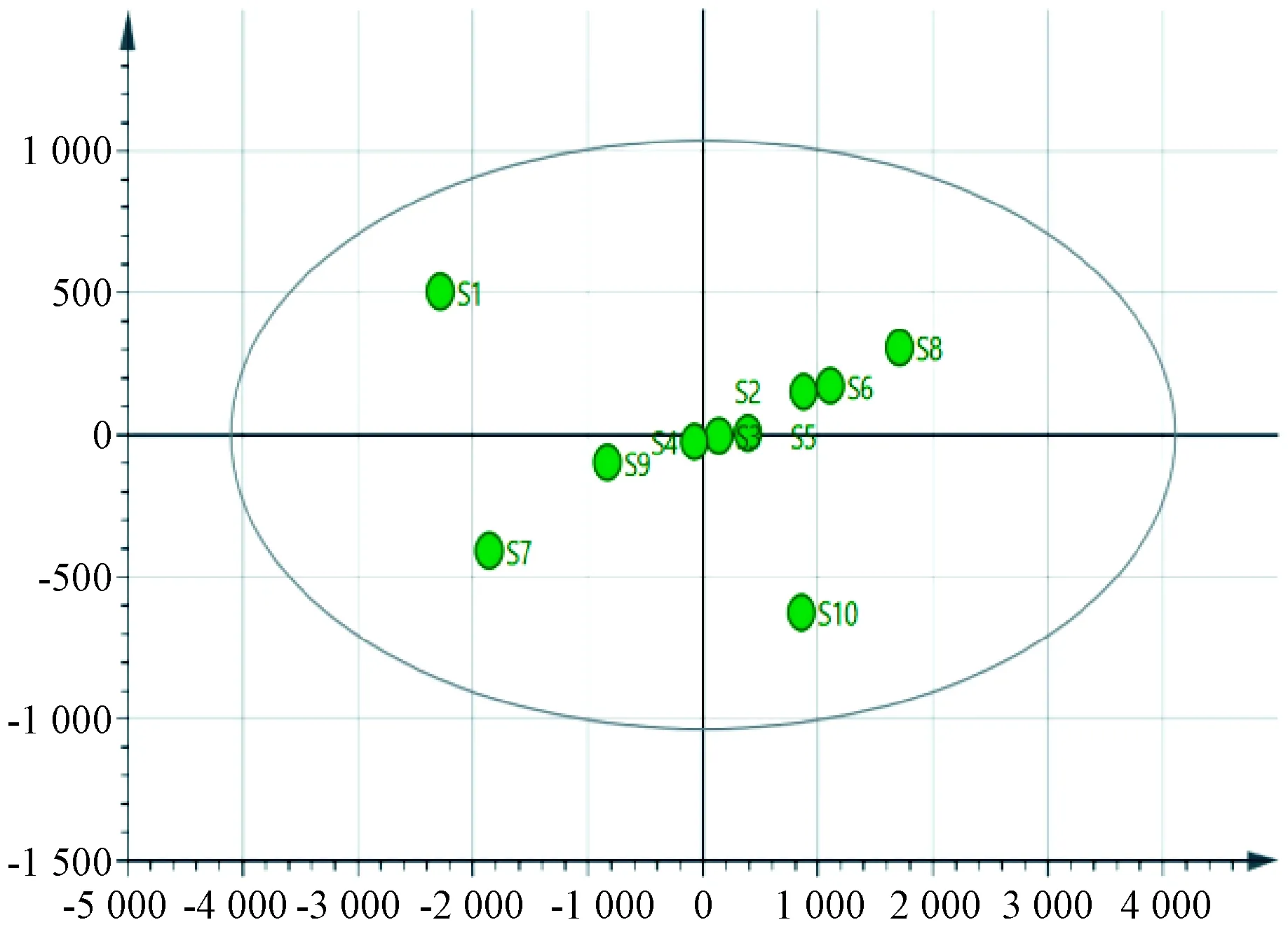
图5 主成分分析散点得分图
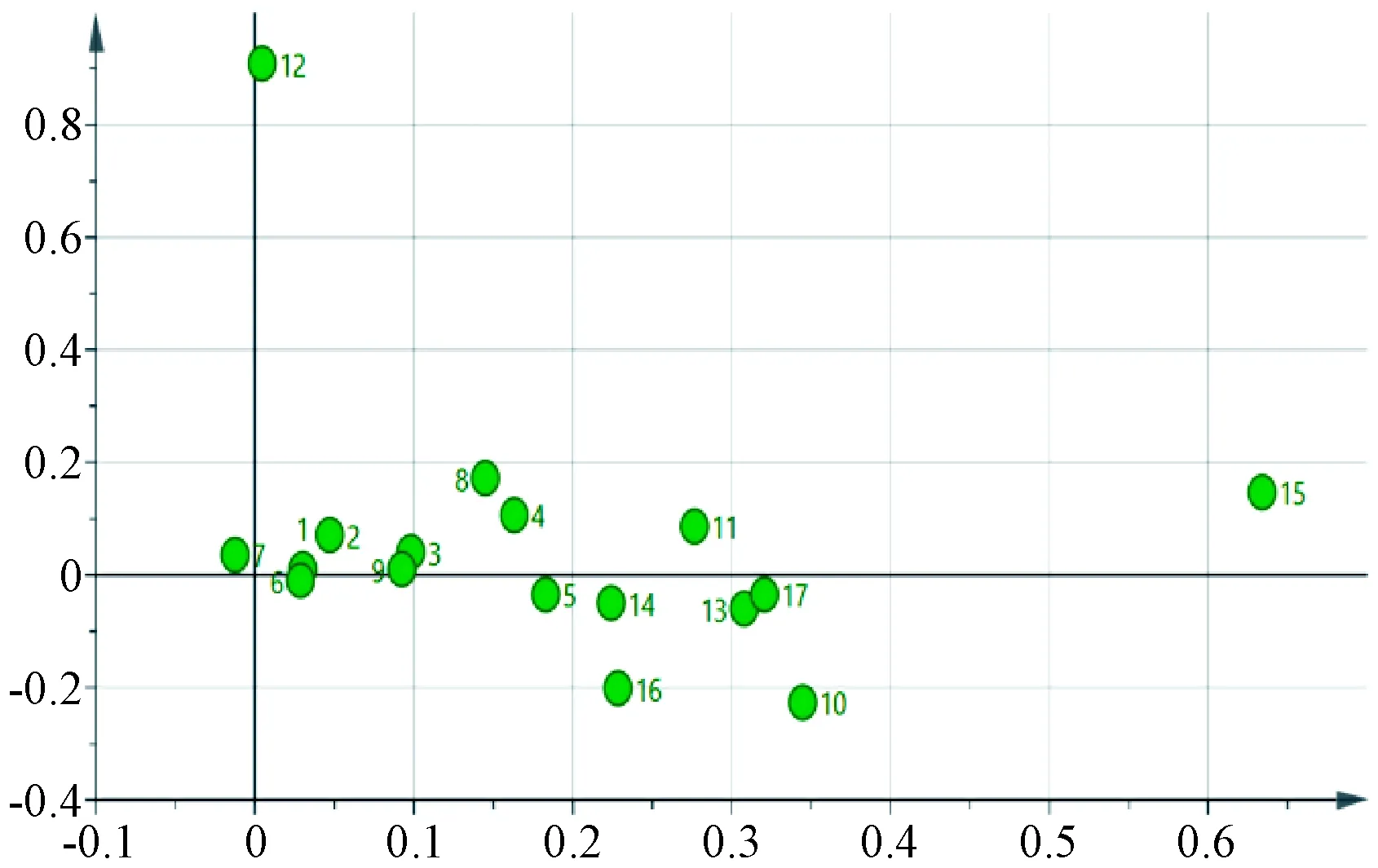
图6 主成分分析载荷图
2.2.3 偏最小二乘判别分析(PLS-DA) 将10批样品共有峰峰面积导入SIMCA 14.1软件,采用PLS-DA模型,经Permutatons验证,得到Q2为负值,表明模型可靠,不存在过度拟合现象,建模成功[12,14-15]。得分散点图见图7,可知相似度高的样品聚合为一类,与主成分分析结果基本一致。载荷图见图8,距离原点越远的点权重值越大,在区分样本中的作用越大。图9显示,在95%置信区间内4号峰(秦皮乙素)、10号峰、12号峰、15号峰的变量重要性投影值(VIP值)均大于1,为引起批次间差异的主要标志性成分。

图7 偏最小二乘判别分析散点得分图

图8 偏最小二乘判别分析载荷图

图9 偏最小二乘判别分析VIP值图
2.3 秦皮乙素含量测定 主成分分析、偏最小二乘判别分析显示,4号峰(秦皮乙素)变化既可影响质量评分,也是引起批次差异的主要标志性成分,故对其含量进行测定[17-19]。
2.3.1 色谱条件 πNAP COSMASIL C18(4.6 mm×250 mm,5 μm)色谱柱;流动相甲醇(A)-0.1%磷酸(B),梯度洗脱(0~28 min,75%B;29~41 min,45%B;42~51 min,60%B;52~60 min,75%B);体积流量1.0 mL/min;柱温25 ℃;检测波长345 nm;进样量10 μL,色谱图见图10。由此可知,秦皮乙素色谱峰与其他成分色谱峰达到基线分离,分离度大于1.5,理论塔板数大于7 000,阴性无干扰,表明该方法专属性良好。

1.秦皮乙素1.aesculetin
2.3.2 方法学考察
2.3.2.1 线性关系考察 精密吸取“2.1.1.1”项下对照品溶液,依次倍量稀释,得到系列质量浓度,分别精密吸取10 μL,在“2.3.1”项色谱条件下进样测定。以对照品峰面积(Y)对其质量浓度(X)进行回归,得方程为Y=30 415X-2 470.1(r=0.999 9),在0.414 1~106 μg/mL范围内线性关系良好。
2.3.2.2 精密度试验 精密称取本品1.0 g,按“2.1.1.2”项下方法制备供试品溶液,在“2.3.1”项色谱条件下进样测定6次,测得秦皮乙素峰面积RSD为0.28%,表明仪器精密度良好。
2.3.2.3 稳定性试验 精密称取本品1.0 g,按“2.1.1.2”项下方法制备供试品溶液,常温下于0、2、4、6、8、12、14、16、18、20、22、24 h在“2.3.1”项色谱条件下进样测定,测得秦皮乙素峰面积RSD为0.70%,表明溶液在24 h内稳定性良好。
2.3.2.4 重复性试验 精密称取本品1.0 g,按“2.1.1.2”项下方法平行制备6份供试品溶液,在“2.3.1”项色谱条件下进样测定,测得秦皮乙素含量RSD为0.58%,表明该方法重复性较好。
2.3.2.5 加样回收率试验 精密称取6份秦皮乙素含量已知的本品1.0 g,加入340 μg/mL对照品溶液,按“2.1.1.2”项下方法制备供试品溶液,在“2.3.1”项色谱条件下进样测定,计算回收率,结果见表4。

表4 秦皮乙素加样回收率试验结果(n=6)
2.3.3 样品含量测定 精密称取4批本品各1.0 g,每批3份,按“2.1.1.2”项下方法制备供试品溶液,在“2.3.1”项色谱条件下进样测定,计算含量,结果见表5。
2.3.4 限度确定 根据表5结果,结合紫花地丁采收季节、贮藏条件与时间、制剂生产水平,建议每1 g额日赫木-8散中含秦皮乙素不得低于321.2 μg/g。
3 讨论
3.1 色谱柱选择 预实验发现,Agilent SB C18色谱柱可实现更多色谱峰的较好分离,符合指纹图谱宏观研究目的,故本实验选择其进行额日赫木-8散HPLC指纹图谱研究。另外,πNAP C18色谱柱虽然分析时间相对较长,但秦皮乙素分离度良好,可能与其硅胶固定相上键合的萘乙基有关,故本实验选择其进行各成分含量测定。
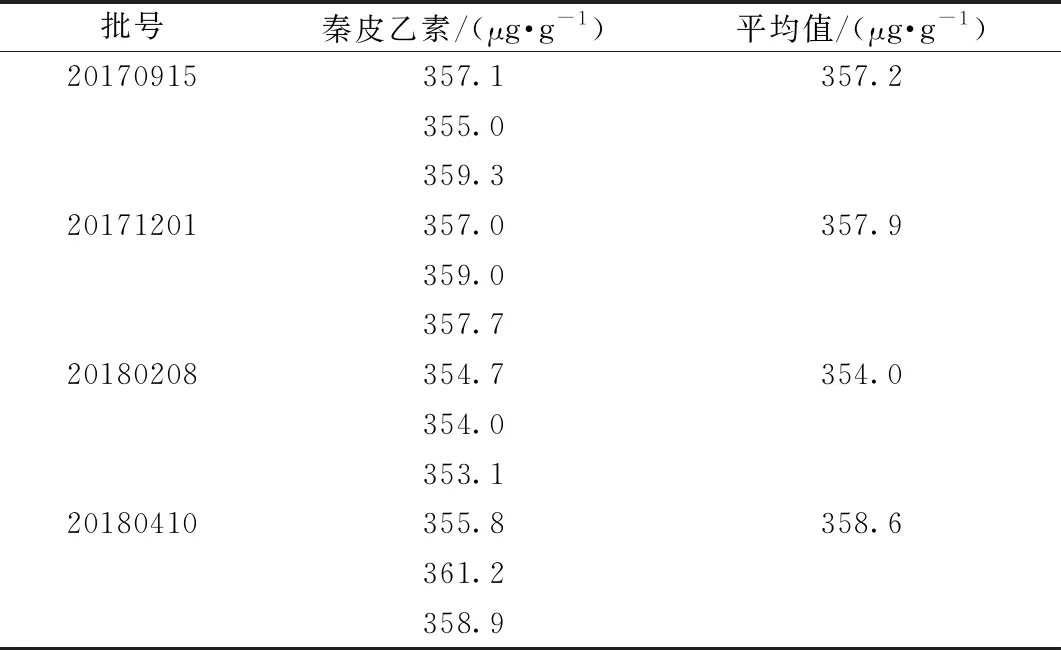
表5 秦皮乙素含量测定结果(n=3)
3.2 化学模式识别与含量测定研究 本实验采用3种化学模式识别方法[20-21],其中聚类分析表明,当类间距为5时,10批样品聚为3类,提示各批样品之间虽然相似度较高,但却仍存在差异;PCA表明,3个主成分的累积方差贡献率为91.677%,可代表样品大部分信息,但与聚类分析结果存在一定差异,可能与评价指标[13]不同有关;通过比较主成分和差异性质量标志物,确认秦皮乙素(4号峰)为共同标志化合物。秦皮乙素具有抗炎、抗菌、镇痛、抗氧化、抗肿瘤、免疫调节等作用[22-23],与额日赫木-8散传统功效密切相关,故选择该成分作为含量测定指标。
4 结论
本实验建立额日赫木-8散HPLC指纹图谱,并测定秦皮乙素含量,该方法简便准确,可为控制全方质量提供参考。

