2型糖尿病周围神经病变的影响因素分析
万芳
(九江市第一人民医院 内分泌科,江西 九江 332000)
2型糖尿病周围神经病变(diabeitc Perip heral neuropathy,DPN)是糖尿病的主要并发症,导致糖尿病患者发病和死亡的最重要和最常见并发症之一,且随着我国人口老龄化及生活方式改变,发病率呈逐年上升趋势[1]。糖尿病周围神经病变是糖尿病足重要的始动因素,在糖尿病病程中可逐渐出现,病情反复发作,也是导致患者截肢或死亡的最常见病因[2-3]。该病发病机制尚未完全阐明,有几种病理生理机制被认为有助于DPN,有证据表明,高血糖引起的细胞损伤是最重要的促成因素。其他因素,如肥胖、血脂异常、神经营养支持和胰岛素信号传导受损以及微血管疾病,会导致氧化应激、线粒体功能障碍和炎症[4]。本研究通过对2型糖尿病周围神经病变的影响因素进行分析,为DPN个体化的临床诊疗提供新的思路。
1 资料与方法
1.1 一般资料 收集2021年1月至2022年5月在我院内分泌科住院的181例T2DM患者,糖尿病诊断均符合1999年WHO糖尿病诊断标准。DPN诊断标准:即有明确的糖尿病病史;在确诊糖尿病时或之后出现神经病变;临床症状和体征与DPN表现相符;以下有2项或以上者:①温度觉异常。②尼龙丝检查显示,足部感觉减退或消失。③振动觉异常。④踝反射消失。⑤神经传导速度(NCV)检查提示有2项或以上减慢。排除合并有严重心、脑、肝、肾疾病患者;排除感染、血液性疾病(包括贫血)、免疫性疾病及肿瘤;排除其他原因引起的周围神经病变。根据患者是否并发DPN将其分为观察组(T2DM合并DPN,n=75)与对照组(T2DM未合并DPN组,n=106)。知情同意并签署知情同意书,本研究已获得我院伦理委员会的批准(伦理号:JJSDYRMYY-YXLL-2022-230)。
1.2 研究方法 记录患者的一般资料,包括年龄、性别、病程、BMI指数、SBP、DBP等指标;患者抽取清晨空腹时静脉血(抽血前禁食水10~12 h)进行血生化及常规检查,包括WBC、UACR、Scr、SUA、TG、LDL-C、HDL-C、HbA1c、FPG、2hPG、FC-P、2hC-P等指标。稳态模型评估胰岛素抵抗指数(HOMA-IR)=空腹血糖×空腹胰岛素/22.5,其中空腹血糖的单位是mmol/L,空腹胰岛素是μU/mL;血NLR=中性粒细胞绝对值/淋巴细胞绝对值;LAGE(最大血糖波动幅度)=日内最大和最小血糖值之差;PPGE(餐后血糖波动幅度)=每餐餐后的血糖值减去餐前的血糖值,将三餐的这3个差值求和,然后再除以3,算出平均值;SDBG(血糖水平标准差)=一日内多点血糖的标准差。肌电图应用丹迪Keypoint-2肌电图仪检测。
1.3 统计学方法 采用SPSS21.0统计学软件对数据进行分析。计量资料进行正态性检验和方差齐性检验,符合正态分布的计量资料以均数±标准差()表示,组间比较采用独立样本t检验,不符合正态分布的计量资料以中位数及四分位数[M(P25,P75)]表示,采用Wilcoxon秩和检验;计数资料以构成比(%)表示,采用χ2检验。采用二元logistic回归分析DPN患病的影响因素。以P<0.05表示差异有统计学意义。
2 结果
2.1 两组患者的资料比较 病程、BMI指数、收缩压、糖化血红蛋白、空腹胰岛素、空腹C肽、HOMAIR、TG、HDL-C、Scr、SUA、FBG、LAGE、PPGE、SDBG、性别等比较,差异无统计学意义(P>0.05)。观察组年龄、NLR高于对照组,餐后2 h胰岛素、2 h C-P、DBP舒张压水平明显低于对照组,差异有统计学意义(P<0.05)。见表1。
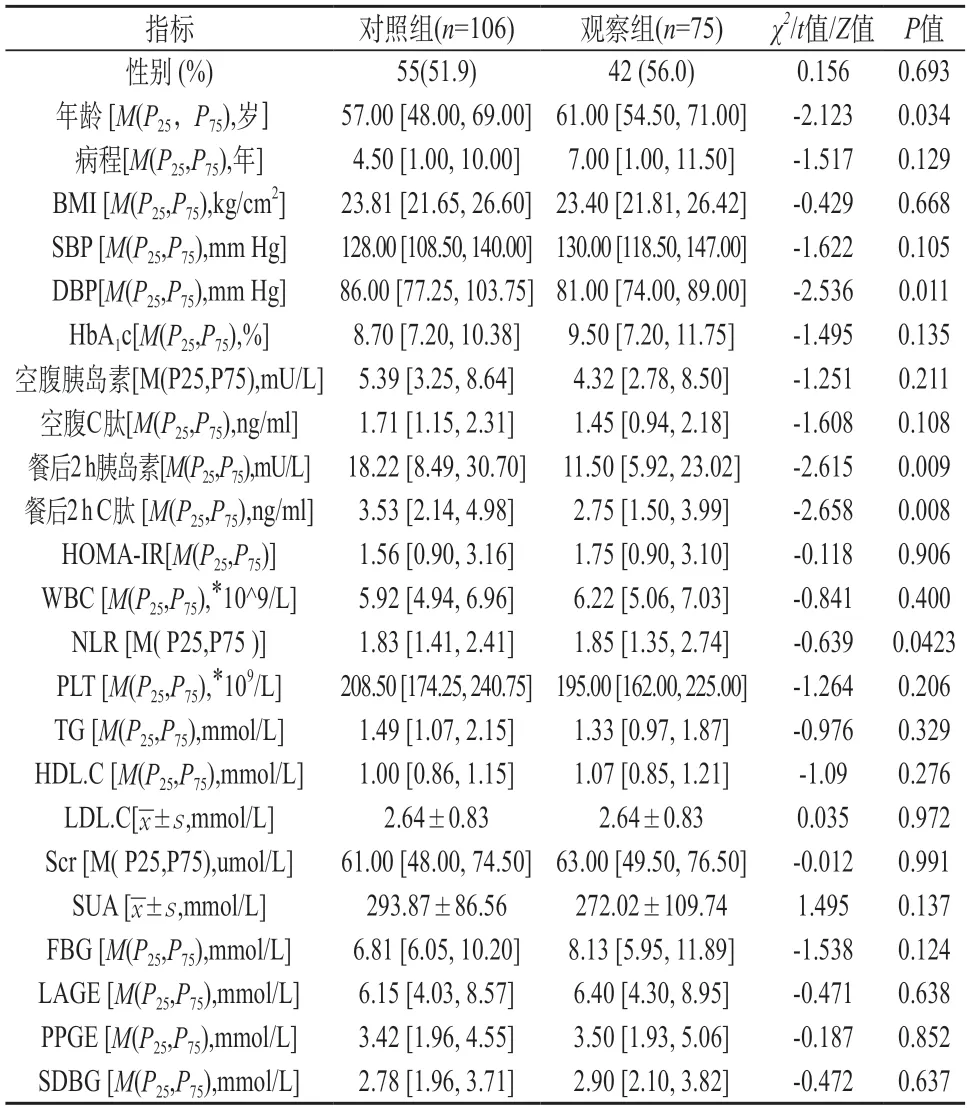
表1 两组一般资料比较
2.2 Logistic 回归分析 Logistic 回归分析结果显示,年龄、NLR是发生DPN的危险因素。见表2。
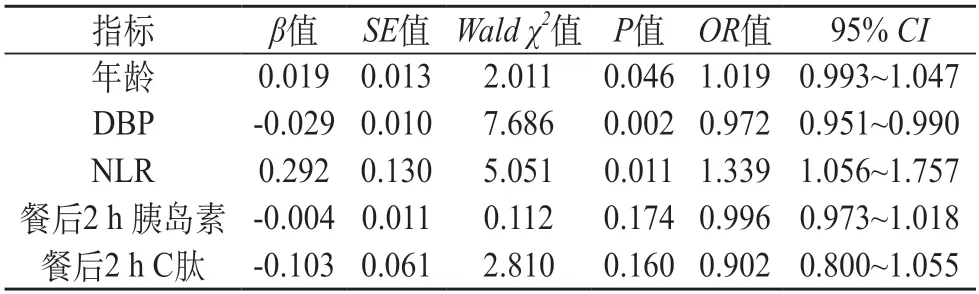
表2 T2DM发生DPN的危险因素
3 讨论
目前全世界约有5.37亿人患有糖尿病,使其成为21世纪全球最大的流行病[5]。糖尿病最常见的慢性并发症之一是DPN,它是指在排除其他原因的情况下,糖尿病患者出现与周围神经功能障碍相关的症状。在罹患糖尿病的最初几年,5.00%~10.00%的患者会出现神经病变,20年后有6.00%~70.00%的患者会出现某种形式的糖尿病周围神经病变[6]。患有糖尿病性感觉神经病变的患者足部溃疡和截肢的风险增加25.00%。与患有糖尿病但没有周围神经病变的人相比,患有糖尿病神经病变的人的3年生存率降低了约20.00%[7]。
DPN的临床表现各不相同[8]。有文献显示,仅有25.00%~30.00%的DPN患者会经历疼痛[9],而多达50.00%的DPN患者可能没有任何症状[10]。DPN伴有疼痛的患者可能会出现刺痛感、麻木感、异常性疼痛以及足部或手部刺痛等症状[11]。DPN的经典临床特征是大小神经纤维的进行性损伤。DPN的疼痛通常以特定的对称、远端到近端的模式发生,从脚趾尖开始向近端进展。具体症状将取决于大与小纤维是否受到影响。小纤维容易产生灼热、电击、刺伤、痛觉过敏和异常性疼痛,而大纤维会导致麻木、刺痛和平衡不良。下肢感觉丧失使DPN患者的足部和腿部受伤、溃疡和感染的风险更高,反过来又增加了DPN患者截肢的风险[12]。T2DM合并DPN患者由于缺乏感觉和疼痛,特别容易患足部感染和溃疡[8]。
本研究结果提示,观察组年龄、NLR高于对照组,餐后2 h胰岛素、餐后2 hC肽水平明显低于对照组,差异有统计学意义(P<0.05)。Logistic相关性分析提示:年龄、NLR是发生DPN的危险因素。
T2DM及其并发症已被证明是一种炎症性疾病和免疫系统功能障碍。研究表明,慢性炎症有助于T2DM患者DPN的发生和发展。DPN的周围神经损伤涉及多种不同机制,其中关键作用是氧化应激、炎症和线粒体功能障碍[13]。糖尿病中增加的葡萄糖代谢导致多元醇、己糖胺和蛋白激酶C途径的过度激活和糖基化终产物形成和(或)受体激活。血脂异常和高血糖进一步诱导并促炎细胞因子和趋化因子的释放,从而导致炎症介导和免疫介导的神经毒性。微血管功能障碍和下游DNA降解、内质网应激和线粒体功能障碍最终导致神经元细胞死亡[14]。很多非感染性疾病都存在着炎症、氧化应激反应。一般而言,由各种途径激活和维持的炎症损伤在糖尿病及其并发症的发展中起重要作用。中性粒细胞/淋巴细胞(NLR)是目前国外新提出的炎性因子,代表慢性炎症状态的两个主要成分(高中性粒细胞和低淋巴细胞)的组合。NLR代表体内中性粒细胞和淋巴细胞的平衡。中性粒细胞与炎性反应密切相关,淋巴细胞反映免疫调节途径[15]。它们可以反映全身炎症,以及先天免疫反应(由中性粒细胞介导)和适应性免疫反应(由淋巴细胞介导)[16]。高血糖引起的非特异性炎性反应可能导致外周血细胞水平的变化,这可能解释了异常的NLR值。一些临床研究提出,NLR值与DM及其并发症有关。Duman等[17]的研究表明,NLR与年龄、空腹血糖和HbA1c密切相关。日本的一项研究表明,NLR可能是评估具有较高蛋白尿程度的糖尿病患者的潜在因素,表明NLR可能预测微血管并发症的存在[18]。已有研究表明NLR与糖尿病及糖尿病视网膜病变、糖尿病肾病关系密切[19-21]。
随着年龄的增长和病程的延长,胰岛β细胞逐渐减少,从而导致糖尿病的相关并发症。由于年龄的增长以及遗传和环境因素的影响,中老年人已成为糖尿病的高危人群。虽然DPN的机制仍不清楚,但已经提出炎症、氧化应激和线粒体功能障碍是DPN病理变化中涉及的3个主要改变。所有这些变化都与衰老过程有关[22]。在大多数DPN流行病学研究中,年龄作为评估最多的不可改变的危险因素,已被发现与T2DM患者的DPN发病率高度相关[22]。对于糖尿病病程超过25年的老年患者,大约一半患有DPN,这可能与功能障碍和生活质量下降有关[23]。与糖尿病老年人DPN风险增加相关的因素包括女性、糖尿病病程较长、视网膜病变、中风、高血压、血脂异常和足部溃疡病史[24]。另有研究提示中粒细胞计数随年龄呈上升趋势,而淋巴细胞计数呈下降趋势,NLR与年龄呈正相关[25]。本研究提示年龄是糖尿病周围神经病变的危险因素。
综上所述,随着年龄的增长、NLR水平的升高,糖尿病周围神经病变风险增高;年龄、NLR是发生DPN的危险因素。

