天麻素全载药可溶性微针的制备及体外经皮渗透性研究
王舒慧,杨明,朱卫丰,陈丽华,李哲,吴文婷,管咏梅
(江西中医药大学/现代中药制剂教育部重点实验室,江西 南昌 330004)
天麻为兰科植物天麻GastrodiaelataBl.的干燥块茎,含苷类、酚类、甾醇、有机酸及糖类等多种成分,天麻素是天麻的主要活性成分[1]。天麻素药理作用广泛,不良反应小,在预防和治疗中枢神经系统相关疾病中发挥着积极作用。目前,天麻素临床上主要给药方式为口服和注射给药。口服后由于其首过效应明显,生物利用度较低,且有胃肠道不良反应;注射剂由于直接注射入血液中,毒副作用较大且患者耐受性差[2-5]。中枢神经系统疾病的特点是患者精神压力较大,且一般病程较长,往往需要多次给药[6]。将天麻素开发成经皮制剂则更加安全有效,能够将其血药浓度稳定在治疗窗,避免了肝首过效应,减少胃肠道副反应,提高生物利用度;具有一定缓释作用,能够减少给药次数,提高患者顺应性[7-9]。
微针是指多个长度小于1 mm的细小针尖以阵列方式连接在基座上组成的贴片[10]。微针作为一种新型经皮递药技术,能突破皮肤角质层的屏障作用,提供一种将药物输送到皮肤的微创途径,可以使亲水性小分子药物、生物大分子药物以及疫苗等原本不适合于经皮给药的药物通过皮肤吸收[11-12]。其中可溶性微针因其载药量高、生物相容性好、制备简单等优点而备受关注[13-14]。相比于仅针尖或背衬载药可溶性微针,全载药可溶性微针可实现针尖和背衬全方位载药,提高药物的载药量和皮肤透过量,实现药物透皮递送[15]。因此,本研究进行天麻素全载药可溶性微针制备工艺研究,以实现天麻素经皮给药的目的,为天麻素和此类水溶性小分子药物经皮给药提供借鉴。
1 材料
微针模具(台州微芯医药科技有限公司);BS124S电子分析天平(德国Sartorius公司);TGL-20MC台式高速冷冻离心机(湖南湘鑫仪器仪表有限公司);KQ3200E超声波清洗器(昆明市超声仪器有限公司);EPED-ESL-10TH实验室级超纯水器(南京易普易达科技发展有限公司),Agilent 1260高效液相色谱仪(美国Agilent公司);QUANTA 250扫描电子显微镜(美国FEI公司);TA.newplus物性分析仪(美国ISENSO公司);GZX-9140 MBE数显鼓风干燥箱(上海博讯实业有限公司医疗设备厂)。
天麻素对照品(批号:JOT-10053,质量分数98.47%,成都普菲德生物技术有限公司);聚乙烯吡咯烷酮K30(PVP K30,批号:JO629A,大连美仑生物技术有限公司);透明质酸(HA,批号:C12295411,上海麦克林生化科技有限公司);氯化钠注射液(批号:2009220721,辰欣药业股份有限公司);乙腈(色谱级,批号:DW194121201,湖北弗顿科学技术有限公司);超纯水[电阻率:18.2 MΩ·cm(25 ℃),南京易普易达科技发展有限公司];台盼蓝(批号:1019JO53,北京索莱宝科技有限公司)。
SPF级健康SD大鼠,体质量(200±20)g,购自江西中医药大学实验动物中心,许可证号:SCXK(赣)2019-0004。所有动物实验遵循江西中医药大学动物实验伦理委员会有关实验动物管理和使用的规定,均符合3R原则,实验动物伦理批号:JZLLSC20220534。
2 方法与结果
2.1 HPLC方法学考察
2.1.1 色谱条件 色谱柱为ACE Excel C18(250 mm×4.6 mm,5 μm),流动相为乙腈-0.1%磷酸水溶液(5∶95),柱温25 ℃;检测波长为280 nm;体积流量1.0 mL·min-1;进样量10 μL。
2.1.2 对照品溶液的制备 精密称取天麻素对照品25 mg,加入超纯水溶解,定容至25 mL,得1 mg·mL-1天麻素对照品溶液。
2.1.3 供试品溶液的制备 将制得的可溶性微针,分别加15 mL超纯水使其完全溶解,过0.22 μm微孔滤膜,即得。
2.1.4 专属性检验 将对照品、空白可溶性微针及全载药可溶性天麻素微针制得的溶液进样分析,记录色谱图(图1)。
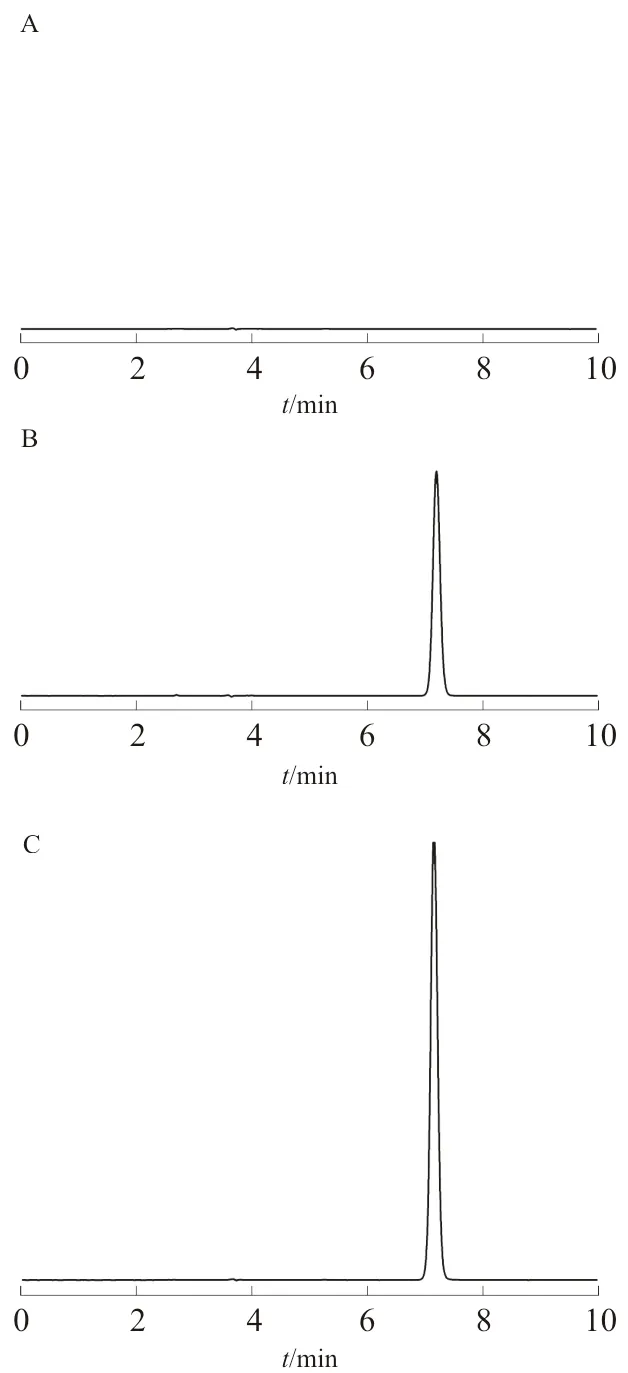
图1 空白可溶性微针(A)、天麻素对照品(B)、全载药天麻素可溶性微针(C)HPLC图
2.1.5 线性关系考察 取“2.1.2”项下对照品溶液,用超纯水稀释成4、25、50、100、250、400、500 μg·mL-1的系列对照品溶液,在“2.1.1”项色谱条件下进样测定,以进样质量浓度为横坐标(X),峰面积为纵坐标(Y),进行线性回归,得回归方程为Y=17.909X-5.347 2,r=0.999 9,结果表明天麻素在4~500 μg·mL-1时,质量浓度与峰面积具有良好的线性关系。
2.1.6 精密度试验 取低、中、高3个浓度标准品溶液(25、200、400 μg·mL-1),在“2.1.1”项色谱条件下进行测定,连续进样6次,记录峰面积,结果表明,天麻素低、中、高质量浓度溶液的精密度RSD分别为0.15%、0.14%、0.05%,表明仪器精密度良好。
2.1.7 重复性试验 取天麻素可溶性微针6份,分别溶解配制成质量浓度约为146.21 μg·mL-1的供试品溶液,过0.22 μm微孔滤膜,按“2.1.1”项下色谱条件测定质量浓度,结果表明,天麻素实际质量浓度平均值为(146.47±0.21)μg·mL-1,RSD为0.14%,该方法重复性良好。
2.1.8 稳定性试验 取供试品溶液,于0、2、4、6、8、10、12、24 h进样,按“2.1.1”项下色谱条件测定质量浓度。结果显示,24 h之内样品的RSD为0.06%,表明供试品溶液在24 h内稳定性良好。
2.1.9 加样回收率试验 取9份供试品溶液,分别加入同体积质量浓度为25、100、200 μg·mL-1对照品溶液,涡旋混合,过0.22 μm微孔滤膜,按“2.1.1”项下色谱条件测定质量浓度。以计算的质量浓度值和真实质量浓度值之比计算加样回收率。结果显示低、中、高质量浓度的加样回收率分别为(100.52±1.17)%、(97.86±0.54)%、(99.01±0.04)%,RSD分别为1.17%、0.55%、0.04%,结果表明加样回收率符合方法学要求。
2.2 天麻素全载药可溶性微针的制备
通过预试验最终筛选出PVP K30为制备微针针尖的最佳材料,HA为制备微针背衬层的最佳材料。
品牌的资产评估有比较成熟的模型可以借鉴,在没有统一的阅读推广评估系统情况下,品牌资产评估不失为阅读推广服务直观的评估方式。
采用两步离心法制备可溶性微针。针尖材料的制备:按一定比例分别称取天麻素与PVP K30于烧杯中,并加入一定量的超纯水,配制质量分数为50%的PVP K30溶液。背衬材料的制备:按一定比例分别称取天麻素与HA于烧杯中,并加入一定量的超纯水,配制成质量分数为10%的HA溶液。将背衬材料倒入微针模具中,3 000 r·min-1离心10 min,刮去针尖外多余的基质溶液,干燥器室温干燥30 min后,倒入背衬材料,3 000 r·min-1离心10 min,将模具置于干燥器内30 ℃干燥24 h后脱模即得。
2.3 天麻素全载药可溶性微针的表征
参照“2.2”项下方法制备天麻素全载药可溶性微针,用HPLC法测定其载药量,并进行形态学、机械性能、皮肤穿刺性能和恢复性能考察。
2.3.1 形态学考察 将所制备的微针置于扫描电子显微镜下,观察其形态学特征,见图2。结果发现,微针整体排列整齐,分布均匀,针体呈四棱锥状、粗细均匀,长度为800 μm,底部直径为410 μm,中心间距为800 μm。

图2 天麻素可溶性微针扫描电镜图
2.3.2 微针含药量测定 取6片制得的天麻素全载药可溶性微针,分别溶于15 mL超纯水中,按“2.1.1”项下色谱条件测定质量浓度,结果显示所得每片微针含药(5.45±0.14)mg。
2.3.3 机械性能检查 利用物性分析仪来表征可溶性微针机械性能,选择1/2探头,设置测前速率为0.5 mm·s-1,测时速率为0.5 mm·s-1,测后速率为15 mm·s-1;触发力为0.049 N[16]。通过物性分析仪测量微针针尖在探头下压过程中所受的应力与探头位移之间的关系,所得的压变曲线见图3。随着物性分析仪探头的移动,所受的应力逐渐变大,力与位移曲线并未出现中断或突然下降的情况,说明微针在受力过程中并未出现断裂[17]。由图3可知,当位移压缩至0.8 mm时,应力可达(1.215±0.05)N。微针刺破皮肤所需的刺入力需大于0.05 N[18],本研究制得的天麻素全载药可溶性微针的断裂力要远大于皮肤的刺入力,表明微针有较好的力学力度保证顺利刺入皮肤。
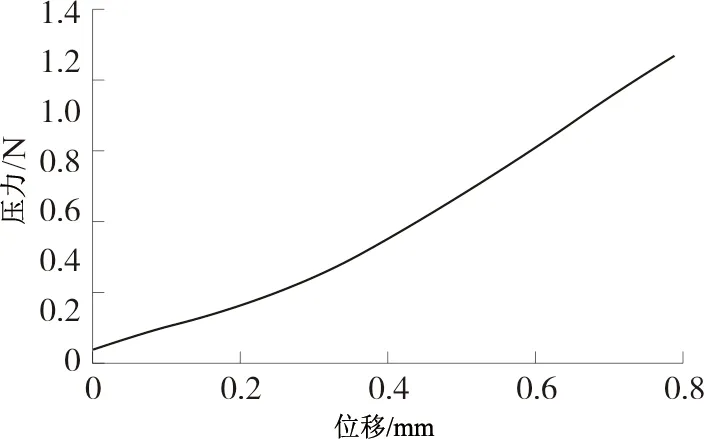
图3 天麻素全载药可溶性微针压变-应力曲线(n=3)
2.3.4 皮肤穿刺性能 离体皮肤的处理:取健康SD大鼠,腹腔注射10%水合氯醛,麻醉后用剃毛器剔干净腹部的毛,取下皮肤,剥离脂肪组织和筋膜,用生理盐水反复清洗后,用滤纸吸干,再用锡箔纸包裹,然后放入-20 ℃冰箱中保存。实验结束后,处死大鼠。

图4 经微针扎过后皮肤台盼蓝染色结果
(2)组织学检查 将SD大鼠用水合氯醛麻醉,腹部去毛擦干后,将载药微针快速压入脱毛的皮肤处按压30 s后移除微针,1 min内立即剥离微针穿刺后的皮肤,放到4%多聚甲醛中固定24 h,脱水、浸蜡、包埋、切片、干燥、HE染色后,拍照观察离体皮肤的刺入情况。如图5所示,皮肤最外层呈深紫色的部分为薄薄的一层角质层,中间较薄的紫色为表皮层,最下面很厚的淡紫色部位为真皮层。天麻素可溶性微针可以成功刺破了皮肤角质层,进入到表皮层,表明微针突破了角质层的屏障,且未触及到真皮层神经末梢,能够起到无痛给药的效果。
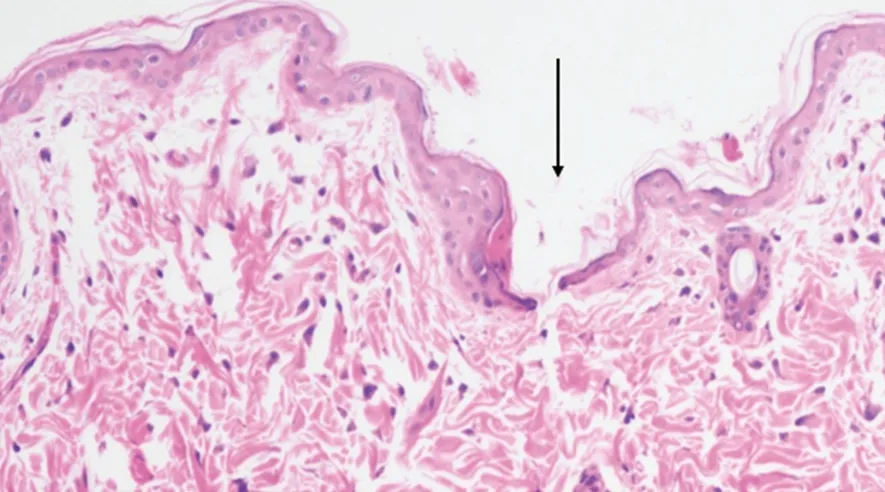
图5 微针刺入大鼠皮肤后的组织切片图(×100)
2.3.5 皮肤恢复考察 对大鼠进行麻醉并固定四肢,将微针压入大鼠背部脱毛处皮肤,并用医用胶布固定。5 min后,拔出微针,观察皮肤的恢复情况,期间每隔0.5 h对微针扎入的皮肤部位拍照,直至皮肤完全恢复,结果见图6。皮肤恢复实验结果显示,微针拔出后可以明显地在皮肤表面看到规则排列的微小针孔。微针在拔出1 h内皮肤恢复较快,针孔逐渐变得模糊。2 h后,微针扎过的皮肤部位几乎观测不到针孔,与周围的皮肤纹理一致,已经完全恢复。因此,本研究制备的微针生物相容性好,对皮肤无明显损伤。

图6 皮肤经微针扎过后的恢复情况
2.4 体外经皮渗透试验
向Franz透皮扩散试验仪(有效扩散面积为1.13 cm2,接收室容积为15 mL)内注入生理盐水作为接收液,另按“2.3.5”项下方法取下大鼠腹部皮肤,将鼠皮置于供给池与接收池之间,角质层朝向供给池,皮肤组织朝向接收室,封口后置于池中[水浴(37±0.2)℃,350 r·min-1]平衡30 min。将制备好的微针剪掉针尖周围背衬[面积为0.9 cm×0.9 cm,载药量为(1.92±0.14)mg],并施加一定力度的力使微针刺入鼠皮,同时设立溶液对照组(药物含量同载药微针),排除气泡使药物贴合皮肤上层,开始计时。此后于1、2、4、6、8、10、12 h取样0.8 mL,同时补充等量的37 ℃接收液,将透皮接收样品液用0.22 μm微孔滤膜滤过,按“2.1.1”项下色谱条件测定其中药物含量。通过公式(1)计算累积渗透量(Qn),通过公式(2)计算累积渗透率。以累积渗透率为纵坐标、对应的时间(t)为横坐标作图,绘制药物累积渗透曲线。对透皮实验的数据进行模型拟合,求出的斜率即为稳态透皮速率Jss,见表1。
(1)
累计渗透率(%)=Qn/载药量×100%
(2)
式中Qn为第n个时间点的单位面积累计透过量,A表示有效透皮面积,Cn为第n个点测得的药物浓度,V为接收池体积,Vi为每次取样体积。
结果见图7,微针组天麻素在前4 h内快速释放,累积渗透率为(84.60±15.79)%,随后释药速率变缓,12 h后累积渗透率为(87.98±9.84)%。而溶液对照组天麻素在前12 h的累积渗透率仅为(12.10±5.88)%。因此,天麻素可溶性微针可大大地提高天麻素的皮肤透过量,并能增加药物经皮渗透速率,显著提高药物的透皮效果。
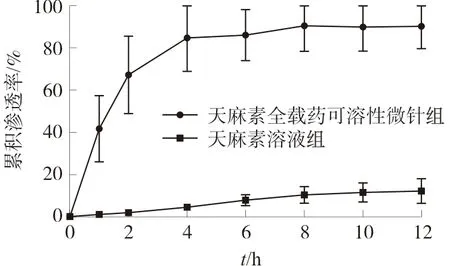
图7 天麻素全载药可溶性微针及其溶液对照的透皮累积渗透曲线
3 讨论
本研究通过两步离心法,成功制备了天麻素全载药可溶性微针。微针由针尖与背衬层2部分构成,针尖的主要组成材料为PVP K30,背衬层则由HA构成,其中针尖和背衬层均含有药物天麻素。制成的微针呈四棱锥状,针尖机械性能良好,可刺穿大鼠皮肤,背衬层柔韧平整,贴合皮肤。微针处理后的皮肤在2 h内即可恢复到原来的状态,安全性良好。体外透皮试验表明,微针对天麻素经皮递药具有极大的促进作用,全载药微针前4 h内快速释放天麻素,其累积渗透率已大于80%,在12 h内药物基本释放完全,药物累积渗透率约为87%,而溶液对照组天麻素12 h内累积渗透率仅为12%。
本文所制备的天麻素全载药可溶性微针能有效穿透皮肤,克服角质层屏障,经皮递送效率高,成功实现了水溶性药物经皮给药,有望应用于亲水性药物高效精准、无痛微创的经皮递送,并为给药剂量大、给药次数频繁、生物利用度低的药物给药方式设计提供了思路。此外,研究过程中发现由于制备微针的材料PVP K30极易吸潮,受外界环境湿度的影响大,所制备的可溶性微针必须密封储存,故针尖层的设计有必要开展进一步研究。

