医疗器械创新项目评价机制及转化策略研究
陈薇薇 田耘 栾笑笑 田金 薛昕昀 李亦林 冷文 刘振临 时晨希 北京大学第三医院医学工程处 (北京 100191)
内容提要: 研究了技术法务对六大医疗器械创新主体“政、产、资、用、学、研”,以及对医疗器械创新大赛赛程设计和评价规则的作用,提出了相关转化策略,供医疗器械改进、设计、研发、投资转化、评价、成果管理工作参考。
现代医疗器械是聚集知识、技术、资本的高科技产品。目前,我国医疗器械年产业增速已突破10%,年总产值万亿,技术创新市场前景广阔[1]。但因其关系人民群众生命健康,国家政策监管技术安全性、有效性和质量可控性,技术产品化周期较长。如何快速、准确评价医疗器械创新项目,高效转化优质项目,已成为医疗器械六大创新主体“政、产、资、用、学、研”共同关注的问题。医疗器械创新大赛作为新形势下该问题的解决方案,亟需技术法务解读政策,助力创新,提速项目转化。
1.医疗器械创新主体
2021年,我国研发R&D经费支出已达我国GDP的2.44%,比上年增长14.2%[2]。从医疗器械制造、计算机制造、医药制造、信息化学制造和电子及通讯制造,五大高技术产业相关情况图(图1)看出,医疗器械制造在专利中发明占比、新品收支比和单体机构研发人员数这三项均不占优,但其单项新品研发成本低于其他四大制造,投入仅电子及通讯制造的35%,收支比可达60%[3]。医疗器械制造投入产出较好,具备一定增长潜力。
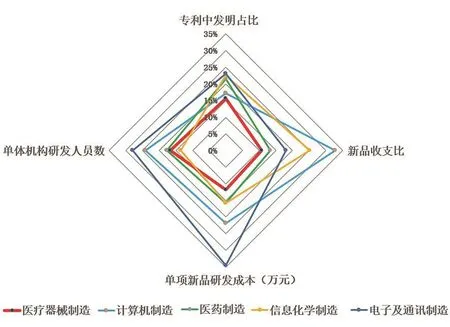
图1. 2021年高技术产业相关情况
国家各项科技创新政策陆续颁布,医疗器械创新大赛进行百余场,收集医疗器械创新项目数万个[4]。六大医疗器械创新主体“政、产、资、用、学、研”,作为核心参与方,其各自作用和代表机构详见表1,可按作用方向分为提供创新支撑资源的创新外部主体“政、产、资”,和产生创新原动力的创新内部主体“用、学、研”。

表1. 医疗器械六大创新主体作用和代表机构
1.1 外部主体:创新支撑
医疗器械创新外部主体“政、产、资”,为医疗器械创新项目提供导向监管、生产经营、资金供给、资源支撑和保障。
“政”即政府部门,进行导向监管和制度创新,如推出“揭榜挂帅”行业募集项目,多部门联动出台产业园扶持、孵化器优待、快速市场准入、税收减免等举措,聚焦创新资源在“支持、鼓励、引导、限制和禁止”不同政策方向上的分布,尤其关注项目的宏观视角和政策顺应性。
“产”即企业,开展生产经营和渠道创新,70%以上的企业设立了研发部门,输出和吸纳技术交易总额分别占全国90%和75%以上,每个新产品开发项目,经费支出达240余万元,收入可达3000余万元,平均收益回报高达12倍,尤其关注项目的技术领先性和商业价值[5]。
“资”即投资机构,提供资金保障和模式创新,包括早期投资(包括种子轮、天使轮、Pre-A轮、A轮及B轮投资)、后期投资(包括D轮及后期轮次、IPO)、企业上市后投资(包括并购、增发、战略投资),以及“募、投、管、退”的投后管理,提供资金保障的同时,要求项目的市场、政策、技术、管理、法律诉讼等风险规避,尤其关注项目的融资策划和法务规制能力。
因此,技术法务可满足上述创新项目要求,进行政策解读、技术分析和资源导入,有效盘活医疗器械创新项目的资源渠道。
1.2 内部主体:创新原动力
医疗器械创新内部主体“用、学、研”,为医疗器械创新项目提供技术评测、内涵建设、应用试验,作为内生动力形成有实际价值的医疗器械创新。
“用”即医疗机构,提供使用评测和场景创新。以聚焦健康促进,服务人民生命全周期、健康全过程的高等院校附属临床医学院/医院为例,其引进国外先进医疗器械,积累应用经验,融合临床医学和工程技术等多学科知识,参与国内医疗器械创新研发[6]。技术法务相关人员根据缓解病痛、缩短病程、降低民众负担的研发目标,提出需求与改进建议,承担真实世界数据分析与临床试验研究等核心基础工作,实现市场价值以真正惠及临床患者,“学”即高等院校,进行人才培养和理论创新[7]。“研”即科研院所,提供应用研究和技术创新。从2020年基础研究、应用研究、试验发展R&D人员全时当量占比图(图2)看出,“学”40%人力投入在基础研究或应用研究,“研”40%人力投入在应用研究或试验领域,而总体研发80%人力投入在试验领域[8]。可见离不开医疗器械使用端“用”场景下的技术法务协同。
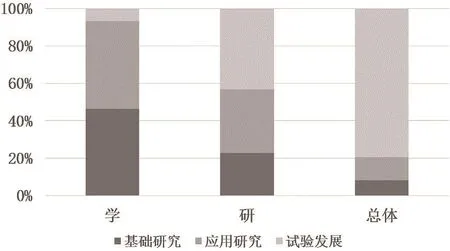
图2. 2020年基础研究、应用研究、试验发展R&D人员全时当量占比(全时当量:Full Time Employee,FTE,指国际通用比较科技人力投入指标,即R&D全时人员(全年从事R&D活动累积工作时间占全部工作时间的90%及以上人员)工作量与非全时人员按实际工作时间折算的工作量之和。)
2.医疗器械创新项目评价机制
医疗器械创新大赛,为上述六大医疗器械创新主体和技术法务联动创新转化,提供了平台和解决方案。通过六大主体自身参与,协会、学会、行会、商会联合举办等,以会议论坛、项目征集、成果发布、方案分享、商业推介、官方洽谈、路演展示等方式开展比赛。赛程设计和评价规则,组成科学公正的评价机制,可有效实现医疗器械创新信息快速定向传播,以及技术和市场投融资需求的精准嫁接,推进医疗器械项目交汇融合和递延合作,有利于加快医疗器械创新定制化成果加工、集成、熟化、包装、推介、撮合、交易和转化[9]。
①问卷调查:分别在干预前、干预结束后3个月、干预结束后6个月采用骨质疏松知识量表、骨质疏松自我效能量表、长版国际身体活动量表、糖尿病病人生存质量调查表对研究对象骨质疏松知识、骨质疏松自我效能、身体活动量、生存质量进行问卷调查。所有问卷均获得原作者同意和授权。调查前告知调查对象此次活动可无理由随时退出,且不承担任何惩罚和风险。②糖化血红蛋白检测:分别在干预前和干预后6个月随访结束时对研究对象进行糖化血红蛋白检测。所有研究对象均在同一医院(重庆医药高等专科学校附属医院)进行抽血检测。
2.1 赛程设计
医疗器械创新大赛的赛程设计,包括举办时间、创新项目征集及分组、赛制、评审专家、奖励方式等,其深度评审、行业聚焦、市场对接、转化扶持等要素,均体现了医疗器械行业特色。
医疗器械创新大赛的举办时间,多集中在年初医疗器械产业政策密集出台后的年度中下旬。项目征集涵盖医学影像、生命支持、医用材料、植介入器械、手术康复、体外诊断等技术领域,并设置当年新兴领域专题比赛。以中国医疗器械协会举办的全国医疗器械创新大赛为例,将创新项目分为三组[10]:①初创组,要求参赛团队尚未在国内注册成立企业,核心成员不能少于3人,并有创业计划;②企业组,要求参赛团队为合法注册,且未上市融资的企业,从事高新技术产品研发、制造、生产及服务业务;③专业组,要求参赛团队为科研院所、医院等事业单位。三组参赛团队均应真实存在,并无科研及商业诚信问题,应都具有专属专利、课题、文献等创新成果。按实际征集项目数量,设定初赛、复赛、决赛、总决赛。邀请临床、科研、医疗器械注册审评、投融资、技术法务等行业专家,根据书面初评1~2周、答辩演讲复评5~8min、临场问答2min的评价规则打分。
随后,按照分值排名,年终揭晓各级奖项,包括颁发名次证书、给排名前列的项目拨付启动奖金,对不同分值的创新项目,提供技术法务专业支持、下游企业合作渠道、CDMO平台服务、基金投资融资机会、优先推荐注册、针对性创业辅导、商业模式设计、提升项目研发深度、协助产品改进、提升客群可接受度、落户孵化器、享受政府配套产业园政策、享受减免租税政策、多平台媒体报告、展览合作、精品论坛学习、行业推广等奖励[11]。
2.2 评价规则
医疗器械创新大赛评价规则,包括评价维度和权重,用于筛选具有孵化或转化潜力的项目,提升医疗器械创新项目的转化对标能力。评价维度,包括应用、技术、时间、团队、避险价值五个方面,并在此基础上,医疗器械技术法务相关人员根据不同创新项目所处的技术市场、行业现状、经济成本,科学设定指标权重。
应用价值,即临床实际使用实现度。包括使用场景、对象、方式、成本、特点,通过对比原有应用空白和不足,结合发病率、病死率、高复杂度、高负担等负价值的消除,展现新技术方案的质量改进或效率提升优势,需要提供临床循证和病组研究证据。
技术价值,即技术领域市场供给现况,以及技术积累度和研发难易度。需要提供与现有技术方式的衔接、替代或补偿,技术成本经济测算,对方法学和技术路线重复性、稳定度和可信度等方面的技术评价。如植入物创新项目需考虑植入后的环境应力影响,器械创新项目需考虑消毒灭菌、生物安全性和实际使用寿命,材料学创新项目需考虑研发方向、技术验证以及注册上市情况。
时间价值,即项目研发和落地效率性。需要对标技术主题,梳理现有生产工艺、产业渠道,评估产品化周期和时间投入。
团队价值,即项目实施人员组成结构合理性。好项目通常技术占三成,管理占七成。团队是创新项目落地的关键因素,项目创始人背景、过往经历和经验积累尤为重要。团队中需要包括懂临床、懂技术、懂法务、懂市场的技术法务成员,仅靠一个科学家或医生通常难以支撑项目开展。
在科学公正的评价规则下,选手们怀揣解决临床问题、为疾病诊治提供精准技术保障、借助平台影响力取得项目融资的梦想,积极参与和展示医疗器械创新项目,力争从“赛场”走向“市场”。
3.医疗器械创新项目转化策略
医疗器械创新大赛作为创新主体信息高效对接的平台,在一定程度上解决了医疗器械创新项目转化率低的问题,相应的转化策略如下。
3.1 技术法务建立系统性评价机制,提升项目质量
“政、产、资、用、学、研”是医疗器械创新大赛参与主体,也是医疗器械创新主体。各方均不能全面理解和评估医疗器械创新项目的真实技术价值,使医疗器械研发项目极易出现下述问题:有些项目对于产品作用机制、生物学疾病机制、光电工程定律基础理论研究不深,工学设计经不起实践考验,忽略风险,低估成本,高估收益,甚至产生资源浪费;有些项目实际效果样本量少,技术对比少,所解决问题描述的论据不充分,忽视质量指引,未关注现有技术的标准和指南,对技术成熟度理解不深;有些项目从临床研究入手,过分关注科学学术性,忽视了项目应用的系统性和真实性,导致难以落地实施;有些项目在团队合作中未引入法务保障,研发中出现巨大分歧,导致项目进展缓慢甚至终结。上述情况,均导致项目难以转化,效果不佳。
技术法务建立的系统性评价机制,可有效串联六大创新主体,使技术商品化,从而具备价格属性。即用技术能力,清晰阐述创新项目与市场现有医疗器械的技术符合度和相关度,从适应症广泛、缩短疗程、减少痛苦、提高诊疗依从性、加快患者重返社会,降低社会负担等角度,客观评估医疗器械创新项目技术有效性及产品成本。用法务能力从使用安全性、市场接受度、专利保护程度等角度,进行方案优化和呈现,规避同质化错路、弯路。在商业活动中,发挥价值意识和谈判能力,保护项目核心利益。在创新医疗器械上市注册时,保证产品不背离发明人的应用指引,直接对标市场渠道,使有价值的创新得以保护,被保护好的创新更能体现价值。
3.2 技术法务充分分析项目信息,形成转化积累
医疗器械创新大赛成为广泛的信息获取渠道、深度的医疗器械专业市场、产品技术管线的综合知识库,技术法务通过参与讲演座谈、实地考察、条件共建,形成项目应用实践和评测、技术研发思路和方案、转化周期和设计、团队组建方式和运营、风险规避和管控等经验,相关数据可靠度,远高于在互联网平台收集的技术成果、专利供给、融资项目、技术需求、企业路演、技术能力等难以追溯的信息,是创新项目后续发展的隐性资源[13]。可形成发明人素养指标、发明技术潜力和商业价值判断能力、实际项目开展能力、项目目标达成能力、项目成果对等协商谈判能力,为驱动创新安装“飞轮”,完成卓有成效的创新项目转化。
4.讨论
医疗器械创新项目,是现阶段科技和社会高速发展的技术产物,凝结了“政、产、资、用、学、研”六大创新主体的潜能,以大赛作为平台,依托技术法务,转化效率远高于“手术支持、技术咨询、技术交流会、展览会、学习班”等既往模式,科学评价机制提升转化效能。但在现阶段模式推广,还有下述难点。
4.1 技术法务人才团队建设
技术法务需懂政策、懂技术、懂市场、懂医疗器械技术和临床应用,属于交叉专业复合型人才。目前散在医工专业、专利代理机构、法律服务机构以及临床中,其知识背景和专业经历,往往局限于从业领域,需要结合工程技术、法律职业、知识产权技术、商业市场和临床医学等多学科知识运用,要求技术法务人才具备较高的学习能力、反思能力、沟通能力和复盘迭代能力,需要基于实践打磨方向,通过项目铸就能力,还需依靠行业标杆形成新模式,带动一批人才形成和梯队建立,提升项目转化效率。
4.2 先进智能化信息工具的运用
创新项目从想法到产品,将会产生大量有价值的信息,为技术概念验证、技术发展预测提供可靠指引,也为转化协议定价、挂牌交易、拍卖、资产评估等技术市场交易提供定价参考,技术法务应发挥专业能力,在基础建设和规划上发力,运用先进智能化工具,建立一系列行之有效的运行规则,构建跨行业、跨部门、跨地区的科技成果库、需求库、案例库和评价工具方法库,供六大创新主体联动使用和同步更新,提升项目转化效率。
5.小结
“积跬步,方能至千里”。在医疗器械创新大赛“以评促进”的平台功能下,技术法务对有效整合医疗器械创新项目的市场和产能,助力转化,实现项目的社会价值和商业价值,将发挥更为显著的助推作用,从而形成有效的医疗器械创新项目转化策略。

