液相色谱-质谱/质谱法测定鸡蛋粉中 喹诺酮类药物残留
◎ 张 威,胡婷婷,秦培余,姜 珊,陈 露,刘晨曦,刘婉秋
(吉林省辽源市食品质量安全检测中心,吉林 辽源 136200)
随着时代的发展,消费者对食品的要求已不再局限于简单的维持生命和果腹,对食品的安全、营养和滋味提出了更高的要求[1]。随着人们生活节奏的加快,方便、营养、快捷的食品更加受到人们的追捧。而鸡蛋粉的出现正好满足了人们的这一需求。
现行有效的国家标准未对鸡蛋粉中兽药残留检测方法作出具体的要求。因检测方法的不足,不合格的鸡蛋粉产品在市场中大肆流通。液相色谱-质谱/质谱法可根据被测物(鸡蛋粉)的特征离子、保留时间等结构信息,以较高的灵敏度和选择性,准确判定待测物是否为阳性,避免了假阳性样品的检出[2]。该方法的确立从传播途径上减少了残留现象,弥补了我国在鸡蛋粉中喹诺酮类药物残留检测方法的空缺,为市场监督执法部门对市售及出口鸡蛋粉的监督管理提供了科学的数据保障,规范了养殖户的行为,对于从源头上控制抗生素的使用具有重要意义。
1 材料与方法
1.1 仪器与设备
液相色谱-质谱/质谱仪:配备电喷雾离子源(ESI)(美国AB SCIEX公司);天平:感量为0.01 g(YP202N)和0.000 1 g(BSA124S-CW);高速大容量冷冻离心机:6 000 r·min-1(TG20KR-D);涡旋混合器(QL-8665,6);氮吹仪(TTL-DCII)。
1.2 材料与试剂
喹诺酮类混合标准对照品(浓度:100 mg·L-1,体积:1 mL,编号:IST47508-100M),包括恩诺沙星(CAS号:93106-60-6)、环丙沙星(CAS号:85721-33-1)、诺氟沙星(CAS号:70458-96-7)、培氟沙星(CAS号:6159-55-3)、沙拉沙星(CAS号:98105-99-8)、洛美沙星(CAS号:98079-51-7)、依诺沙星(CAS号:74011-58-8)和氧氟沙星(CAS号:82419-36-1);甲酸(安谱,CAS:64-18-6);乙腈(色谱纯fisher);净化管(Wondapak QuEChERS P/N5010-015204);色谱柱(岛津Shim-pack GIST C18100 mm×2.1 mm,2 µm P/N227-30001-04)。
1.3 试验方法
1.3.1 样品前处理
(1)提取。称取2 g(精确至0.01 g)鸡蛋粉样品于50 mL具塞离心管中,加入10 mL 2%甲酸乙腈涡旋30 s,超声提取10 min后,于6 000 r·min-1离心10 min,上清液待净化。
(2)净化。取上清液2 mL于QuEChERS SPE净化管中,涡旋30 s,于6 000 r·min-1离心5 min,取上清液1 mL,于40 ℃水浴氮气吹至近干,加入1 mL 0.1%甲酸水溶液+0.1%甲酸乙腈溶液(9+1)定容,超声波振荡5 min,过0.2 µm微孔滤膜,供HPLC-MS/MS测定。
(3)标准溶液配制。准确量取8种喹诺酮类混合标准对照品1 mL,用乙腈溶解并定容于100 mL棕色容量瓶中,配制成浓度为1.0 µg·mL-1的标准储备液。将标准储备溶液逐级稀释成浓度为1.0 µg·L-1、 5.0 µg·L-1、10.0 µg·L-1、20.0 µg·L-1、25.0 µg·L-1、 50.0 µg·L-1和100.0 µg·L-1的8种喹诺酮类药物标准工作溶液,现用现配。
1.3.2 色谱条件
流动相A:0.1%甲酸水溶液;流动相B:0.1%甲酸乙腈;梯度洗脱条件参见表1;流速:0.1 mL·min-1;进样量:20 µL;柱温:40 ℃。
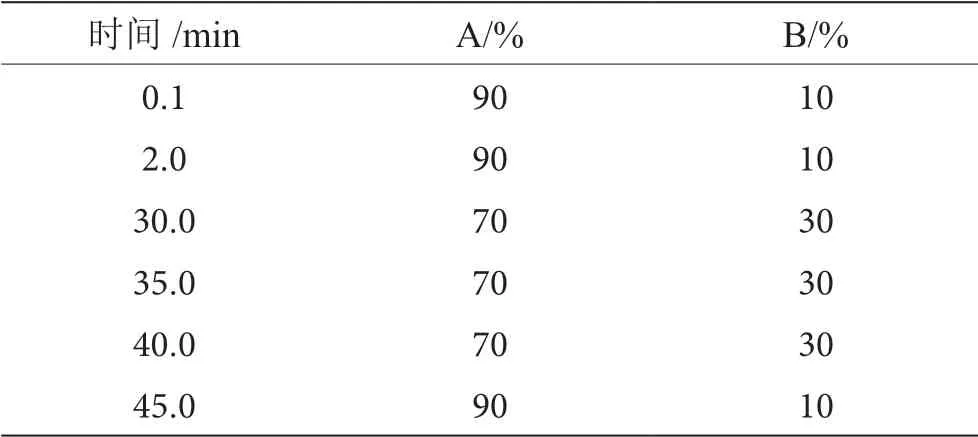
表1 梯度洗脱条件表
1.3.3 质谱条件
电离方式:电喷雾电离(ESI);扫描方式:正离子扫描,多反应监测(MRM);电离电压:5.5 kV;离子源温度:550 ℃;气帘气压力(CUR):10 psi;雾化气压力:50 psi;辅助气压力:50 psi;定性离子对、定量离子对、去簇电压、碰撞能量见表2。
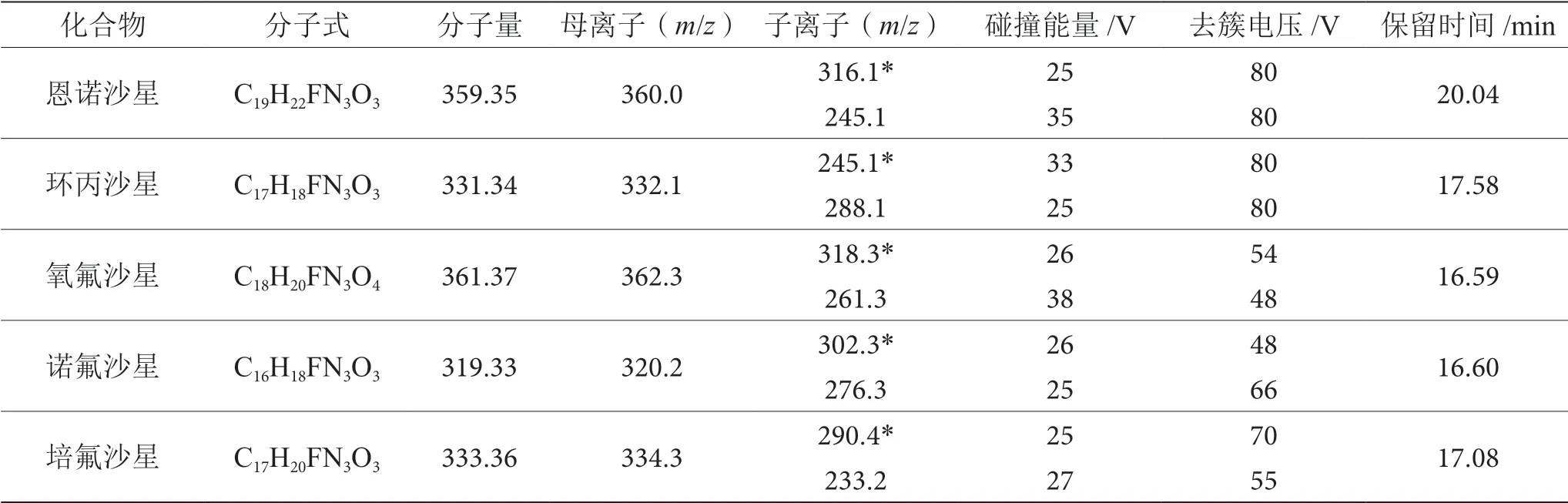
表2 8种喹诺酮类药物定性离子、定量离子、去簇电压、碰撞能量、保留时间表
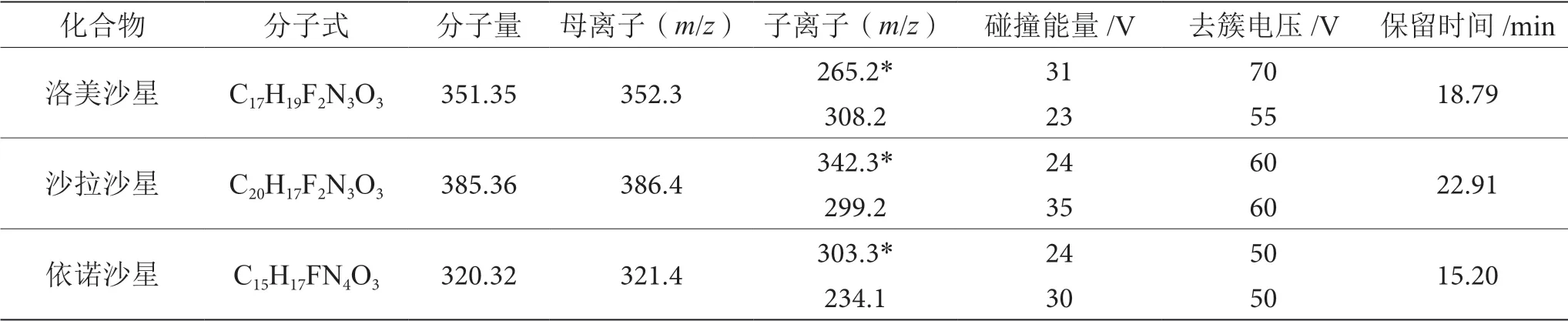
续表2
2 结果与分析
2.1 样品前处理条件优化
2.1.1 提取溶剂优化
分别使用0.2%甲酸乙腈、0.5%甲酸乙腈、2.0%甲酸乙腈、5.0%甲酸乙腈以及0.5%甲酸甲醇、1.0%甲酸甲醇、5.0%甲酸甲醇和10.0%甲酸甲醇作为提取溶液对鸡蛋粉中的8种喹诺酮进行提取,发现8种喹诺酮药物不溶或者微溶于甲醇,而蛋白质在甲醇中的溶解性较强,乳化现象严重,提取效果不明显,回收率较低。乙腈能使蛋白质变性[3],有利于目标化合物的提取,加入一定浓度的酸化乙腈溶液可以有效提取目标化合物,同时沉淀蛋白[4],大大提高提取率。但酸的浓度过高,也会发生严重的乳化现象。因此,比较了响应值的强度及回收率,最终确定提取溶液的浓度为2.0%甲酸乙腈。不同浓度甲酸乙腈提取液提取效果见图1。
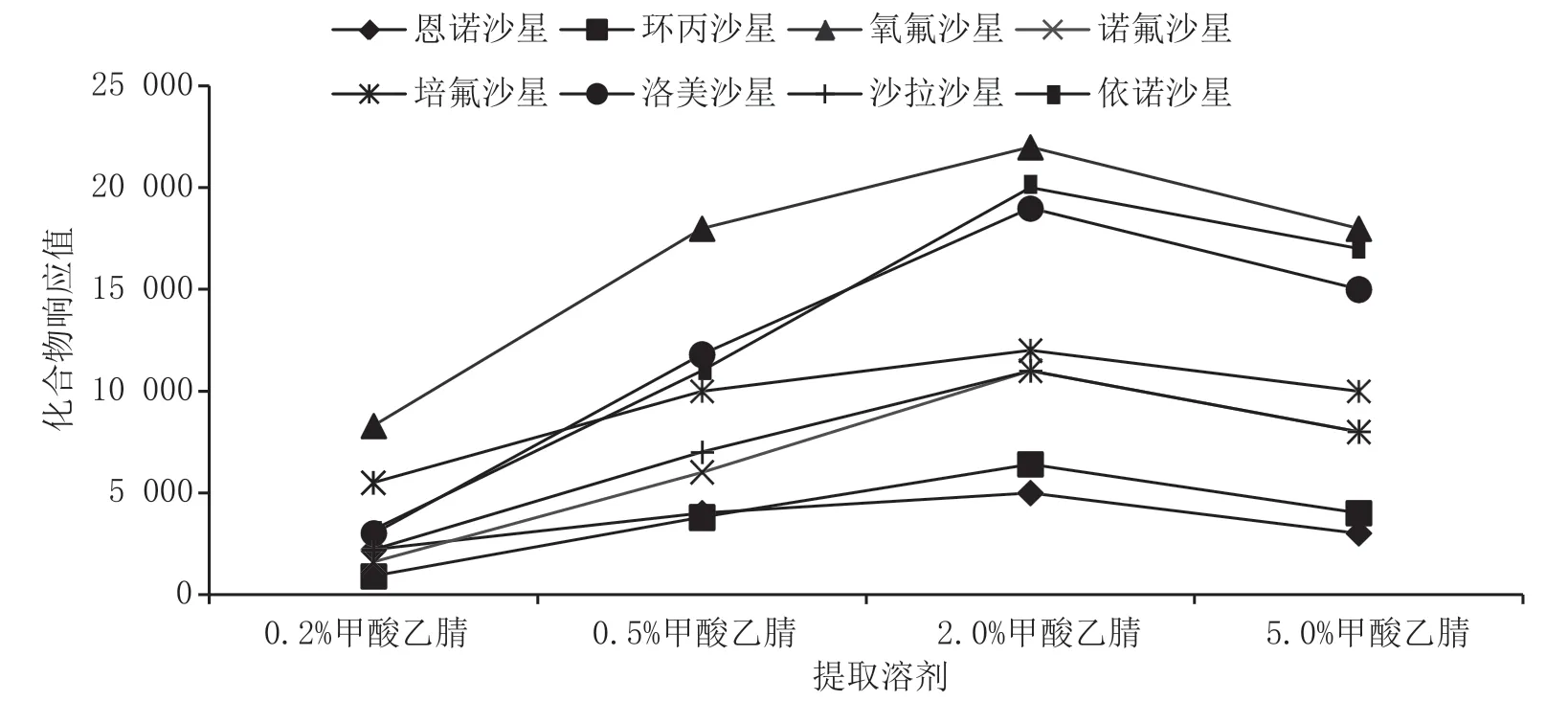
图1 不同浓度甲酸乙腈提取液提取效果图
2.1.2 净化装置的优化
固相萃取是常用的兽药残留检测的有效方法[5]。有研究表明,酸化乙腈的提取液未净化会导致较强的基质效应[6-7],而EDTA-Mcllvaine缓冲液由于提取液混浊而导致固相萃取柱堵塞[8],从而使回收率大大降低。考虑鸡蛋粉是粉状物质,基质复杂,蛋白质含量较高,QuEChERS SPE净化管可完全避免堵柱现象的发生,本次试验选用QuEChERS SPE净化管,减少了洗涤溶剂的时间,提高了净化效果。
2.2 色谱条件的优化
8种喹诺酮化合物的极性相似,因此梯度较大的流动相比例不利于化合物在色谱柱中的分离,比较了近60种不同梯度的流动相,结合响应值的强度,回收率、保留时间等因素,最终确定流动相中的有机相为0.1%甲酸乙腈溶液,无机相为0.1%甲酸水溶液。洗脱条件如表1所示。
2.3 质谱条件的优化
将8种喹诺酮混合标准物质用乙腈稀释至浓度0.2 mg·kg-1,以20.0 µL·min-1的流速注入质谱仪,在ESI+模式下进行Q1扫描,确定母离子。再进行MS2扫描,依据不同的碰撞能量和去簇电压,选择响应值最强的两对离子作为子离子,最后确定8种喹诺酮化合物的MRM条件,见表2。
2.4 线性关系、方法检出限、回收率
将8种喹诺酮类药物标准工作溶液,按照上述色谱和质谱条件测定,外标法定量。得到8种喹诺酮化合物的线性关系均大于0.999,线性关系良好。根据特征质量色谱峰的信噪比S/N≥3所对应的浓度作为本方法的检出限,8种喹诺酮的方法检出限均为 1.0 µg·kg-1。8种喹诺酮化合物的线性关系见表3。
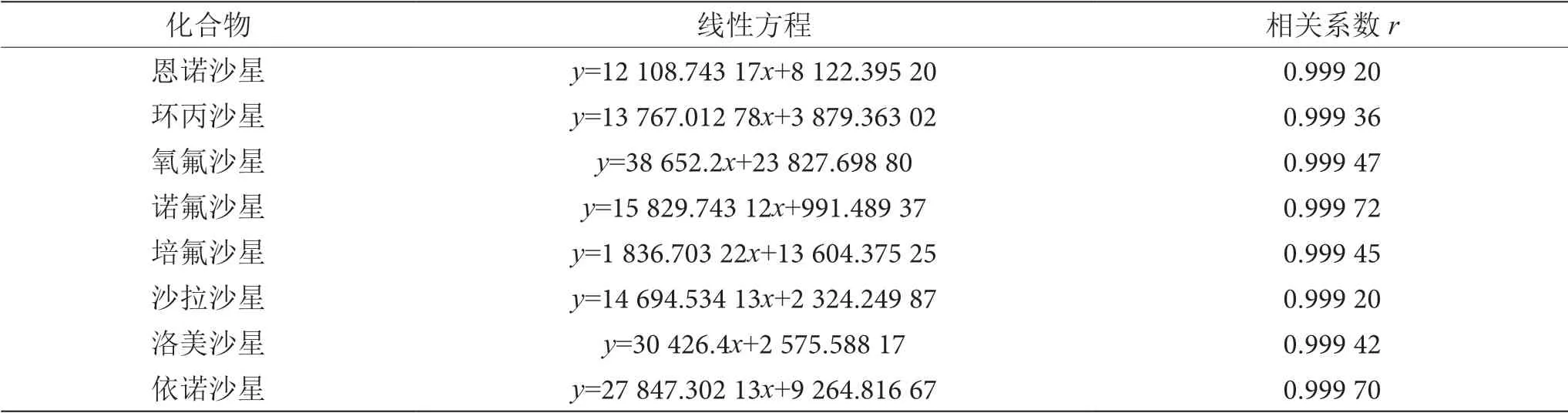
表3 8种喹诺酮类化合物的线性方程及相关系数表
在空白鸡蛋粉中添加0.01 mg·kg-1,0.02 mg·kg-1, 0.10 mg·kg-13个浓度水平的对照品溶液,每个浓度平行测试6次。回收率在73.2%~102.0%,RSD小于23%,满足兽药残留检测的要求(见表4)。
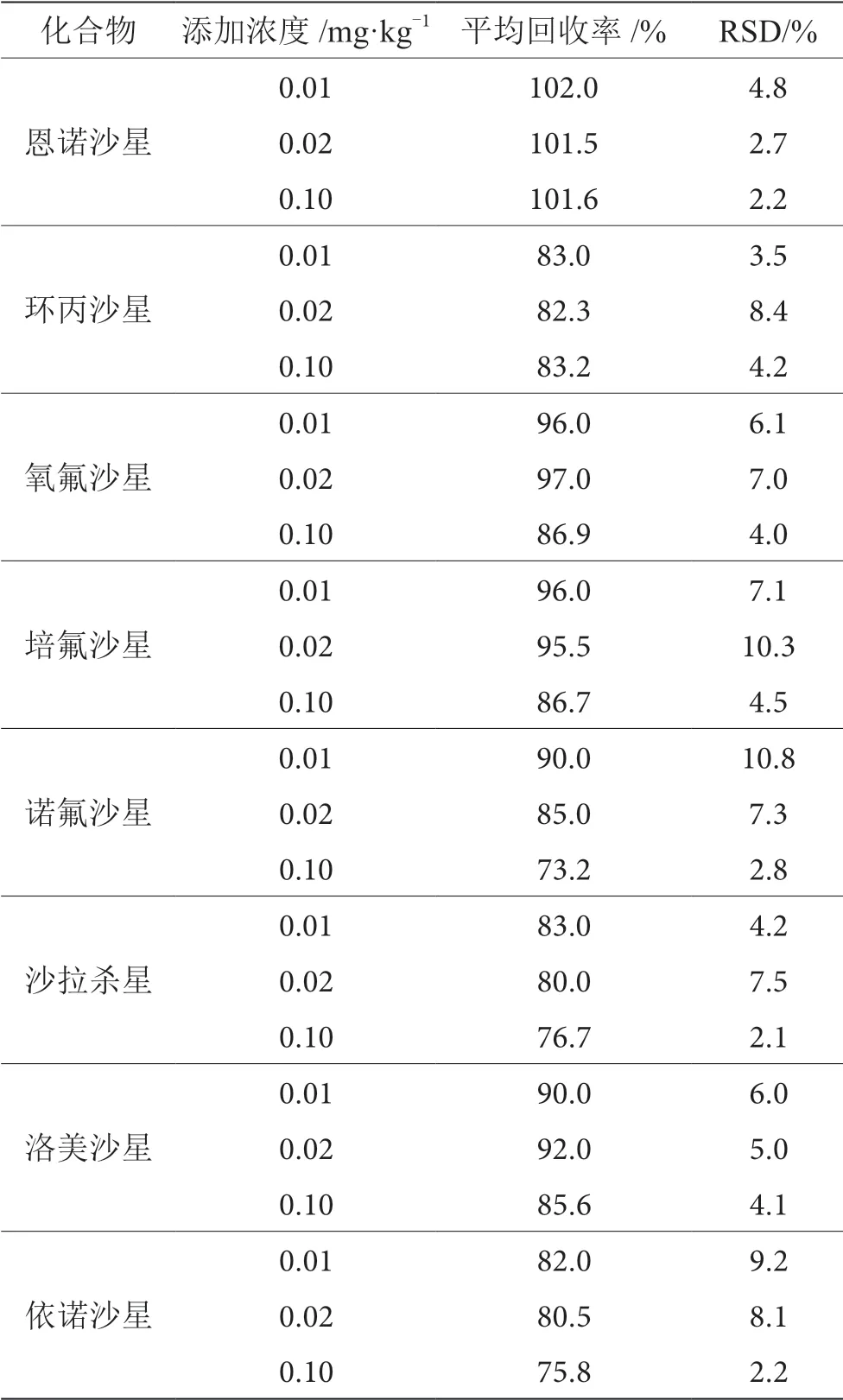
表4 8种喹诺酮化合物在鸡蛋粉中不同添加浓度回收率、RSD表(n=6)
3 结论
本研究建立了鸡蛋粉中8种喹诺酮类药物残留的液相色谱-质谱/质谱法。该方法灵敏度高,准确性好,操作简便,经济投入较低,可以满足企事业等检测机构对兽药残留检测的需要。

