VN 基材料的电子结构调控和超电容性能研究
张东彬,常 智,滕艾均*,刘天豪,代 宇,彭显著,杜光超,康 举
(1.鞍钢集团北京研究院有限公司,北京 102211;2.攀钢集团钒钛资源股份有限公司,四川 攀枝花 617000;3.攀钢集团研究院有限公司,钒钛资源综合利用国家重点实验室,四川 攀枝花 617000;4.北京石油化工学院,深水油气管线关键技术与装备北京市重点实验室,北京 102617)
0 引言
超级电容器(超电容)因其快速充放电、良好的倍率性能和循环稳定性等特性,近年来受到了越来越多人的关注[1]。根据超电容储能机制的不同,可以分为双电层电容和法拉第赝电容[2],其中,法拉第赝电容因其基于活性物质的氧化还原反应的充放电机理,有望储存更多的电子,实现更高的充放电容量,是目前超电容电极材料的一类主要研究对象。现阶段,对于这类材料的研究,主要集中在锰、镍、钴、钒等过渡金属化合物[3]。
相比于其他过渡金属元素,钒因其具有多种价态变化,有望发生更多的氧化还原反应,被广泛应用于储能领域[4-6]。目前的研究报道主要集中在V2O5、V2O3、VO2等钒的氧化物或氢氧化物[7]。事实上,与其他钒的氧化物/氢氧化物相比,氮化钒(VN)具有更好的导电性,可以实现快速的电子/离子输运过程,有望表现出更加优异的电化学性能[8-9]。同时,通过电子结构调控,可以改变VN 基材料的晶体结构,进一步提升其超电容性能。然而,目前为止,对于VN基材料电子结构调控机制的探索以及电子结构调控与超电容性能间内在关系的研究还鲜有报道。
基于上述讨论,笔者采用氨解氮化的方法,成功制备出了VN 和Fe-VN 材料。通过利用XRD、HRTEM 和DFT 计算等方法,系统的探究了Fe 元素的掺杂对VN 结构和电化学性能的影响。研究结果表明,Fe 元素的引入并不改变VN 的微观形貌和物相结构,但是由于Fe 与V 的电负性差异,使得电荷发生自发转移,进而改变了VN 的电子结构状态,使得Fe-VN 具有更优异的导电性和电解液润湿性,进而表现出良好的电化学性能。通过Fe 元素的掺杂,提供了一种新型的高性能超电容电极材料,并且提出了一种利用电子结构调控来改善材料电化学性能的新思路。
1 试验方法
本文中所涉及的V2O5、尿素、硫酸铁等试剂药品均采购于国药集团化学试剂有限公司,其纯度均为分析纯,且均未经过进一步提纯处理。
1.1 VN 材料的制备
称取0.2 g V2O5和5 g 尿素(质量比1∶25)分别置于瓷舟中。将尿素置于管式炉的上风口中,将V2O5置于管式炉的下风口中,在N2气氛下,以3 ℃/min的升温速率,在550 ℃保温2 h,进行氨解氮化试验,从而制得VN 材料。为了尽可能消除氨解氮化反应过程中残余碳的影响,利用碱性化学氧化刻蚀液(AOES 溶液,具体配制方法详见参考文献3)[3]在60 ℃条件下进行氧化刻蚀,从而得到目标产物VN。
1.2 Fe-VN 材料的制备
Fe-VN 材料制备的过程与VN 材料制备基本一致。不同点在于,将0.02 g 的硫酸铁与V2O5充分研磨混合后一起置于管式炉下风口。其余条件和步骤1.1 相同,所得到的产物标记为Fe-VN。
1.3 物相和结构信息表征
利用X 射线衍射仪对反应产物进行XRD 表征,参数具体为:扫描范围为3°~70°、扫描速率为10°/min、Cu Kα 射线、射线管电压为40 kV。利用高分辨透射电镜(HRTEM)对样品进行微观形貌表征,其相应加速电压为200 kV。利用X 射线光电子能谱仪进行样品中各组成元素的XPS 表征,各项参数具体为:压强为2 × 10-9Pa、Al Kα。利用接触角测试仪对样品进行润湿性测试,测试溶液为1 mol/L KOH 电解液。
1.4 电化学性能测试
采用上海辰华760E (CHI 760E,CH Instruments Inc.,Chenghua,Shanghai)电化学工作站对所制备的产物进行超电容性能测试。各项电化学性能测试的具体参数为:循环伏安(CV)曲线测试的扫速为100 mV/s;恒电流充放电(GCD)曲线测试的窗口电压为-0.2~-1 V,充放电电流密度为1 A/g;循环稳定性测试的电流密度为10 A/g,循环充放电次数为1 000 圈;交流阻抗(EIS)测试时交流电的频率范围为100 kHz 至0.01 Hz,振幅为5 mV,电压为开路电压。
1.5 理论计算
采用平面波密度泛函理论(DFT)+U 计算方法对VN 和Fe-VN 的电子结构进行优化模拟。具体各参数为:Fe 元素、V 元素的U值分别为5.0、3.25 eV,截断能520 eV,自洽场(SCF)1×10-4eV,1×1×1 k点,并采用超柔赝电势的方法。
吸附能的计算根据下述方程式计算得到:

其中,E(facet/OH-)为优化后吸附结构的能量;E(OH-)是OH-的能量;E(facet)为优化后的VN 基材料的(200)晶面的能量。
2 结果与讨论
图1(a)、(b)为优化后的VN 和Fe-VN 的晶体结构模型,通过结构对比可以看出Fe 元素的引入并没有显著改变VN 的微观晶体结构。同时,将所制备的VN 和Fe-VN 进行XRD 分析,由图1(c)所示,Fe 元素的引入并未导致XRD 曲线中出现新的特征衍射峰,说明Fe 元素被成功引入到VN 晶体结构中。此外,Raman 结果(图1(d))也表明,Fe 元素的引入并没有使得VN 产生新的特征峰,即Fe 元素的引入并没有改变VN 材料的物相结构,这一结构与XRD 表征的结论是一致的。
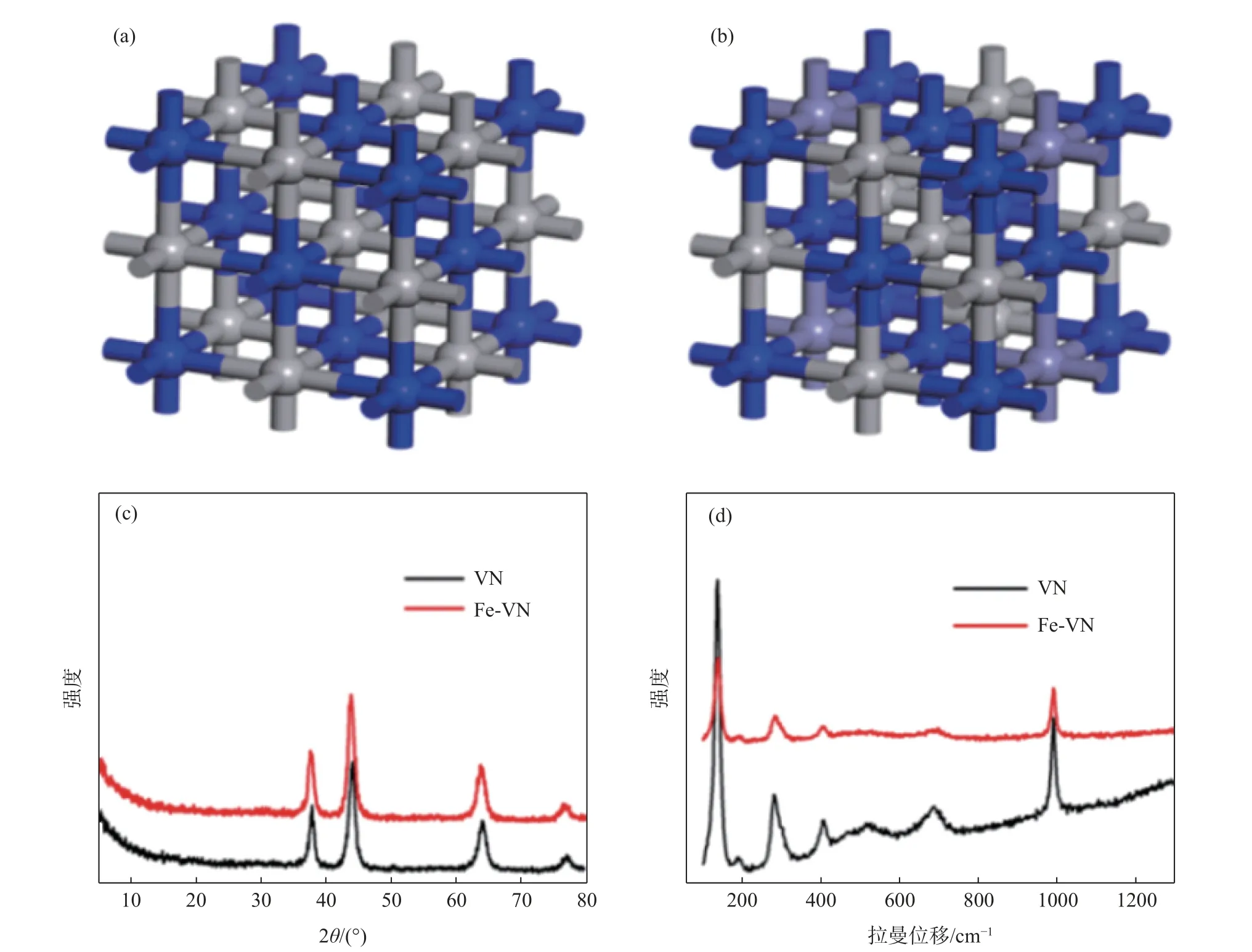
图1 VN(a)与Fe-VN(b)的晶体结构模型,XRD(c)和Raman(d)表征Fig.1 The crystal structure of (a)VN and (b)Fe-VN.(c)XRD and (d)Raman spectra
利用HRTEM 对VN 和Fe-VN 进行表征,其结果如图2 所示。可见,VN 和Fe-VN 均表现出纳米颗粒状,同时,无论是VN 还是Fe-VN 均观测到晶面间距为0.21 nm 的晶格条纹,进一步分析可以将其归属于(200)晶面。将所得到的晶面进行FFT 转换,不难看出,无论是VN 还是Fe-VN,其衍射斑点均表现为典型的单晶结构,说明Fe 的引入不会改变VN 的晶相结构信息,这一结论也与此前的XRD 和Raman 结果一致。通过EDS 和Mapping 分析可以看出,所得到的Fe-VN中,Fe、V、N元素都均匀的分布在材料的表面(碳元素的来源可能是由于导电胶的存在),并且Fe 与V 元素的比例约为1∶20,基本与反应的物料投放比例是一致的。
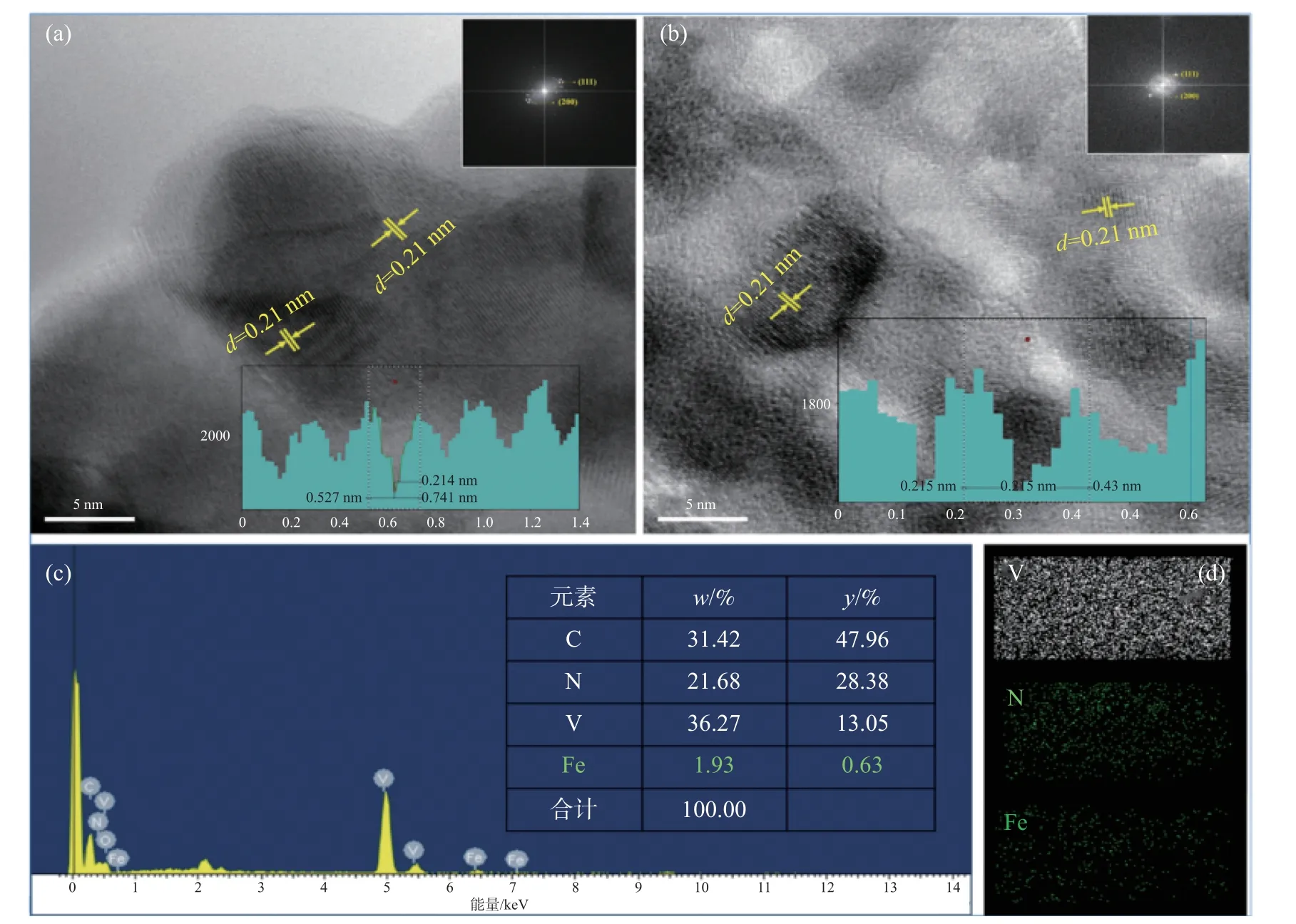
图2 VN(a)与Fe-VN(b)的HRTEM 表征及Fe-VN 的EDS(c)和Mapping(d)表征Fig.2 The HRTEM images of (a)V and (b)Fe-VN.(c)EDS and (d)mapping of Fe-VN
为了探究Fe 元素的引入对VN 基材料电化学性能的影响,以所制备的VN 基材料作为工作电极,1 mol/L KOH 溶液为电解液,进行三电极体系测试,其结果如图3 所示。由图3(a)可见,在-0.6 V 和-0.8 V 左右的氧化还原特征峰应归属于V3+的氧化还原特征峰,对比峰电流大小变化可以看出,Fe 元素的引入使得VN 基材料表现出更大的氧化还原峰电流,而该氧化还原能力的变强使得材料的电化学储能容量得到提升。此外,通过对比CV 曲线的面积可以看出,Fe 元素引入后,CV 曲线的面积具有一个明显的增加,说明Fe 元素的引入使得VN 的比容量有了较大的提升。为了进一步说明容量变化,我们进行了GCD(恒电流充放电)测试。如图3(b)所示,在1 A/g 电流密度条件下(电压窗口为-0.2~-1.0 V),Fe-VN 材料的放电时间为275 s,对应比容量为343.75 F/g,相较而言,VN 材料的放电时间仅为113 s,对应比容量为141.25 F/g。该结果表明,通过引入Fe 元素可以显著的提升VN 材料的超电容性能。为了进一步说明Fe 元素的引入对VN 材料的影响,还进行了EIS 曲线测试。如图3(c)所示,在高频区段,Fe-VN 的EIS 曲线具有比VN 更小的半圆和更小的截距,这说明相比于VN,Fe-VN具有更小的体系电阻(Rct)和液接电阻(Rs),即由于Fe 元素的引入,使得VN 具有更优异的电子/离子导电性,因此,表现出更优异的电化学性能。
对于电极材料,除了拥有良好的比容量,较好的循环稳定性也是一项关键的性能指标。我们在10 A/g 的电流密度条件下,对VN 和Fe-VN 电极材料进行循环充放电测试,以表征材料的循环寿命。如图3(d)所示,经过1 000 次循环充放电后,Fe-VN仍能保持85%的初始容量,明显优于VN(1 000 次循环充放电后仅能保持57%的初始容量),表现出良好的循环稳定性。

图3 VN 与Fe-VN 的电化学性能测试Fig.3 The electrochemical performances of VN and Fe-VN
为了进一步说明Fe 元素的引入对VN 电子结构所产生的影响,对其进行XPS 表征,以研究电子结构与性能之间的构效关系,结果如图4 所示。从图4 可以看出,在全谱图中新出现了Fe 元素特征峰,进一步说明了我们成功的将Fe 元素引入到VN 中。通过分峰拟合(图4(c))可以看出,V 的2p3/2可以拟合出分别归属于V5+-O(V1)、V3+-O(V2)和V3+-N(V3)的三个峰。对比Fe 元素掺杂前后,不难发现由于Fe 元素的掺杂,使得有部分V1 和V2 峰发生了红移,即Fe 元素的掺杂导致了V 元素中价态的降低。与此同时,从图4(d)可以看出,N 元素的变化趋势与V 元素相反,由于Fe 元素的引入,N 的2p3/2发生了蓝移。分析这一结果可以推测出,电子发生了从Fe 元素到N 元素到V 元素的电子转移,进而导致V 元素价态的降低、N 的电荷密度增加。
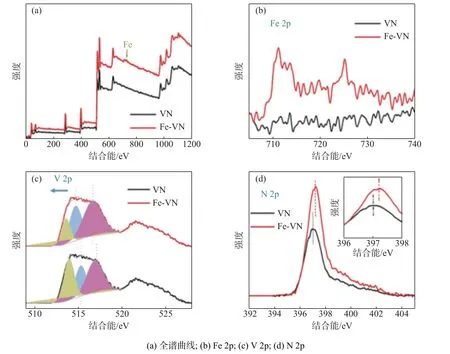
图4 VN 与Fe-VN 的XPS 表征及分峰拟合Fig.4 The XPS spectra of VN and Fe-VN
通过第一性原理计算,可以进一步解释电子结构变化过程。图5(a)、(b)为VN 和Fe-VN 的差分电荷密度分布。通过对比Fe 掺杂前后VN 和Fe-VN 中V 活性位的电荷密度差异,不难看出,Fe 掺杂后,V 活性位的电荷密度相较于纯相的VN 中V位点的电荷密度更高,这一结果与XPS 测试结果是一致的。分析其原因,可能是由于Fe(1.83)的电负性大于V(1.63),同时,相较于V(Fe 掺杂后替代了部分V 的位置),Fe 的电子云密度更大,进而造成了电子从Fe 元素到N 元素到V 元素自发转移。另一方面,V 位点附近的电子云密度的增加还会影响VN 键的键长变化。如图5(c)、(d)所示,Fe 掺杂后,VN 键的键长变得更长(0.203 6 nm 变为0.223 0 nm)。同时,由于键长变长,将使得V-N 键更容易断裂,更有利于OH-的吸附,进而表现出良好的电解液润湿性。

图5 Fe-VN(a,c)和VN(b,d)的差分电荷密度分布对比及相应晶体结构Fig.5 The differential charge density distribution and crystal structures of (a,c)Fe-VN and (b,d)VN
为了说明Fe 元素的引入对VN 材料电解液润湿性的影响,进行了接触角性能测试,同时,利用DFT 模拟计算,分析了VN 和Fe-VN 的(200)晶面对OH-的吸附能力大小,其结果如图6 和表1 所示。

表1 VN 和Fe-VN 的(200)晶面对OH-的吸附能Table 1 The adsorption energy of (200)lattice plane for OH-

图6 VN 和Fe-VN 的接触角性能测试及(200)晶面对OH-的吸附能计算Fig.6 (a)Contact angle tests and (b,c)adsorption energy of (200)lattice plane of VN and Fe-VN
通过对比可以直观地看出,相较于VN,Fe-VN在电解液中具有更小的接触角,表现出更优异的电解液润湿性。经过Fe 元素的引入,(200)晶面对OH-的吸附能由-13.53 eV 降为-15.12 eV。更负的吸附能值说明,Fe 元素的引入有利于增加材料在电解液中的润湿性,两者结果一致。良好的电解液润湿性有利于电解液与电极材料表面的充分接触,有利于电子/离子的快速输运,进而实现快速的氧化还原反应,因此,Fe-VN 可以表现出优异的电化学性能。
综合上述分析结果可以看出,通过Fe 元素的引入,可以实现对VN 的电子结构调控,使得Fe-VN具有更好的导电性和电解液润湿性,提升了材料的电子/离子输运性能,进而表现出良好的超电容性能。
3 结论
通过理论计算和试验制备,系统探究了Fe 元素的引入对VN 材料的电子调控作用机制,通过对制备出的Fe-VN 超电容电极材料进行相关的物相信息表征和电化学性能测试,揭示了Fe-VN 材料优异的超电容性能与电子结构之间的构效关系,验证了利用电子结构调控来进行VN 材料超电容性能改进的可行性。此外,该工作有助于启发更多读者进一步关注电子结构调控策略在高效超电容电极材料领域的开发与研究。

