腹腔镜与胆道镜微创取石术联合治疗胆囊结石并胆囊息肉的临床效果观察
周雷升,王光辉
(青岛市黄岛区中心医院普外科,山东青岛 266555)
近年来,随着我国生活水平的提高使人们饮食结构的发生改变,胆囊疾病的发生率也随之攀升,现已备受社会各界的广泛关注[1]。胆囊结石(gallstone,GS)与胆囊息肉(gallbladder polyps,GP)均是临床常见的胆囊疾病,其中GS主要为胆固醇结石或以胆固醇为主的黑色素结合与混合性结石,GP是出现于胆囊壁并向胆囊腔隆起或突出的病变[2]。目前,外科手术是治疗GS合并GP合并的首选方案,但两者合并后症状更为复杂,进一步增加了术中操作难度[3]。随着微创技术的日益完善,腹腔镜与胆道镜微创技术也在胆囊系统疾病中发挥了重要的作用,具有创伤小、并发症少、恢复快的优势[4]。然而,一些研究对于腹腔镜与胆道镜微创取石术联合治疗GS并GP的效果仍有疑虑[5-6]。鉴于此,本研究探讨该联合术式用于治疗GS并GP的效果,现报道如下。
1 资料与方法
1.1 一般资料 选取2019年10月至2021年5月青岛市黄岛区中心医院收治的92例GS并GP患者,按照随机数字表法分为对照组(46 例,行腹腔镜胆囊切除手术)和研究组(46 例,行腹腔镜与胆道镜微创取石术)。对照组中男、女患者分别为24、22例;年龄22~65岁,平均年龄(42.05±5.45)岁;体质 量 指数(BMI)17.65~26.45 kg/m2,平均BMI(23.00±1.12)kg/m2;GS病 程1~8年,平均GS病程(3.20±0.52)年;GP病程6个月~6年,平均GP病程(2.25±0.45)年;息肉数目:单发26例,多发20例;合并基础疾病:糖尿病6例,高血压4例,冠心病2例。研究组中男、女患者分别为25、21例;年龄22~63岁,平均年龄(42.00±6.02)岁;BMI 17.60~26.43 kg/m2,平均BMI(23.12±1.08)kg/m2;GS病 程1~8年,平均GS病程(3.18±0.60)年;GP病程8个月~6年,平均GP病程(2.28±0.50)年;息肉数目:单发25例,多发21例;合并基础疾病:糖尿病5例,高血压5例,冠心病2例。两组患者一般资料比较,差异无统计学意义(P>0.05),组间具有可比性。本研究经青岛市黄岛区中心医院医学伦理委员会批准,患者及家属均对研究知情并签署知情同意书。纳入标准:①符合《外科学》(第9 版)[7]中GS及GP的诊断标准;②术前3个月未发作急性胆囊炎;③胆囊壁厚<4 mm;④无上腹部手术史;⑤脂肪餐后2 h超声提示胆囊收缩>30%;⑥生命体征平稳。排除标准:①严重心血管疾病;②处于急性炎症期;③重要器脏异常;④恶性肿瘤;⑤免疫系统及内分泌系统疾病;⑥其他消化系统疾病;⑦凝血功能异常;⑧妊娠或哺乳期患者;⑨精神异常。
1.2 研究方法 对照组患者行腹腔镜胆囊切除手术。患者取仰卧位,行气管插管全身麻醉,术前留置导尿管。在脐正下方开放1 cm弧形切口,气腹针置入并建立人工二氧化碳(CO2)气腹,压力控制在10~12 mmHg(1 mmHg=0.133 kPa)。予腹腔镜(日本奥林巴斯株式会社,型号:S190)置入后分别在右侧肋缘下及剑突处开放切口,置入操作器械,观察视野下腹腔情况,分离胆囊与胆总管,明确“三管一壶腹”关系,将胆囊切除并予以充分的止血。观察术区有无渗血与胆汁漏等情况,解除气腹,以生理盐水对腹腔进行冲洗,常规留置引流管,关闭切口。研究组患者行腹腔镜与胆道镜微创取石术。患者取仰卧位,在其肚脐孔上缘开放2 cm孤形切口,气腹针置入后建立人工CO2气腹,压力控制在10~12 mmHg。将腹腔镜及套管针(1 cm)置入,探查肝脏及胆囊情况,明确胆囊的粘连度、外观及周围血运,再次明确是否保留胆囊。在腹腔镜的观察下,明确胆囊位置,在胆囊底部开放小切口(1.5 cm),若胆囊壁光滑且周围无粘连可以缝合胆囊底部,之后再予以牵引处理,经右上腹切口将胆囊提起,再于底部开放小切口(1 cm),胆囊壁以缝线悬吊,并置入胆道镜(日本奥林巴斯株式会社,型号:CHF-V)内,充分冲洗胆汁。通过胆道镜对胆囊息肉进行钳夹,取出后冰冻送至活检。通过取石篮取出胆囊结石,针对体积过大的结石可将胆囊移至腹壁切开,吸出胆汁后取出结石,体积过小难以取出的颗粒结石则予以生理盐水冲洗。完成上述操作后多次在胆道镜下检查结石与息肉是否完全切除,若未见残留,且无活动性出血,以生理盐水对腹腔进行冲洗,关闭切口。
1.3 观察指标 ①比较两组患者术中与术后指标。指标包括手术操作时间、术中失血量、术后首次排气时间、术后首次离床活动时间及住院时间。②比较两组患者术后并发症发生率。并发症包括胆汁漏、胆道感染、肝外胆管损伤、胰腺炎及消化不良。③比较两组患者复发情况。术后随访12个月,参照《胆囊良性疾病治疗决策的专家共识(2011版)》[8]中的标准对GS及GP复发情况进行观察与记录。GS复发:影像学观察下胆囊内数量不等强回声光团,光团后通常伴有尾影,体位改变时光团位置发生变化,临床表现为右上腹阵发性疼痛,或伴有右侧肩胛放射性疼痛,合并胆管梗阻时伴有黄疸表现。GP复发:影像学观察下呈高回声或稍强回声,后方一般不伴有声影,不随体位变化而变化,患者无典型症状,或偶尔有上腹部疼痛、恶心呕吐等症状。
1.4 统计学分析 采用SPSS 23.0统计学软件处理数据。符合正态分布的计量资料以(x)表示,组间比较行独立样本t检验;计数资料以[例(%)] 表示,组间比较行χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者术中与术后指标比较 两组患者手术操作时间比较,差异无统计学意义(P>0.05);研究组患者术中失血量少于对照组,术后首次排气时间、术后首次离床活动时间、住院时间均短于对照组,差异有统计学意义(P<0.05),见表1。
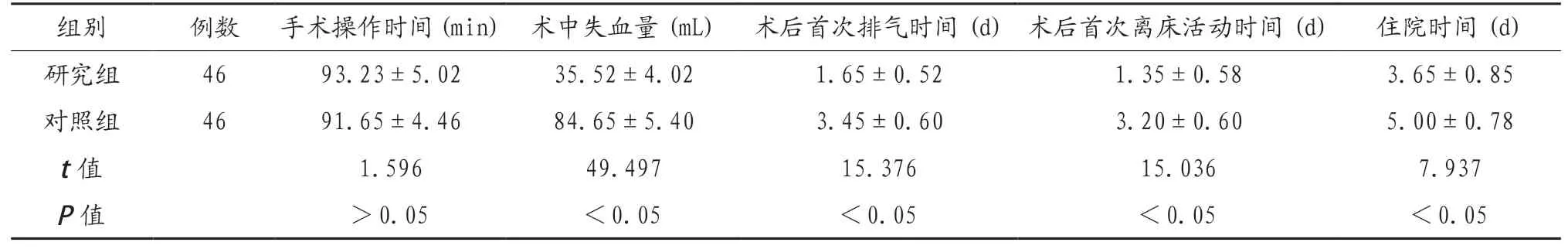
表1 两组患者术中与术后指标比较(x)
2.2 两组患者术后并发症发生率比较 研究组患者术后并发症发生率低于对照组,差异有统计学意义(P<0.05),见表2。

表2 两组患者术后并发症发生率比较 [例(%)]
2.3 两组患者复发情况比较 随访12个月后,两组患者总复发率比较,差异无统计学意义(P>0.05),见表3。

表3 两组患者复发情况比较 [例(%)]
3 讨论
GS与GP均是临床常见的胆囊疾病,主要采取外科手术方式治疗。近年来微创腹腔镜技术的普及进一步降低了胆囊切除术的创伤性,一度被认为是治疗GS的“金标准”[9]。同时,胆囊切除术也是治疗GP的主要方法,临床将超过1 cm的GP作为手术指征[10]。然而,多数GP患者的胆囊功能仍处于正常状态,加之多为胆固醇息肉,虽有恶性病变的可能性,但对患者的威胁性并不大[11]。胆囊的功能是储存和浓缩胆汁,参与食物的吸收与消化,切除胆囊后增大胆管具有一定的胆囊储备能力,但却失去了收缩功能,给患者的消化功能造成不良影响,甚至造成消化系统生理功能紊乱。因此,越来越多的报道认为在GS并GP患者中开展保胆手术具有可行性[12]。
腹腔镜联合胆道镜技术是一种新型的胆囊取石术,内镜下操作利于术者全面观察胆囊与周围组织情况,明确有无胆囊炎症、粘连及脏器出血损伤等问题,其中胆道镜的使用能够识别胆囊内壁与胆囊腔是否存在异常,以便更好地清除结石与息肉,避免病灶残留[13]。同时,腹腔镜联合胆道镜技术中未对胆囊三角区进行分离,操作简便,有效减少了肌肉与血管损伤。为了进一步完善GS并GP患者的治疗方案,本研究对92例患者分别应用了腹腔镜胆囊切除术与腹腔镜联合胆道镜技术治疗。
本研究结果显示,研究组患者术中失血量低于对照组,术后首次排气时间、术后首次离床活动时间、住院时间均比对照组短,两组患者手术时间比较,差异无统计学意义。与常规腹腔镜胆囊切除术相比,虽然腹腔镜与胆道镜微创取石术的手术操作时间不具优势,但保胆手术的创伤性更为轻微,能够有效减少术中失血量,加快术后康复速度。本研究结果显示,随访12个月后,两组患者总复发率无明显差异。研究组患者术后并发症发生率比对照组低。这提示相较于常规腹腔镜胆囊切除术,腹腔镜与胆道镜微创取石术并未增加GS与GP的复发风险,考虑与内镜直视下视野良好,充分清理了胆囊管或胆囊颈部的残留结石与息肉有关[14]。同时,腹腔镜与胆道镜微创取石术保留了胆道的完整性,术中无需解剖胆囊三角区,减少了胆道感染、肝外胆管损伤及术后消化不良等并发症发生率,为患者的生活质量提供了有利的保障[15]。需要注意的是,为了保证GS并GP患者的治疗效果与安全,临床应严格掌握保胆手术指征。
综上所述,相较于腹腔镜胆囊切除术,腹腔镜与胆道镜微创取石术联合治疗GS并GP可减少术中出血量,降低并发症发生率,缩短术后康复进程,且未增加复发率,具有临床应用价值。

