零价铁锰复合材料的制备及其对锑的去除研究*
陈元铉 陈思浩 余明霞 周 颖 王伟彤 龙建友
(广州大学环境科学与工程学院,广东 广州 510006)
随着现代工业的迅猛发展及含锑矿产资源的过度开发,锑大量排放,对环境造成了一定的污染[1]。锑毒性与砷类似,过量的锑对人体具有致癌性,已被美国及欧盟列入优先控制污染物范畴。我国《工业水污染物排放标准》(GB 4287—2012)规定:废水中总锑的直接和间接排放限值均为100 μg/L,锑作为污染物在环境中主要以Sb(Ⅲ)和Sb(Ⅴ)形式存在,并能在环境中迁移转化,对周边的生态环境产生严重的破坏及威胁人类健康,若不及时加以处理,不仅会对环境及人体健康造成不同程度的损害,而且也会造成巨大的经济损失[2-3]。因此,对含锑废水的去除迫在眉睫。目前,去除水中锑的方法主要有吸附[4]、离子交换[5]、电化学处理[6]、生物修复[7]等。吸附是一种简单易行的废水处理技术,一般适用于处理量大、浓度范围广的水处理体系,该方法性能优良,成本低廉,吸附剂可回收,与其他方法相比,具有更强的实用性。
在众多吸附剂材料中,零价金属材料在近年研究中备受关注,如零价铁[8]、零价铝[9]、零价锌[10]、零价铜[11]、零价锰[12]等。其中零价铁材料自身无毒,成本相对较低;表面积大,使得活性位点密度更大,对有毒金属去除效率更高;同时自身的磁性使其在分离方面具有独特的优势,因而成为众多零价金属中的研究热点[13]。然而,尽管零价铁材料有众多优点,但它在溶液中分散性差和自身的团聚特点[14],使得单一零价铁在实际应用中受限。相比零价铁的还原电位(-0.44 V)[15],零价锰具有更强的还原电位(-1.18 V),而且体积小、表面积也大[16],在环境污染处理应用方面具有很大潜力。
由于零价铁的磁选性和零价锰优异的还原能力,本实验结合这两种零价金属材料,探索解决零价铁材料在应用上的缺陷,以期制备出一种既拥有良好磁分离性又具有优秀吸附性能的复合材料。实验中使用硼氢化钠还原法制备零价铁锰复合材料,研究该复合材料对水中Sb(Ⅲ)和Sb(Ⅴ)的去除效果,通过改变反应初始pH、反应时间、溶液初始浓度和共存阴离子浓度等实验条件,研究该材料对Sb(Ⅲ)和Sb(Ⅴ)的吸附性能与吸附机理,为去除水中Sb(Ⅲ)和Sb(Ⅴ)提供一种新的研究思路和途径。
1 材料与方法
1.1 实验材料与实验器材
氯化铁、硫酸锰、硼氢化钠、焦锑酸钾、酒石酸锑钾、偏硅酸钠、碳酸钠、磷酸钠、硫酸钠均为分析纯,购自上海某生化科技有限公司。
1.2 实验方法
1.2.1 零价铁锰复合材料(nZVMn/I)的制备
采用硼氢化钠还原法[17]还原氯化铁和硫酸锰制得零价铁和零价锰质量比为1∶2的复合材料,具体合成方法是配置0.136 7 mol/L的氯化铁溶液50 mL、0.172 0 mol/L的硫酸锰溶液50 mL和0.600 0 mol/L的过量硼氢化钠溶液100 mL,在厌氧条件下,用蠕动泵先将硫酸锰溶液恒定流速缓慢通入正在搅拌的硼氢化钠溶液中,待硫酸锰溶液完全通入硼氢化钠溶液后,再通入氯化铁溶液,待氯化铁溶液完全通入后继续反应30 min。体系中的反应方程见式(1)和式(2):

(1)

(2)
反应结束后静止10 min,去掉上清液,用去离子水将沉淀洗涤3遍,放入冷冻干燥器中干燥24 h。干燥后得到nZVMn/I密封保存于干燥器中备用。
1.2.2 nZVMn/I对水中Sb(Ⅲ)和Sb(Ⅴ)的吸附
分别以酒石酸锑钾和焦锑酸钾溶于去离子水配制1 000 mg/L的Sb(Ⅲ)和Sb(Ⅴ)储备液,不同浓度的Sb(Ⅲ)和Sb(Ⅴ)模拟废水以储备液稀释制得。如无特殊说明,实验溶液体积为20 mL,溶液初始pH为7.0,反应时间为1 h,反应温度为25 ℃,吸附剂投加量为1 g/L,反应结束后用0.22 μm滤膜过滤,过滤后的样品加体积分数为50%的硝酸0.2 mL保存,用 PerkinElmer Nexion 300电感耦合等离子体发射光谱(ICP-OES)仪测定其中的Sb(Ⅲ)和Sb(Ⅴ)浓度。
2 结果与分析
2.1 材料表征
2.1.1 扫描电子显微镜(SEM)和透射电子显微镜(TEM)表征
利用SEM和TEM对nZVMn/I的表面和内部结构进行观察,结果如图1所示。图1(a)显示,材料的表面是由类似球体的结构簇拥而成的,表面十分粗糙;图1(b)、图1(c)和图1(d)显示,材料的内部结构为交叉相接的棒状结构,在交织而成的棒状结构上有一些非均匀分布的球状颗粒。而TEM图像(见图1(e)和图1(f))更加证实了nZVMn/I是由颗粒状和不规则的交织棒状结构所组成。在先前的研究中可知,零价锰为交织的棒状结构[18]9936,而零价铁则为簇拥的球状颗粒[19]。nZVMn/I拥有疏松多孔的结构,这种结构不仅使得吸附剂材料拥有较大比表面积,而且更有利于锑快速扩散到材料的内部,提高材料的吸附性能。
2.1.2 比表面积和空隙结构
比表面积和孔隙结构是吸附剂材料吸附污染物的关键参数。吸附剂材料的比表面积、孔径和孔体积采用N2吸附/脱附法测定。图2(a)为nZVMn/I的N2吸附/脱附曲线,采用BET多点法计算得到nZVMn/I的比表面积为220.45 m2/g,孔体积为0.51 cm3/g。图2(b)为通过BJH法计算的孔径分布图,计算得到的平均孔径为15.84 nm。较大的比表面积和孔体积有助于锑污染物快速进入材料内部,与材料充分接触,有利于吸附反应的进行。
2.1.3 X射线光电子能谱(XPS) 表征
nZVMn/I在Mn 2p的拟合分峰如图3(a)所示,Mn 2p3/2可分为639.6、641.1、642.1、643.3 eV 4个峰,分别对应Mn0、Mn(Ⅱ)、Mn(Ⅲ)和Mn(Ⅳ)[20-22],质量分数分别为2.5%、37.8%、32.2%和27.5%,说明材料成功合成零价锰。图3(b)为nZVMn/I在Fe 2p的分峰拟合结果,706.5、710.9、712.3 eV处的峰分别对应Fe0、Fe(Ⅱ)和Fe(Ⅲ)[23],质量分数分别为0.9%、39.9%、60.2%,说明材料成功合成零价铁。
2.2 吸附性能
2.2.1 初始pH对nZVMn/I吸附锑的影响

2.2.2 共存阴离子对nZVMn/I吸附锑的影响
2.3 锑的吸附机理
2.3.1 吸附动力学
为探究吸附剂材料在吸附过程中的动力学参数,本实验研究了吸附时间对Sb(Ⅲ)和Sb(Ⅴ)吸附量的影响。实验结果如图6所示,在50 mg/L的Sb(Ⅲ)初始质量浓度下,吸附剂在0~60 min对Sb(Ⅲ)吸附速率较高,吸附量随吸附时间迅速增大,这可能是由于在吸附过程开始时,nZVMn/I自身疏松的结构,使得锑可以迅速在材料内部扩散,同时吸附材料表面提供的大量活性位点,有利于锑与吸附剂结合,吸附过程到达60 min后,材料对Sb(Ⅲ)的吸附量缓慢下降。在Sb(Ⅴ)初始质量浓度为50 mg/L时,60 min后材料对Sb(Ⅴ)的吸附量增加缓慢,这是由于吸附剂表面的活性位点被污染物占据,逐渐趋于饱和,吸附变得缓慢。在10 mg/L的初始质量浓度下,nZVMn/I对Sb(Ⅲ)和Sb(Ⅴ)的吸附过程中,0~60 min为快速吸附阶段,60 min后达到吸附平衡。表1 显示了nZVMn/I对Sb(Ⅲ)和Sb(Ⅴ)吸附的准一级和准二级动力学模型参数,由R2可知,吸附材料对Sb(Ⅲ)和Sb(Ⅴ)的吸附过程更符合准二级动力学模型,说明nZVMn/I对Sb(Ⅲ)和Sb(Ⅴ)的吸附属于化学吸附[27]。
2.3.2 等温吸附线
为探究吸附剂对Sb(Ⅲ)和Sb(Ⅴ)的最大吸附量,分别对Sb(Ⅲ)和Sb(Ⅴ)进行了等温吸附实验,所得实验数据分别使用Langmuir模型和Freundlich模型进行拟合(见图7)。表2 列出了等温吸附拟合参数,Langmuir模型和Freundlich模型的R2均大于0.9,说明两种模型均能有效描述nZVMn/I对Sb(Ⅲ)和Sb(Ⅴ)的吸附,而Freundlich模型的拟合度更好,表示nZVMn/I表面可能是多层非均相的[28]。由表2中Langmuir模型参数可知,nZVMn/I对Sb(Ⅲ)和Sb(Ⅴ)的最大吸附量分别是614.622、241.702 mg/g。
本研究同时采用硼氢化钠还原法制备了零价锰(记为nZVMn),将其与nZVMn/I对锑的吸附性能进行对比。硼氢化钠还原法制备的零价铁(记为nZVI)对锑的吸附性能已有相关研究。表3 为3种材料的除锑性能比较。nZVI对Sb(Ⅲ)和Sb(Ⅴ)的吸附量低于其余两种材料,nZVMn对Sb(Ⅴ)有较高的吸附量,nZVMn/I对毒性较大的Sb(Ⅲ)的吸附量高于nZVI和nZVMn。由此可见,复合材料中的nZVMn和nZVI对Sb(Ⅲ)的去除起到协同作用,使其成为含锑废水处理过程中潜在的良好吸附剂。
2.3.3 傅立叶红外光谱(FTIR)分析
从图8可以看出,吸附前的nZVMn/I在3 425 cm-1处有明显的宽吸收峰,这归因于材料带有的水中的羟基引起的伸缩振动[30],1 627 cm-1处出现的吸收峰是吸附剂材料中物理吸附的水分子的弯曲振动吸收峰[18]9936。1 339 cm-1处的峰是nZVI周围形成的Fe3O4、Fe2O3和FeOOH所引起的[31],吸附Sb(Ⅲ)和Sb(Ⅴ)后吸收峰强度降低,推测材料表面发生氧化。在1 155、1 068、985 cm-1处的吸收峰是铁和锰氧化物表面的羟基的弯曲振动峰[32],在1 116 cm-1处出现的吸收峰可归因于金属羟基的弯曲振动[33],在867 cm-1处检测到的峰是Fe-OH弯曲振动引起的[34],吸附后上述吸收峰强度有不同程度地减弱,由此推测在水中吸附锑时,材料的金属羟基基团参与了反应。吸附前在608 cm-1处检测出的吸收峰和吸附后在550 cm-1处检测出的吸收峰可归因于材料中的Mn-O[35-36],吸附前608 cm-1处的峰强度较弱,在吸附后向550 cm-1偏移并且强度增加,这可能与Mn-O-Sb的形成有关,推测Mn-O在除锑过程中发挥作用[37]。
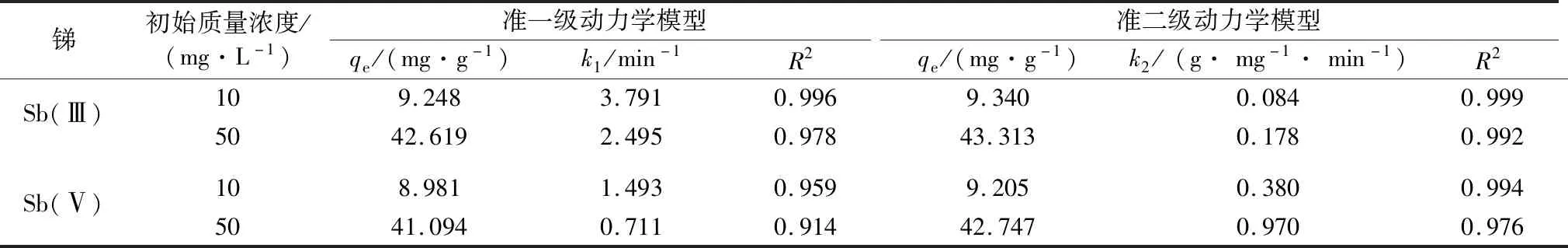
表1 吸附动力学模型参数1)Table 1 The fitting parameters of the adsorption kinetic models

表2 等温吸附模型参数1)Table 2 Isotherms parameters

表 3 不同吸附剂去除Sb(Ⅲ)和Sb(Ⅴ)的效能比较Table 3 Comparison of antimony Sb(Ⅲ) and Sb(Ⅴ) capacities for different adsorbents
3 结 论
(1)采用硼氢化钠还原法制得nZVMn/I,以零价锰为内核,铁锰氧化物为外壳,铁氧化物附着在nZVMn和锰氧化物上,材料结构明显具有疏松多孔的特点,更有利于锑快速扩散到材料的内部,提高吸附性能。
(2)nZVMn/I具有高效吸附Sb(Ⅲ)和Sb(Ⅴ)的特性,在 25 ℃的反应温度,1 h 的反应时间条件下Sb(Ⅲ)和Sb(Ⅴ)的去除率在初始pH为2~10的范围内可稳定在96.7%以上,该条件下,材料对Sb(Ⅲ)和Sb(Ⅴ)的最大吸附量分别可达614.622、241.702 mg/g。
(3)nZVMn/I吸附Sb(Ⅲ)和Sb(Ⅴ)的过程更符合准二级动力学模型,Langmuir模型和Freundlich模型均能有效描述材料对Sb(Ⅲ)和Sb(Ⅴ)的吸附。

