球囊辅助夹闭术治疗颅内大型和巨大型动脉瘤
彭俊强 赵文元 陈劲草
目前,颅内动脉瘤的治疗方法有多种,且取得了很好的效果。但是颅内大型和巨大型动脉瘤(large and giant intracranial aneurysms,LGIAs),因其巨大的体积以及合并的特殊情况,如瘤颈巨大、钙化和容易生长血栓等情况[1],治疗更具有挑战性。球囊辅助动脉瘤夹闭术是近几年用于治疗LGIAs的手术方法[2],且取得了一定效果。2017~2020 年运用球囊辅助夹闭术治疗32例LGIAs,现报道如下。
1 资料和方法
1.1 病例选择标准 纳入标准:①DSA、MRA、CTA 等确诊为颅内动脉瘤;②动脉瘤直径≥15 mm;③同意行球囊辅助夹闭术;④病人及家属对手术方案知情同意并签署知情同意书。排除标准:①动脉瘤直径<15 mm;②保守治疗;③合并其他系统严重疾病。
1.2 一般资料2017~2020年行球囊辅助夹闭术治疗LGIAs 共35 例,其中2 例因动脉瘤合并严重钙化术中改为血管内治疗,1例因瘤颈部过于巨大无法夹闭而改为血运重建术。最终纳入32 例,其中男12 例,女20例;平均年龄(58.3±6.9)岁。入院时Hunt-Hess分级Ⅰ~Ⅱ级22例,Ⅲ~Ⅳ级10例。入院时GCS评分3~8 分3 例,9~15 分29 例。头痛15 例,眩晕8 例,动眼神经麻痹6例,突然意识丧失2例,一侧肢体乏力1例。术前Fisher分级0~2级25例,3~4级7例。
1.3 手术方法 在复合手术室进行手术。先行DSA,找到动脉瘤位置,然后在DSA 导引下经股动脉穿刺送入球囊。根据颈内动脉有无狭窄以及动脉瘤所处位置,即球囊是否能够到达决定球囊放置的位置。对于颈内动脉严重狭窄或者球囊不能到达者,将球囊放置在颈内动脉近心端;对于颈内动脉无明显狭窄,血管情况良好球囊能到达者,将球囊置在动脉瘤瘤颈部进行阻断。采用Scepter C 球囊进行临时阻断。根据动脉瘤位置选取合适手术入路,仔细解剖并暴露动脉瘤。在夹闭动脉瘤前扩张球囊以阻断血流,如果动脉瘤塌陷的不好还可反向抽吸血流,以达到最佳可夹闭的程度。若手术时间较长,还可按需数次扩张球囊阻断血流,每次阻断时间10~15 min,但阻断之间需间隔3~5 min。夹闭完成后,探查动脉瘤周围分支血管以确认有无误夹。再次行DSA,若动脉瘤颈部有明显残留或载瘤动脉狭窄,则调整动脉瘤夹,直到动脉瘤完全或近完全夹闭。术中同时采用电生理监测以确保治疗效果。若术中电生理指标出现异常,则立即暂停手术操作并找到可能的原因或调整操作,尽可能使各项指标恢复到正常范围后再进行手术,以最大化减轻手术对病人的影响。
1.4 预后的评价 术后行CTA复查了解夹闭效果,以Raymond 分级评估夹闭效果。出院时,应用GOS 评分评估预后。末次随访,应用改良Rankin量表(modified Rankin scale,mRS)评分评价预后,0~2 为预后良好,3~6分为预后不良。
2 结果
2.1 影像学结果32例共32个LGIAs,其中大型动脉瘤(直径15~25 mm)22 例,巨大型动脉瘤(直径≥25 mm)10例。囊形动脉瘤21例,梭形或夹层动脉瘤11例。动脉瘤位置:颈内动脉眼动脉段8例,颈内动脉后交通段10 例,大脑中动脉M1~M2 段4 例,颈内动脉前交通动脉段7例,大脑前动脉A1~A2段3例。
2.2 手术结果32 例均在球囊辅助下行动脉瘤夹闭术,术后即刻造影显示完全或近完全闭塞率是100%。23 例球囊放置在颈内动脉近心端,9 例放置在动脉瘤瘤颈部。11例因术中造影示动脉瘤瘤颈残留而调整动脉瘤夹位置,2例术中造影示载瘤动脉狭窄而调整动脉瘤夹位置。8 例扩张球囊后动脉瘤并没有很好的解除压力而反向抽吸血流,最终成功夹闭。5 例术中动脉瘤再破裂,出血量在400 ml 以下,没有发生很严重的出血。4 例动脉瘤严重钙化而使用排栅技术,电灼动脉瘤后进行动脉瘤夹闭。出院时GOS评分4~5分14例,1~3分18例。
2.3 随访结果2 例失访,2 例死亡。剩余28 例随访3~25 个月(中位数12.5 个月)。13 例出现短期神经功能障碍:7 例短期肢体肌力下降,4 例短期视力下降,2例癫痫。6例表现出长期神经功能缺损:3例一侧肢体偏瘫,2 例动眼神经麻痹,1 例视力下降。28例影像随访显示,动脉瘤完全和近完全闭塞27 例(96.4%),1例复发;预后良好23例,预后不良5例。
2.4 典型病例
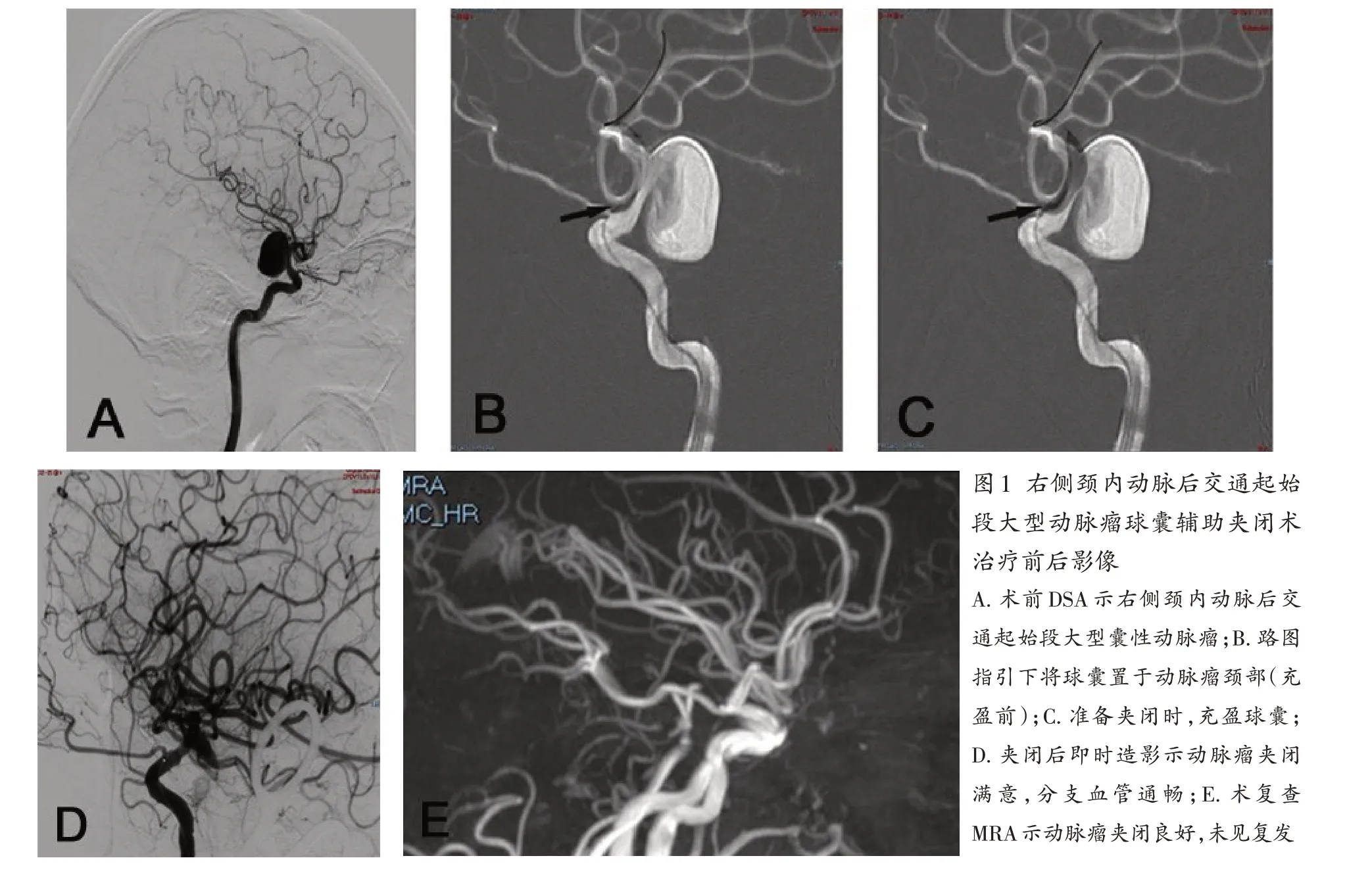
病例1:54 岁男性,因突发头痛7 h 入院。既往史无特殊。入院时体格检查:左下肢肌力4级,颈项强直2指。入院后DSA检查示右侧颈内后交通段大型囊性动脉瘤,直径18 mm×20 mm。完善准备后,行球囊辅助下动脉瘤夹闭术。术中动脉瘤夹闭良好,载瘤血管通畅,无分支血管误夹。影像学随访14个月,未见动脉瘤复发,mRS评分1分。见图1。
病例2:50 岁女性,因间断头晕1 个月余入院。既往有高血压病史6年,规律服用降压药物,血压控制可。入院时体格检查:右侧动眼神经麻痹。入院后DSA 检查示右侧颈内动脉后交通段大型动脉瘤,直径16 mm×14 mm。完善准备后,行球囊辅助下动脉瘤夹闭。术中动脉瘤夹闭良好,载瘤血管通畅,无分支血管误夹。影像学随访11个月,未见动脉瘤复发,mRS评分2分。见图2。
3 讨论
LGIAs 约占颅内动脉瘤的5%[3],容易生长血栓[4],巨大的体积易造成压迫效应,合并一些穿支血管以及更易伴严重动脉粥样硬化等情况,其治疗确一直是难点[5,6]。近几年,复合手术在神经外科领域逐渐发展起来,球囊辅助夹闭技术是其中之一,并且其优势正越来越受到关注。
动脉瘤闭塞率一直是动脉瘤治疗的重点。本文病例术后即刻造影示11 例动脉瘤瘤颈部分残留,2例载瘤动脉狭窄,及时调整动脉瘤夹后,完全和近完全闭塞率是100%,随访完全和近完全闭塞率是96.4%。Roessler 等[7]认为动脉瘤夹闭术中,传统荧光造影有着近10%的漏检率,而且荧光造影也不能显示较深的分支血管。本文病例术后即刻完全和近完全闭塞率较高,与球囊辅助夹闭术中实时造影是分不开的。球囊辅助在血管内介入治疗中运用较多,诸如球囊辅助栓塞宽颈动脉瘤,以及球囊闭塞实验评估病人侧支循环[8]。球囊辅助动脉瘤夹闭术中,球囊可以放置在颈内动脉的近心端和瘤颈部,适合不易通过临时动脉瘤夹阻断血流的病人,以及可避免颈部血管暴露带来创伤。另外,有些侧支循环较为发达的病人,即使球囊临时阻断血运,但是动脉瘤仍然不能很好的解除压力时,还可以反向抽吸血流,为动脉瘤的夹闭提供充足空间,进而能更好地夹闭动脉瘤[10]。本文9例球囊放置在动脉瘤瘤颈部,在夹闭动脉瘤时起到一定的动脉瘤塑形作用。本文5例出现术中破裂出血,得益于球囊的临时阻断,成功地控制了载瘤血管的血流,没有发生严重出血的情况,术后也没有因为过度临时阻断血流或者误夹主要血管而发生大面积脑梗死。开颅夹闭术治疗后循环动脉瘤一直被认为效果不佳,但是Kienzler 等[9]报到球囊辅助下夹闭基底动脉瘤,且取得了较好的效果。因此,球囊辅助夹闭动脉瘤,可以把介入球囊技术和开颅夹闭技术结合起来,这是传统手术所不具备的。

LGIAs 手术治疗预后值得关注。几十年前,夹闭术治疗巨大动脉瘤的病死率高达20%,随着医疗技术的提高以及先进手术设备的出现,病死率已经降至了10%[3,11]。本文2 例(6.7%)死亡,和长期卧床导致肺炎等并发症有关,并不是手术直接造成。可以说球囊辅助夹闭术治疗LGIAs有着较低手术病死率。另外,Ota 等[12]关于LGIAs 外科治疗的结果显示术后6 个月mRS 评分0~2 分病例是78%。Luzzi 等[5]报道显示巨大动脉瘤外科治疗预后良好率为75.7%。本文病例出院时GOS 评分4~5 分的比例为43.8%,随时间推移病人情况逐渐好转,末次随访预后良好的比例为82.1%。因此,球囊辅助夹闭术治疗LGIAs是一种较优的手术方式,能使病人受益。
另外,复合手术室背景下球囊辅助夹闭动脉瘤也具备能够快速转换手术场景的能力。李培良等[13]报到复合手术室背景下术中评估技术可以快速转换手术方式,提高复杂脑血管疾病治疗成功的几率。本文病人在行球囊辅助夹闭术时,有病人因瘤颈巨大无法夹闭而改为血管重建术,也有病人因瘤内合并严重钙化,无法很好夹闭而改为血管内治疗,最终显著提高了治疗效果。
综上所述,球囊辅助夹闭术治疗LGIAs 是一种有效的方式,成功夹闭率高,病死率低,预后良好。

