非布司他治疗终末期肾病伴高尿酸血症的效果及患者发生心血管事件的影响因素分析
严成君 ,李屾 ,马维维 , 刘猛,王芳煜
(皖西卫生职业学院附属医院·六安市第二人民医院,1.肾内科及血透室;2.骨科;3.药剂科,安徽 六安 237000)
终末期肾病(end stage renal disease,ESRD)是慢性肾病的第五期,该阶段肾脏平滑肌细胞及肾小球系膜细胞增生,肾小球基底膜足细胞损伤,以致肾脏功能发生渐进性、不可逆性退减,同时产生因肾功能丧失继发的一系列代谢紊乱及功能异常[1]。高尿酸血症(hyperuricemia,HUA)是ESRD患者全死亡的暴露因素,而积极治疗降低血尿酸患者可明显延长终点事件的发生时间[2]。而心血管事件的发生是引发ESRD患者死亡的主要原因,心血管疾病发生又与高尿酸等密切相关[3]。非布司他隶属于非嘌呤选择性黄嘌呤氧化酶抑制剂,通过紧密结合钼蝶呤相关通道,抑制黄嘌呤氧化酶与底物结合,进而发挥降尿酸的作用[4-5]。此外,该药还通过改善肾小球滤过率,发挥ESRD患者残存肾功能的保护作用。本研究拟探讨非布司他治疗ESRD合并HUA的临床疗效及安全性,并分析患者预后发生心血管事件的危险因素。
1 资料与方法
1.1 一般资料
选取2019年3月至2021年4月皖西卫生职业学院附属医院收治的ESRD合并HUA患者80例为研究对象,根据治疗方式不同分为观察组及对照组,每组各40例。对照组行别嘌醇治疗,观察组行非布司他片治疗。纳入标准:(1)符合中华医学会肾脏病学分会发布的《糖尿病肾脏疾病临床诊疗中国指南》中对ESRD的相关诊断标准[6],肾小球滤过率将至15 mL/(min·1.73 m2);(2)符合中华医学会内分泌学分会发布的《中国高尿酸血症与痛风诊疗指南 (2019)》中关于HUA的相关诊断标准[7],正常嘌呤饮食状态下,非同日两次空腹血,测定血尿酸水平男性或者绝经期女性的血尿酸用尿酸酶测定法,测定值>420 μmol/L,或者非绝经期女性的血尿酸值>362 μmol/L;(3)入组患者透析血管通路为自体动静脉内瘘或长期导管,透析频率3次/周,4 h/次,碳酸氢钠透析液,透析流量2 000 mL/min,低分子肝素钙抗凝;(4)患者及家属均知情并同意。排除标准:(1)合并原发性心脏疾病患者;(2)合并严重器质性脑、肺、肝脏疾病或功能异常患者;(3)合并终末期肾病腹膜透析、肾移植患者;(4)合并半年内服用免疫抑制剂;(5)合并半年内发生心脑血管急性事件患者;(6)临床资料不全或依从性差者。两组患者一般资料比较,差异无统计学意义(P>0.05)。见表1。
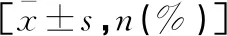
表1 两组患者一般资料比较
1.2 方法
1.2.1 治疗方法 所有入组患者均进行常规治疗,包括低盐、低嘌呤低蛋白饮食、补充α酮酸,采用促红细胞生成素改善贫血,钙通道阻滞剂或β受体阻滞剂控制血压,服用碳酸氢钠纠正电解质紊乱等。观察组在常规治疗基础上给予非布司他片(杭州朱养心药业有限公司)40 mg/次,1次/d,持续干预12周;对照组在常规治疗基础上给予别嘌醇(广东彼迪药业有限公司)100 mg/d,1次/d,持续干预12周。
1.2.2 观察指标 (1)收集两组患者的一般临床资料,包括性别、年龄、既往史、个人史。(2)收集治疗前及干预周期结束后肾功能筛查及相关血清学指标:分别于治疗前及干预周期结束后1 d,采集患者清晨空腹静脉血5 mL,采用尿酸酶-过氧化物酶偶联法检验血尿酸(SUA)水平,混合试剂混匀,自动生化分析仪(罗氏公司Cobas6000)按仪器说明书要求进行测定,试剂盒购自合肥莱尔生物科技有限公司。(3)硝酸还原法检测血清一氧化氮(NO)水平:按步骤加入样本和R1、R2混合实际,37 ℃水浴60 min,加入R3、R4,抽提室温静置40 min 3 500~4 000 rpm,离心40 min,取上清0.5 mL,加入显色剂,静置10 min,550 nm波长,0.5 cm光径测定,试剂盒购自上海懋康生物科技有限公司。(4)放射免疫法检测血清内皮素(ET)-1、血肌酐(SCr)水平:取静脉血2 mL,注入含10%乙二胺四乙酸钠(NaEDTA)30 μL和抑肽酶40 μL的试管中,混匀,4 ℃ 3 000 rpm离心10 min,分离血浆待测或-20 ℃以下保存,操作严格按照说明书进行,ET-1检测试剂盒购自上海邦景实业有限公司;血肌酐检测试剂盒购自上海抚生实业有限公司。(5)胶乳颗粒增强免疫浊度法检测血清胱抑素C(Cys-C)水平:配制待测样品及不同浓度的标准品,分别加入酶标仪的孔板的不同微孔中,然后在各个微孔中先后加入由浓度15~30 g/L的表面活性剂和浓度0.01~0.1 mmol/L的缓冲液组成的R1试剂,由浓度为0.2~2.0 g/L的偶联有抗体的胶乳微球、质量浓度为0.01~0.1%的防腐剂、浓度为0.01~0.1 mmol/L的缓冲液组成的R2试剂,将孔板放入酶标仪中,在30~40 ℃下恒温震荡1~5 min,生成不溶性复合物,酶标仪自动在546 nm波长处检测各个微孔中免疫复合物的吸光值,根据不同浓度的标准品吸光值拟合标准曲线,并自动根据标准曲线计算待测样品中待测物浓度,试剂盒购自上海初态生物科技有限公司。(6)免疫层析法检测血清N末端B型利钠肽前体(NT-proBNP):试剂条标记线一端浸入待测标本中,2~5 s后在标本加样处加一定量待检样本,平放于水平桌面上,5~20 min内观察结果,试剂盒购自上海梵态生物科技有限公司。(7)化学发光法检测血清心肌肌钙蛋白T(cTnT):设标准孔7孔,依次加入100 μL不同浓度的标准品;空白孔加100 μL,余孔加待测样品100 μL,酶标板加上覆膜,37 ℃温育5 h;弃去液体,甩干,不用洗涤;每孔加入100 μL检测溶液A,酶标板加上覆膜,37 ℃温育1 h;弃去孔内液体,自动洗板机洗涤,重复上述步骤洗涤检测溶液B;每孔加底物溶液100 μL,覆膜避光温育10 min,在微孔板型多功能化学发光仪上测量化学发光信号(RLU值),试剂盒购自上海西格生物科技有限公司。(8)双抗体夹心法检测血清超氧化物歧化酶(SOD)水平:分别设置空白孔、待测样品孔。在酶标包被板上待测样品孔中先加样品稀释液40 μL,再加待测样品10 μL(样品最终稀释为5倍),将样品加于酶标板孔底部,尽量不触及孔壁,轻轻晃动混匀;37 ℃温育30 min,30倍浓缩洗涤液用蒸馏水30倍稀释备用;洗涤后静置拍干,加酶;重复温育、洗涤操作;每孔加显色剂,避光显色,加终止液50 μL,终止反应;450 mm波长依序测量各孔吸光度,试剂盒购自合肥莱尔生物科技有限公司。(9)硫代巴比妥酸法检测血清丙二醛(MDA)水平:标准管、标准空白管、测定管、测定空白管各10 ng/mL标准品;漩涡混匀器混匀,试管口用保鲜薄膜扎紧,用针头刺一小孔,95 ℃水浴40 min;取出后流水冷却,然后4 000 rpm,离心10 min,使沉淀完全;取上清,吸取上清比色时用移液器吸取上清加入比色皿中,尽量避免倾倒,以免沉淀进入比色皿,影响吸光度; 把比色皿置于532 nm处,1 cm光径,蒸馏水调零,测各管吸光度值,试剂盒购自合肥莱尔生物科技有限公司。(10)二硫代二硝酸苯甲酸显色法检测血清谷胱甘肽过氧化酶(GSH-Px):分别制备溶血液上清液、血清上清液、组织上清液等样品待测,测定管0.5 mL上清液、4.5 mL 5,5′-二硫代双 (DTNB)混匀,室温放置10 min后,420 nm处测定吸光度,试剂盒购自合肥莱尔生物科技有限公司。(11)酶联免疫吸附法检测血清C反应蛋白(CRP)、白细胞介素-6(IL-6)、D-二聚体(D-D)水平:配置标准品,加样洗板,每孔加入第一抗工作液100 μL,将反应板充分混匀后置37 ℃ 60 min,继续重复洗板两次;每孔加入底物工作液100 μL,置37 ℃暗处反应15 min;每孔加入100 μL终止液混匀;30 min内用酶标仪在450 nm处测吸光值,CRP、IL-6检测试剂盒购自武汉赛培生物科技有限公司4;D-D测试盒购自上海酶联生物科技有限公司。(12)采集患者清晨第一次排尿尿中段100~200 mL,采用尿素酶偶联法检测尿素浓度,尿素酶分解尿素产生氨,在谷安脱氢酶的作用下使DADH氧化为NAD+,通过340 nm吸光度的降低值计算尿素含量,试剂盒购自上海尚宝生物科技有限公司。(残余肾功能[8]RRF=肾尿素氮清除率/肾肌酐清除率)。
1.2.3 临床疗效观察[9]显效:SUA水平较治疗前水平降低≥25%,停药后疗效维持时间≥3个月;有效:SUA水平较治疗前水平降低≥15%,停药后疗效维持时间≥1个月;无效:SUA水平较治疗前无明显变化甚至升高。总有效率=(显效+有效)例数/总例数×100%。
1.2.4 观察不良反应及随访 记录治疗过程中两组患者不良药物反应的发生情况;干预结束后随访观察6个月,记录两组患者发生心血管事件的情况。
1.3 统计学分析

2 结果
2.1 两组患者治疗前后血清学指标及残余肾功能比较
治疗后,两组患者血清SUA、ET-1、SCr、Cys-C、cTnT、MDA、D-D、IL-6、CRP水平均低于治疗前,且观察组低于对照组(均P<0.05);血清NO、SOD、GSH-Px水平均高于治疗前,且观察组高于对照组(均P<0.05);两组患者残存肾功能治疗后均有降低,但观察组高于对照组,差异有统计学意义(P<0.05)。见表2。
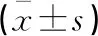
表2 两组患者治疗前后血清学指标及残余肾功能比较
2.2 两组患者临床疗效比较
观察组治疗后显效率40%、有效率35%、总有效率75%,对照组治疗后显效率22.5%、有效率30%、总有效率52.56%;观察组总有效率高于对照组,差异有统计学意义(P<0.05)。见表3。

表3 两组患者临床疗效比较[n(%)]
2.3 两组患者治疗过程中不良药物反应情况比较
观察组患者治疗中1例发生头晕,不良反应发生率为2.50%,对照组1例皮疹,2例轻度肝功能异常,不良反应发生率为7.50%,两组不良反应发生情况比较,差异无统计学意义(P>0.05)。
2.4 患者预后发生心血管事件的危险因素分析
通过预后6个月随访患者发生心血管事件记录发现,观察组1例发生缺血性心脏病,2例心力衰竭,对照组3例发生心肌梗死,2例缺血性心脏病,5例心力衰竭;将预后发生心血管事件患者与未发生患者分为两组,比较患者一般资料及治疗前临床指标进行统计学分析发现,性别、BMI、血压、血糖、治疗药物、SUA、SCr、Cys-C、cTnT、SOD、GSH-Px、MDA、D-D、IL-6、CRP水平均与患者发生心血管事件有关(P<0.05);将上述差异项纳入二元Logistic回归分析发现,血压、SUA、Cys-C、cTnT、MDA、D-D均是影响患者预后发生心血管事件的独立危险因素(P<0.05)。见表4及表5。
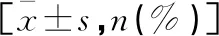
表4 患者预后发生心血管事件的单因素分析
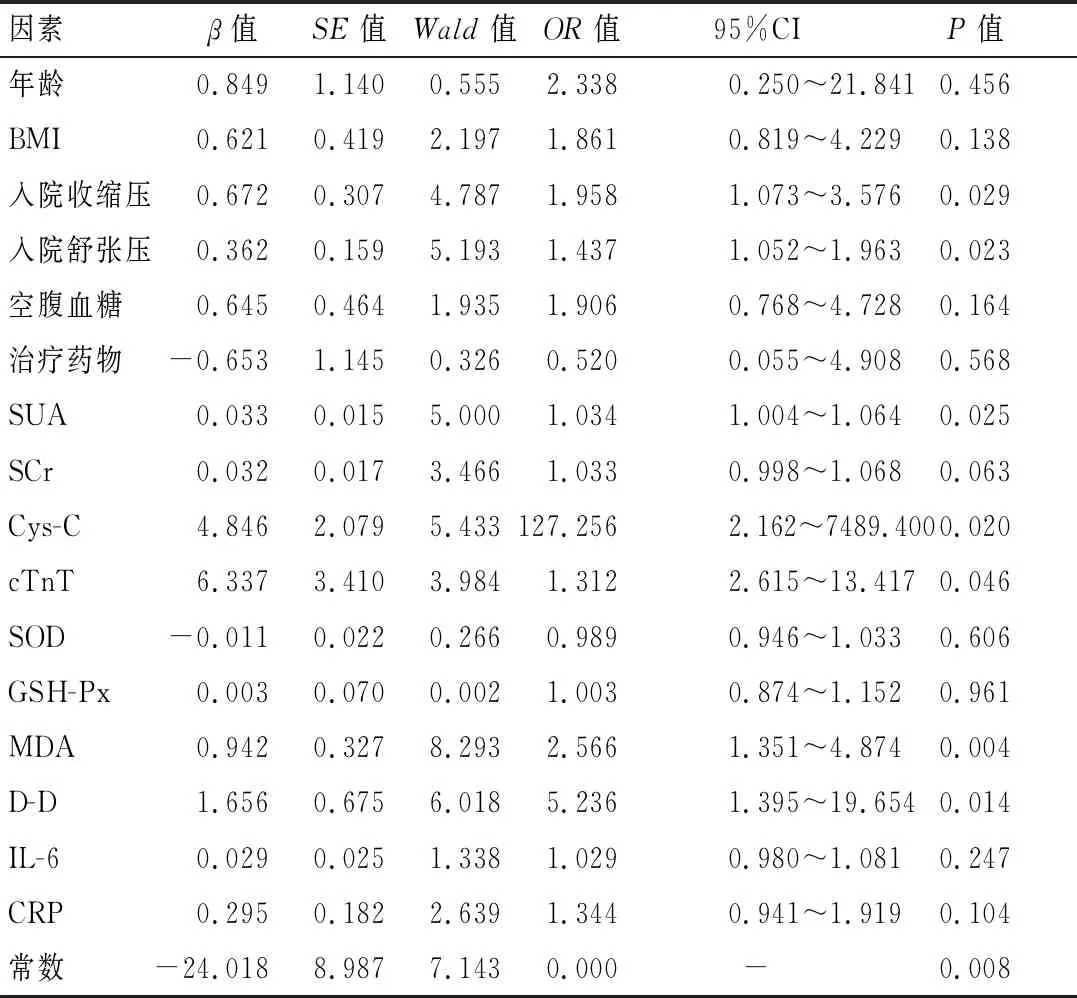
表5 患者预后发生心血管事件的多因素分析
3 讨论
尿酸的形成和排泄在正常机体内存在动态平衡,但慢性肾病患者肾功能异常,血尿酸和换嘌呤氧化酶通过促进慢性炎症,损害内皮功能,加速氧化应激反应,激活肾素-血管紧张素系统等途径,加剧肾脏纤维化[10]。循证医学[11-12]证实,血清尿酸的升高与ESRD患者全因和心血管死亡有关。目前临床通过降低血尿酸水平,延缓肾脏疾病进展的治疗方案受到广泛肯定,其中别嘌醇与医保限定非布司他均是临床降尿酸的常用药物。别嘌醇是黄嘌呤氧化酶抑制剂的代表药物,其通过黄嘌呤氧化酶抑制尿酸的产生,但因其常见用药不良反应(如皮疹、胃肠道紊乱、肝肾损害)而在临床应用中存在一定的局限性[13-14]。与其相较,医保限定非布司他在肾功能影响少程度较小,还具有一定的肾功能保护作用,对糖尿病、慢性肾病合并高尿酸血症患者疗效更佳[15]。本研究显示,治疗后两组患者SUA水平均低于治疗前,炎性因子如IL-6、CRP水平均降低,观察组疗效更佳。此外,在比较两组有关血管内皮性能、氧化应激反应、凝血、及心肌细胞影响发现,观察组对上述考察指标的改善情况均明显优于对照组;干预期间,观察组的药物不良反应发生率也明显低于对照组,与上述研究[15]基本吻合。虽然与别嘌醇相比,医保限定非布司他在降低ESRD合并HUA患者SUA的功能上表现尚佳,但观察组患者预后6个月内仍有3例患者发生心血管事件,而对照组更多。尽管已知高血尿酸是影响患者预后心血管事件的相关风险,但尚有其他危险因素影响ESRD合并HUA患者的预后状态。
超过50% ESRD患者死亡归因于心血管疾病,而心血管疾病发生归因于高血压的比例超过30%,而高血压患者同行伴随其他心血管危险因素的占比超过31.9%[16],高血压对ESRD合并HUA患者预后的不良影响。cTnT、CRP等与ESRD患者预后发生心血管事件密切相关[17]。ESRD患者长期处于微炎症状态,而炎症因子可介导相关细胞因子持续刺激血管内皮及心肌细胞,诱发亚临床心脏微血管改变,使cTnT水平升高。本研究将预后发生心血管事件患者与未发生患者分为两组,比较两组的资料发现,性别、BMI、血压、血糖、治疗药物、SUA、SCr、Cys-C、cTnT、SOD、GSH-Px、MDA、D-D、IL-6、CRP水平均是ESRD患者预后发生心血管事件的可疑影响因素,其中血压、SUA、Cys-C、cTnT、MDA、D-D均为独立危险因素。由于ESRD患者代谢紊乱导致内环境改变,尤其是肾脏对尿内毒素的排出及滤过作用降低,使如羰基化合物、晚期糖基化终产物、氧化修饰低密度脂蛋白等毒素刺激细胞大量生成活性氧,并降低抗氧化作用,诱导机体发生氧化应激反应[18]。然而长期处于氧化应激转态下的ESRD患者,一方面通过介导一氧化氮失活,加重血管皮损伤,而血管内皮损伤可刺激血小板凝聚,促进D-D等凝血因子分泌,加重血管内皮损伤负效应;另一方面促进单核巨噬细胞活化,诱导炎症相关基因表达,加剧炎症因子对心肌细胞的损伤[19]。Cys-C是近年来反应肾小球过滤变化的理想同源标志物,其可与组织蛋白酶、同型半胱氨酸等相互作用,参与心肌梗死、动脉粥样硬化等心血管病理过程[20]。
综上,非布司他可改善终末期肾病伴高尿酸血症患者的SUA水平,保护残存肾功能,改善血管内皮功能;血压、血清SUA、Cys-C、cTnT、MDA、D-D水平均是影响患者预后发生心血管事件的独立危险因素。

