120例血液透析患者尿毒症瘙痒症发生情况及影响因素分析*
陈晴 陈仁芬 谢丽红 蒋小妹
近年来,由于慢性肾病和糖尿病肾病患者的患病率较高,终末期肾病的发病率也有所增加。血液透析是治疗终末期肾病的主要治疗方式,而尿毒症瘙痒症(UP)则是患者极为常见的一种并发症,主要症状为皮疹、脱屑、皮肤干燥及瘙痒等,加重了患者心理负担,严重影响患者治疗依从性及生活质量[1]。目前,对于UP的发生机制并未完全明确,多数学者指出,该病并非单纯皮肤病变,而是系统性病变,其病理生理学涉及尿毒症毒素、免疫、炎症反应、肥大细胞激活和阿片受体失衡的复杂相互作用[2-3]。本研究分析了血液透析患者UP发生情况及影响因素,为血液透析患者制定针对性干预措施提供参考依据,现将结果报告如下。
1 资料与方法
1.1 一般资料
选取福建中医药大学附属龙岩人民医院2020年1月-2021年6月收治的120例血液透析患者作为研究对象。纳入标准:(1)年龄在18岁以上;(2)均接受血液透析治疗,且治疗时间在3个月及以上;(3)病例资料齐全,原发疾病清楚;(4)认知功能、语言功能等正常,均可有效沟通。排除标准:(1)伴有银屑病、荨麻疹、湿疹或者过敏性皮炎等原发皮肤疾病;(2)存在胆汁淤积或者系统性红斑狼疮等系统性疾病;(3)伴有恶性肿瘤;(4)入组前3个月内出现严重感染、手术,并应用降血脂或抗生素药物;(5)既往精神疾病或者长期服用镇静药和/或抗抑郁药;(6)正在参与其他临床研究。男75例,女45例;年龄≥60岁47例,<60岁73例;学历:初中及以下33例,高中及以上87例;透析治疗时间6~75个月,平均(25.02±6.12)个月;透析方式:血液透析(HD)55例,血液透析滤过(HDF)/HD+血液灌流(HP)65例;原发病类型:糖尿病肾病30例,非糖尿病肾病90例。本研究经医院伦理委员会批准,患者自愿参加本次研究,且签署知情同意书。
1.2 方法
根据有无UP对所有患者进行分组。UP诊断标准:(1)2周内至少有3 d出现不同程度皮肤瘙痒症状,且1 d内出现数次瘙痒,每次均至少持续数分钟,同时排除其他疾病导致的皮肤瘙痒;(2)以某种特定方式出现瘙痒,且持续时间在6个月以上;符合以上1项即可诊断为UP[4]。采用双盲录入法行数据录入,以减少人为性错误,并进行二次核对,以确保数据的准确性。收集所有患者基线资料及实验室指标,通过医院电子病历系统进行收集,基线资料包括性别、年龄、学历、透析治疗时间、透析方式、糖尿病肾病(是、否);实验室指标包括甲状旁腺激素、C反应蛋白、血钙、血磷、血红蛋白、血钾、尿素清除指数(Kt/V)、血清β2-微球蛋白、白蛋白、血尿素氮、血肌酐,通过Daugirdas法对Kt/V进行计算,研究开始后,在患者上机前抽取静脉血进行指标检测,实验室指标通过查询电子病历收集。
1.3 观察指标
统计分组情况,对血液透析患者UP发生进行单因素及多因素分析。
1.4 统计学处理
本研究数据采用SPSS 22.0统计学软件进行分析和处理,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,多因素Logistic回归分析法分析血液透析患者UP发生的影响因素,P<0.05为差异有统计学意义。
2 结果
2.1 分组情况
120例患者中,56例发生UP纳入UP组,发生率为46.67%,64例未发生UP纳入非UP组。
2.2 血液透析患者UP发生的单因素分析
UP组糖尿病肾病占比、甲状旁腺激素、血磷、C反应蛋白、β2-微球蛋白水平均明显高于非UP组,HDF/HD+HP、Kt/V≥1.5占比均明显低于非UP组(P<0.05),两组年龄、性别、学历水平、透析治疗时间、血钙、血红蛋白、血钾、白蛋白、血尿素氮、血肌酐比较差异均无统计学意义(P>0.05),见表1。
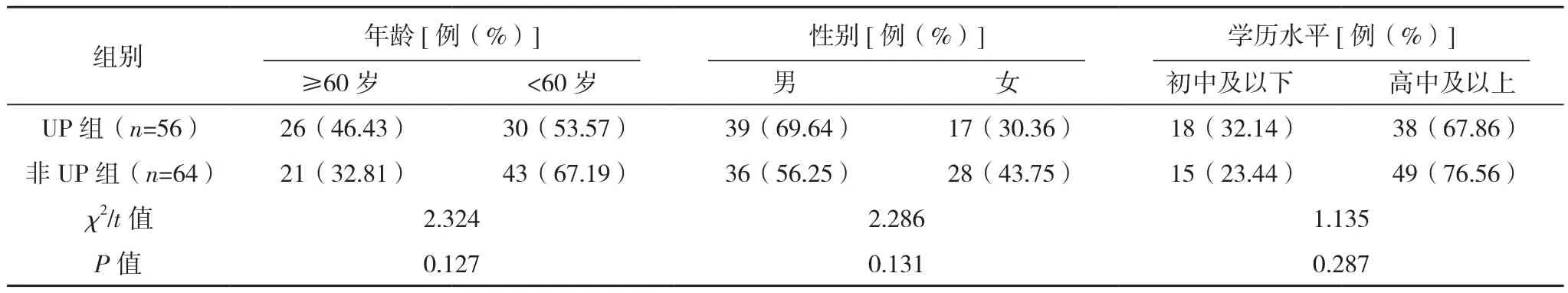
表1 血液透析患者UP发生的单因素分析
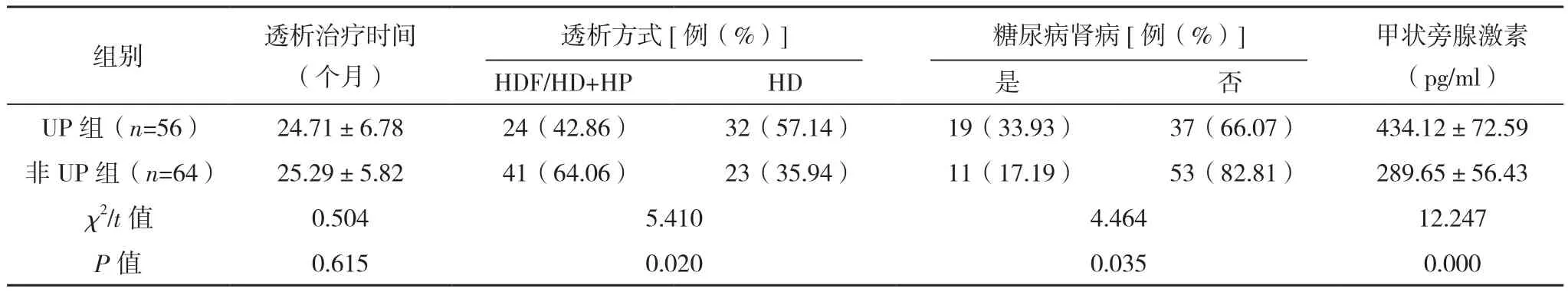
表1(续)
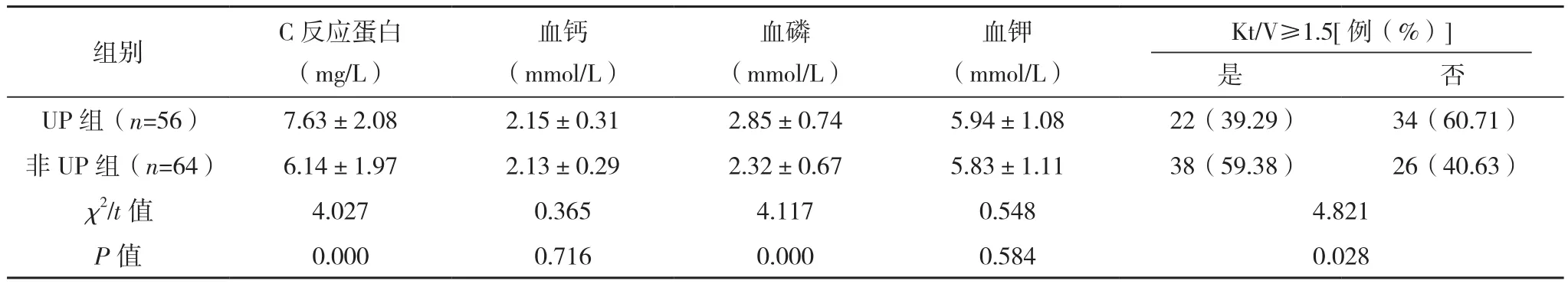
表1(续)
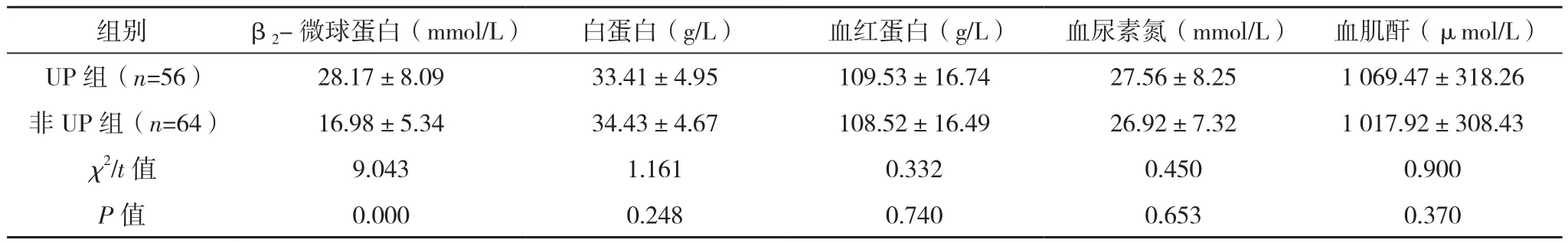
表1(续)
2.3 血液透析患者UP发生的多因素分析
将单因素中差异有统计学意义的指标作为自变量,并进行赋值,将UP(有=1,无=0)作为应变量进行多因素Logistic回归分析。结果显示,血磷、甲状旁腺激素、C反应蛋白、β2-微球蛋白、糖尿病肾病均是血液透析患者发生UP的独立危险因素(P<0.05),HDF/HD+HP、Kt/V≥1.5均是血液透析患者发生UP的保护因素(P<0.05),见表2。
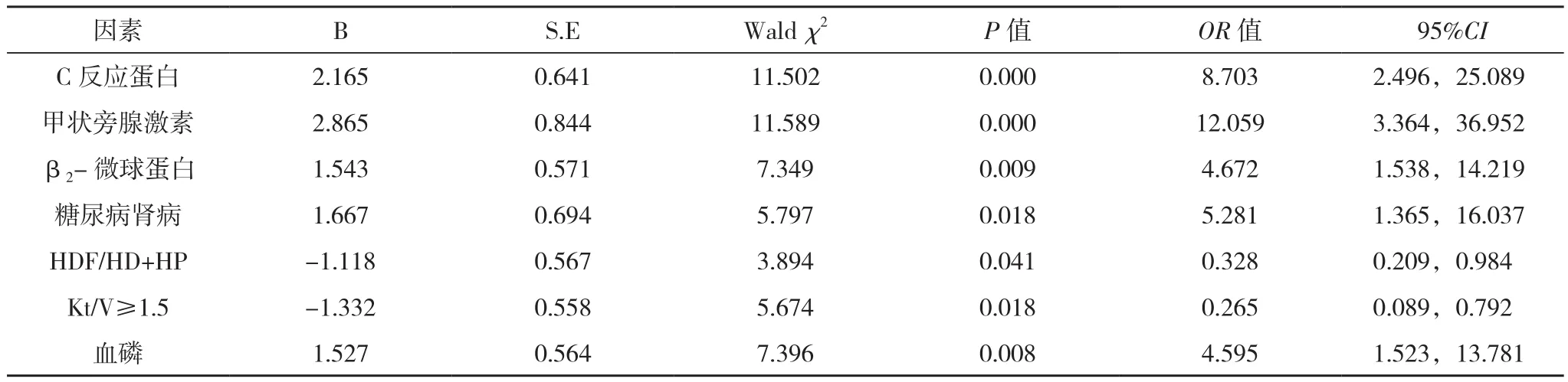
表2 血液透析患者UP发生的多因素分析
3 讨论
研究证实,血液透析患者大多存在着皮肤损害问题,包括UP、坏死、色素沉着、结节性痒疹、硬化、紫癜及皮肤干燥等,皮肤损害问题发生率接近100%,其中UP是最为常见的一种并发症[5]。本研究中,120例血液透析患者中UP发生率为46.67%,这与刘广敏等[6]的研究结果(46.5%)相近,说明血液透析患者易出现UP。虽然UP在血液透析患者中较为常见,但是其成因复杂,对其发病机制并未完全明确,尿毒症及非尿毒症因素参与了UP的发生及发展。研究指出,UP与血液透析的死亡存在密切关系,存在UP的患者其死亡风险明显高于无UP者[7]。因此,早期认识血液透析患者UP情况,并及时给予规范科学诊治,有助于降低患者死亡风险。
马宛宛[8]通过多因素Logistic回归分析发现,瘦素、原发病糖尿病、Kt/V≥1.5、CRP、iPTH、β2-微球蛋白是维持性血液透析患者皮肤瘙痒的主要危险因素(OR=2.543、5.364、1.137、1.260、7.665、1.582)。本研究中,UP组糖尿病肾病占比、甲状旁腺激素、血磷、C反应蛋白、β2-微球蛋白均明显高于非UP组,HDF/HD+HP、Kt/V≥1.5占比均明显低于非UP组(P<0.05)。进一步分析发现,血磷、甲状旁腺激素、C反应蛋白、β2-微球蛋白、糖尿病肾病均是血液透析患者发生UP的独立危险因素(P<0.05)。与上述研究结果相近。
甲状旁腺素可促进组胺释放,组胺具有较强的血管舒张作用,增加微静脉及毛细血管的管壁通透性,造成血浆进入组织当中,引起局部组织水肿的发生,同时还造成镁离子及钙盐等物质沉积于皮肤中,从而造成UP的发生[9]。尿毒症患者往往存在不同程度的炎症反应,肿瘤坏死因子-α、IL-6等炎症因子水平明显升高。C反应蛋白为常用炎症标志物,本研究中,血液透析患者UP与C反应蛋白存在密切关系,这与免疫假说相符,该假说认为UP并非局部皮肤病变,而是全身性炎症性疾病,C反应蛋白等炎症因子介导UP形成及加重UP进展[10]。目前,在血液透析患者中关于原发疾病类型对UP的影响并为统一认识,有学者指出,原发疾病类型为糖尿病肾病的患者更易出现UP,糖尿病会导致尿毒症毒素分子堆积,从而引发瘙痒[11]。不过也有研究指出,糖尿病状况并未引起或者加重UP[12]。因而还需要进一步研究证实。虽然皮肤瘙痒在血液透析患者中较为常见,但是其成因复杂,对发病机制并未完全明确,钙磷代谢障碍等尿毒症及非尿毒症因素参与了皮肤瘙痒的发生及发展。HD治疗对大、中分子毒素清除效果一般,血磷、β2-微球蛋白水平较高,导致大、中分子毒素在体内沉积及磷等矿物质沉积于皮肤中,从而诱发UP。
研究发现,不同血液透析方式对血液透析患者UP的干预效果不同,常规血液透析联合血液滤过或者血液灌流可减少UP的发生及减轻UP程度[13]。本研究还发现,HDF/HD+HP、Kt/V≥1.5均是血液透析患者发生UP的保护因素(P<0.05)。相较于单纯进行血液透析治疗,血液滤过及血液灌流不仅可进一步提高小分子毒素清除效果,可提高β2-微球蛋白、甲状旁腺激素等大、中分子毒素清除效果,从而减少了毒素聚积。Kt/V则是评价血液透析治疗效果的一个主要指标,一般Kt/V越高则透析越充分,毒素清除效果越好。因此,HDF/HD+HP、Kt/V≥1.5可作为血液透析患者发生UP的保护因素。
综上所述,血液透析患者易出现UP,糖尿病肾病及高水平血磷、甲状旁腺激素、C反应蛋白、β2-微球蛋白患者是UP发生的高危人群,而采取HDF/HD+HP及提高Kt/V有助于减少UP的发生,值得临床重视。

