抗中性粒细胞胞质抗体相关性血管炎肾损伤的临床病理特点及预后影响因素分析
陈 越 李 馨 卢玉秋 周 莹 余 晨
抗中性粒细胞胞质抗体(antineutrophil cytoplasmic antibody,ANCA)相关性血管炎(antineutrophil cytoplasmic antibody-associated vasculitis,AAV)是一类以血清ANCA阳性和小血管壁坏死性炎症为主要特征的少见自身免疫性疾病[1]。AAV包括3种亚型,显微镜下多血管炎(MPA)、肉芽肿性多血管炎(GPA)和嗜酸细胞性肉芽肿性多血管炎(eGPA)[1]。AAV可累及全身多个系统和器官,以肾脏受累尤为常见。AAV累及肾脏时往往提示患者有较高的死亡风险[2]。AAV肾损伤的主要临床表现包括血尿、蛋白尿、高血压和肾功能损害等,疾病进展迅速,短时间内可致不可逆性肾衰竭,甚至危及患者生命[3]。本研究回顾性分析同济大学附属同济医院肾内科AAV肾损伤患者的临床病理特点及预后,探讨AAV肾损伤患者的预后影响因素,以期更好地指导临床诊断和治疗。
1 对象与方法
1.1 研究对象 收集2011年7月—2019年7月在同济大学附属同济医院首诊为AAV的65例患者资料,男女比例为1.2∶1,平均年龄为70.6岁,60.0岁以上患者为56例(86.2%)。MPA为纳入患者的主要临床亚型(60例,92.3%)。纳入标准:①符合Chapel Hill会议提出的AAV诊断标准[4];②血清ANCA阳性;③存在经肾脏活组织检查(简称活检)证实的肾损害,或临床表现为血尿、蛋白尿和(或)肾功能不全,无合并其他原因引起的肾损害证据。排除标准:①继发性血管炎;②合并其他自身免疫性疾病;③随访时间≤3个月,且未达到终点事件的患者。本研究经医院伦理委员会审核、批准[伦理号:(同)伦审第(K-W-2021-009)号],患者或其监护人均知情同意。
1.2 研究方法与分组 本研究为回顾性、观察性临床研究。收集临床资料包括:性别、年龄、受累系统、治疗方案、ANCA血清学结果、起病时血肌酐(sCr)水平、起病时是否存在急性肾损伤(AKI)、24 h尿蛋白定量(UPE)、尿红细胞(RBC)计数、血清白蛋白(sALB)、血红蛋白(Hb)、血白细胞(WBC)计数、血小板计数、血中性粒细胞比例、CRP、血清补体3(C3)、ESR、估算的肾小球滤过率(eGFR)、疾病活动度及合并症等。
根据改良的肾脏疾病饮食公式(MDRD)评估患者eGFR。AKI的诊断标准参照2012年改善全球肾脏疾病预后组织(KDIGO)指南,符合以下情况之一即可确诊:48 h内sCr升高水平超过26.5 μmol/L(0.3 mg/dL);sCr升高超过基线1.5倍(确认或推测7 d内发生);尿量<0.5 mL/(kg·h),且持续6 h以上[5]。对于不能确定基线sCr水平的患者,以患者就诊前6个月内或病程中最低sCr水平为基线值。应用伯明翰系统性血管炎活动度评分(BVAS)评估疾病活动度。部分患者行肾穿刺活检,肾组织分别行光学显微镜(简称光镜)、免疫荧光染色和电子显微镜(简称电镜)检查,观察肾脏病理学改变,并根据Berden病理分型标准进行病理分型[6]。应用Charlson合并症指数对患者合并症情况进行量化。终点事件定义为全因死亡。根据随访期内是否发生终点事件,将患者分为终点事件组和非终点事件组。随访结束时间为2019年12月31日或发生终点事件。
2 结 果
2.1 一般资料及肾脏受累情况 17例患者在随访期内发生终点事件,纳入终点事件组;其他48例患者被纳入非终点事件组。终点事件组中有13例患者死亡原因为肺部感染。纳入患者起病时,AAV肾损伤的主要表现为血尿(53例,81.5%)、蛋白尿(57例,87.7%)、肾功能不全(45例,69.2%)和AKI(40例,61.5%)。患者尿RBC计数的中位数为70/μL,24 h UPE的中位数为1.0 g,eGFR的平均值为43.1 mL/(min·1.73 m2),起病时需急诊行肾脏替代治疗的患者12例(18.5%)。
终点事件组患者在确诊AAV时的年龄、Charlson合并症指数均显著高于非终点事件组(P值均<0.05)。终点事件组患者起病时eGFR显著低于非终点事件组,而起病时sCr水平和发生AKI的患者比例均显著高于非终点事件组(P值均<0.05)。见表1。
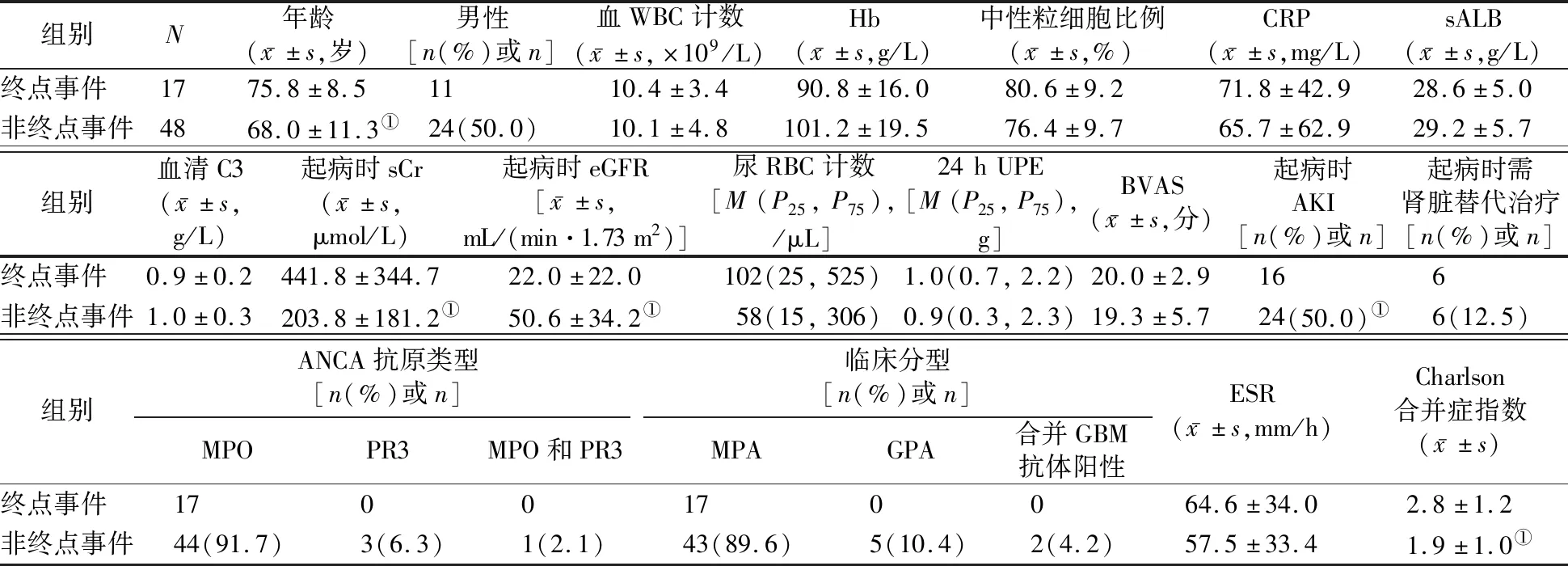
表1 终点事件组与非终点事件组患者的基线资料及肾脏受累情况比较
2.2 肾脏病理学特征 26例(40.0%)患者行肾脏病理学检查,终点事件组9例,非终点事件组17例。 其中,以新月体型最多,为10例(38.5%),其次为局灶型和混合型各6例(23.1%),硬化型最少为4例(15.4%)。终点事件组与非终点事件组间各肾脏病理学分型的比例的差异无统计学意义(χ2=4.780,P>0.05),见表2。

表2 终点事件组与非终点事件组患者肾脏病理学分型比较 (n)
9例(34.6%)患者肾组织存在免疫球蛋白沉积,7例(26.9%)患者存在C3沉积;4例(15.4%)患者存在中重度肾小管间质慢性病变,其余22例(84.6%)患者肾小管间质无病变或仅为轻度慢性病变。
2.3 肾脏外受累情况 纳入患者中,肾脏外受累脏器以呼吸系统最多见,为62例(95.4%),随后依次为系统性受累49例(75.4%,包括乏力、发热和体重下降等),耳鼻喉和心血管系统受累各10例(15.4%),神经系统受累7例(10.8%),黏膜和眼受累5例(7.7%),皮肤受累3例(4.6%),以及消化系统表现2 例(3.1%)。终点事件组与非终点事件组间肾脏外各系统受累的患者比例的差异均无统计学差异(P值均>0.05)。见表3。

表3 终点事件组与非终点事件组患者肾脏外受累情况比较 [n(%)或n]
2.4 起始治疗方案 终点事件组应用糖皮质激素联合免疫抑制剂治疗的患者14例,单用糖皮质激素2例,未应用免疫抑制剂1例;非终点事件组应用糖皮质激素联合免疫抑制剂治疗的患者40例(83.3%),单用糖皮质激素5例(10.4%),未应用免疫抑制剂3例(6.3%)。两组间应用各治疗方案的患者比例的差异无统计学意义(χ2=0.315,P>0.05)。
2.5 生存曲线和预后不良的危险因素分析 本研究患者的随访时间范围为1~70个月,中位随访时间为10个月。AAV肾损伤患者的生存曲线如图1所示,2年和5年的生存率分别为80.2%和45.1%。
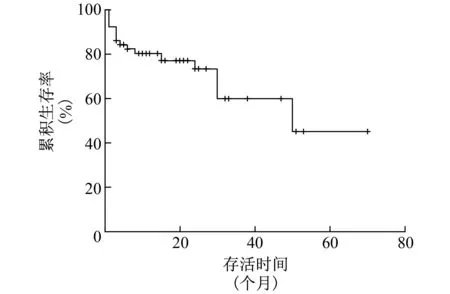
图1 AAV肾损伤患者的生存曲线
单因素回归分析结果显示,高龄、中性粒细胞比例增高、起病时较高的sCr和血清C3水平是患者预后不良的影响因素。将上述变量及性别纳入多因素Cox回归分析发现,在校正性别、 年龄、 中性粒细胞比例和血清C3水平后,起病时较高的sCr水平是AAV肾损伤患者预后不良的独立危险因素(P=0.003),见表4。进一步绘制起病时sCr这一变量的ROC曲线,计算AUC为0.757(95%CI为0.626~0.887),最佳截断值为108.5 μmol/L(灵敏度为0.941,特异度为0.500)。

表4 影响AAV肾损伤患者预后的单因素和多因素Cox回归分析
3 讨 论
AAV是老年继发性肾脏疾病的常见病因[7]。既往本团队对接受肾活检的老年患者进行研究[8]发现,AAV是该人群继发性肾脏疾病的最常见病因。本研究中AAV患者的平均年龄超过70岁,60岁以上老年患者占86.2%,可见AAV多发生于高龄人群。AAV各亚型的发病率在不同的地区有显著差异。欧洲以GPA最为常见,MPA则在亚洲占主导地位[1]。本研究中的AAV患者以MPA为主,占92.3%,与国内另一研究中心报道的90.5%相近[9]。
AAV可累及全身多系统,其中以肾脏和呼吸系统较为常见[10]。本研究显示,AAV肾损伤的主要表现为轻中度蛋白尿伴镜下血尿、肾功能受损;肾外受累中以呼吸系统最为常见,系统性受累次之。因此,对于老年患者出现多系统受累表现,尤其是有轻中度蛋白尿、血尿合并肾功能异常时,需要考虑AAV,以实施迅速有效的治疗措施来改善其预后。AAV累及肾脏时可通过肾脏病理学检查协助诊断并评估患者肾脏损伤的程度,但是由于各种原因,多数患者并未行肾活检术。本研究中仅有40.0%的AAV肾损伤患者接受了肾活检术。Berden等[6]根据肾小球病变的特点对AAV肾损伤进行病理学分型发现,硬化型患者肾脏预后较差,其余依次为混合型、新月体型和局灶型。本研究以全因死亡作为终点事件进行分组发现,终点事件组患者中新月体型比例较高,非终点事件组患者中局灶型较高,但是两组间不同病理学分型的患者比例的差异无统计学意义。本研究中进行肾脏病理学检查的患者数量较少,故研究结果可能存在偏倚,因此需要进一步扩大样本量,延长随访时间来明确Berden分型与AAV患者存活率的相关性。
既往研究[11]显示,未经治疗的AAV患者1年存活率仅为20.0%。然而,随着免疫抑制治疗的应用与普及,AAV患者的总体生存率得到显著改善。本研究中AAV肾损伤患者的2年和5年的生存率分别是80.2%和45.1%。尽管如此,AAV患者死亡率仍高于普通人群,而死亡的主要原因为免疫抑制治疗引起的不良事件,特别是感染性疾病[11]。本研究结果显示,肺部感染是发生终点事件的患者的主要死亡原因。因此,对于AAV患者,感染性疾病的防治极为重要。有研究[5]结果表明,AAV患者的预后与其起病时的年龄和sCr水平密切相关。本研究结果显示,发生终点事件的患者起病年龄显著较高,且起病时sCr水平也更高。进一步分析发现,起病时较高的sCr水平是AAV肾损伤患者预后不良的独立危险因素。除年龄和肾功能外,高BVAS、低白蛋白血症、低补体血症等也与AAV患者的预后不良有关[9]。
总之,AAV肾损伤的临床表现具有多样性,轻重不一。经过有效的治疗,AAV肾损伤患者的总体生存率显著增高。AAV患者的治疗方案需要结合其年龄和起病时sCr水平等进行个体化制订,同时应重视感染的预防性治疗,以提高患者总体生存率。

