PRKAG2 突变心脏综合征1 例及文献复习
杨莹 谢勇 黄图城 陈样新 王景峰
PRKAG2 突变心脏综合征由PRKAG2 基因突变造成所编码的腺苷酸活化蛋白激酶(adenosine monophosphate-activated protein kinase,AMPK)的调节亚基γ2 结构和功能发生异常所致,以心肌肥厚、心室预激和传导系统疾病为主要表现的一种罕见的常染色体显性遗传病[1]。其临床表型多样,多为个案或家系报道,目前尚无大样本数据报道其发病率及预后。本文报道1 例PRKAG2 突变心脏综合征患者,并介绍PRKAG2 相关诊疗进展。
1 病例摘要
患者男性,61 岁,2019 年6 月因“反复活动后胸闷伴气促7 天”就诊于当地医院。7 天前开始出现活动后胸闷,伴气促,无心悸,无头晕、黑矇、晕厥,休息后可缓解,症状反复发作。心电图示窦缓,房早,心室预激(A 型);心脏彩超示左室壁非对称性肥厚,考虑肥厚型心肌病。住院期间心率波动于23-60 次/分,为窦律,予异丙肾上腺素静滴后转入我院,查心电图示窦缓,房早,完右,心室预激(A 型),T波倒置。
家族中无猝死或确诊为肥厚型心肌病者。
查体:体温36.6℃,脉搏52 次/分,呼吸20 次/分,血压130/72 mmHg,双肺呼吸音清,未闻及干湿性啰音。心律不齐,可闻及早搏,二尖瓣听诊区可闻及3/6 级收缩期吹风样杂音,向左腋下传导。双下肢无水肿。
辅助检查:
(1)动态心电图(异丙肾上腺素维持过程中):1.窦性心律,心率:39-101 次/分(平均:56 次/分),偶见窦性心律不齐,心率在60 次/分或以下占总数78%。2.检出单个房性早搏10355 个,成对房早160 对,检出房性心动过速3次,均为连发3 个房早,频率最快为145 次/分。偶见房早未下传,检出大于2 秒的R-R 间期共1 次,最长为2.07 秒(11:18)。3.呈心室内传导阻滞。4.呈心室预激图像改变。
(2)超声心动图:LA 33 mm,LVDd 33 mm,IVSd 26 mm,LVPWd 19 mm,EF 69%;探及左室腔中部高速射流,峰值流速3.4 m/s,峰值压差47 mmHg。考虑肥厚型心肌病(双室肥厚,左室腔内梗阻);起搏器置入术后;二尖瓣轻-中度返流;三尖瓣轻度返流;左室收缩功能正常,舒张功能减低。
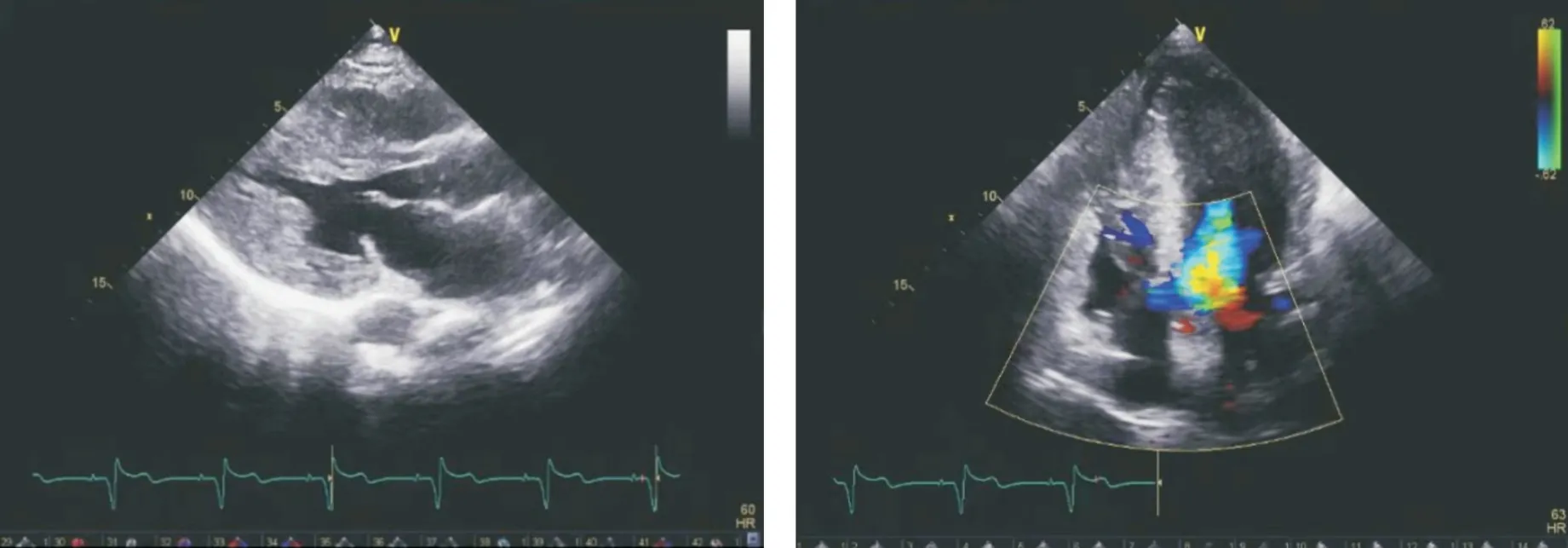
图1 心脏彩超
(3)血清、尿液免疫固定电泳:均未发现异常单克隆条带。
(4)冠脉造影+左心室造影+左心室流出道测压。
冠脉呈右优势型,左主干、前降支、回旋支、右冠均未见明显狭窄,管壁光滑,远端血流TIMI3 级。室间隔肥厚,左室流出道梗阻明显,测压可见明显压力阶差。心尖导管进入困难,未行压力阶差测定。
(5)基因检测及家系分析:

表1 左室流出道测压结果
对患者及家系成员进行全外显子基因检测分析,结果显示,患者携带PRKAG2 的1 个杂合变异,变异位点chr7:151261304(c.1444G>T,p.Ala482Ser),属于错义突变。30岁儿子携带该变异,其妻和28 岁儿子未携带该变异,由于患者的父母均已去世,无法验证变异的遗传来源。
其30 岁儿子目前携带有基因突变,心脏彩超暂未有心肌肥厚表现,常规心电图暂无心室预激或传导障碍表现,暂予动态观察。
综上,结合患者临床表现、辅助检查及基因测序结果,考虑为PRKAG2 突变心脏综合征。治疗上,建议植入ICD,患者因经济原因植入永久起搏器,并予小剂量ACEI 口服。目前随访3 年,患者心肌肥厚进展缓慢,心功能无明显下降,生活质量较前改善。
2 讨 论
PRKAG2 心脏综合征临床表现异质性大,发病年龄不一,典型表现可有胸闷、胸痛、心悸、活动后气促以及晕厥等,也可合并肌痛、肌无力等心脏外症状,晚期可出现心力衰竭并进行性加重的表现[2,3]。大多数携带相同PRKAG2基因突变的患者,临床表现也大致相同,但部分也可表现为不同的临床特征。
目前诊断PRKAG2 心脏综合征尚无统一标准,辅助检查可有以下表现:
(1)心电图表现多样,典型表现为心肌肥厚、心室预激、心房颤动或心房扑动、进展性传导系统障碍(如窦房结功能不良、房室传导阻滞、束支阻滞或心室内阻滞)等改变[1]。本例患者心电图有预激波,发病时未发作预激综合征,起搏器植入后,程控也暂未发现预激综合征发作。文献报道大多数PRKAG2 患者有预激表现,携带常见的p.Arg302Gln 或p.Asn488Ile 突变者,预激发生率高于其他基因突变者(50%vs28%,P=0.002)[3];且携带p.Arg302Gln 突变者的预激发生率要高于p.Asn488Ile 突变者(79%vs58%,P=0.008)[1,4]。由此推测预激的发生可能和基因突变的类型相关。
(2)超声心动图下,心肌肥厚常累及左心室,且以室间隔受累多见,可导致严重的左心室流出道梗阻[1]。本例患者发病时也合并了严重的心室内梗阻,植入起搏器后得到一定程度的改善。而Lopez-Sainz 等人报道的队列中,患者均无严重的流出道梗阻(LVOT>30 mmHg)或SAM 征[3]。
(3)心脏磁共振(cardiac magnetic resonance,CMR):近年来,CMR 在鉴别心肌肥厚的病因方面有了长足的进步:①钆对比剂延迟强化(late gadolinium enhancement,LGE)是检测心肌纤维化的金标准;②高分辨率纵向弛豫时间定量成像(T1 mapping)和③心肌细胞外容积(extracellular volume,ECV)可以早期识别弥漫纤维化;④心肌应变可以反映左室功能[5]。目前尚无PRKAG2 相关的特异性CMR影像学诊断标准。本例患者入院时考虑严重窦缓,未及时完善CMR 检查;后续治疗中植入永久起搏器,不能耐受CMR 检查。
(4)心内膜心肌活检(EMB):EMB 是鉴别和确诊心肌炎、心肌病病因的重要手段之一,近年来受到高度重视。由于部分心肌病变呈局灶性分布,EMB 有漏检可能,结合超声心动图、CMR 等结果,可进一步降低漏诊率。PRKAG2 心脏综合征的心肌组织病理可见PAS 染色阳性的糖原空泡,可与淀粉样变等其他导致心肌肥厚的疾病鉴别,但目前也尚无统一的病理学诊断标准。
(5)基因检测:基因检测是目前诊断心肌病的金标准。近期研究也表明,携带PRKAG2 等致病或可能致病的基因突变者,不论有无典型临床表现,均可导致心衰、房颤、全因死亡的风险增加[6,7]。Lopez-Sainz 等人报道的患者,98%的基因突变属于错义突变,部分新发现的基因突变不满足ACMG 致病或可能致病的标准,但与符合ACMG标准的基因突变者相比,两组的临床特点和事件发生率没有统计学差异;考虑到这部分患者有典型症状或者组织病理学特点,研究者仍将其纳入了分析[3]。因此,对于年轻的严重心肌肥厚患者,尤其是合并早发房颤、心室预激、需起搏器植入或者有猝死家族史的患者,需注意筛查心肌肥厚原因;其次,对于查出先证者的家族,应及早进行家系筛查,鉴别出高危家属,同时对无症状携带者,应密切随访,有助于了解疾病进程、指导治疗和判断预后。本文报道的突变位点既往未见报道,但结合患者的临床表现和检查结果,我们仍考虑将其诊断为PRKAG2 心脏综合征。本例患者的一位儿子也携带有该突变,目前暂无临床表现,予密切随访,定期复查心电图和超声心动图。
治疗上,对于合并有预激综合征等心律失常者,建议行心内电生理检查,必要时行射频消融术,术后定期随访;合并心力衰竭患者,予规范化抗心衰治疗,严重时可考虑心脏移植;合并窦房结功能不良或高度房室传导阻滞者,必要时植入起搏器;对于有严重左室肥厚、晕厥、猝死家族史、恶性心律失常或心脏骤停幸存者,可考虑植入ICD。随着筛查手段的升级和医务人员对此类疾病的认识及关注增加,将来可能有更为完整的诊疗策略,有望利用酶学替代治疗、CRISPR/Cas9 基因编辑等根治方法,将明显改善患者预后。
本病例仍存在一些不足之处:患者入院后严重窦缓,考虑病情危重,未及时完善CMR 检查,行起搏器植入后不能耐受CMR 检查。治疗上,针对本例患者,ICD 是否优于起搏器?目前,PRKAG2 者植入ICD 尚未达成共识,本例患者主要表现为病窦(严重窦缓,室内阻滞),无晕厥或先兆晕厥的表现,也无猝死家族史,但患者心电图有预激表现,虽未捕捉到心动过速发作,仍需警惕预激合并室颤甚至猝死的可能。住院期间反复建议患者植入ICD,患者因经济原因选择起搏器。目前程控随访3 年,未有恶性心律失常事件发生。将来如患者有恶性心律失常或EF 进行性下降,建议升级为ICD。
本研究为回顾性研究,且研究项目不涉及个人隐私和商业利益,经医院伦理委员会审查批准(伦理编号:SYSKY-2022-127-01),已豁免知情。

