天津市细颗粒物短期暴露对慢性心力衰竭患者心力衰竭加重再入院的影响及易感人群的探索
邢璐宇 陈欣 孙洁
(1.天津医科大学一中心临床学院,天津 300110;2.天津市第一中心医院心脏科,天津 300110)
心力衰竭(心衰)是一种常见的慢性反复发作的疾病,是多种疾病的终末阶段,具有较高的致残率及致死率,全球发病人数巨大,给社会带来极重的经济负担[1]。大气污染是心血管疾病的危险因素,既往许多研究[2-3]表明,无论是动物还是人类,心衰的发生和发展与大气污染相关。慢性心衰患者可通过控制诱发因素,从而减少心衰加重再入院次数,改善预后[4]。
大气污染物主要包括细颗粒物(particulate matter 2.5,PM2.5)、可吸入颗粒物(particulate matter 10,PM10)、二氧化硫(SO2)、一氧化碳(CO)、二氧化氮(NO2)和臭氧(O3),其大气中PM2.5为悬浮于空气中空气动力直径≤2.5 μm的颗粒,被广泛认为是空气中的重要污染物。不同地区空气污染水平存在差异,天津市作为华北地区主要城市之一,具有一定的区域代表性,本研究拟分析天津市PM2.5短期暴露与慢性心衰加重住院的相关性及易感人群的特征,为改善慢性心衰患者的预后提供指导和依据。
1 对象和方法
1.1 研究对象
研究对象资料来源于天津市第一中心医院心脏科的住院病历系统,2018年1月1日—2020年12月31日收治入院于天津市第一中心医院心脏科的慢性心衰患者,住院总例次为1 699例次。根据纳入及排除标准,最终筛选出心衰住院1 167例次,病例资料的筛选、录入及各种信息的核对均由两人完成,资料纳入尊重患者隐私,数据真实可信。
纳入标准:(1)既往心衰病史诊断明确,病史>3个月;(2)既往因心衰住院于本院或外院,此次患者具有明显憋喘、双下肢水肿、心率快、肺部湿啰音等症状体征再入院;(3)超声心动图显示舒张性或收缩性心衰;(4)出院首要诊断为心衰。
排除标准:(1)年龄<18岁;(2)天津市内六区以外区域;(3)恶性肿瘤、严重肝肾功能障碍患者;(4)病历资料不全者。
收集慢性心衰患者的相关临床资料,包括性别、年龄、就诊日期、吸烟史、饮酒史、既往史(高血压、糖尿病、心房颤动、陈旧性心肌梗死、陈旧性脑梗死和慢性阻塞性肺疾病)、肺部感染、纽约心功能分级以及心衰病因。
1.2 大气污染物及气象数据
大气污染物及气象数据均由天津市气象局提供,数据权威可靠。大气污染物数据包括PM2.5、PM10、SO2、CO、NO2和臭氧8小时平均浓度(O3-8h),气象数据包括温度、湿度、风速和气压。PM2.5、PM10、SO2、CO和NO2数据资料均为日平均浓度。
1.3 统计方法
运用SPSS 25.0软件对慢性心衰患者临床数据、大气污染物及气象数据进行描述性统计分析,计算大气污染物及气象数据各项指标的均值、标准差、最小值、P25、平均值、P75及最大值。采用Spearman对大气污染物和气象因素相互之间的相关性进行分析。
本研究采用病例交叉对照研究来探讨PM2.5短期暴露对慢性心衰加重入院风险的影响,其基本原理是每一位研究对象以自身作为对照,从而减少个体间差异产生的影响,本研究按照时间分层设定短期暴露的时间为1周,病例组慢性心衰患者发生心衰加重再入院的当天—入院前7 d即滞后0~7 d(lag0~7)PM2.5的暴露,入院当天为滞后0 d即lag0、入院前1 d为lag1,以此类推,对照组为同一研究对象在未发病前PM2.5暴露的相同时间段,同样设置为7 d,匹配对照组的lag0~7患者暴露的PM2.5浓度,减少危险因素暴露的时间差异所导致的偏倚。病例组与对照组时间段的匹配原则是使其同处于某年/某月/同是“星期几”,可有效控制季节、节假日、“星期几”等混杂因素的影响。以同一病例发病和未发病作为结局,采用条件逻辑回归模型,将不同滞后天数的PM2.5纳入回归模型,结果用OR值及95%CI来呈现。分析随着PM2.5在日均浓度水平上每增加10 μg/m3,慢性心衰加重再入院的风险变化,OR最大表示发病风险最大,即为最佳滞后天数。为识别暴露于PM2.5发生心衰加重再入院的患者是否存在易感人群,对人群特征进行分层分析。考虑到污染物、气象因素之间的相互作用,因此研究中在控制气象因素的条件下又分别采用单污染物和多污染物模型进行分析,以P<0.05具有统计学意义。
2 结果
2.1 患者基本特征
2018年1月1日—2020年12月31日符合纳入标准的慢性心衰住院患者为1 167例次,患者相关临床数据描述详见表1。

表1 心衰患者的临床特征
2.2 大气污染物和气象因素基本数据分析以及Spearman相关系数分析
PM2.5、PM10、SO2、NO2和O3-8 h日均值分别为(52.43±41.51)μg/m3、(83.96±52.05)μg/m3、(11.08±6.08)μg/m3、(43.96±19.63)μg/m3和(103.92±60.99)μg/m3,CO日均值为(1.00±0.45)mg/m3,大气污染物PM2.5年平均质量浓度是《环境空气质量标准》(GB3095-2012)二级标准限值(35 μg/m3)的1.50倍。详见表2。

表2 2018—2020年大气污染物基本信息
对大气污染物和气象因素进行Spearman相关系数分析,结果可见PM2.5、PM10、SO2、NO2和CO日均浓度两两间为正相关,其中PM2.5和PM10相关性最为显著(r=0.80,P<0.01),O3-8h与其余4种大气污染物为负相关,污染物与气象因素以及气象因素之间同样具有一定相关性,见表3。PM2.5与PM10和CO具有较高的正相关性,为避免PM10和CO对本研究的影响,建立PM2.5+PM10、PM2.5+CO双污染物模型分析。

表3 2018—2020年天津市大气污染物及气象资料间的Spearman相关系数分析
2.3 大气PM2.5短期暴露与慢性心衰加重再入院风险的关系
在控制其余空气污染物及气象因素的混杂因素后,单污染物模型中PM2.5浓度每增加10 μg/m3,可增加慢性心衰患者的心衰加重再入院风险,在lag0(OR=1.029 8,95%CI1.004 6~1.055 6)、lag2(OR=1.012 4,95%CI1.001 0~1.040 1)、lag3(OR=1.012 9,95%CI1.006 7~1.021 2)、lag4(OR=1.013 5,95%CI1.007 7~1.030 8)和lag5(OR=1.014 2,95%CI1.002 6~1.029 4)均增高,其中最佳滞后期为lag0,即PM2.5浓度每增加10 μg/m3,因心衰加重的住院风险增加2.98%,P<0.05,详见表4。

表4 滞后0~7 d中PM2.5浓度每增加10 μg/m3与慢性心衰加重再入院风险的关系
在多污染物模型中,在调整SO2、NO2、O3-8h污染物及气象因素后,PM2.5+PM10、PM2.5+CO多污染物模型随着PM2.5浓度每增加10 μg/m3,可导致慢性心衰患者心衰加重再入院风险增加,但影响并不显著,差异未见统计学意义,见表5。
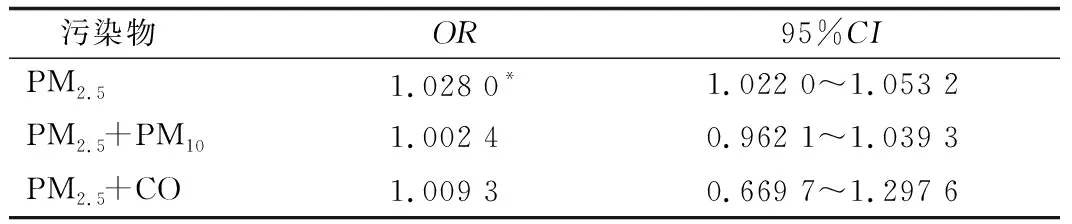
表5 多污染物模型中PM2.5浓度每增加10 μg/m3与慢性心衰加重再入院风险的关系
2.4 大气PM2.5浓度每增加10 μg/m3与慢性心衰加重再入院患者的敏感性分析
在控制其他空气污染物及气象因素的混杂因素后,分别对年龄、性别、吸烟和饮酒史等人群特征进行分析以明确慢性心衰加重的易感人群,当PM2.5浓度每增加10 μg/m3,年龄≥65岁、既往合并高血压、肺部感染、心衰病因为血管性心脏病的慢性心衰患者心衰加重再入院的风险更高,分别对应后面的OR值及95%CI(OR=1.089 9,95%CI1.009 8~1.223 9;OR=1.074 1,95%CI1.070 7~1.077 9;OR=1.067 8,95%CI1.029 8~1.278 7;OR=1.035 6,95%CI1.009 5~1.374 4),P<0.05,详见表6。而PM2.5浓度的改变对性别,既往是否吸烟、饮酒,是否存在糖尿病、冠心病、心肌梗死、脑卒中、慢性阻塞性肺疾病以及心功能分级等这些人群特征的影响无统计学差异。
3 讨论
大气污染物对心衰加重的影响存在一定的滞后性[5],在诸多国内外研究中得到证实。北京一项研究[6]采用时间序列分析,在单污染物模型中,当PM2.5浓度每增加10 μg/m3,心衰再入院疾病加重风险在最佳滞后期lag0增加1.21%(95%CI0.27~2.15)。太原市一项研究[7]采用病例交叉研究方法对大气污染物与心血管疾病住院的相关性进行了探讨,研究发现单污染物模型中,PM2.5浓度每增加10 μg/m3,心血管疾病住院风险增加,且在lag3、lag4对入院存在滞后影响具有统计学意义(P<0.05),lag4为最佳滞后期(OR=1.076,95%CI1.015~1.119)。澳大利亚塔斯马尼亚州一项观察性研究[2]发现,在PM2.5单污染物的泊松回归中,PM2.5浓度每增加10 μg/m3,心衰加重风险在lag1(OR=1.29,95%CI1.15~1.42)最高(P<0.001)。本研究发现短期暴露PM2.5,慢性心衰加重再入院风险在lag0、lag2、lag3、lag4和lag5均增高,最佳滞后期为lag0(OR=1.029 8,95%CI1.004 6~1.055 6)。本研究与上述北京的研究结果相近,可能与天津和北京相邻有关,众多研究显示出PM2.5暴露增加心衰加重再入院风险,且存在滞后性,趋势基本相似。
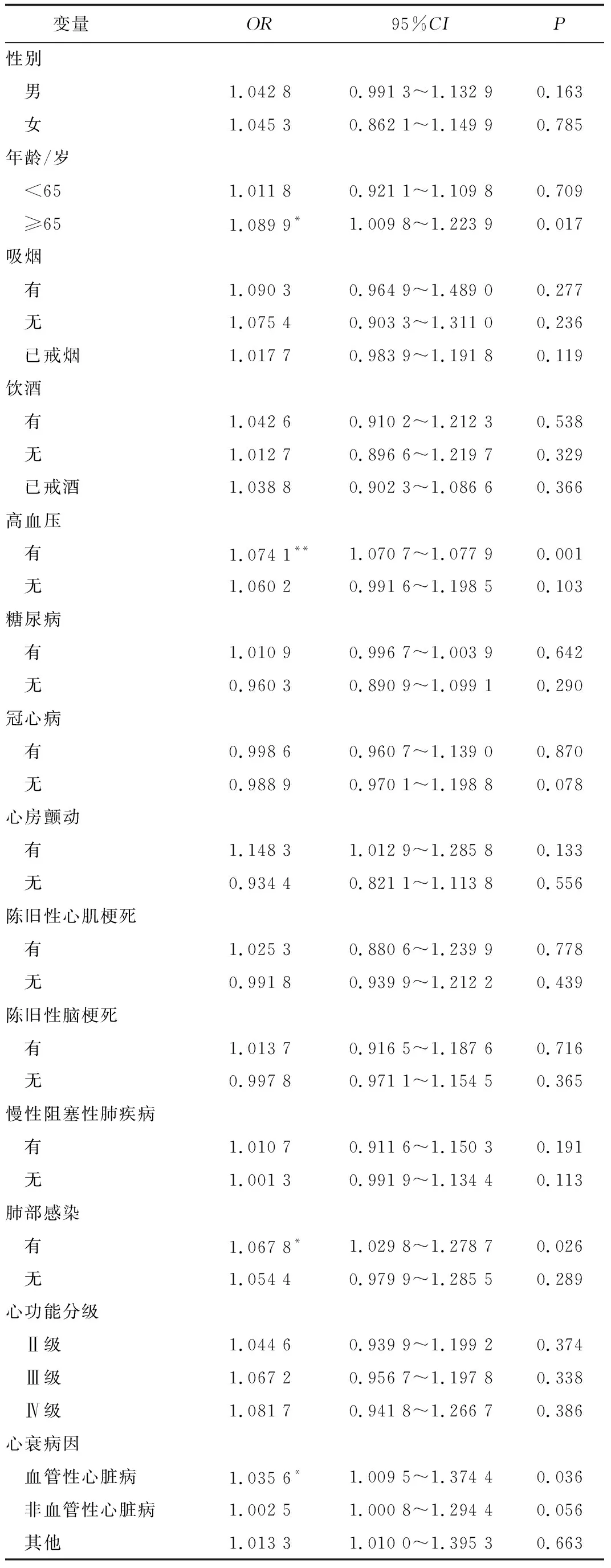
表6 大气PM2.5浓度每增加10 μg/m3与慢性心衰加重再入院患者的敏感性分析
在PM2.5短期暴露的人群特征分析中,许多研究发现心衰入院患者中存在潜在的易感人群。关于北京地区一项研究[8]显示,PM2.5短期暴露浓度每增加10 μg/m3,年龄≥65岁的患者心衰日住院率增加0.320%(95%CI-0.005%~0.650%),女性住院率增加0.430%(95%CI-0.005%~0.870%),但未见统计学差异。一项针对中国26个大城市大气污染对慢性心衰患者影响的研究[9]报道,PM2.5浓度每增加其四分位间距,在已有糖尿病患者中心衰再入院风险增加2.4倍(95%CI1.1~3.7),在高血压、血管性心脏病和慢性阻塞性肺疾病中未见明显差异。本研究发现,在年龄≥65岁,既往合并高血压、肺部感染、血管性心脏病的慢性心衰患者中,对PM2.5短期暴露浓度的增加更易感,暴露于同等PM2.5浓度时,可能因为年龄≥65岁老年人基础疾病多,自身抵抗力弱,更易出现心衰加重。肺部感染可能导致肺部炎症性改变,影响呼吸功能,造成缺氧,加重心脏负荷,尤其可能诱发心衰急性加重。血管性心脏病导致心肌细胞功能减退和心室重塑等,导致心衰的发生和发展。
PM2.5暴露使慢性心衰加重入院的最佳滞后期及易感人群存在差异,这可能与各地区气候因素、污染物的水平、污染物成分的构成和不同人种、人群特征等方面存在差异有关,需大样本研究去探索。
大气污染物是诱发心衰发病的一个重要因素[10]。大气污染与心衰住院率及死亡率密切相关,PM2.5暴露可通过调节肺氧化应激、炎症和心室重塑等,影响整个心衰的进展[11-12]。应积极做好健康宣教,重视污染预警,对于年龄≥65岁及基础疾病多的人群应更加重视大气污染物对自身的影响,降低心衰的发生风险。
本研究中天津市第一中心医院作为天津市大型三甲医院之一,是天津市重要的心衰中心,患者数量多。本试验仍存在不足:选取天津市内六个区心衰住院患者,未涉及全市,存在局限性,需大量数据及更广泛的覆盖面进一步研究;本研究只着重探讨了PM2.5的单污染物模型对慢性心衰患者心衰加重入院风险的影响,未对全部的双污染物或多污染物模型进行探讨。

