液相色谱法测定E-和Z-烯草酮含量
强 伟,王 英,薛建强,潘朝晖
(江苏龙灯化学有限公司,江苏昆山 215301)
烯草酮(clethodim),是1987年由美国Chevron公司研制、日本住友化学公司开发的一种选择性环己烯酮类除草剂。该除草剂主要通过抑制禾本科植物乙酰辅酶A羧化酶,破坏脂肪酸的合成而致效[1],主要登记用于防除大豆、油菜等作物田一年生和多年生禾本科杂草,且对双子叶作物安全。
IUPAC对烯草酮的化学命名因其异构体而不同。最初,烯草酮的化学名称为(5RS)-2-2-(E)- 1-[(2E)-3-氯烯丙氧基亚氨基]丙基-5-[(2RS)-2-(乙硫基)丙基]-3-羟基环己-2-烯-1-酮,有效成分仅指C=N位为E构型的烯草酮。2008年,有厂商认为产品中存在有活性的Z构型烯草酮[2],2010年7月其化学名称更新为(5RS)-2-2-(EZ)-1-[(2E)-3-氯烯丙氧基亚氨基]丙基-5-[(2RS)-2-(乙硫基)丙基]-3-羟基环己-2-烯-1-酮,并将C=N位的Z构型烯草酮也写入名称里。根据EU法规283/2013的定义,如果异构体的名称不包含在IUPAC名称内,则被认为是杂质[3]。因此,烯草酮IUPAC名称的更新所带来的影响是,烯 草酮有效成分应为E构型和Z构型之和,即丙烯基上E构型(2E)、酮肟基上E和Z异构体的混合物(1EZ)。与烯草酮有效成分构型不一样的其他异构体,只能视为烯草酮原药的杂质。烯草酮E和Z构型见图1。
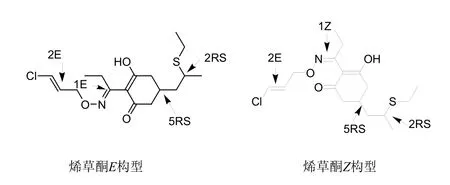
图1 烯草酮E、Z构型化学结构式
目前,有关烯草酮有效成分测定尚无CIPAC或AOAC方法,而GB/T 22614—2008[4]中给出了用烯草酮锂盐作为标准品,高效液相色谱法正、反相定量有效成分的方法,但均未标注和包含Z构型。基于此,本文采用2种商业化烯草酮标样,参考国标方法,测定了3个不同厂家的烯草酮原药含量,并考察了溶剂、时间等因素对烯草酮含量的影响,以期为烯草酮含量测定提供技术指导。
1 材料与方法
1.1 仪器
Agilent 1200高效液相色谱仪,具有二极管阵列检测器及色谱工作站(美国安捷伦科技有限公司);XS205电子天平(精度为0.000 01 g,梅特勒-托利多科技(中国)有限公司);SK5200型超声波仪(上海科导超声仪器有限公司)。
1.2 试剂
二氯甲烷和正己烷:色谱纯(西班牙萨劳Scharlau有限公司);冰醋酸:色谱纯[阿拉丁试剂(上海)有限公司];乙腈:色谱纯[赛默飞世尔科技(中国)有限公司];甲酸:色谱纯(上海麦克林生化科技有限公司);蒸馏水(自制)。
1.3 供试药剂
标样1:国内商业化烯草酮锂盐标准品,Z+E纯度标示值99.5% [国家农药质量监督检验中心(沈阳)];标样2:烯草酮标准品,Z+E纯度标示值92.05% (西格玛公司);试样1:山东先达农化股份有限公司(厂家1);试样2:河北兰升生物科技有限公司(厂家2);试样3:江苏云帆化工有限公司(厂家3)。
1.4 色谱检测条件
正相色谱法:色谱柱XDB-CN (250 mm×4.6 mm,5 μm)(美国安捷伦科技公司),流动相:ψ(二氯甲烷:正己烷∶冰醋酸)=0.75∶99.25∶0.5 (体积比),经滤膜过滤和脱气;流速1.0 mL/min;柱温:40 ℃;检测波长:254 nm;进样体积:5 μL;在上述色谱条件下,烯草酮E-和Z-构型的保留时间分别约为11.6 min和10.5 min (图2)。
反相色谱法:色谱柱XDB-C18(150 mm×4.6 mm,3.5 μm)(美国安捷伦科技公司),流动相:ψ[乙腈:水(0.1%甲酸调pH 3.0)]=70∶30 (体积比),经滤膜过滤和脱气;流速1.0 mL/min;柱温:40 ℃;检测波长:254 nm;进样体积:5 μL;在上述色谱条件下,烯草酮E-和Z-构型的保留时间分别约为7.6 min和2.5 min (图2)。
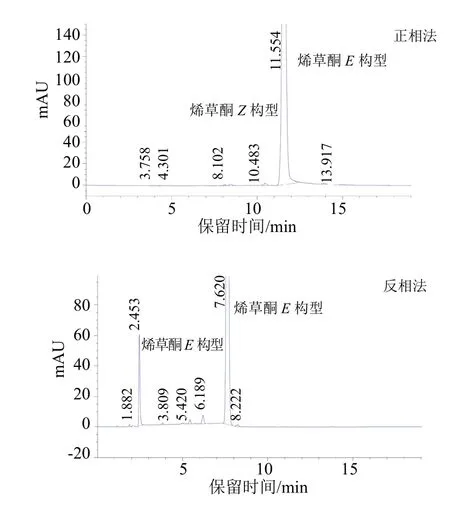
图2 烯草酮原药高效液相色谱图
1.5 测定步骤
1.5.1 标样及样品溶液配制
称取烯草酮标样或烯草酮原药样品各25 mg (精确至0.01 mg),分别置于50 mL容量瓶中,正相方法中加1 mL二氯甲烷,3滴冰乙酸和20 mL流动相振摇,超声使之溶解,恢复室温后,用流动相定容至刻度,摇匀;反相方法中加1 mL二氯甲烷,3滴冰乙酸和20 mL乙腈振摇,超声使之溶解,恢复室温后,用乙腈定容至刻度,摇匀。
1.5.2 测定
在上述操作条件下,待仪器稳定后,连续注入数针标样溶液,直至相邻2针烯草酮峰面积相对变化小于1.2%后,按照标样溶液、样品溶液、样品溶液、标样溶液的顺序进行测定。
1.5.3 计算公式
样品中E或E、Z之和的质量分数按下式计算:

式中:Asam为样品中E或E、Z之和的峰面积;Astd为标样中E或E、Z之和的峰面积;Wstd为标样的质量;Wsam为样品的质量;P为标样的纯度(%)。这里,烯草酮锂盐折算成烯草酮的系数为0.983。
2 结果与分析
2.1 定量结果
按1.4节条件测定烯草酮有效成分含量,结果见表1。从表1可以看出,不论是标样1还是标样2,正相还是反相条件,同一样品的含量(E+Z)差异不大。正相条件下,Z的贡献比较小;反相条件下,Z的贡献较大,这与反相条件中使用到了乙腈溶剂有很大关系。
2.2 烯草酮稳定性考察
据报道,烯草酮及相关代谢物均表现出几何异构、互变异构和对映体异构3种类型。由于互变异构的存在,有效成分及相关代谢物的2种异构体E和Z的比例不是恒定的,会发生相互转换,这2种形式的转换平衡与溶剂相关[5]。
本文在正相和反相条件下,分别考察了不同极性的稀释剂如正相流动相、正己烷、乙腈分别溶解烯草酮原药后,24 h内的纯度变化。从图3及图4可以看出,同一厂家及不同厂家的样品,用不同溶剂溶解后,不论是正相还是反相条件下,在0、8、16、24 h内,E、Z之和纯度变化不大。
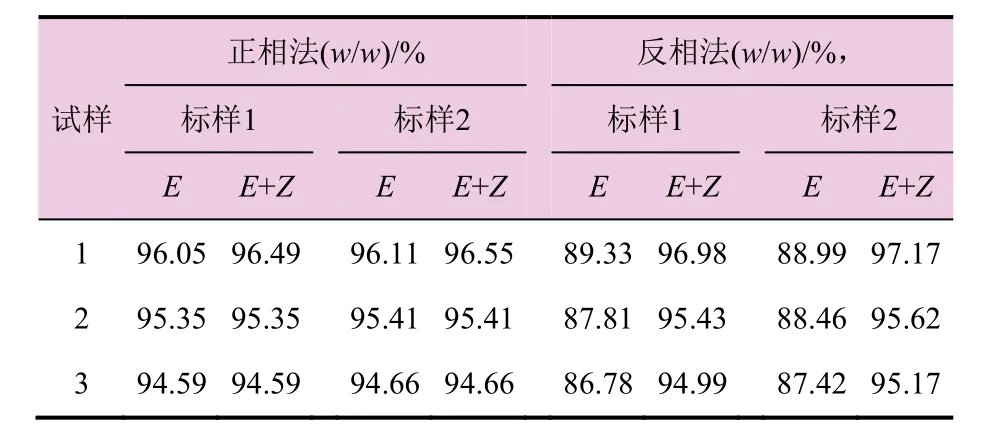
表1 烯草酮原药正反相定量结果
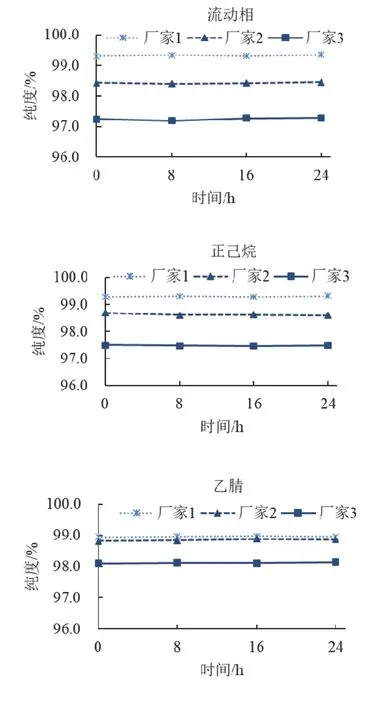
图3 正相法中不同溶剂对烯草酮E、Z之和稳定性的影响
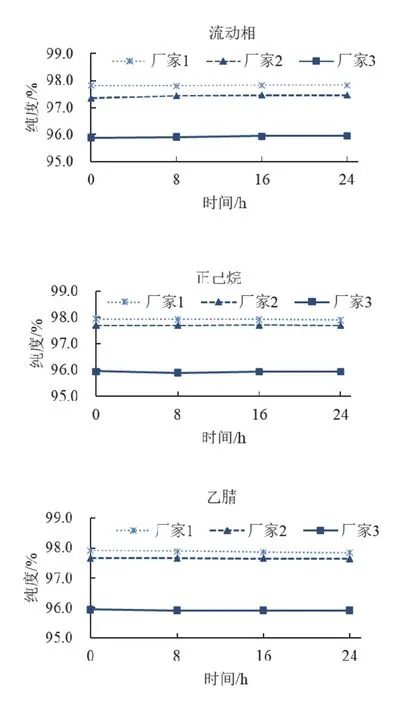
图4 反相法中不同溶剂对烯草酮E、Z之和稳定性的影响
3 结 论
烯草酮样品有效成分定量测定结果证实,不管是用烯草酮锂盐做标样还是烯草酮做标样,正相条件下,Z构型对烯草酮含量的贡献很小,且有的厂家产品中含量不明显,这可能与工艺不同有关;反相条件下,Z构型含量较高,对有效成分影响大。若将烯草酮的Z构型含量计入有效成分后,不管在正相还是反相条件下,烯草酮含量都相对稳定。
在稳定性考察中发现,正、反相条件下,使用不同溶剂(流动相、正己烷及乙腈)对不同厂家的烯草酮有效成分E、Z构型之和影响较小,且基本一致,24 h内相对稳定;另外,在反相条件下,不同厂家烯草酮样品用乙腈溶解时其样品Z构型纯度明显高于用流动相和正己烷溶解时的样品纯度。
因此,在烯草酮分析方法中准确定性出Z构型,并将其计入有效成分中,不管是正相还是反相高效液相色谱法,均可用于测定烯草酮有效成分含量,这将有利于解决国内不同检测单位分析结果的差异问题。

