超声心动图参数联合血清学指标预测脓毒症患者心肌损伤的临床价值
陈春燕 程 伟 钟仕利 肖 洪 伍正彬 彭 霁 唐 昊
脓毒症可导致器官功能障碍, 诱发多器官功能障碍综合征、脓毒症休克等, 心脏功能障碍是其严重并发症, 一旦发生可累及肾脏, 引发肾功能障碍, 导致预后不良[1]。文献[2]报道, 脓毒症患者心功能不全的发生率可达40%~50%, 合并心肌损伤后器官衰竭及死亡的发生率可增至70%~90%。超声心动图可较好地反映心脏收缩及舒张功能, 在评价脓毒症患者心肌损伤中具有较高的临床价值。研究[3-4]显示, 糖化血红蛋白(glycosylated hemoglobin, HbA1c)高水平是导致心肌损伤的独立危险因素, 髓过氧化物酶(myeloperoxidase, MPO)可参与心肌再灌注损伤, 脑利钠肽(brain natriuretic peptide, BNP)、肌钙蛋白I(troponin I, cTnI)均为心肌损伤标志物, 在评估心肌损伤方面亦有较高的价值。基于此, 本研究旨在探讨超声心动图参数联合血清学指标在预测脓毒症患者心肌损伤中的应用价值。
资料与方法
一、研究对象
选取2017年12月至2021年4月我院收治的脓毒症患者88例。纳入标准:①符合《第三版脓毒症与感染性休克定义国际共识》诊断标准[5];②年龄<80岁;③临床资料完整。排除标准:①严重心、脑、肾疾病、急性病毒性心肌炎及严重精神-神经功能障碍患者;②合并恶性肿瘤患者;③有心血管疾病病史者;④治疗后72 h死亡或出院者。根据是否合并心肌损伤[6]分为心肌损伤组39例和非心肌损伤组49例, 心肌损伤组中男21例, 女18例, 年龄36~75岁, 平均(53.21±8.43)岁, 体质量指数(BMI)19~28 kg/m2, 平均(22.59±2.61)kg/m2;非心肌损伤组中男28例, 女21例, 年龄35~78岁, 平均(54.03±8.76)岁, BMI 19~28 kg/m2, 平均(23.49±2.57)kg/m2。另选50例我院同期健康体检者为对照组, 男30例, 女20例, 年龄31~77岁, 平均(53.74±8.51)岁, BMI 19~28 kg/m2, 平 均(23.09±2.45)kg/m2。各组一般资料比较差异均无统计学意义。本研究经我院医学伦理委员会批准, 所有受检者均知情同意。
二、仪器与方法
1.超声心动图检查:使用Philips EPIQ 7C彩色多普勒超声诊断仪, 二维超声心动图检查使用S5-1探头, 频率1.0~5.0 MHz;三维超声心动图检查使用X5-1探头, 频率1.0~5.0 MHz。受检者取左侧仰卧位, 嘱其平静呼吸, 同步心电图, 先使用二维超声心动图于胸骨旁左室长轴切面测量舒张末期左室后壁厚度(left ventricular posterior wall thickness at end-diastole,LVPWd)和收缩末期左室后壁厚度(left ventricular posterior wall thickness at end-systole, LVPWs);然后切换为三维模式, 于心尖四腔观清晰显示左房, 获取连续4个心动周期的动态图像并存图, 结束后脱机分析。使用QLAB 8.1软件, 选择3DQ模式, 自动获得左房时间-容积曲线, 测量左房最大容积、左房最小容积、左房收缩前容积, 计算左房每搏量(left atrial stroke volume, LASV)、左房扩张指数(left atrial extension index, LAEI)、左房整体射血分数(left atrial ejection fraction, LAEF)。以上参数均重复测量3次取平均值, 所有操作均由同一具有5年工作经验的超声医师完成。
2.血清学指标检测:患者于入院后第2天抽取空腹肘静脉血。HbA1c采用高效液相色谱法测定;MPO采用全自动免疫定量分析仪检测;BNP和cTnI均采用化学发光免疫分析法测定(试剂盒购于武汉明德生物科技股份有限公司)。上述操作均严格遵循试剂说明完成。
三、统计学处理
应用SPSS 22.0统计软件, 计量资料以±s表示, 多组间比较采用单因素方差分析, 两组比较采用LSD-t检验。应用Pearson相关分析法分析超声心动图参数与血清学指标的相关性;绘制受试者工作特征(ROC)曲线分析超声心动图参数联合、血清学指标联合及两者总联合预测脓毒症患者心肌损伤的价值, 计算曲线下面积(AUC)。P<0.05为差异有统计学意义。
结 果
一、各组超声心动图参数比较
各组LVPWd、LVPWs、LASV、LAEI、LAEF比较差异均有统计学意义(均P<0.05)。对照组、非心肌损伤组、心 肌 损 伤 组LASV、LAEI、LAEF均 依 次 减 低, LVPWd、LVPWs均依次增高, 各组两两比较差异均有统计学意义(均P<0.05)。见表1和图1~3。
表1 各组超声心动图参数比较(±s)
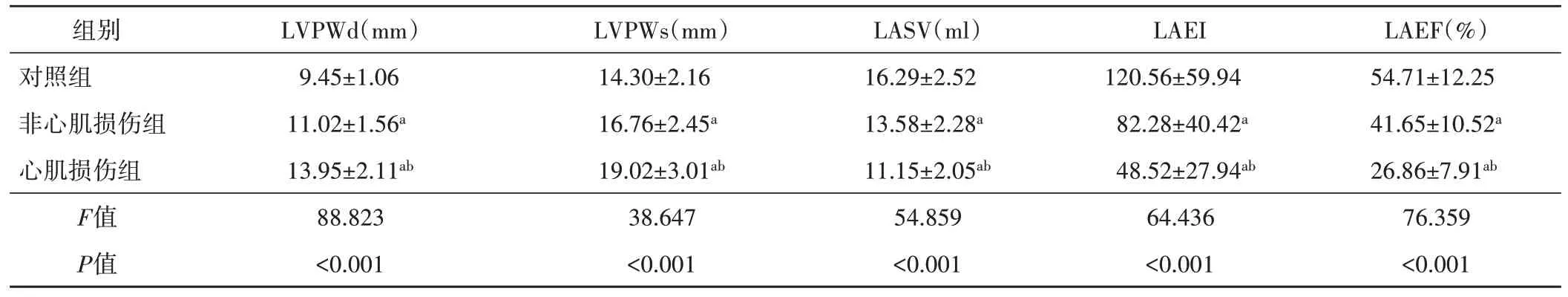
表1 各组超声心动图参数比较(±s)
与对照组比较, aP<0.05;与非心肌损伤组比较, bP<0.05。LVPWd:舒张末期左室后壁厚度;LVPWs:收缩末期左室后壁厚度;LASV:左房每搏量;LAEI:左房扩张指数;LAEF:左房整体射血分数
组别对照组非心肌损伤组心肌损伤组F值P值LVPWd(mm)9.45±1.06 11.02±1.56a 13.95±2.11ab 88.823<0.001 LVPWs(mm)14.30±2.16 16.76±2.45a 19.02±3.01ab 38.647<0.001 LASV(ml)16.29±2.52 13.58±2.28a 11.15±2.05ab 54.859<0.001 LAEI 120.56±59.94 82.28±40.42a 48.52±27.94ab 64.436<0.001 LAEF(%)54.71±12.25 41.65±10.52a 26.86±7.91ab 76.359<0.001
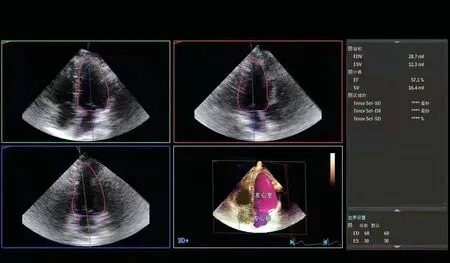
图1 对照组三维超声心动图
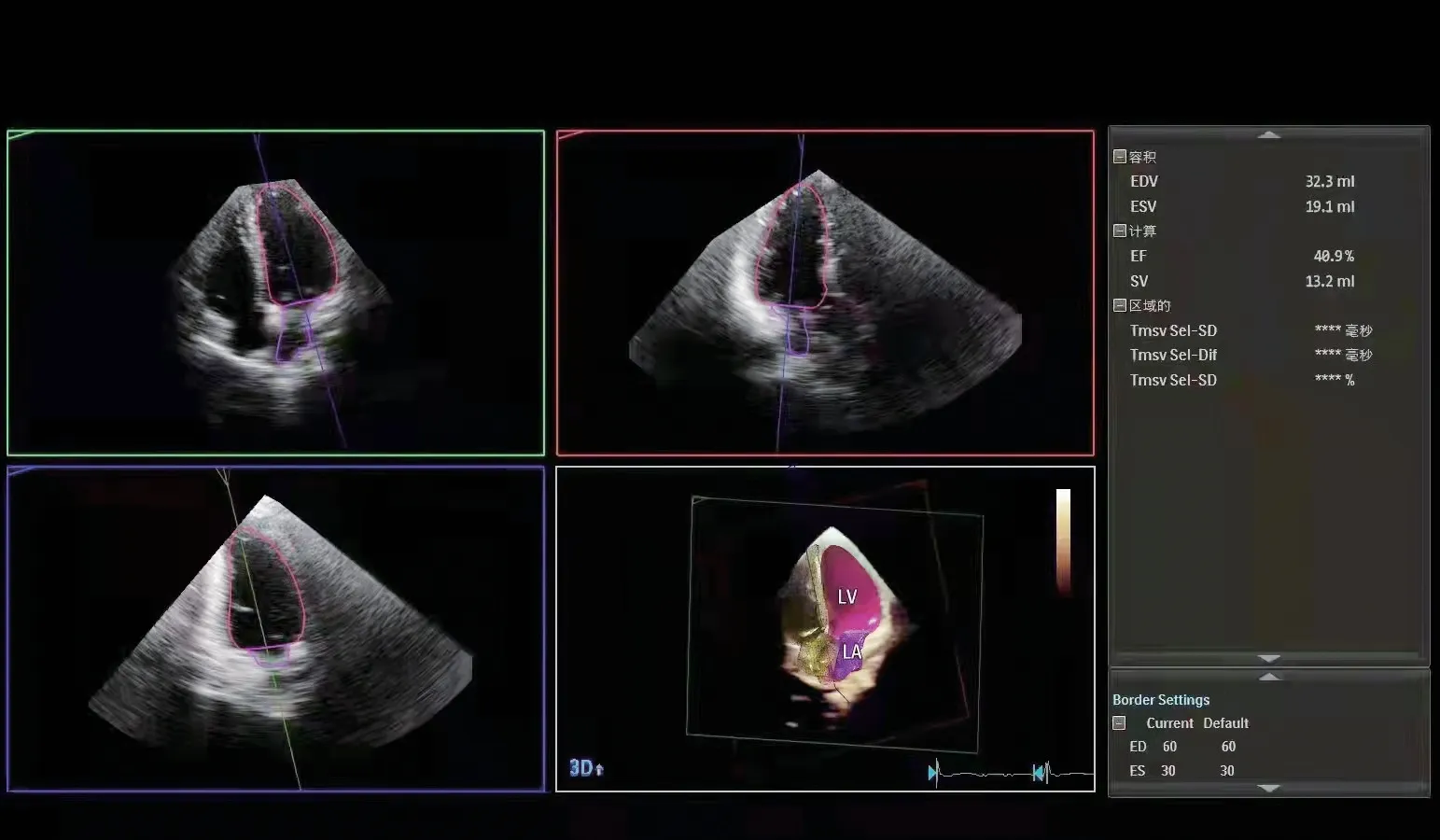
图2 非心肌损伤组三维超声心动图
二、各组血清学指标比较
各组HbA1c、MPO、BNP、cTnI比较差异均有统计学意义(均P<0.05)。对照组、非心肌损伤组、心肌损伤组HbA1c、MPO、BNP、cTnI均依次增高, 各组两两比较差异均有统计学意义(均P<0.05)。见表2。
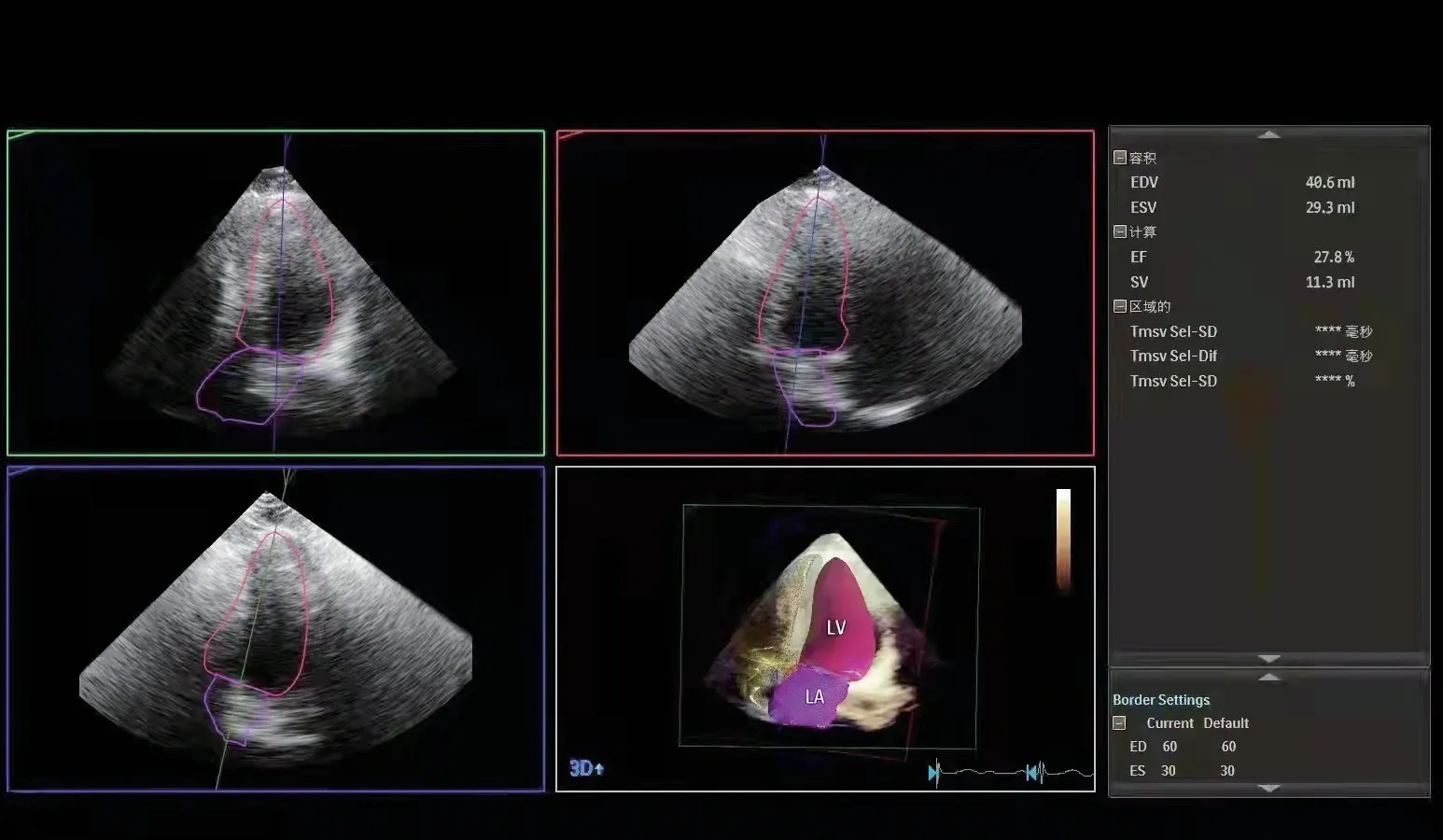
图3 心肌损伤组三维超声心动图
表2 各组血清学指标比较(±s)
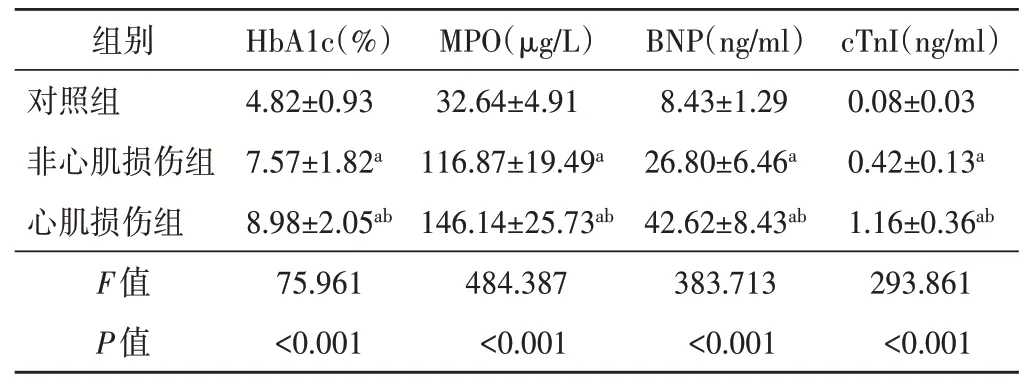
表2 各组血清学指标比较(±s)
与对照组比较, aP<0.05;与非心肌损伤组比较, bP<0.05。HbA1c:糖化血红蛋白;MPO:髓过氧化物酶;BNP:脑利钠肽;cTnI:肌钙蛋白I
组别对照组非心肌损伤组心肌损伤组F值P值HbA1c(%)4.82±0.93 7.57±1.82a 8.98±2.05ab 75.961<0.001 MPO(μg/L)32.64±4.91 116.87±19.49a 146.14±25.73ab 484.387<0.001 BNP(ng/ml)8.43±1.29 26.80±6.46a 42.62±8.43ab 383.713<0.001 cTnI(ng/ml)0.08±0.03 0.42±0.13a 1.16±0.36ab 293.861<0.001
三、相关性分析
Pearson相 关 性 分 析 显 示, LVPWd、LVPWs与HbA1c、MPO、BNP、cTnI均 呈 正 相 关(均P<0.05);LASV、LAEI、LAEF与HbA1c、MPO、BNP、cTnI均呈负相关(均P<0.05)。见表3。
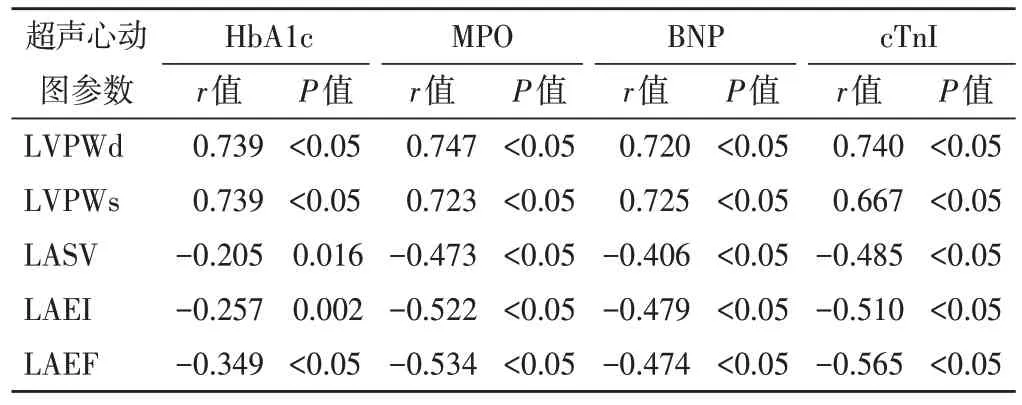
表3 超声心动图参数与血清学指标的相关性分析
四、ROC曲线分析
ROC曲线分析显示, 超声心动图参数联合[公式为:超声心动图参数联合=LVPWd+0.265/0.629×LVPWs+(-0.368/0.629)×LASV+(-0.019/0.629)×LAEI+(-0.100/0.629)×LAEF]、血清学指标联合[公式为:血清学指标联合=HbA1c+(-2.862/-1.657)×MPO+(-0.981/-1.657)×BNP+(-1.661/-1.657)×cTnI]及两者总联合[公式为:总联合=LVPWd+0.265/0.629×LVPWs+(-0.368/0.629)×LASV+(-0.019/0.629)×LAEI+(-0.100/0.629)×LAEF+(-1.657/0.629)×HbA1c+(-2.862/0.629)×MPO+(-0.981/0.629)×BNP+(-1.661/0.629)×cTnI]预测脓毒症患者心肌损伤的AUC分别为0.802、0.810、0.887。见表4和图4。
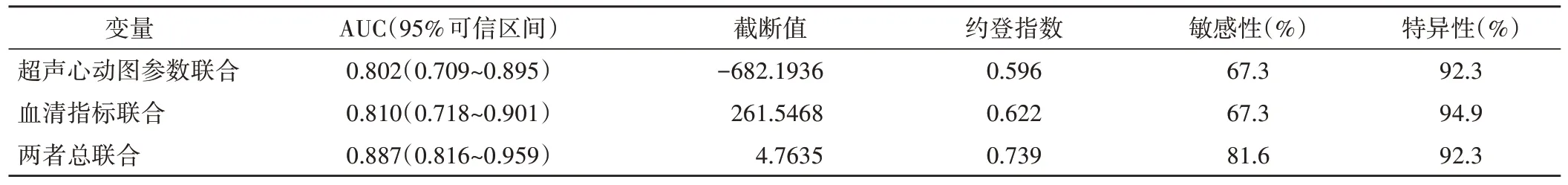
表4 超声心动图参数联合、血清学指标联合及两者总联合对脓毒症患者心肌损伤的预测价值
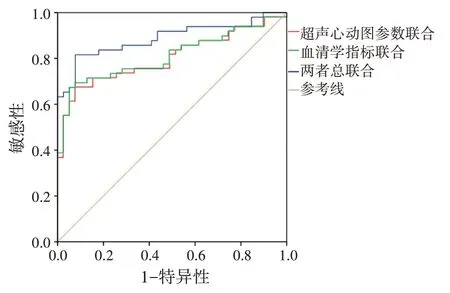
图4 超声心动图参数联合、血清学指标联合及两者总联合预测脓毒症患者心肌损伤的ROC曲线图
讨 论
脓毒症具有起病急、系统性炎症反应重, 预后差等特点。心肌损伤为脓毒症严重并发症之一, 其可加快疾病进程, 增加患者发生器官衰竭甚至死亡的风险。近年来, 临床上关于脓毒症的研究逐渐增多, 但关于脓毒症心肌损伤的发病机制仍不明确。因此探讨脓毒症心肌损伤相关预测因子, 为临床诊断脓毒症心肌功能障碍及评估预后提供参考仍是亟待解决的问题。
目前临床评估左室功能的“金标准”是心导管术, 但其具有侵入性, 费用较高, 且对操作者水平要求高, 临床推广应用有一定局限。超声心动图具有操作简便、价廉、无创、可重复性等优点, 临床应用较广泛。研究[7]显示, 脓毒症心肌损伤超声心动图主要表现为心脏收缩功能异常、左室舒张功能受损、射血分数降低及血管低反应性。另有研究[8]显示, 脓毒症心肌损伤主要表现为心脏舒张、收缩功能障碍或二者同时存在, 超声心动图可表现为以下3类:①左心大小正常, 舒张功能降低;②左心扩大, 舒张功能降低;③左心扩大, 收缩及舒张功能降低。本研究结果显示, 各组LVPWd、LVPWs、LASV、LAEI、LAEF比较差异均有统计学意义(均P<0.05);对照组、非心肌损伤组、心肌损伤组LASV、LAEI、LAEF均依次减低, LVPWd、LVPWs均依次增高, 各组两两比较差异均有统计学意义(均P<0.05)。提示脓毒症患者可能同时存在心室舒张功能与收缩功能障碍, 从而加速心肌功能受损。ROC曲线分析显示, 超声心动图参数联合预测脓毒症患者心肌损伤的AUC为0.802, 提示超声心动图可有效评估脓毒症患者心脏收缩与舒张功能, 反映其心肌损伤情况。
BNP、cTnI均为心肌损伤诊断及预后评估的有效指标[9]。其中BNP与心脏功能紧密相关, 可作为无症状及早期心力衰竭的筛查指标[10]。研究[11]显示, 脓毒症发生时, 高血糖可介导炎性炎症反应级联放大, 释放大量IL-6、TNF-α、自由基, 增加机体炎症反应, 导致内皮细胞凋亡及心肌损伤。脓毒症患者高血糖时, 糖分解底物减少, 脂肪酸增多, 心肌收缩能力降低, 导致力衰竭及心律失常的发生率增高。高水平HbA1c为心肌损伤的独立影响因素, 且与cTnI呈正相关, 因此对早期心肌损伤的检测具有重要价值。另外, 脓毒症发生时中性粒细胞活化并聚集于心肌组织, 刺激炎症介质、急性期反应蛋白等大量释放, 进而引起心肌损伤[11]。MPO为中性粒细胞、单核细胞及巨噬细胞分泌的过氧化物酶, 参与心肌再灌注损伤, 当心肌缺血再灌注时, 中性粒细胞浸润可产生大量溶酶体酶MPO, 因此MPO不仅可以反映心肌浸润中性粒细胞数量, 还能体现其激活程度, 可作为心肌损伤中性粒细胞浸润的标志因子[12]。韩斌等[13]研究显示, MPO水平在脓毒症心肌损伤中显著升高, 且与cTnI呈正相关。本研究结果显示, 各组HbA1c、MPO、BNP、cTnI比较差异均有统计学意义(均P<0.05);对照组、非心肌损伤组、心肌损伤组HbA1c、MPO、BNP、cTnI均依次增高, 各组两两比较差异均有统计学意义(均P<0.05)。提示血清学指标能准确评估脓毒症患者心肌损伤, 有助于临床医师及早采取干预。ROC曲线分析进一步显示, 血清学指标联合预测脓毒症患者心肌损伤的AUC为0.810, 表明其对脓毒症心肌损伤具有一定预测价值。
本研究相关性分析显示, LVPWd、LVPWs与HbA1c、MPO、BNP、cTnI均呈正相关, LASV、LAEI、LAEF与HbA1c、MPO、BNP、cTnI均呈负相关(均P<0.05)。与杜桂彬等[14]研究结论一致。ROC曲线分析显示, 超声心动图参数联合血清学指标预测脓毒症患者心肌损伤的AUC为0.887, 提示两者总联合能更准确地评估心肌损伤程度, 有助于及时干预治疗, 改善患者预后。
综上所述, 超声心动图参数联合血清学指标在预测脓毒症患者心肌损伤中具有较好的临床应用价值。但本研究样本量较少, 今后仍需行大样本研究进一步验证。

