钯催化的偕二氟化合物的双醚化反应
刘新莲,李琳,黄银爱,谭露琪,彭金宝
(五邑大学 生物科技与大健康学院,广东 江门 529020)
烯丙基偕二氟化合物是一类重要的含氟化合物,该结构不仅存在于药物中,也是合成其他化合物的重要前体. 其合成方法的研究一直是有机化学十分重要的领域,过渡金属催化的醚化反应是有效的方法之一,尽管这种策略具有直观性,但该方法也具有一定的挑战性[1-5]. C—F键活化是目前有机氟化学研究的热门领域之一,通过C—F键官能化来构建目标化合物分子已经成为有机合成的重要手段,也是有机化学中的重要挑战. 但由于C—F键具有极高的键能,其选择性活化研究进展缓慢,开创性的工作主要集中在各种非催化反应,包括化学计量的硅介导的氢化脱氟、低价铌介导的氢化脱氟和有机铝试剂介导的三氟甲苯活化. 然而,这些方法通常需要相对苛刻的反应条件,因此化学选择性差. 近年来,C—F键活化的研究更多关注于过渡金属催化的选择性的C—F键活化.过渡金属催化也成为目前实现多氟化合物C—F键官能团化的主要策略之一[6-10]. 迄今为止,使用Ni、Fe、Rh、Ir、Cu催化剂设计的选择性C—F键活化已经得到了深入的研究. 与以往的方法相比,这类反应通常在较为温和的条件下进行,并以较高的产率得到了目标产物. 这些反应同时具有极好的选择性和官能团兼容性. 其中,偕二氟化合物就是一种经典的有多个C—F键的化合物,至今已有许多关于偕二氟化合物烯丙基化或亚甲基化的报道,但迄今为止鲜有偕二氟化合物醚化反应的报道. 本文选择苯酚和偕二氟化合物作为研究的起始材料,对之进行钯催化的偕二氟化合物的双醚化反应的研究.
1 背景介绍
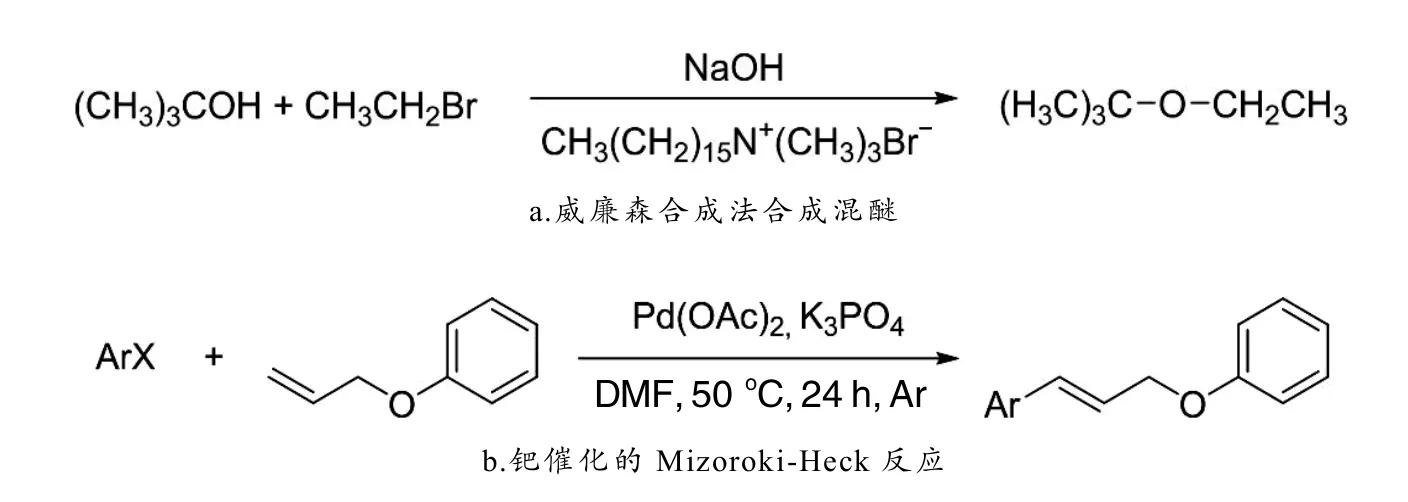
成醚类化合物的最常用的方法是利用醇钠与卤代烃RX的SN2反应,即Williamson反应(图1-a).该反应选用伯卤代烷时效果最好,仲卤代烷的消除产物较多,而叔卤代烷在强碱(醇钠)的作用下,只能得到烯烃. 因此在合成混醚时,必须选择适当的原料组合. 另外,Mitsunobu反应和芳环上的亲核取代反应也是合成芳基醚类化合物的常用方法,可用于合成脂肪醚、环醚及芳基醚.
烯丙基芳基醚结构广泛存在于天然产物和药物分子中,在生物制药和许多精细化学品的研究领域都有着非常重要的作用[11-13]. 此外,在有机合成领域,烯丙基芳基醚还是许多有机反应的重要起始原料,如Claisen重排反应[14]、[1,3]-σ迁移反应和烯丙基取代反应[15]. 一直以来,科研工作者都在探究更加简单高效的合成烯丙基芳基醚的方法. 过渡金属催化合成烯丙基芳基醚的反应已经取得了许多进展,使用苯酚盐或过量的苯酚作为外源亲核试剂,大多数方法在反应过程中产生了Pd、Rh和Ir的烯丙基中间体. 1995年,GOU等[16]通过钯催化苯酚和烯丙基碳酸酯的醚化反应很容易地制备了各种烯丙基芳基醚,该过程的区域选择性取决于温度. 1997年,SATOH等[17]利用钯和异丙醇钛协同催化烯丙醇与酚类化合物的醚化反应,以中等至良好的产率得到了烯丙基苯基醚类化合物.2009年,MINO等[18]使用钯催化烯丙基芳基醚与芳基碘化物的Mizoroki-Heck反应(图1-b),在非常温和的反应条件下,使用催化量的醋酸钯在DMF中、50°C下以腙作为配体,以良好的产率得到了一系列烯丙基芳基醚的产物. 然而,文献报道的诸多合成方法对C—Br键或者C—I键的活化比较多,很少有对C—F键进行活化的. Pan等[19]2020年报道了铑催化的烯丙基二氟化物的不对称芳基化,即在手性二烯-铑络合物催化下,从容易获得的E-烯丙基二氟化物与芳基硼酸反应得到高产率的手性单氟烯烃(图1-c),并具有完美的对映体选择性(ee)> 99%和高水平的Z/E选择性(高达 20 :1).受文献报道和前期工作的启发,我们设想用苯酚和偕二氟化合物作为原料,利用钯促进的C—F键醚化反应制备相应的烯丙基苯基醚衍生物(图1-d).
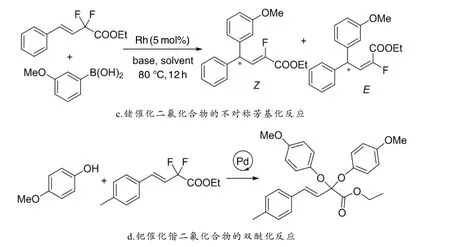
图1 醚化反应背景介绍
2 钯催化偕二氟化合物双醚化反应的条件筛选
如图2所示,本研究的偕二氟化物底物[20]很容易从廉价的商业来源(烯烃和溴二氟乙酸乙酯)中一步制备,且有较高的产率和选择性.
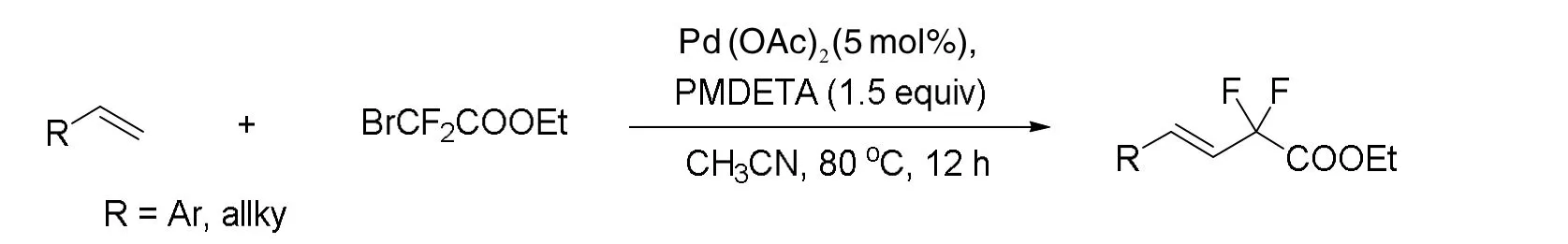
图2 偕二氟化合物的合成
如图3所示,我们以苯酚、二氟烯烃作为模板底物,醋酸钯作为催化剂,三(对甲苯基)膦(P(p- tolyl)3)作为配体,碳酸铯作为碱,甲基叔丁基醚作为溶剂,在90°C的温度下尝试了本文设计的双醚化反应. 经过10 h的反应,能够以56%的产率得到相应的双醚类化合物(表1-3).
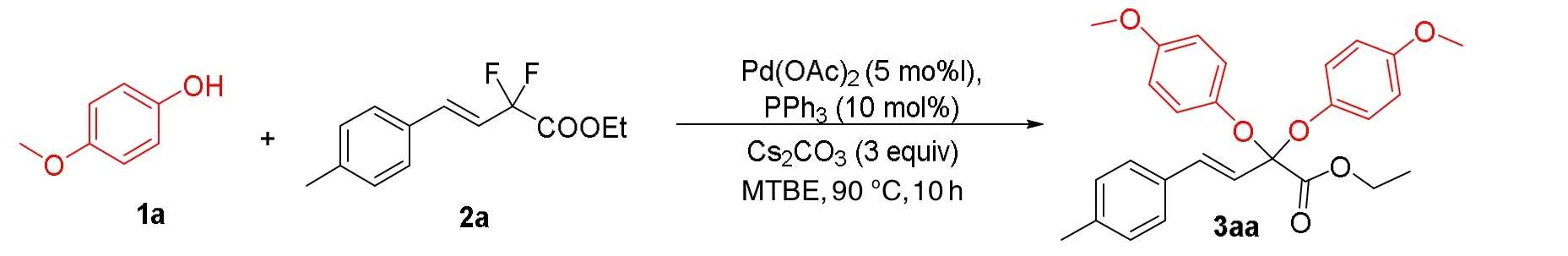
图3 钯催化偕二氟化合物双醚化反应
按表1所列方案,我们确定了优化的反应条件:
1)催化剂的筛选. 催化剂对目标产物产率的影响比较明显. 表1-1~1-4表明,二价钯的催化剂都能够以中等至良好的产率得到目标产物;但PdCl2的催化产率较低,基本上没有目标产物. 通过筛选,选择 Pd(OAc)2作为催化剂时,产率可以达到56%. 此外,我们尝试不用催化剂来完成该反应历程,但结果不理想,反应完成后,没有检测到任何产物.
2)配体的筛选(表1-5~1-9). 以 Pd(OAc)2作为最优的催化剂,当使用单齿配体 P(p-tolyl)3时,能够以56%的产率得到目标产物,所以首先筛选了一些单齿配体. 我们发现,一系列三芳基单齿膦配体比较适合该反应,如PPh3获得了23%的产率(表1-5). 随后,我们又尝试了大位阻的单齿配体 BuPAd2,但是结果不理想,基本观察不到产物(表1-6). 另外,电子性质相似而位阻更大的三芳基单齿膦配体如 P(o-tolyl)3,也不能使反应进行(表1-7). 单齿配体除 P(p-tolyl)3外,其余配体都不太适合. 我们又对双膦配体进行了筛选,当使用双膦配体Xantphos时,产率只有15%(表1-8);当选用DPPP作为配体,只以30%的产率得到了相应的双醚类化合物(表1-9). 这表明配体的空间位阻效应对反应历程影响比较明显. 综上,我们选用 P(p-tolyl)3作为最终的配体.
3)碱的筛选(表1-10~1-13). 以苯酚、二氟烯烃作为模板底物, Pd(OAc)2为催化剂,P (p-tolyl)3为配体,甲基叔丁基醚作为溶剂的条件下,对碱进行了筛选. 可以看到, Na2CO3只得到了20%的产率(表1-11),而强碱 Cs2CO3的反应效果更好(表1-3);有机碱中TEA不能使反应进行,DBU可以得到30%的产率.
4)溶剂的筛选(表1-14~1-17). 该反应在非极性溶剂中效果较好,其中,在甲苯溶剂以40%的产率得到双醚类化合物(表1-15);在醚类溶剂如THF和dioxane,分别以25%和31%的产率得到产物(表1-16~1-17). 而当使用极性溶剂如乙腈时,几乎检测不到反应产物(表1-14). 最终,以甲基叔丁基醚作为最优溶剂,产率达到56%(表1-3).
5)反应温度的筛选(表1-18~1-21). 温度对该双醚化反应同样起着重要的影响. 当温度降低到60°C时,产物产率达到了68%(表1-18). 当温度降低到70°C时,产物产率达到了76%(表1-19).当温度达到80°C时,产物产率为54%(表1-20). 而当温度继续增加到110°C时,就观察不到目标产物了(表1-21). 因此,我们后续的反应都是在70°C下进行的.
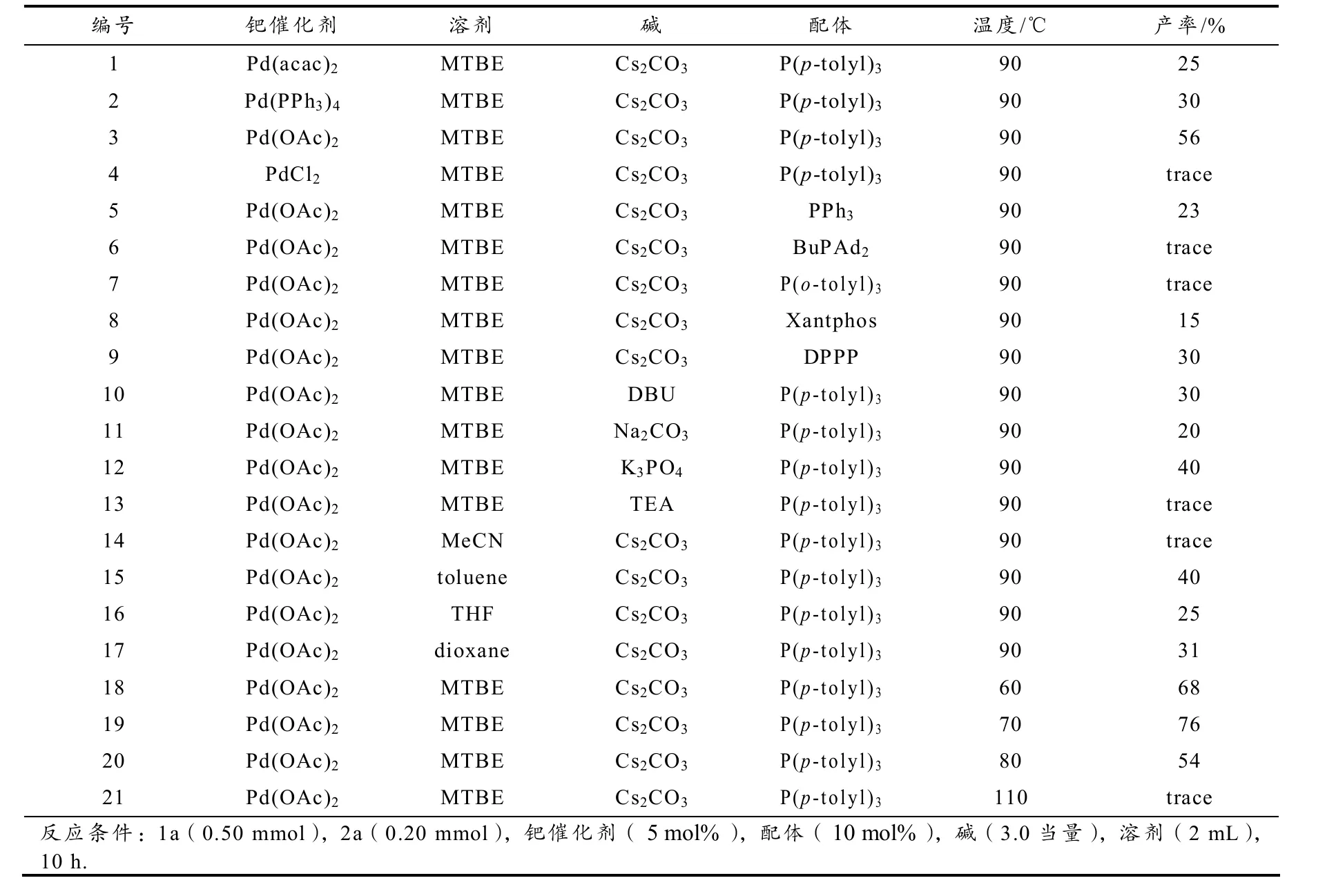
表1 双醚化反应的优化
综上,本文确定的最优反应条件:苯酚(0.5 mmol)、二氟烯烃(0.20 mmol)、醋酸钯(5 mol%)、P(p-tolyl)3(10 mol%)、碳酸铯(0.6 mmol)、甲基叔丁基醚(2 mL)、70°C、10 h. 该条件下能够以76%的产率得到相应的醚类化合物.
3 反应的底物适应性
为了说明该醚化过程有良好的底物适应性,我们对不同苯酚的底物范围进行了拓展,具体如图4所示:1)总体来讲,大多数不同取代基的苯酚都能够以中等至良好的产率得到目标产物(3aa-3ap);同时,对于大部分底物,除了双醚化的产物之外,我们也观察到了部分单醚化的产物,以及少量双醚化产物水解的副产物. 2)当苯环对位上含有如甲基、乙基、叔丁基等给电子基团时,分别以37%、50%和51%的产率得到对应的醚类化合物(3ac、3af、3ah). 3)当苯环对位上含有氯、溴等吸电子基团时,分别以30%和65%的产率得到对应的醚类化合物(3ae、3ai). 这表明,电子效应对于该反应有影响. 4)不同取代基团在苯环邻位和对位时对产物产率有不同影响,而取代基的空间位阻效应对该反应没有显著的影响(3ac vs 3an,3ab vs3ad vs3ai). 邻位有溴取代的底物,以60%的产率得到了相应的醚类化合物(3ad);间位有溴取代的底物,以40%的产率得到了相应的醚类化合物(3ab);对位有溴取代的底物,以65%的产率得到了相应的醚类化合物(3ai). 5)当苯酚的苯环上含有两个取代基时,也能够以中等的产率得到对应的醚类产物. 例如,4-溴-3-甲氧基苯酚可以以43%和50%的产率得到相应的目标产物(3aj)和(3ak),3,5-二甲基苯酚也可以以38%的产率得到相应的醚类化合物(3ao),3,4-二甲基苯酚也可以以35%的产率得到相应的醚类化合物(3am).6)苯环上没有取代的偕二氟底物与4-溴苯酚反应,也得到了60%的产物(3ap).
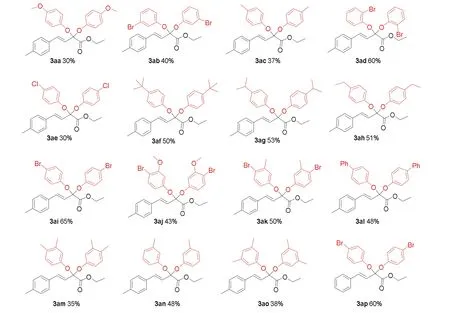
图4 双醚化反应的底物拓展
4 结论
本文利用偕二氟化合物和苯酚作为简单的前体,发展了钯催化的偕二氟化合物的双醚化反应,合成了这类烯丙基芳基醚类化合物. 这种双醚化反应方法具有条件温和、操作简单的特点,是一种有价值的合成方法. 本文结果也为醚类化合物合成提供了一个新的思路.
5 实验部分及数据
5.1 试剂、溶剂和分析方法
除非另有说明,所有反应均在氮气气氛下进行. 所有试剂均来自商业来源并且未经进一步纯化直接使用. 所有溶剂均通过标准技术干燥并在使用前蒸馏. 使用石油醚(沸点60~90°C)和乙酸乙酯作为洗脱剂在硅胶(200~300目)上进行柱层析. NMR光谱记录在Bruker Avance上(500 MHz的1H NMR、126 MHz的13C NMR),波谱数据以 CDCl3(1H NMRδ7.26,13C NMRδ77.16)作为溶剂. 高分辨率质谱(HRMS)由Thermo Fisher Scientific获得. 其主体由两部分组成:Thermo Scientific的UltiMate 3000系列液相系统和Thermo Scientific Q-Exactive组合四极杆Orbitrap质谱仪. 所有耦合常数(J)均以Hz为单位. 使用以下缩写描述峰分裂:s =单峰,d =双峰,dd =双双峰,t =三峰,dt =双三峰,q =四峰,m =多重峰.
5.2 偕二氟化合物合成的一般操作
在50 mL双口瓶中,称取溴二氟乙酸乙酯(1.53 g,7.50 mmol,1.5当量),PMDETA(五甲基二亚乙基三胺)(1.30 g,7.50 mmol,1.5当量)和碘化亚铜(95.30 mg,0.50 mmol,10 mol%),使用双排管抽换N23次,之后往体系中加入苯乙烯(521.00 mg,5.00 mmol,1.0当量)和10 mL的乙腈. 混合物在80°C油浴下搅拌12 h,TLC监测反应完成后,冷却至室温,往体系中加入水(10 mL),混合物分别用乙酸乙酯(20 mL)萃取3次. 合并有机层,用饱和食盐水洗涤,有机相用无水 Na2S O4干燥. 过滤浓缩滤液,粗产物用柱层析法纯化(乙酸乙酯/己烷=1/20)得到产物1a为无色油状物(1.02 g,产率90%).
5.3 钯催化的偕二氟化合物的双醚化反应的一般操作
以3aa为例,在15 mL厚壁耐压管中,称取二氟烯烃(48.00 mg,0.20 mmol)、对甲氧基苯酚(62.00 mg,0.50 mmol)、醋酸钯(2.25 mg,5 mol%), P(p- tolyl)3(3.08 mg,10 mol%),碳酸铯(195.00 mg,0.60 mmol),使用双排管抽换N23次,之后往体系中加入2 mL的MTBE,密封后置于70°C下反应10 h. 之后,冷却至室温,过滤浓缩滤液,粗产物用柱层析法纯化(乙酸乙酯/己烷= 1 : 100 ~ 1 :50)得到产物.
5.4 化合物的合成及部分波谱数据
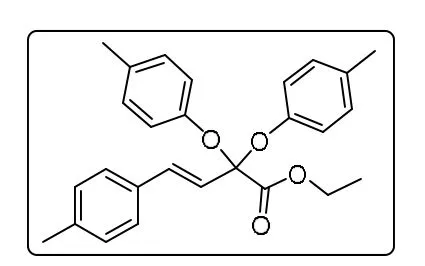
根据上述钯催化的偕二氟化合物的双醚化反应的通用合成方法,用4-甲基苯酚和偕二氟化合物制备. 产物用乙酸乙酯/石油醚 = 1 :100纯化得到3ac为黄色液体.1H NMR(500 MHz,CDCl3)δ7.28 (d ,J= 7.8 Hz,2H), 7.14 (t ,J= 8.6 Hz,6H),7.08 (d,J= 16.1 Hz,1H), 7.04 (d ,J= 8.4 Hz,4H), 6.27 (d ,J= 16.1 Hz,1H),4.16 (d d,J= 13.9 7.0 Hz,2H), 2.34 (s ,3H), 2.26 (s,6H), 1.09 (t ,J= 7.1 Hz,3H).13C NMR (126 MHz,CDCl3)δ167.7,152.047,138.778,CDCl3)δ167.7,152.047,138.778135.537,132.778,132.5,129.8,129.427,127.1,124.3,119.4,101.7,62.4,20.7,13.9.
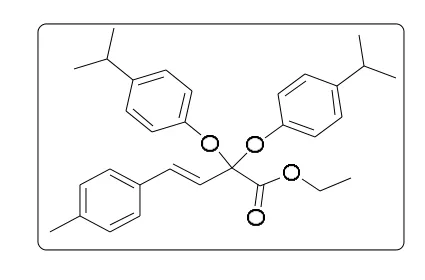
根据上述钯催化的偕二氟化合物的双醚化反应的通用合成方法用4-异丙基苯酚和偕二氟化合物制备. 产物用乙酸乙酯/石油醚 = 1 :100纯化得到3ag为黄色液 体.1H NMR(500 MHz,CDCl3)δ7.28 (s ,2H), 7.17 (d ,J= 8.5 Hz,4H),7.13 (d,J=7.7 Hz,2H), 7.08 (d ,J= 8.5 Hz,5H), 6.27 (d ,J= 16.1 Hz,1H), 4.15 (q ,J= 7.1 Hz,2H),2.83 (dt,J= 13.7,6.9 Hz,2H), 2.34 (s ,3H), 1.19 (d ,J= 6.9 Hz,12H),1.01 (t,J= 7.1 Hz,3H).13C NMR(126 MHz,CDCl3)δ167.5,152.2,143.3,138.6,135.4,132.7,129.3,127.0,127.0,124.3,119.1,101.6,62.1,33.3,24.1,21.3,13.7.
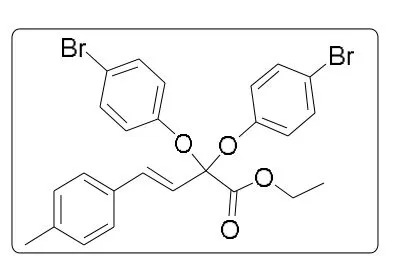
根据上述钯催化的偕二氟化合物的双醚化反应的通用合成方法,用4-溴苯酚和偕二氟化合物制备. 产物用乙酸乙酯/石油醚 = 1 :100纯化得到3ai为深黄色油 状 液 体.1H N MR (500 MHz,CDCl3)δ7.36 (d ,J= 9.0 Hz,4H),7.30 ~7.24 (m , 2H),7.15 (d,J= 7.9 Hz,2H), 7.12 (d ,J= 9.0 Hz,4H), 7.06 (d ,J= 16.1 Hz,1H),6.2 2 (d,J=16.1 Hz,1H), 4.19 (q ,J=7.1 Hz,2H ), 2.35 (s ,3H), 1.11 (t ,J= 7.1 Hz,3H).13C NMR(126 MHz,CDCl3)δ166.8,153.1,139.3,136.4,132.4,132.3,129.6,127.2,122.9,121.0,116.0,101.7,62.8,21.4,13.9.
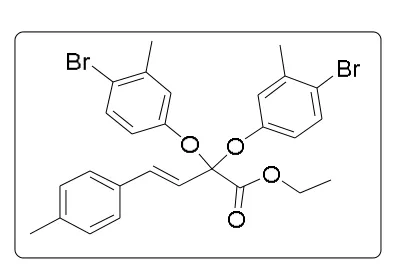
根据上述钯催化的偕二氟化合物的双醚化反应的通用合成方法,用4-溴-3-甲氧苯酚和偕二氟化合物制备. 产物用乙酸乙酯/石油醚 = 1 :100纯化得到3ak为黄色液体.1H NMR(500 MHz,CDCl3)δ7.39 (d,J= 8.8 Hz,2H),7.30 (d,J=8.0 Hz,2H) , 7.18 ~7.13 (m ,4H), 7.10 (d ,J= 16.1 Hz,1H), 2.7.00 (d d,J= 8.8,8 Hz,2H),6.25 (d,J= 16.1 Hz,1H), 4.21 (q ,J= 7.1 Hz,2H), 2.39 ~2.31 (m ,9H),1.13 (t,J= 7.1 Hz ,3H).
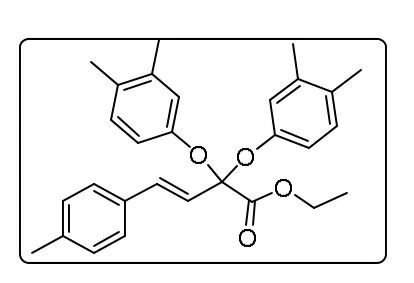
根据上述钯催化的偕二氟化合物的双醚化反应的通用合成方法用3,4-二甲基苯酚和偕二氟化合物制备. 产物用乙酸乙酯/石油醚 = 1 :100纯化得到3am为黄色液体.1H NMR(500 MHz,CDCl3)δ7.28 (d,J= 8.0 Hz,2H),7.13 (d,J=7.9 Hz,2H) , 7.08 (d ,J= 16.1 Hz,1H), 7.05 (s ,2H), 7.01 (d d,J= 8.4,2.1 Hz,2H),6.97 (d,J=8.3 Hz,2H ), 6.26 (d ,J= 16.1 Hz,1H), 4.18 (q ,J= 7.1 Hz,2H), 2.34 (s ,3H ), 2.18 (d,J= 17.2 Hz,12H),1.09 (t,J=7.1 Hz,3H) .13C NMR(1 26 MHz,CDCl3)δ167.8,152.3,138.7,137.6,135.4,132.9,131.1,130.2,129.4,127.1,124.5,120.7,116.6,101.6,62.3,21.4,20.1,19.1,13.9.
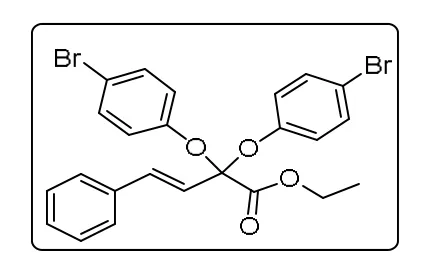
根据上述钯催化的偕二氟化合物的双醚化反应的通用合成方法,用4-溴苯酚和偕二氟化合物制备. 产物用乙酸乙酯/石油醚 = 1 :100纯化得到3ap为黄色液体.1H NMR(500 MHz,CDCl3)δ7.59 (d ,J= 8.1 Hz,2H ), 7.46 (d ,J= 8.1 Hz,2H),7.37 (d,J= 8.9 Hz,4H), 7.12 (t ,J= 9.7 Hz,5H), 6.35 (d ,J= 16.1 Hz,1H),4.1 9 (q,J=7.1 Hz,2H), 1.11 (t,J= 7.1 Hz,3H).13C NMR(126 MHz,CDCl3)δ166.5,153.0,138.4,135.2,132.5,127.5,126.8,125.9,125.9,120.9,116.4,101.4,63.0,14.0.

