CalliSpheres载药微球在中晚期非小细胞肺癌合并咯血中的应用效果*
江强 黄燕群 王红珍 许玉华
非小细胞肺癌(NSCLC)发生率约占全部肺癌的85%,手术为治疗NSCLC 的主要方法,但多数NSCLC 患者确诊时已处于中晚期,手术切除率低,患者5 年生存率<15%[1]。咯血为中晚期NSCLC 患者的常见症状,多数患者由于咯血窒息或大量失血而死亡,病情进展快速[2]。放疗、化疗联合内科用药是治疗中晚期NSCLC 合并咯血的主要方法,但治疗效果不理想且不良反应较多,临床应用具有一定局限性。经支气管动脉化疗灌注栓塞术是治疗肺癌的重要介入治疗手段,获得的近期疗效优于全身化疗效果[3]。明胶海绵颗粒与碘化油为经支气管动脉化疗灌注栓塞术中常用的栓塞材料,但明胶海绵颗粒与碘化油栓塞不彻底且并发症发生率较高[4]。近年来随着栓塞材料的不断研发及应用,CalliSpheres载药微球作为一种新型栓塞材料,具备血管栓塞及化疗药物局部缓释的双重作用,促使肺癌组织缺血、缺氧及坏死[5-6]。鉴于此,本研究将探讨CalliSpheres 载药微球在中晚期NSCLC 合并咯血患者中的应用效果。现报道如下。
1 资料与方法
1.1 一般资料 选择2019 年6 月-2020 年12 月于江西省胸科医院治疗的60 例中晚期NSCLC 合并咯血患者。纳入标准:(1)NSCLC 患者均经病理学或细胞学明确诊断;(2)临床分期:Ⅲ、Ⅳ期;(3)具有1 个或多个可测量病灶;(4)美国东部肿瘤协作组(ECOG)评分≤2 分。排除标准:(1)预计生存期<3 个月;(2)具有手术史;(3)存在脑部或肺以外的转移病灶;(4)凝血功能障碍;(5)合并无法控制的糖尿病或高血压。按随机数字表法将患者分为两组,各30 例。本研究获本院医学伦理委员会批准。患者签署知情同意书。
1.2 方法 两组术前均常规行CT 血管成像检查,明确肿瘤供血血管并排除其他原因所致咯血(肺结核、支气管扩张等);患者可在无活动性出血或出血停止时行支气管动脉栓塞治疗,采用改良Seldinger 技术,经右侧股动脉穿刺,置入5F 动脉鞘,沿动脉鞘导入5F 造影导管,按照术前胸部CT血管成像结果,导管头置于支气管动脉开口行血管造影,见对比剂从血管内溢出,并可见支气管动脉增粗、迂回、增生的血管丛,证实为肿瘤供血血管;采用同轴导管法,将微导管超选择插入支气管动脉病变分支内,避开脊髓供血动脉。观察组采用CalliSpheres 载药微球经支气管动脉化疗灌注栓塞术治疗,经微导管注入0.9%氯化钠溶液稀释过的60~90 mg 顺铂(生产厂家:江苏豪森药业集团有限公司,批准文号:国药准字H20040813,规格:6 mL∶30 mg),采用20 mL 0.9%氯化钠溶液冲管;吡柔比星(生产厂家:瀚晖制药有限公司,批准文号:国药准字H20045983,规格:10 mg)20~40 mg 与CalliSpheres 微球(苏州恒瑞迦俐生生物科技有限公司生产,规格:300~500 μm)混匀后缓慢经微导管注入,采用20 mL 5%葡萄糖注射液(GS)冲管。对照组采用支气管动脉栓塞术、化疗治疗:微导管超选至支气管动脉病变分支内,混匀300~500 μm的聚乙烯醇颗粒与造影剂,通过5 mL 注射器缓慢推注,待血流减慢,停止注射,采用5 mL 0.9%氯化钠溶液缓慢冲管,加用明胶海绵颗粒栓塞,至造影剂在主干血管滞留;术后按期行内科静脉化疗,第1~5 天静脉滴注注射用顺铂(生产厂家:齐鲁制药有限公司,批准文号:国药准字H37021357,规格:20 mg)20 mg/m2;第1 天静脉滴注注射用培美曲塞二钠[生产厂家:苏州二叶制药有限公司,批准文号:国药准字H20203594,规格:0.5 g(按C20H21N5O6计)]500 mg/m2;21 d 为1 个周期,治疗2~4 个周期。化疗方案按病理类型选择。
1.3 观察指标及评价标准(1)临床疗效:治疗3 个月后评估疗效,所有目标病灶动脉期增强显影消失为完全缓解(CR);所有目标病灶的基线最长径总和缩小≥30%为部分缓解(PR);所有目标病灶的基线最长径总和缩小未达PR 或增加未到进展(PD)为稳定(SD);所有目标病灶的基线最长径总和增加≥20%或出现新病灶为PD,依据CR、PR计算总有效率。(2)止血效果:行支气管动脉化疗栓塞后大咯血立刻停止,或24 h 内停止为完全止血;仅痰中带血,或日最大咯血量减少>50%,咯血次数减少为不完全止血;未达到以上标准为无效,依据完全止血、不完全止血病例计算止血总有效率。(3)肿瘤标志物:治疗前、治疗3 个月后采集两组空腹静脉血,采用电化学发光法测定癌胚抗原(CEA)水平。(4)统计两组治疗期间不良反应发生情况。(5)术后随访12 个月,统计两组生存率。
1.4 统计学处理 采用SPSS 22.0 软件分析数据,计数资料以率(%)表示,用χ2检验;计量资料用()表示,组间比较采用独立样本t 检验,组内比较采用配对t 检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组一般资料比较 观察组男18 例,女12 例;年龄37~76 岁,平均(58.97±4.61)岁;ECOG 评分0~2 分,平均(1.15±0.40)分;临床分期:Ⅲ期14 例、Ⅳ期16 例。对照组男16 例,女14 例;年龄36~78 岁,平均(59.11±4.55)岁;ECOG 评分0~2 分,平均(1.13±0.39)分;临床分期:Ⅲ期17 例、Ⅳ期13 例。两组一般资料相比,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组临床疗效比较 观察组治疗总有效率高于对照组,差异有统计学意义(χ2=4.444,P=0.035),见表1。

表1 两组临床疗效比较[例(%)]
2.3 两组止血效果比较 两组止血总有效率比较,差异无统计学意义(χ2=0.480,P=0.488),见表2。

表2 两组止血效果比较[例(%)]
2.4 两组CEA 水平比较 治疗前两组CEA 水平比较,差异无统计学意义(P>0.05);治疗后观察组CEA 水平低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组CEA水平比较[ng/mL,()]
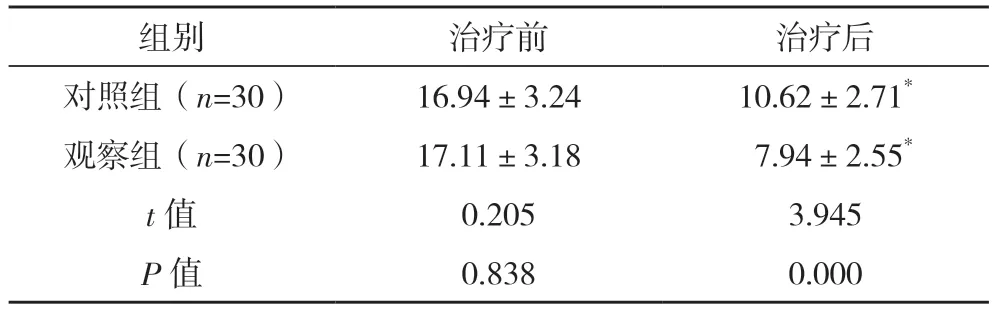
表3 两组CEA水平比较[ng/mL,()]
*与治疗前比较,P<0.05。
2.5 两组不良反应发生情况比较 两组恶心、呕吐、发热、疼痛、呼吸困难、胸痛发生率比较,差异均无统计学意义(P>0.05),见表4。
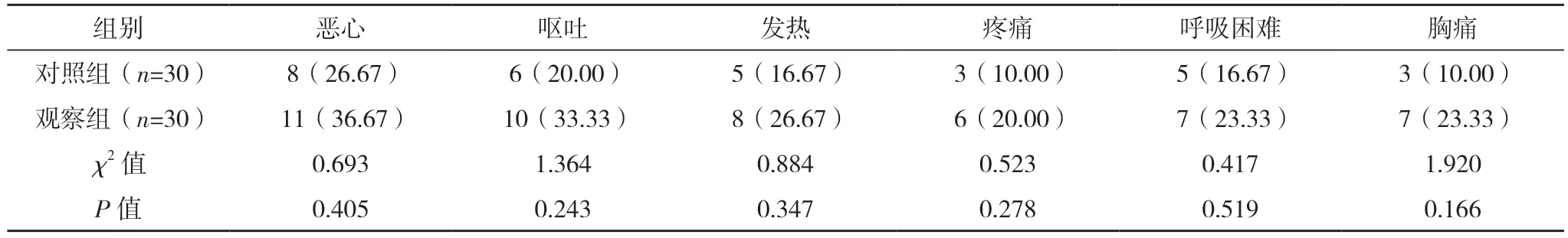
表4 两组不良反应比较[例(%)]
2.6 两组生存率比较 术后随访12 个月,两组生存率比较,差异无统计学意义(χ2=0.739,P=0.390),见表5。

表5 两组生存率比较[例(%)]
3 讨论
咯血作为中晚期NSCLC 患者较为严重的并发症,保守治疗往往难以对中晚期NSCLC 合并咯血患者的病情进行有效控制[7]。目前支气管动脉栓塞术是治疗肺癌并大咯血患者的优选方法,能够快速控制出血,对肿瘤滋养动脉血流进行阻断,进而导致细胞缺氧,对肿瘤细胞进行杀伤[8-9]。
在支气管动脉栓塞术中,明胶海绵颗粒是常用的栓塞剂,但作为临时栓塞剂,其稳定性差,难以达到临床上期望效果[10]。聚乙烯醇颗粒作为一种高分子材料,具有良好的生物相容性及安全性,不溶于水,在体内不降解,属于永久性栓塞剂,将聚乙烯醇颗粒+明胶海绵颗粒联合治疗咯血具有更好的疗效[11]。载药微球作为一种新型栓塞剂,可负载阿霉素、伊立替康及顺铂等正电荷化疗药物,载药量为5~45 mg/mL,具有缓释抗肿瘤药物的能力[12-13]。王芹等[14]研究指出,针对晚期NSCLC 患者,CALLISPHERES®载药微球、支气管动脉化疗药物灌注联合治疗效果优于传统化疗,可延长患者的无进展生存时间(PFS)、中位生存期(OS),且安全性高。本次研究结果显示,观察组治疗总有效率高于对照组,治疗后CEA 水平低于对照组(P<0.05);两组止血总有效率及生存率、不良反应发生率比较相近。提示CalliSpheres 载药微球经支气管动脉化疗灌注栓塞术与支气管动脉化疗栓塞联合化疗治疗中晚期NSCLC 合并咯血患者的止血效果相当,但与支气管动脉化疗栓塞联合化疗治疗比较,CalliSpheres 载药微球经支气管动脉化疗灌注栓塞术治疗中晚期NSCLC 合并咯血肿瘤控制效果更佳,有利于提高近期总有效率,降低肿瘤标志物水平,且不良反应并未增加。CalliSpheres 载药微球经支气管动脉化疗灌注栓塞术治疗可克服部分静脉化疗药物无法通过生理屏障的不足,可提高肿瘤局部药物浓度,增强杀伤肿瘤细胞能力[15-16]。CalliSpheres 载药微球结构稳定,膨胀系数小,能够避免由于装载药物后对血管造成的堵塞,且化疗药物、CalliSpheres载药微球各自保持理化性质稳定,不会产生化学反应[17-18]。CalliSpheres 载药微球可与化疗药物紧密结合,达到靶血管后,可对肿瘤血管进行栓塞,并可将化疗药物缓慢释放,对肿瘤进行攻击,抑制肿瘤再生[19-20]。但本次研究中仅纳入60 例中晚期NSCLC 合并咯血患者,且仅随访12 个月,同时由于条件所限,肿瘤标志物仅检测了CEA 一项,结果数据存在局限性,还有待临床深入分析研究,以进一步证实CalliSpheres 载药微球在中晚期NSCLC 合并咯血患者中应用效果。
综上所述,CalliSpheres 载药微球在中晚期NSCLC 合并咯血患者中可控制咯血,提高抗肿瘤效果,降低CEA 水平,且不良反应并未增加。

