球霰石型碳酸钙的调控制备研究进展
王 鑫,韦 明,刘 琨
(1.中南大学资源加工与生物工程学院,长沙 410083;2.中南大学矿物材料及其应用湖南省重点实验室,长沙 410083;3. 广西夏阳环保科技有限公司,南宁 530009)
0 引 言
碳酸钙是一种非常重要的无机非金属材料和工业原材料,具有价格低廉、来源广泛、无毒、便于生产加工、形貌可控等优点[1-3],常以粉体助剂的形式广泛应用于造纸、土木建筑、塑料、涂料、油墨、密封胶、黏结剂、化妆品、食物、橡胶制品、生物保鲜、润滑油、纤维复合材料、药物载体材料等[4],因此关于碳酸钙的研究一直是非金属矿深加工领域和无机非金属材料领域的热点。
碳酸钙有三种常见的晶型[5-7]:文石、球霰石、方解石。从热力学稳定性角度来看,方解石型是热力学最稳定的晶型,在自然界中广泛存在;而球霰石型是最不稳定的,处于亚稳定态[4],在自然界中仅存在于某些鱼类的耳石器官、海鞘的骨针、甲壳动物组织中[8]。在这三种晶型中,球霰石型相比其他两种晶型,除了具有常规的性质,如密度低、白色无味、酸分解性和化学稳定性等之外,还具有中空或多孔结构、粒径分布均匀、微纳米级尺寸、亲水性较高、比表面积较大、溶解性和分散性较好、生物兼容性与安全性较好、降解性好、相变能力较强、机械性能与热稳定性良好、球形分布等特点[4]。所以,球霰石型碳酸钙在日用、生物医药、新材料等领域极具应用前景和经济效益。但是球霰石结构不稳定,在潮湿环境或水溶液中极易转换为文石和方解石,因此实现球霰石型碳酸钙的稳定调控制备是十分有必要的。本文介绍了球霰石型碳酸钙的形貌结构和性质应用,着重阐述了近些年来球霰石型碳酸钙的制备和稳定方法以及各种方法的优缺点,并提出一些可行的建议,旨在为实现工业上球霰石型碳酸钙的稳定制备提供理论参考。
1 球霰石型碳酸钙的性质与应用
1.1 球霰石型碳酸钙的结构与形貌特点
目前普遍认为球霰石型碳酸钙属于六方晶系,为P63/mmc空间群,CO2-3三角平面斜交于三次轴[9-11],导致其CO2-3基团平行于C轴[4,12]。相比较于方解石的CO2-3基团垂直于C轴,平行结构都具有一定的滑移,这也就解释了球霰石的不稳定性和松散性[4,12]。关于球霰石型碳酸钙的具体晶体结构,普遍认可的是2012年Mugnaioli等[13]所提出的六角形对称结构,该结构是在前人的大量研究基础之上,利用分子动力学模拟以及优化几何计算方法,提出的球霰石结构模型(如图1所示)。
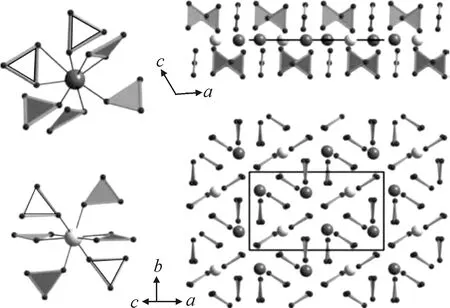
(左边:两个来自不同碳酸基团(白,CO2-3(1);黑,CO2-3(2))的氧原子参与钙离子的配位(下为Ca(1);上为Ca(2))。右边:[010]和[103]面(等价于[001]面先前的六方结构模型)阐明了层状结构和Ca2+的伪六边形的排列。Left: two oxygen atoms from different carbonic acid groups (white gray, CO2-3 (1); black gray, CO2-3 (2)) participate in thecoordination of calcium ions(figure below, Ca (1); figure above, Ca (2)).Right: [010] and [103] planes (equivalent to the previous hexagonal structure model for the [001] plane) illustrate thelayered structure and the pseudo-hexagonal arrangement of Ca2+.)图1 球霰石型碳酸钙晶体结构[13]Fig.1 Crystal structure of vaterite calcium carbonate[13]
球霰石型碳酸钙在自然界中极少存在,通常球霰石是一个由纳米尺寸的微晶球粒组成的多晶球霰石,而不是方解石和文石那样的单晶体。在实验室合成时,颗粒形貌不仅与晶体结构有关,也与制备条件有很大关系。通常实验制备的球霰石型碳酸钙常以球状聚集体的形式存在,而方解石型碳酸钙常以规则的菱面体形式存在,文石型碳酸钙则易形成针状。此外,球霰石型碳酸钙还具有圆盘形、薄片形、六角形、透镜形等形貌。球形形貌的球霰石型碳酸钙被认为是最有应用前景的一种碳酸钙。
1.2 球霰石型碳酸钙的性质与应用
球霰石型碳酸钙属碳酸钙产品中的一类,实验室制备的球霰石型碳酸钙相比于另外两种晶型,除了具有碳酸钙的常规性质(低密度性、白色无味、酸分解性和化学稳定性等性质)之外,还具有中空或多孔结构、球形规则、粒径分布均匀、微纳米级的颗粒尺寸(通常为0.05~5 μm)、较高的亲水性和比表面积、降解性好等特征[4]。球霰石型碳酸钙的重要物理性质如表1[14-16]所示,结构表征的特征参数如表2[14]所示。

表1 球霰石型碳酸钙的重要物理性质[14-16]Table 1 Important physical properties of vaterite-type calcium carbonate [14-16]

表2 球霰石型碳酸钙结构表征的特征参数[14]Table 2 Characteristic parameters for the structural characterization of vaterite-type calcium carbonate[14]
相比于方解石型和文石型碳酸钙,球霰石型碳酸钙由于其独特的结构和性质,在众多领域内具有更好的应用性能和前景。球霰石热力学性质不稳定,在水中易转换为方解石,因此,利用该相变过程,球霰石型碳酸钙可作为一种胶凝体促使水泥颗粒的积聚、水化,提高混凝土的强度和耐久性[4,17]。另外,我国的碳酸钙产品主要是用作填充剂和添加剂,在研究中发现,球霰石有较大的比表面积、良好的分散性、球形尺寸分布均匀等特性,对于油墨、塑料、纸张、涂料等产品填充性能的提高、产品流动性和光泽度的改善能力要明显优于其他两种晶型碳酸钙。同时球霰石型碳酸钙是多孔或中空的微纳米级颗粒,比表面积较大,具有良好的生物降解性和生物兼容性,且分解条件温和、分解速度可控,因此使用其装载药物对人体更加安全,装载效率也比其他晶型的碳酸钙更高[18-19],相比于其他的载体,在价格上也更具有竞争力。除此之外,有研究表明球霰石型碳酸钙在复合材料和仿生材料的制备领域同样有广泛应用,如球霰石型碳酸钙能增强涂料的附着能力、延缓羟基磷灰石的释放速率、增加羟基磷灰石在人体内的降解速率[4,20]、提高复合材料的生物相容性和生物活性等[4,21]。因此,实现球霰石型碳酸钙的工业稳定制备极具经济效益。
2 球霰石型碳酸钙的制备研究进展
球霰石型碳酸钙主要有两种生成途径,即溶解再结晶途径(如图2[22]所示)和固-固相直接转化途径[23]。目前认为溶解再结晶途径是球霰石型碳酸钙生成的主要途径,即:在溶液中无定形碳酸钙作为初始相生成,由于结构内部松散,会快速发生相变成为球霰石型碳酸钙。但是球霰石型碳酸钙的溶解度较高,又会发生溶解并继而发生方解石型碳酸钙的成核生长,这样的过程不断发生,使得球霰石型碳酸钙逐渐转变为方解石型碳酸钙[14,22]。针对球霰石型碳酸钙的结晶生长原理形成了两种理论,一种是基于纳米粒子的聚集理论,另一种是经典晶体生长理论[14]。聚集理论适用于解释核壳微球[14,24]和空心球霰石颗粒[14,17]的形成;晶体生长理论一般用于球晶生长机制的解释,其常被用来解释球状和哑铃形等多种形貌的球霰石型碳酸钙颗粒的形成[14,25]。

图2 CaCO3从非晶相转变为球霰石型和方解石型的形成示意图[22]Fig.2 Schematic diagram of the formation of CaCO3 from amorphous phase to vaterite and calcite[22]
从形成途径与机理出发,目前主要是通过抑制溶解再结晶过程来制备高纯度的球霰石型碳酸钙。当前,常见的制备方法根据合成过程中所涉及到的原理可以划分为碳化法、复分解法和热分解法三种。
2.1 碳化法
碳化法是利用含可溶性钙盐的碱性溶液作为钙源,通过向溶液中通入CO2气体并控制工艺条件制备球霰石型碳酸钙[4,14]。钙源主要分为氢氧化钙的水溶液和氯化钙的碱性溶液两种,因此也确定了碳化法制备的两大体系:Ca(OH)2-H2O-CO2反应体系和CaCl2-NH3·H2O-CO2反应体系。大量研究表明,这两种体系均可较好地制备出球霰石型碳酸钙。
2.1.1 Ca(OH)2-H2O-CO2反应体系
常温下,氢氧化钙固体在水中的溶解度很低,因此Ca(OH)2-H2O-CO2反应体系制备得到的碳酸钙产品中常常存在残余的氢氧化钙,导致产品纯度降低。另外,Ca(OH)2-H2O-CO2反应体系制备的碳酸钙主要是立方结构的方解石型[26],若要制备高纯度球霰石不仅需要加入晶型调控剂,而且要严格控制反应条件。Lai等[27]用甘氨酸作为晶型调控剂成功得到了球霰石型纳米碳酸钙,虽然制备得到的球霰石纯度较好,但是过程中对反应体系的各项因素都需要严格控制,而在实际工业中难以实现。通常在实际应用中,Ca(OH)2-H2O-CO2反应体系主要是用来制备轻质碳酸钙(包括纳米碳酸钙)的一种重要方法。
2.1.2 CaCl2-NH3·H2O-CO2反应体系
CaCl2-NH3·H2O-CO2反应体系的碳化工艺是合成球霰石型碳酸钙较为有效的方法,虽然添加剂仍是影响产物晶型的重要因素,但是通过严格控制反应条件就可以制备出球霰石型碳酸钙[26]。在该反应体系中,NH3·H2O和CO2的来源又可以分为两种形式:直接加入和分解产生。第一种是在CaCl2溶液中直接加入NH3·H2O和通入CO2即可完成制备,如Ding等[28]在不使用任何添加剂的情况下,仅通过控制反应温度便制备出高纯的球霰石型碳酸钙产品。第二种是通过化合物(如尿素、碳酸氢铵、碳酸铵等)升温分解产生的NH3和CO2与CaCl2溶液反应生成球霰石型碳酸钙,亦称为扩散法[14,29-30]。Zhang等[31]利用碳酸氢铵分解产生的NH3和CO2对CaCl2溶液进行碳化反应,并采用复合添加剂(L-赖氨酸与无水对氨基苯磺酸)作为晶型调控剂,实验结果表明,当复合添加剂的复配比为5 ∶1时,球霰石在其与方解石的混合相中占主要成分。胡艳丽等[32]利用碳酸铵分解产生的NH3和CO2对CaCl2溶液进行碳化反应,并用L-天冬氨酸作为晶型调控剂,实验结果表明,随着L-天冬氨酸浓度的增加,碳酸钙晶体的生长速度明显变慢,体系中球霰石型碳酸钙所占比例减少,且随着碳化反应时间的延长,球霰石型碳酸钙逐渐转化为方解石型碳酸钙。从这两种NH3·H2O和CO2来源的实验中可以看出,前者的反应速度迅速,仅通过控制工艺条件便可以制备出球霰石型碳酸钙,实用性较强,不足之处在于过程中会使用大量的氨水,因此后续需要考虑氨水回收与循环利用。而后者则是利用气体的扩散进行反应,反应速度明显慢于前者,通常反应完全需要几十个小时,并且这种体系一般是用于模拟自然界中的球霰石型碳酸钙的生成,实际工业应用存在较大难度。
碳化法的本质是利用CO2气体在碱性溶液溶解反应得到的CO2-3与溶液中的Ca2+发生沉淀反应制备碳酸钙,因此碳酸钙的生成速率与CO2气体的溶解速率密切相关,碳酸钙的产品质量也与CO2气体在水中的分散度密切相关。而在常温常压下,CO2气体在水中的溶解速率和分散度较低,因此使用碳化法制备球霰石型碳酸钙的效率和产率较低[4]。但是碳化法具有成本低廉、工艺设备简单等优点,目前已是国内外用于制备各类型碳酸钙产品的主要工业生产方式。同时,国内外研究者通过使用气体分散器等装置增加了CO2气体在溶液中的传质速率和分散度,提高了球霰石型碳酸钙的效率和产率,因此利用碳化法制备球霰石型碳酸钙极具应用前景。
2.2 复分解法
复分解法是指将钙盐溶液和碳酸盐溶液在一定条件下进行混合发生复分解反应,同时加入晶型调控剂并控制反应温度、浓度等因素来调控制备球霰石型碳酸钙[4,14,33]。一般情况下,制备时可以将一种溶液快速混入到另一种溶液中进行反应[14,34-35],也可以将一种溶液通过控制加入速率的方式引入到另一种溶液中进行反应[14,30],同时需要辅以搅拌以促进复分解反应的进行。目前,常采用将钙盐溶液通过滴加的方式引入到碳酸盐溶液中进行复分解反应制备球霰石型碳酸钙[36],常用反应流程如图3[37]所示。
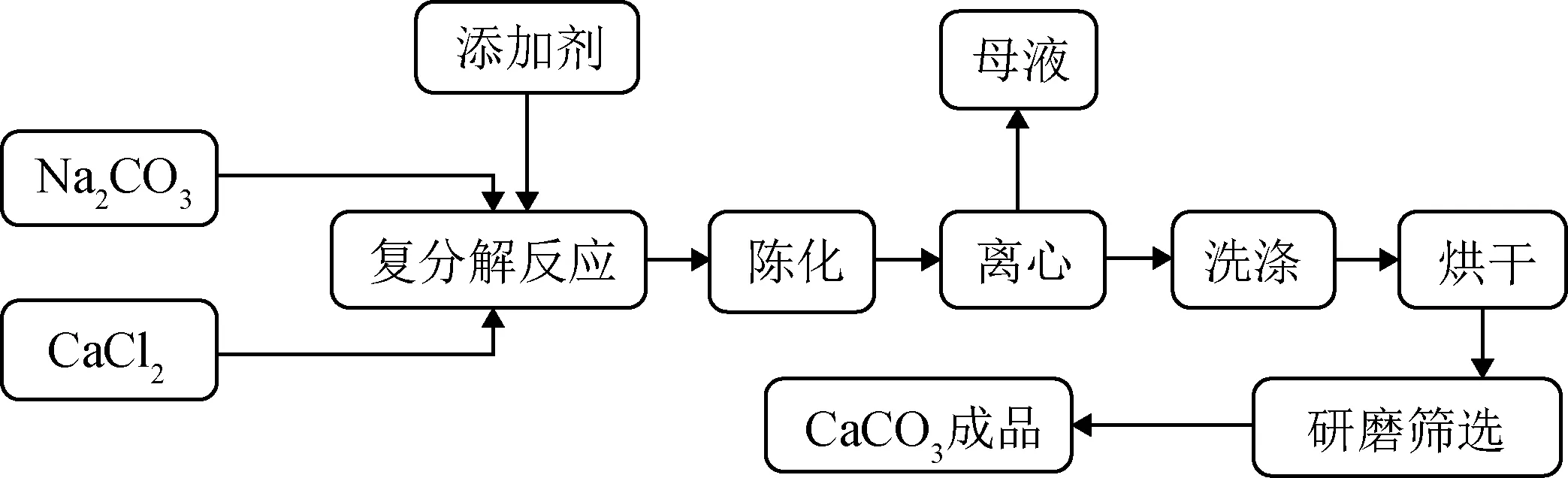
图3 复分解法制备球霰石型碳酸钙的反应流程[37]Fig.3 Reaction process for preparing vaterite-type calcium carbonate by double decomposition method[37]
由于复分解法发生在溶液体系中以及使用过程中通常要加入晶型调控剂,因此复分解法可以按照以下两种分类法细分:按照复分解反应发生的体系种类可分为常规复分解法、溶剂热法、微乳液法、凝胶结晶法;按照加入的晶型调控剂种类可分为模板法、生物矿化合成法和共沉淀法,这三种方法分别对应三类常见的晶型调控剂(高分子聚合物/表面活性剂类、氨基酸/蛋白质等有机大分子类和无机物类)。大量研究表明,复分解法能较好地控制球霰石的晶型和形貌。
2.2.1 按反应发生体系种类分类
常规复分解法是指在水溶液体系中制备球霰石型碳酸钙的方法,主要受制于反应温度和时间、体系pH值、晶型调控剂种类和剂量、搅拌方式等因素[4]。同时,有研究指出通过控制反应条件而不加入添加剂也可以制备高质量的球霰石型碳酸钙。如Mori等[33]在不添加晶型控制剂的前提下,利用K2CO3和CaCl2溶液在室温下进行复分解反应,着重考察了搅拌方式对产品质量的影响,实验表明通过均匀、高剪切和持续的搅拌方式可以制备出纯的球霰石型碳酸钙。当使用双缸式均质器进行搅拌时,制备纯的球霰石需要将两种盐溶液中的一种缓慢加入到另一种之中;当使用超声波均质器时,则需要将一种溶液快速添加到另一种溶液之中。但通常情况下,常规复分解法往往需要通过加入晶型调控剂以优化操作流程和稳定球霰石型碳酸钙的晶型和形貌,这就导致生产成本的增加。
溶剂热法是用有机溶剂代替水,把一种或几种前驱体溶解于有机溶剂中,在液相或超临界条件下制备材料的方法[38]。Li等[9]利用尿素-氯化钙作为原料,在100~150 ℃下,分别用乙二醇、1,2-丙二醇和甘油溶液作为溶剂研究了球霰石型碳酸钙的合成。实验发现,多元醇不仅是球霰石型碳酸钙生成的促进剂,更是稳定剂;同时,温度越高越有利于球霰石型碳酸钙的生成。然而,溶剂热法需要高温高压的反应条件,存在设备要求高、日常维护成本较高、技术难度大、能耗大且反应不便于控制等缺点,因此不适用于合成球霰石型碳酸钙。
将两种互不相溶的溶剂通过表面活性剂的作用产生大量直径为5~100 nm的液滴,从而形成微乳液体系。微乳液可分为正相微乳液(水包油型)和反相微乳液(油包水型),制备球霰石型碳酸钙则常用反相微乳液,将分别溶于相同的两份微乳液中的钙盐和碳酸盐混合,控制反应工艺参数,在乳液中的液滴小区域内发生复分解反应使晶粒成核并生长,然后再与溶剂分离,最终可以得到直径为几纳米至几十纳米、粒径均一、分散性良好、纯度高(90%(质量分数)为球霰石相)的球霰石型碳酸钙颗粒[39-40]。该方法中,表面活性剂对产物有较大影响,Kang等[41]在研究反相微乳液法时发现,表面活性剂十二烷基硫酸钠与水混合比例的提高会使得在微乳液中制备的球霰石型碳酸钙明显向方解石相转化。微乳液法制备球霰石型碳酸钙具有操作简便、产品纯度高、粒径分布均匀、分散性好等优点,有很好的应用前景。但是制备过程中使用了大量有机物,后续在产品的分离、提纯与有机相的回收、循环使用方面都存在一定难度,增加了生产成本。
凝胶结晶法本质上与微乳液法相近,前者是利用有机介质,而后者是利用有机凝胶。凝胶结晶法是将含有CO2-3和Ca2+的高活性组分化合物经过溶解、形成溶胶、脱水之后形成凝胶再固化、热处理等工序制备得到球霰石型碳酸钙的方法[39]。实际工业中要想获得特殊晶型和形貌的碳酸钙,需要在制备过程中加入控制剂,以此实现碳酸钙的形貌与晶型的导向作用。目前关于凝胶结晶法制备球霰石型碳酸钙的研究甚少,这可能与凝胶结晶法本质上存在晶核碰撞不稳定、晶粒生长速度下降、溶液对流和紊乱受到抑制的原因有关,对于制备特定晶型碳酸钙时仍存在众多困难。同时凝胶结晶法的工序十分繁琐复杂,需高温条件处理产品,因此凝胶结晶法暂不具有工业制备球霰石型碳酸钙的潜力。
2.2.2 按晶型调控剂的种类分类
模板法制备球霰石型碳酸钙的基本原理是在溶液中首先形成的无定形碳酸钙会相变成纳米级的球霰石型碳酸钙微粒,然后这些纳米颗粒在适宜模板的表面积聚和包裹形成核壳结构,最后再选用合适的方法(如溶剂溶解、化学反应或高温锻烧)去除模板。因此模板法制备得到的球霰石型碳酸钙多为多孔或中空的微球[4],如图4[4]所示。模板法有软模板法和硬模板法之分,其区别在于所使用的模板剂种类不同,制备球霰石多采用软模板法,而软模板法所用的模板剂多为高分子聚合物/表面活性剂类。研究表明十二烷基苯磺酸钠[42]、油酸[43]、瓜尔胶[44]、聚苯乙烯磺酸钠[45]等都可以作为软模板用于制备球霰石。通常情况下,模板法制备得到的球霰石型碳酸钙粒度均一、结构相对固定,且制备方法简单、制备条件温和。但是模板法的影响因素众多,并且模板剂被包裹在球霰石内部,因此后续去除模板剂难以彻底,导致产品的纯度受到影响,这使模板法的发展受到了一定限制。

图4 实验室制备的球霰石型碳酸钙SEM照片[4]Fig.4 SEM image of vaterite calcium carbonateprepared in the laboratory[4]
生物矿化法也称仿生合成法,是近些年才逐渐发展起来的一种新的合成方法。生物矿化法通常是需要有机基质的参与,通过模拟生物体内的反应,利用有机大分子与无机离子二者之间界面处的静电匹配、几何匹配以及立体化学匹配等物理化学作用,从分子水平上实现无机矿物的调控制备[46]。生物矿化法主要采用氨基酸/蛋白质等有机大分子作为有机基质,但是形式上与模板法十分相似,且合成的材料与生物矿物相比也十分相似,因此,生物矿化法与利用高分子化合物(与生物分子性质和结构相似的高分子化合物)作为模板剂的模板法,在研究内容与结论上十分混淆,影响了生物矿化法的发展[46]。目前已发现的能用于球霰石型碳酸钙生物矿化法合成的有机基质有:多肽[47]、精氨酸[48]、甘氨酸[30]、丙氨酸[49]、L-赖氨酸[50]、牛血清白蛋白/可溶性淀粉[51]等。生物矿化法合成的球霰石型碳酸钙纯度高、粒度均匀、制备方法简单,具有应用前景;但是生物矿化法主要是通过添加一些有机基质模拟生物体内的反应制备材料,其效率和产率存在一定的不足;同时生物矿化法是新兴的方法,制备机理及影响机制尚不清楚,仍然需要发展一段时间。
离子促沉淀法指在复分解体系中,适当的加入一些无机添加剂,使得添加剂与CO2-3和Ca2+之间发生作用从而促进球霰石型碳酸钙的生成。如Zn2+、Al3+、PO3-4可以发生吸附、络合、水解等作用促进球霰石型碳酸钙的生产[52-53]。这种方法原理简单、易于操作、成本低,但是制备的颗粒易团聚导致粒径增大且分散不均匀;同时球霰石型碳酸钙具有特殊形貌与结构,会导致部分吸附在其表面或内部的离子难以去除,从而影响该类球霰石型碳酸钙的应用。
迄今为止,复分解法制备球霰石型碳酸钙的研究较多,所得到的产物具有纯度高、粒度均一、分散性好等优点,但是存在生产效率低、生产成本高、反应过程难精确控制等缺点。同时,使用晶型调控剂虽有利于产物的生成和粒级的优化,但是会提高成本、影响纯度。因此复分解法自身的各项缺陷限制了实际应用,也就导致了目前大多数研究只停留于实验室中。
2.3 热分解法
热分解法是一种制备球霰石型碳酸钙的新型方法,主要是指碳酸氢钙通过受热分解,并控制条件制备得到球霰石型碳酸钙。通常情况下,利用碳酸氢钙的饱和水溶液,通过控制分解温度、分解时间、搅拌方式和外加物等达到制备球霰石型碳酸钙的目的[54-55]。Jiang等[55]发现控制分解温度为70 ℃时,可以得到质量含量为37.4%的球霰石型碳酸钙,且分解温度越高,球霰石型碳酸钙的含量越低。Zeng等[56]还发现,在碳酸氢钙热分解过程中加入油酸可以促进球霰石型碳酸钙的生成。另外,采用碳酸氢钙的微乳液体系进行热分解时,可以制备得到海绵状的球霰石型碳酸钙[57]。热分解法的制备原理简单、流程短、设备要求低,但是产物球霰石型碳酸钙的纯度较低,分解所需时间长,以及分解反应难以控制;同时生产过程中需要的温度高,能耗大,难以实际应用。关于此法的国内外研究较少,在理论和实践方面仍需开展大量工作。
3 球霰石型碳酸钙的调控研究进展
大量关于球霰石型碳酸钙的制备研究表明,除了制备方法本身的影响之外,工艺参数以及所加入晶型调控剂的种类和剂量也起着十分重要的作用。考虑到目前国内外的研究大部分是关于碳化法与复分解法,因此本部分主要针对这两种方法的制备过程中,如何通过调控工艺参数和选择晶型调控剂的种类和剂量来实现球霰石型碳酸钙的调控制备来展开论述。
3.1 工艺条件
3.1.1 碳化法
碳化法制备碳酸钙有Ca(OH)2-H2O-CO2和CaCl2-NH3·H2O-CO2两大体系。前者制备的多为方解石型碳酸钙,不适用于制备球霰石型碳酸钙[26]。因此本文主要阐述CaCl2-NH3·H2O-CO2体系中工艺参数对球霰石型碳酸钙产品的影响,其中主要包括碳化温度与时间、氨水比例、CO2气体浓度与流速、Ca2+浓度等因素。
碳化温度主要影响CO2气体的溶解度,从而影响气体与液体的内部接触时间以及碳化的反应速率;此外CO2气体在水中溶解产生的CO2-3是反应原料之一,会影响晶核成核与成长速度,因此碳化温度能影响碳酸钙产品的形貌和晶型[2]。研究表明,碳化温度越高,能够促进球霰石发生“溶解再结晶”过程向方解石转化,反应温度低有利于球霰石型碳酸钙的生成与稳定[2,29,58]。
通常情况下,CaCl2-NH3·H2O-CO2体系中的NH3·H2O有调节溶液pH值,产生NH+4吸附在碳酸钙某些特殊的晶面并降低表面能,进而稳定该晶面的作用。NH3·H2O的用量越大,溶液的初始pH值越高,且能促进CO2在水中溶解,导致CO2-3浓度增大;当与Ca2+反应生成碳酸钙后,由于Ca2+没有得到及时补充而导致局部CO2-3/Ca2+比例增大,有利于球霰石型碳酸钙的生成[59]。但是研究表明溶液的初始pH值不应高于12,否则生成的碳酸钙晶核小、溶解度大,且晶核易发生“溶解再结晶”过程转变为方解石晶型[29,58]。同时研究也表明溶液的终止pH值在8左右时,制备的球霰石型碳酸钙有较好的质量[2]。
碳化过程中的CO2气体传质经历了气相-气液界面-液相三步过程,因此通入的CO2气体浓度和流速直接影响传质过程的发生。若CO2气体浓度和流速低,则传质推动力小,就导致了溶液中生成的CO2-3浓度小,Ca2+与CO2-3接触机会就会减小,不利于球霰石型碳酸钙的生成[2,60]。因此较高的气流速率和气体浓度不仅可以缩短碳化反应所需要的时间,还可以抑制相变以制备较高纯度的球形球霰石型碳酸钙[4,61]。
由于球霰石型碳酸钙具有热力学不稳定性,在水溶液中球霰石转变为方解石所需的时间通常为几分钟到几个小时[62-63]。随着反应时间的延长,方解石会越来越多,所以在水溶液体系中制备球霰石型碳酸钙产品时,碳化时间越短越好。
Ca2+浓度的大小直接影响着与溶液中CO2-3的结合情况,Ca2+浓度高,相对来说CO2-3/Ca2+比例减小,不利于球霰石型碳酸钙的生成。因此采用较低浓度的Ca2+溶液有利于球霰石型碳酸钙的生成[2]。
3.1.2 复分解法
复分解法制备球霰石型碳酸钙通常都要加入晶型调控剂,因此大多数的工艺参数条件,如晶型调控剂用量、反应温度、溶液pH值等都与晶型调控剂的种类有关。此外,溶液的搅拌混合速率、反应时间、溶液饱和度等因素对产物质量的影响也具有一定规律。
搅拌混合速率是复分解法制备球霰石型碳酸钙的一个重要因素[64],搅拌强度会影响碳酸钙的成核活化能[30];研究表明复分解法采用均匀、高剪切和持续的搅拌能够得到较好的纯球霰石型碳酸钙颗粒[38]。此外,超声波可以为反应系统提供大量能量,从而产生机械和热效应并促进传质,因此超声搅拌有较好效果,且与普通机械搅拌相比,球霰石型碳酸钙的产物浓度更高[62]。反应时间影响与碳化法的影响是一样的,都表现为反应时间越短越有利于球霰石型碳酸钙的生成。
除上述原因外,复分解反应体系的溶液过饱和度也是重要影响因素。溶液过饱和度S的大小直接影响着溶液中溶质的量。复分解反应制备碳酸钙制备中,溶液过饱和度S的定义公式如下:
S=(αCa2++αCO2-3Ksp)1/2
式中:αCa2+和αCO2-3分别是钙离子和碳酸根离子的活度;Ksp为碳酸钙的溶解度积[14]。在复分解体系中,球霰石型碳酸钙的微颗粒在室温下可以从S<6.5水溶液中沉淀出来,且过饱和度还会影响所形成的碳酸钙颗粒的微晶尺寸等[14,47,64]。因此通过加入添加剂或其他手段改变复分解体系的饱和度可调控球霰石型碳酸钙的生成。
3.2 晶型调控剂
无论是碳化法还是复分解法,在制备球霰石型碳酸钙时加入晶型调控剂,都能得到质量较好的产品。通常情况下,晶型调控剂在溶液中主要是通过以下两方面来稳定生成的球霰石型碳酸钙:一是通过与离子或分子之间的相互作用,改变反应体系的界面性质,降低反应前体的浓度从而降低碳酸钙的成核热力学驱动力;二是晶型调控剂吸附在球霰石型碳酸钙所特有的晶面上,形成位阻以抑制或延迟该晶面发生成核或进一步向稳定晶型的转变[65-66]。晶型调控剂的种类繁多,其中最常用的有氨基酸类、有机酸类、醇类、高分子聚合物类、阴离子表面活性剂等,每一类晶型调控剂的作用机理都不一样。
氨基酸类晶型调控剂(苯丙氨酸、天冬氨酸、亮氨酸等)可以有效促进球霰石相的形成和稳定[32,50]。其机理是C=O键的负电荷会向O原子移动并形成强电场,该电场对Ca2+存在强烈的吸引作用,依靠该静电作用而临时固定在C=O基团附近的Ca2+引发了球霰石型碳酸钙的临界晶核形成;同时有生物实验研究表明,酰胺基能通过N—H—O键与球霰石型碳酸钙的表面形成紧密结合以保持其稳定[66]。此外,也有学者认为氨基酸与有机酸类能促进球霰石型碳酸钙的生成与稳定都是与极性基团羧基有关。他们认为在溶液中存在Ca2+与羧基之间的配位和静电作用和Ca2+与CO2-3的沉淀作用。该两种作用竞争发生,其中前者带负电的羧酸根基团可以和某些特殊的晶面间存在界面分子识别作用,为碳酸钙晶体提供结晶位置,即诱导局部Ca2+浓度增大,同时进一步吸引CO2-3,提高局部过饱和度,促进晶体的成核和异相成核结晶,共同为球霰石的生成提供条件[32]。
醇类晶型控制剂的主要作用机理在于羟基基团(—OH),—OH能形成强电场以吸引晶核改变球霰石型碳酸钙的表面能并使得其在热力学上比其他两种晶型更稳定[9]。有研究表明,醇溶液体系中的球霰石型碳酸钙比水溶液体系中更稳定,存在时间更长。醇类有一元醇和多元醇两类,前者只有乙醇胺能得到纯球霰石型碳酸钙[9,67],而后者都可以促进纯球霰石型碳酸钙的生成[9,68]。
高分子聚合物类晶型调控剂的调控机理多与其组成的单体有关。如聚乙烯醇(polyvinyl alcohol, PVA)是一种含有多羟基的聚合物,可以通过多羟基分子改变结晶过程动力学,加入PVA能促使动力学控制占据主要优势,减缓球霰石型碳酸钙向其他晶型的转变。聚乙烯吡咯烷酮(polyvinyl pyrrolidone, PVP)高分子链中含有大量的C=O基团,C=O基团中的O能够吸引溶液中的Ca2+,这与氨基酸中的作用机理相似,因此能促进球霰石型碳酸钙的形成。
阴离子表面活性剂类调控剂主要依靠阴离子基团和Ca2+之间的相互作用。如十二烷基苯磺酸钠(SDBS)的十二烷基苯磺酸根与Ca2+之间存在较强的静电作用,能够形成较强的Ca—O键,抑制某些特定晶面的生长,利于高效形成球霰石;且浓度越大,抑制效果越明显[42]。此外,阴离子表面活性剂的临界胶束浓度也对产品有着较大影响,如SDBS在达到临界胶束浓度时,开始形成大量的球形胶束,能作为球形模板提供有机/无机界面,使得碳酸钙的晶核能够更容易吸附在胶束上;在此基础上,再利用阴离子基团与Ca2+之间的相互作用,生成质量较好的球霰石型碳酸钙[42]。
4 结语与展望
球霰石型碳酸钙具有独特的物理、化学、生物和机械等特性,在日用、生物医药和新材料等领域极具应用前景。但是球霰石型碳酸钙在制备与处理过程中易向稳定晶型发生转变,尽管近些年来,关于球霰石型碳酸钙的调控制备方法层出不穷,但是这些方法主要在实验室研究中得到了应用,工业化稳定制备仍然没有实现。
在现有诸多方法中,除去热分解法产品纯度低不适于工业化制备外,复分解法和碳化法均具有实际工业应用前景。复分解法虽然能够制备出高纯度、高质量的球霰石型碳酸钙,但是生产成本高、生产效率低、反应过程难精确控制等缺点限制了其工业应用。碳化法设备简单、成本低廉,而且已经在实际工业中用于制备碳酸钙产品,因此其制备球霰石型碳酸钙也更具应用前景,相关的工业应用研究也值得更进一步深入。同时,采用晶型调控剂,将有助于球霰石型碳酸钙的生产以及流程的简化,但是不同药剂的作用机理和使用条件都不相同,因此需要多方考虑择优选择;而且添加晶型调控剂不仅会增加额外成本,也可能会导致球霰石型碳酸钙由于药剂的残留而纯度降低。
综上所述,本文对球霰石型碳酸钙的制备方法进行了全面的综述,并将调控方法和调控剂进行了分类,详细讨论了它们的机理、优缺点及典型实例。结合相关理论,寻找一种新型、便捷、工艺简单易调控的碳化法来制备球霰石型碳酸钙是实现球霰石型碳酸钙工业生产的重点研究方向。

