棒状MgO催化草酸二甲酯酯交换法合成草酸二乙酯的研究
陈芳菊,冯 俊,李 进,李红力,魏 忠,,宋晓玲,,王自庆,
(1.石河子大学 化学化工学院 兵团绿色化工过程重点实验室,新疆 石河子 832000;2.新疆天业(集团)有限公司,新疆 石河子 832000)
近年来,随着煤化工产业的高速发展,合成气经草酸二甲酯(DMO)制乙二醇技术得到快速发展。截至2020年,国内煤制DMO产能已经达到了2×107吨/年,但目前石油价格低,与环氧乙烷路线相比在成本上缺乏竞争力,大大削弱了煤制乙二醇技术的盈利能力[6-7]。因此,以DMO为平台化合物设计高附加值下游产品的合成工艺成为煤化工低碳化发展领域的研究热点之一。万思玉等[8]采用实验和计算相结合的方法,对乙醇和DMO经酯交换法合成DEO工艺过程的可行性进行了系统研究,反应过程如图1所示。研究发现,该反应在80 °C条件下DEO的收率可以达到85%,并提出酯交换法是DEO高效绿色合成的一种新工艺。针对该工艺,研究者围绕高效催化剂的开发开展了大量卓有成效的工作,其中在碳酸钾和甲醇钠等均相碱催化体系中,DEO的最大收率可以达到52.7%[9-10]。尽管均相碱催化在温和条件下即可表现出优异催化活性,但催化剂残留会降低产品品质。针对均相催化剂难分离问题,石磊课题组[11]将MgO-Al2O3-Fe2O3复合氧化物负载在碱金属毒化的Y型介孔分子筛表面,获得了一系列适用于酯交换法合成DEO的高活性催化剂,其中在最优条件下,10%MgO-5%Al2O3-8% Fe2O3/Na-meso-Y(10%、5%和8%分别代表物质占催化剂的质量分数)催化体系中DMO最大转化率和DEO最高选择性分别可以达到97%和82%。
尽管研究者在DMO和乙醇酯交换的高效多相催化剂开发方面取得了一定成果,但是目前报道的催化体系成分复杂,制备过程繁琐。另外,固体催化体系中酯交换法合成DEO的构效关系和反应机理还尚不明确。为此,本文采用共沉淀法制备了一种棒状MgO作为催化剂用于催化DMO和乙醇酯交换合成DEO反应,使用XRD、BET、SEM和CO2-TPD等表征方式探究催化剂的结构和性能,并与活性相关联,以期揭示固体催化剂的构效关系,并尝试提出MgO-P表面DMO和乙醇酯交换反应机理。
1 实验部分
1.1 实验材料与试剂
草酸二甲酯(DMO)、Na2CO3、Al(NO3)3·9H2O和CH3ONa均为分析纯,购自中国上海阿拉丁试剂公司;Mg(NO3)2·6H2O购自天津市福晨化学试剂厂;乙醇(AR,98%)购自天津市盛奥化学试剂有限公司;CaO(≥98%,粉末)和SiO2(≥98%,粉末)购自上海麦克林生化科技有限公司;商业轻质MgO粉末(AR,98%)购自福晨(天津)化学试剂有限公司;所有试剂使用时均未进行纯化处理。
1.2 催化剂制备
将9.0 g Mg(NO3)2·6H2O溶于200 mL去离子水配制均匀溶液,在50 °C下将200 mL Na2CO3溶液(0.4 mol/L)迅速倒入Mg(NO3)2溶液中,继续搅拌10 min后将混合物在50 °C水浴中静置陈化1 h。过滤,滤饼依次用去离子水和无水乙醇洗涤2~3次后烘干。最后将其置于马弗炉中,550 °C焙烧3 h得到棒状MgO,记为MgO-P。将Mg(OH)2在550 °C焙烧3 h得到白色固体记为MgO-T;商业轻质MgO记为MgO-C。
1.3 催化剂评价
将一定计量比的DMO和乙醇加入100 mL三口瓶中,其中DMO和乙醇的物质的量之比为1:2~1:14。将温度升高至设定温度,搅拌均匀后加入催化剂,催化剂占DMO的质量分数为0.5%~6.0%。在50~110 °C下反应0.5~5.0 h后停止反应。采用配有毛细管柱和FID的GC-2014型气相色谱仪对产物的组成进行定量分析。以四氢呋喃(THF)为内标物,通过内标法计算DMO转化率(XDMO,%)和DEO选择性(SDEO,%),计算公式如下:
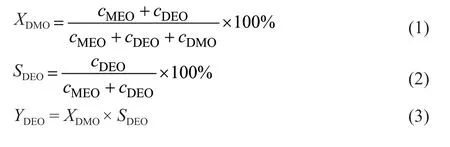
式中,YDEO为DEO的收率,%;cDMO、cDEO和cMEO分别代表产物中DMO、DEO和草酸甲乙酯(MEO)的浓度,mol/L。
在荷里路德宫的一个角落,还有一间不易被发现、专门供小朋友玩耍的房间。这里备有很多王子或公主的道具服装,可以穿着照相,小朋友还可以在这里做手工,无论是绘画、涂色还是连线游戏,主题都与这座宫殿相关。
1.4 催化剂表征
采用日本理学公司的Rigaku Ultimate IV型X射线衍射仪测试催化剂的XRD,Cu Kɑ射线,工作电压40 kV,工作电流45 mA,扫描速率10 (°)/min,扫描范围10°~90°。采用谢乐公式计算催化剂的晶粒尺寸。
N2吸/脱附在Asap 2460型全自动快速比表面积与孔隙度分析仪上完成,比表面积通过BET公式计算,用BJH公式计算平均孔径。
催化剂形貌观察在日本日立公司的SU 8010型场发射扫描电子显微镜上完成。
CO2程序升温脱附(CO2-TPD)在Auto Chem 2910型全自动化学吸附仪上进行。将一定质量催化剂样品置于U型石英管中,在He气氛中500 °C条件下吹扫90 min,降至室温后恒温条件下吸附CO2(30 mL/min)60 min。而后以25 mL/min的He吹扫,将样品温度由50 °C升高至700 °C,用TCD检测器记录催化剂表面的CO2脱附情况。为了保证不同样品的CO2-TPD的区分度更为显著,测试时称量MgO样品的质量为100.0 mg,而CaO和SiO2的质量为50.0 mg。
2 结果与讨论
2.1 催化剂表征
图2为MgO催化剂的XRD谱图,不同催化剂的晶粒尺寸列于表1中。由图2可知,采用不同方法制备的催化剂均在36°、42°、62°和78°出现了MgO的特征衍射峰,说明两种方法均可获得纯相MgO。从衍射峰强度来看,MgO-T和MgO-C衍射峰的强度明显大于MgO-P,结合表1中晶粒尺寸的变化,说明高温焙烧增大了MgO-T和MgO-C的晶粒尺寸。

图2 不同方法制备的MgO催化剂的XRD谱图Fig.2 XRD patterns of MgO catalysts prepared by different methods

表1 不同固体催化剂的织构性质和晶粒尺寸Table 1 Texture properties and pore diameter of different solid catalysts
为获得不同固体催化剂的织构性质,采用N2低温物理吸附技术对不同催化剂进行了测试,结果也列于表1中。可以看出,不同氧化物的比表面积按照SiO2>MgO-P>MgO-C>MgO-T>CaO的顺序递减;总孔孔容的变化趋势与比表面积基本一致。
图3为不同MgO催化剂的SEM照片。由图3可知,MgO-P呈棒状,该催化剂的平均直径约为2 μm,而MgO-T和MgO-C则为不规则的颗粒结构。

图3 不同方法制备的MgO催化剂的SEM照片Fig.3 SEM images of MgO catalysts prepared by different methods
酯交换反应为经典的碱催化反应过程,催化剂表面碱性位数量和强度是影响催化活性的主要因素[12]。因此采用CO2-TPD对不同固体催化剂进行了分析,结果如图4。根据文献[13-14]研究结论,CO2-TPD曲线中低于150 °C、150~450 °C和大于450 °C范围内的CO2脱附峰,分别归因于弱、中强和强碱性位吸附的CO2脱附。弱碱性位与固体氧化物表面羟基浓度有关,而中强碱性位和强碱性则分别是由氧化物表面M2+—O2-和O2-产生的。由图4可知,MgO表面的碱性位为中等强度,而CaO和SiO2表面的碱性位则分别为强碱性和弱碱性,并且MgO-P的碱性位点数量大于MgO-T和MgO-C。
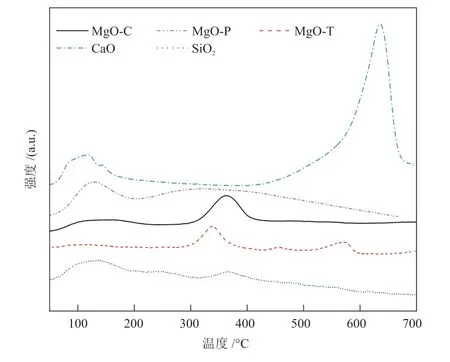
图4 不同固体催化剂的CO2-TPD谱图Fig.4 CO2-TPD spectra of different solid catalysts
2.2 催化剂活性分析
2.2.1 催化剂的筛选
表2列出了不同固体催化剂表面DMO和乙醇酯交换合成DEO的催化性能(评价条件:催化剂占DMO质量分数为1.0%,DMO和乙醇的物质的量之比为1:6,反应温度70 °C,反应时间2.0 h),同时,为了探究MgO-P的活性优势,表2中还列出了酯交换均相碱催化剂(Na2CO3、K2CO3、KOH和CH3ONa)的催化效果。
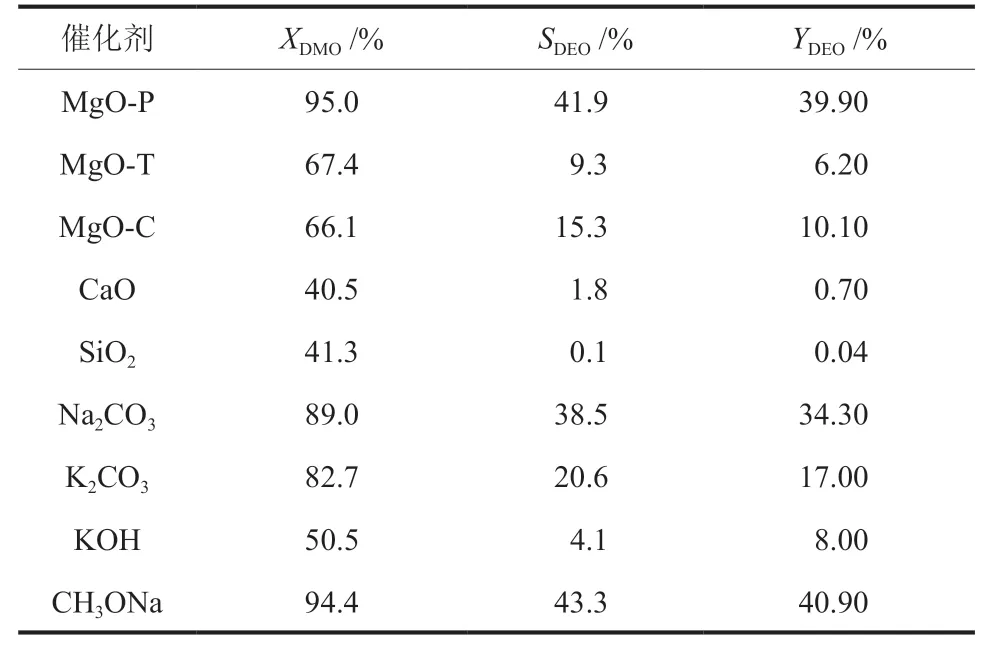
表2 不同催化剂在DMO酯交换合成DEO反应中的催化性能Table 2 Catalytic performance of different catalysts in DMO transesterification to DEO
相同条件下,MgO在酯交换法合成DEO反应中的催化性能明显优于CaO和SiO2,且表面含有最高中等强度碱性位的MgO-P表现出最高催化活性,说明中等强度碱性位是DMO和乙醇酯交换反应的活性位。另外,从表2还可以看出,MgO-P催化体系中DEO的收率与Na2CO3和CH3ONa等均相催化体系相当。因此,本文选用MgO-P作为酯交换反应催化剂,对反应条件进行了优化。
2.2.2 反应条件的优化
在DMO和乙醇的物质的量之比为1:6、反应温度70 °C条件下反应2.0 h,考察了催化剂(MgO-P)占DMO的质量分数对反应活性的影响,结果如图5(a)所示,当MgO-P占DMO的0.5%(质量分数)增至2.0%时,DMO转化率和DEO选择性分别由62.4%和11.5%快速增加到96.3%和47.0%,继续增加催化剂浓度,DMO转化率和DEO选择性均不再发生变化。因此,选择2.0%作为催化剂的最佳质量分数。
当MgO-P占DMO的2.0%、70 °C条件下反应2.0 h后,DMO和乙醇的物质的量之比对酯交换反应性能影响如图5(b)所示。当DMO和乙醇的物质的量之比由1:2增加到1:10时,DMO转化率和DEO选择性由75.3%和39.5%快速增加到96.9%和54.6%,这是由于提高反应物用量促进化学平衡正向移动所导致;继续增加乙醇用量,DEO选择性无明显变化,乙醇用量过高对催化剂产生的稀释作用,降低了DEO选择性[15]。
当MgO-P占DMO的2.0%、DMO和乙醇的物质的量之比1:10、反应2.0 h后,反应温度与DMO转化率和DEO选择性关系如图5(c)所示。当反应温度由50 °C升高到70 °C时,DMO转化率和DEO选择性分别由88.9%和17.3%快速上升到96.7%和55.4%。根据文献[8],由DMO经酯交换反应生成DEO过程为连续反应,DMO先与乙醇通过酯交换反应生成MEO,MEO再经酯交换或歧化反应后生成DEO。在上述反应过程中,第一步酯交换反应为吸热反应,而第二步则为放热反应,总的反应过程表现为放热反应。从热力学角度来说,对于放热反应,升高反应温度不利于化学平衡向正方向移动;但是从动力学角度来看,温度升高可以提高催化剂与反应物碰撞的频率,对反应速率提高产生有利影响[16]。由图5(c)可知,当温度超过70 °C以后,DEO选择性开始降低,主要是高温导致歧化生成DEO的化学平衡向左移动所致。因此,综合考虑温度对反应热力学和动力学影响,选择70 °C为MgO-P的最佳反应温度。
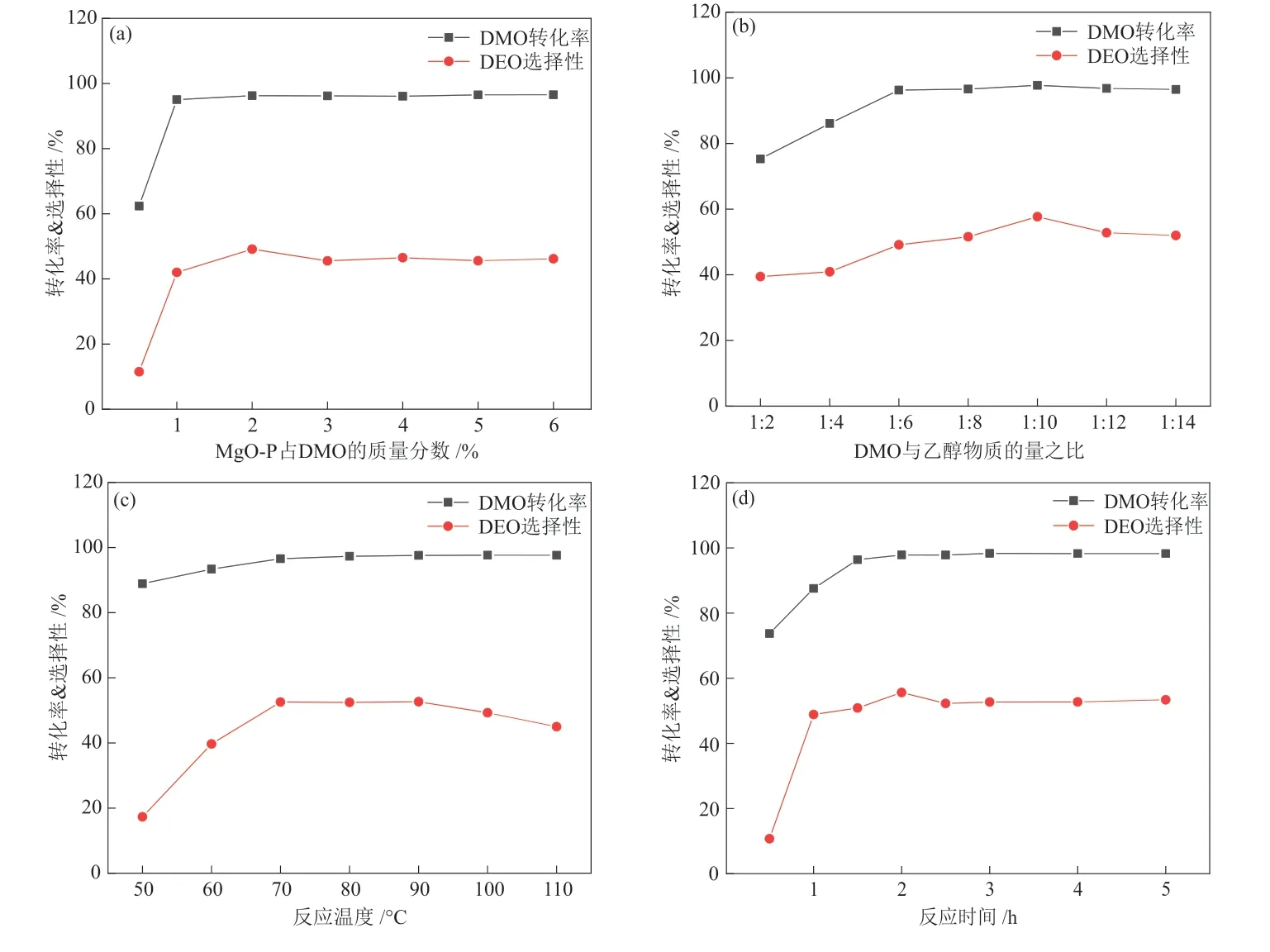
图5 MgO-P占DMO的质量分数(a)、DMO和乙醇的物质的量之比(b)、反应温度(c)和反应时间(d)对DMO转化率和DEO选择性的影响Fig.5 Effect of mass fraction of MgO-P in DMO (a),molar ratio of DMO and ethanol (b),reaction temperature (c) and reaction time (d) on DMO conversion and DEO selectivity
当MgO-P占DMO的2.0%、DMO和乙醇的物质的量之比为1:10、反应温度为70 °C时,不同反应时间对应的DMO转化率和DEO选择性如图5(d)所示。当反应时间由0.5 h延长到2.0 h时,DMO转化率和DEO选择性分别由73.7%和10.7%快速上升到97.7%和57.7%;继续延长反应时间,DEO选择性和DMO转化率均无明显变化。综合条件优化结果可知,当MgO-P占DMO的2.0%时,DMO和乙醇的物质的量之比为1:10,在70 °C反应2.0 h获得DMO转化率和DEO选择性最高,分别可达97.7%和57.7%。
2.3 催化剂重复使用性能
在最优条件下,考察了MgO-P在酯交换法合成DEO反应中的循环使用性能,结果如图6所示。
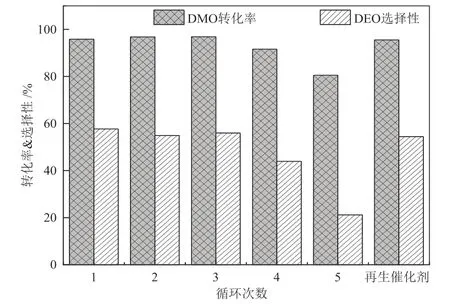
图6 MgO-P重复使用性能Fig.6 Reusability performance of MgO-P
使用后通过简单过滤获得使用后的催化剂,以乙醇多次洗涤后烘干再使用。由图6可知,MgO-P在前3次循环过程中,DMO转化率和DEO选择性几乎没有变化,而在之后的两次循环中,DMO转化率和DEO选择性分别由95.8%和56.0%降低到80.5%和21.2%。图7为反应前后MgO-P的XRD谱图,可以看到重复使用5次后的MgO-P中有明显的Mg(OH)2衍射峰出现,这是由于在重复使用过程中,MgO与物料或环境中的水发生了反应,生成的Mg(OH)2覆盖了MgO-P表面活性位,导致催化剂活性降低。为验证以上假设,将重复使用5次后的MgO-P置于500 °C条件下焙烧2.0 h,进行了XRD分析。由图7可知,再生后催化剂的物相与新制催化剂一致,且再生催化剂活性也可以恢复到新制催化剂水平(见图6)。

图7 反应前/后和再生后MgO-P的XRD谱图Fig.7 XRD patterns of MgO-P before/after reaction and regeneration
2.4 构效关系分析
为了进一步验证中等强度碱性位在酯交换法合成DEO反应中的催化性能,按照文献[17-18]中的方法,将一定计量比的Al(NO3)3溶液浸渍到MgO表面,而后在N2气氛中500 °C条件下焙烧5 h获得一系列不同Al含量的x%Al-MgO催化剂(x为Al占催化剂的质量分数,x=0、1、10、20、30)。考察了Al含量对MgO-P中等强度碱性位数量和催化活性的影响,结果如图8所示。由图8(a)可知,随着Al含量的增加,MgO-P表面中等强度碱性位数量逐渐降低;由图8(b)则可知,DEO收率和中等强度碱性位数量之间存在线性关系,进一步证明MgO表面Mg2+—O2-产生的中强碱性位是DMO酯交换合成DEO的活性位。

图8 不同Al含量MgO-P的CO2-TPD (a)和中强碱性位数量与DEO收率的关系(b)Fig.8 CO2-TPD diagram of MgO-P with different Al contents (a) and relationship between number of medium strength basic sites and DEO yield (b)
参考文献[12,17,19-20]和以上实验结果,本文提出了MgO-P表面DMO和乙醇酯交换合成DEO的反应机理,如图9所示。

图9 MgO-P催化DMO和乙醇酯交换反应合成DEO机理Fig.9 Mechanism of synthesis of DEO by transesterification of DMO and ethanol over MgO-P
乙醇羟基的氢原子被MgO表面的碱性位极化,同时Mg2+活化羰基上的氧原子,乙醇形成的乙氧基阴离子进攻DMO的一个羰基碳,生成MEO,同时甲氧基阴离子离去生成一分子甲醇;接下来,活化乙醇的羟基进攻MEO另一个羰基碳,生成DEO和另一分子甲醇,完成整个酯交换反应循环。
3 结论
本文采用共沉淀法制备了一种棒状MgO,探究了其在DMO和乙醇酯交换法合成DEO反应中的催化性能,考察了反应条件对DMO转化率和DEO选择性的影响。通过XRD、BET、SEM和CO2-TPD等技术表征催化剂结构,系统讨论了催化剂结构与反应性能间的构效关系,并据此提出了MgO-P表面DMO和乙醇经酯交换反应生成DEO的反应机理,得到以下主要结论。
(1)与SiO2和CaO相比,采用共沉淀法制备的MgO-P比表面积大,富含丰富的中强碱性位,在DMO和乙醇酯交换反应中的催化活性最优。
(2)在最优反应条件下,MgO-P表面DMO的最大转化率和DEO的最大选择性,分别可达到97.7%和57.7%;重复使用5次后,由于Mg(OH)2的生成,DMO转化率和DEO选择性分别降低至80.5%和21.2%。
(3)通过Al(NO3)3溶液浸渍MgO制备了一系列中强碱性位数量不同的Al-MgO催化剂,发现中强碱性位和DEO收率之间存在明显的线性关系;并据此提出了MgO-P表面DMO和乙醇酯交换合成DEO的反应机理,即MgO结构中O2-作为碱性位可以极化乙醇分子中羟基氢,生成的乙氧基阴离子可以通过亲核进攻DMO中的羰基碳而引发酯交换反应。

