CoSe2/C复合电催化材料修饰隔膜对高载量锂硫电池性能的影响
韩付超,李福进,陈 良,贺磊义,姜玉南,徐守冬,张 鼎,其 鲁
(1.太原理工大学化学化工学院,太原 030024;2.北京大学化学与分子工程学院,北京 100871)
为了应对当今人类面临的全球气候与能源问题,降低对化石能源的依赖,实现“碳达峰”和“碳中和”已成为全人类的共识,使人们对高效储能技术的需求愈加迫切[1~5]. 在众多储能体系中,锂硫电池因其理论能量密度(2600 W·h/kg)高及原料成本低廉等特点,引起了广泛关注[6~10]. 锂硫电池的储能过程是基于硫物种在电极表面的溶解-沉积反应,该反应机制在为锂硫电池提供高比容量的同时,由于涉及到复杂的多电子转移过程和多相反应,使电池在实际应用过程中也面临诸多的问题[11~13]. 主要表现为充放电过程中产生的长链聚硫离子(Lithium polysulfides,LiPSs)易溶于电解液,在电场和浓度梯度共同作用下会在正负极之间迁移,产生穿梭效应[14],导致活性物质的不可逆流失,同时会腐蚀锂负极,降低电池的循环寿命,制约了其商业化进程.
对于上述问题,通常的解决方案是在电池中引入对LiPSs同时具有吸附和催化转化能力的电催化材料,目的是在减缓LiPSs在电解液中累积的同时,加速其沉积转化过程. 目前,常见的电催化材料包括过渡金属氧化物[15,16]、硫化物[17~19]、磷化物[20~22]、氮化物[23~25]以及硒化物[26,27]等. 其中,以CoSe2为代表的硒化物因其导电性好,且硒作为硫的同族元素,本身与硫的相互作用较强,引起了关注[28,29].Guo 等[30]制备了一种卵黄壳状多孔碳和CoSe2纳米片组成的复合材料,卵黄壳状结构中核壳之间的空腔,不仅可以作为纳米反应器缓解硫的体积膨胀,还可以将碳壳的限域作用与CoSe2的化学捕获作用相结合,明显提升了电池在较高倍率下的循环稳定性. Zhang等[31]设计了一种氮掺杂的CoSe2,实验结合理论计算表明,氮的引入在加速LiPSs 还原反应的同时,还可以有效促进Li2S 的氧化,电化学测试表明,在贫电解液条件下,电池仍能表现出优异的循环性能. 但通常文献报道的过渡金属基电催化材料在隔膜修饰层中的担载量依然较高,不利于能量密度的提高.
本文以ZIF-67为前驱体,在惰性气氛保护下,碳化后经过硒化处理得到了分散在菱形十二面体碳骨架上的CoSe2纳米颗粒(记为CoSe2/C),将其与更为廉价的碳材料混合后用于隔膜修饰,并在CoSe2/C质量分数较低的面载量下,对组装的锂硫电池进行电化学性能测试.
1 实验部分
1.1 试剂与仪器
无水乙醇(分析纯)购自天津市大茂化学试剂厂;甲醇(分析纯)购自天津市申泰化学试剂有限公司;1,3-二氧戊环(DOL,电池级)、乙二醇二甲醚(DME,电池级)、四乙二醇二甲醚(TEGDME,电池级)和锂硫电池电解液[1 mol/L 双三氟甲基磺酸亚胺锂(LiTFSI,电池级)的DOL/DME(体积比为1∶1)溶液,并含质量分数为2%的LiNO3]购自苏州多多化学科技有限公司;乙炔黑(AB,分析纯)、导电碳(Super P,分析纯)和聚偏氟乙烯(PVDF,纯度99%)购自太原力源锂电科技有限公司;硫化锂(Li2S,纯度99.9%)购自阿法埃沙(中国)化学有限公司;Co(NO3)2·6H2O(分析纯)、2-甲基咪唑(分析纯)和高纯硫(纯度99.999%)购自上海阿达玛斯试剂有限公司;硒粉(分析纯,200目)和N-甲基吡咯烷酮(NMP,电子级)购自阿拉丁(中国)试剂有限公司.
EMPYREAN X 射线衍射仪(XRD,CuKα射线源,荷兰PANalytical 公司);Thermo ESCALAB 250Xi X 射线光电子能谱仪(XPS,激发光源为MgKα)和FEI Talos-S 透射电子显微镜(TEM,加速电压200 kV),美国赛默飞公司;Gemini 300 扫描电子显微镜(SEM,工作电压10.0 kV,德国蔡司公司);CT-2001A 型电池测试系统(武汉市蓝电电子股份有限公司);CS3104 型电化学工作站(武汉科思特仪器股份有限公司).
1.2 CoSe2/C的制备
将0.656 g 2-甲基咪唑溶解在50 mL甲醇中,将0.582 g Co(NO3)2·6H2O溶解在50 mL甲醇中,然后将两种溶液混合,于室温下搅拌30 min,静置20 h后离心分离,用甲醇洗涤,然后在60 ℃下干燥12 h,制得ZIF-67.
采用两步高温烧结方法制备CoSe2/C. 将得到的ZIF-67在氩气气氛中以1 ℃/min升温速率,升温至600 ℃并烧结60 min,得到Co/C复合物黑色粉末. 将黑色粉末与硒粉按照质量比1∶1混合均匀,在氩气保护和300 ℃下烧结3 h,得到CoSe2/C. 制备过程见Scheme 1.
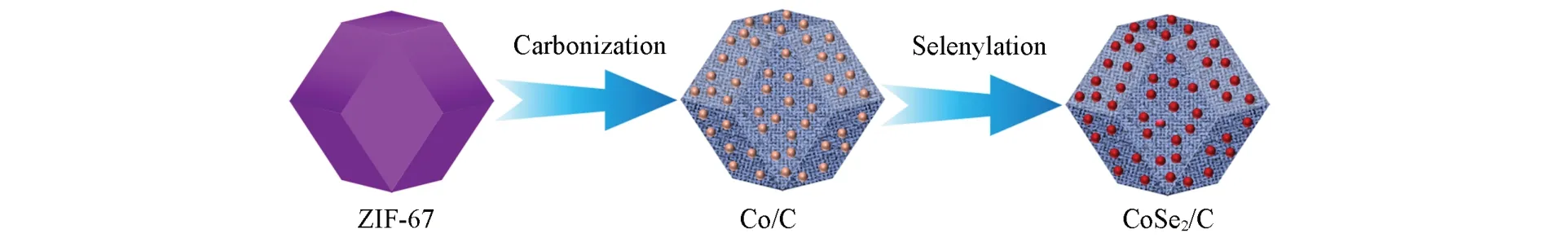
Scheme 1 Schematic illustration of the preparation of CoSe2/C
1.3 CoSe2/C的电化学性能测试
将高纯硫与AB 按质量比7∶3 混合并研磨均匀后,在155 ℃下煅烧12 h 得到碳硫复合物(记为AB@S). 将AB@S,Super P和PVDF按质量比7∶2∶1混合,加适量NMP并进行搅拌. 将得到的均匀浆料涂在铝箔上,在60 ℃下干燥12 h,备用. 将制备的CoSe2/C,Super P和PVDF按质量比3∶6∶1混合,加适量NMP并进行搅拌,再将浆料涂覆于商用Celgard 2400 PP隔膜上,在60 ℃下干燥12 h,将其切成直径为19 mm的圆片,面载量约为0.15 mg/cm2. 作为对照,将Super P与PVDF 按质量比9∶1混合后制成浆料,并对隔膜进行修饰.
扣式电池CR2016 以AB@S 极片为正极,金属锂片为负极,电解液为含有质量分数为2%LiNO3的1 mol/L LiTFSI 的DOL/DME(体积比1∶1)溶液. 电池组装在充满氩气的手套箱(水氧值<1×10-8mol/L)内进行. 电池的充放电测试在Land CT-2001A 测试系统上进行,电压区间为1.7~2.8 V,1.0C=1675 mA/g. 循环伏安(CV)测试在CorrTest CS3104电化学工作站上进行.
1.4 对称电池测试
将CoSe2/C,Super P 和PVDF 按质量比3∶6∶1 混合(将Super P 和PVDF 按质量比9∶1 混合作为对照),涂覆在铝箔上制备电极. 所研究的电极同时作为工作电极和对电极,电解液为含有0.2 mol/L Li2S6和1 mol/L LiTFSI的DOL/DME(体积比1∶1)溶液,电解液体积为50 μL,组装后对其进行CV测试.
1.5 Li2S成核与分解实验
将CoSe2/C,Super P 和PVDF 按质量比3∶6∶1 混合(将Super P 和PVDF 按质量比9∶1 混合作为对照),涂覆在铝箔上制备工作电极. 以制备的工作电极作为正极,锂片为负极,商用Celgard 2400作为隔膜组装电池. 正极一侧电解液为溶解有0.2 mol/L Li2S8和1 mol/L LiTFSI 的TEGDME溶液,负极一侧电解液中不含Li2S8. 对组装电池进行Li2S 成核时,首先在112 μA 恒电流下放电至2.06 V,然后在2.05 V恒电位下放电,记录电流随时间的变化曲线,直到电流降至0.01 μA. 进行Li2S分解测试前,为了保证Li2S沉积完全,先将电池在0.10 mA的电流下恒电流放电至1.70 V,静置60 s后,电池电压会升高,再将其在0.01 mA 的电流下恒电流放电至1.80 V,然后在2.40 V 电压下,对电池进行恒电位充电,并记录其电流变化,直到电流低于0.01 μA.
2 结果与讨论
2.1 CoSe2/C的结构形貌表征

Fig.1 SEM images of ZIF⁃67(A),Co/C(B)and CoSe2/C(C)
由图1(A)的SEM 照片可知,ZIF-67 表面光滑规整,具有菱形十二面体结构. 图1(B)为ZIF-67 经600 ℃高温烧结后得到的Co/C复合材料的SEM照片,图1(C)为CoC和硒粉在氩气保护下300 ℃烧结得到的CoSe2/C复合材料的SEM照片. 可见,相比于ZIF-67前驱体,CoSe2/C复合材料的表面变得粗糙,并附着有纳米颗粒,颗粒在碳骨架上呈均匀分布,尺寸约为30 nm,较小颗粒尺寸能够暴露更多的活性位点,有利于材料对LiPSs的吸附. 如图2(A)所示,通过XRD对CoSe2/C复合材料进行物相鉴定,XRD衍射峰与正交相CoSe2(JCPDS No. 10-0408)一致,同时在20°~25°范围内有一较宽的由ZIF-67高温处理过程中碳化形成的石墨化碳的衍射峰,表明所制备材料是由正交相CoSe2和碳材料复合而成. 通过TEM对材料的形貌进行表征,由图1(C)和图2(B)可知,CoSe2/C复合材料保留了ZIF-67菱形十二面体的几何结构,说明材料在一系列高温处理过程中仍能保持菱形十二面体的结构,具有良好的机械强度和稳定性. 进一步通过高分辨透射电子显微镜(HRTEM)对CoSe2纳米颗粒的结构进行表征,结果如图2(C)所示,晶面间距为0.29 nm,对应于正交相CoSe2的(110)晶面,进一步说明纳米颗粒为正交相CoSe2.

Fig.2 XRD pattern(A),TEM image(B)and HRTEM image(C)of CoSe2/C
通过XPS 可以得到CoSe2/C 的表面结构信息. 从CoSe2/C 的XPS 全谱可见,C,O,N,Co 和Se 元素存在于样品中[图3(A)]. 在Co2p的精细谱[图3(B)]中,778.8和793.8 eV 处的结合能可归属为Co—Se键[32],而780.4和796.1 eV处的结合能则归属于Co—O键[33],Co—O键的形成是由于CoSe2/C暴露在空气中,不可避免地在材料表面形成氧化物薄层[34],伴随着Co信号峰的两个卫星峰表明高氧化态Co的存在,而高氧化态Co的存在能够有效提高材料的催化性能[35,36]. 在Se3d的精细谱[图3(C)]中,54.5和55.3 eV 处的两个峰可归为Se—Co 键[37],59.0和59.8 eV 处的两个峰则可归属为Se—O 键[38],进一步证实了氧化物薄层的形成.

Fig.3 XPS spectra of survey(A),Co2p(B),and Se3d(C)for CoSe2/C
2.2 CoSe2/C的催化动力学
电催化剂对LiPSs 氧化还原反应的催化作用直接影响着电池的性能,因此,采用多种方法揭示了CoSe2/C 对LiPSs 相关转化反应的催化能力. 首先,研究了不同催化剂对液相LiPSs 转化反应的催化能力,以CoSe2/C(或Super P,记为SP)作为对称电池的正负两极,其CV曲线如图4(A)所示,在不含Li2S6的电解液中,电池几乎没有电流响应. 在含有Li2S6的电解液中,CoSe2/C和SP电极的CV曲线均高度对称,其中,CoSe2/C对称电池的CV曲线中存在分别位于-0.11/0.11 V,-0.45/0.45 V和-0.07/0.07 V处的3组氧化还原峰,可分别归属于Li2S6⇌Li2S4,Li2S4⇌Li2S2/Li2S和S8⇌Li2S6的可逆转化反应[39]. SP对称电池的CV曲线电流较低,且未出现多组氧化还原峰,表明CoSe2/C对液相LiPSs之间的转化反应展现出更好的催化能力. 此外,即使在较高的扫描速率下,CoSe2/C对称电池的CV曲线仍保留明显的氧化还原峰(图S1,见本文支持信息),表明即使在高倍率充放电过程中,CoSe2/C仍能提供优异的催化作用.通常认为,液相LiPSs 与固相Li2S2/Li2S 之间的转化是锂硫电池充放电过程的决速步骤[40],故通过计时电流法对Li2S 的沉积和分解过程进行了探究. Li2S 在不同电极表面沉积的计时电流曲线如图4(B)所示,根据法拉第定律计算可知,Li2S在含CoSe2/C的电极上沉积所提供的比容量为77.78 mA·h/g,而在含SP的电极仅提供了55.8 mA·h/g的容量. Li2S沉积曲线的峰值时间(tm,s)与成核反应的速率常数(A,cm-2/s)及生长速率(k,cm/s)存在如下关系[31,41]:
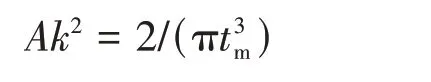
由上式可知,Li2S沉积所对应的峰值时间越早,Li2S的成核和生长的速率越快,也就表明催化剂的引入能够加速液固转化反应的速率. 经计算可得,Li2S在CoSe2/C电极沉积过程的Ak2数值是在SP电极上的2.8倍[图4(C)],表明CoSe2/C的引入能够提高液固转化反应的动力学参数,有效加速了Li2S的成核与生长. 对于固相Li2S 的分解过程,采用相同的电池结构进行测试,首先使Li2S 完全沉积,再将电池在2.40 V下进行恒电压充电,记录电池的电流响应. 如图4(D)所示,相比于SP电极,CoSe2/C电极具有更早的峰值响应时间,而且在分解容量方面,CoSe2/C 电极(126.94 mA·h/g)也高于SP 电极(69.85 mA·h/g),说明CoSe2/C可以有效降低Li2S氧化的过电位,在充电过程中实现Li2S固-液快速转化. 通过以上多种电池结构的测试数据,有力地证明了分布在碳骨架上的CoSe2纳米颗粒,可明显催化LiPSs还原和Li2S氧化反应,降低其电化学势垒,进一步提升电池的电化学性能[42].
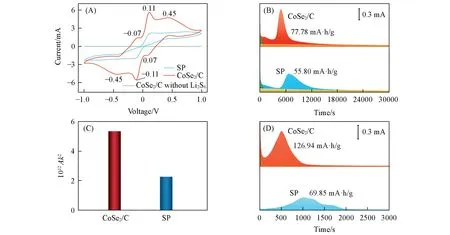
Fig.4 Electrocatalytic performance of CoSe2/C and SP toward various polysulfide involving reactions(A)Cyclic voltammetry curves of Li2S6 symmetric cells;(B)potentiostatic discharge profiles for the nucleation of Li2S;(C)Li2S nucleation and growth value with different electrode;(D)potentiostatic charge profiles for the dissolution of Li2S.
为了进一步评价CoSe2/C 在电池中的催化作用,以AB@S 为正极,锂片为负极,CoSe2/C 或SP 修饰的Celgard 2400为隔膜,组装成扣式电池,首先对其进行了循环伏安测试. 由图5(A)可见,在0.1 mV/s的扫描速率下,含有CoSe2/C与SP隔膜修饰电池的CV曲线相似,还原曲线中2.32和2.03 V处有两个还原峰,分别与S8还原转化为可溶高阶LiPSs 和可溶高阶LiPSs 还原转化为不溶性Li2S2/Li2S 有关. 而在氧化曲线中,在2.31 和2.38 V 处可观察到两个氧化峰,这可能是由于不溶性的Li2S 可逆氧化为可溶高阶LiPSs,进而氧化为S8造成的. 需要指出的是,含CoSe2/C隔膜修饰的电池,其氧化还原峰之间的电压差值(0.28 V)远小于采用SP隔膜修饰的电池(0.31 V),说明CoSe2/C的引入降低了电池的极化作用,进一步证实了其优异的电催化作用. 此外,无论在还原过程还是氧化过程中[图5(B)和(C)],含CoSe2/C隔膜修饰电池的Tafel斜率均低于SP[图5(B)和(C)插图],表明CoSe2/C可以有效地加快LiPSs固-液-固的催化转化动力学.
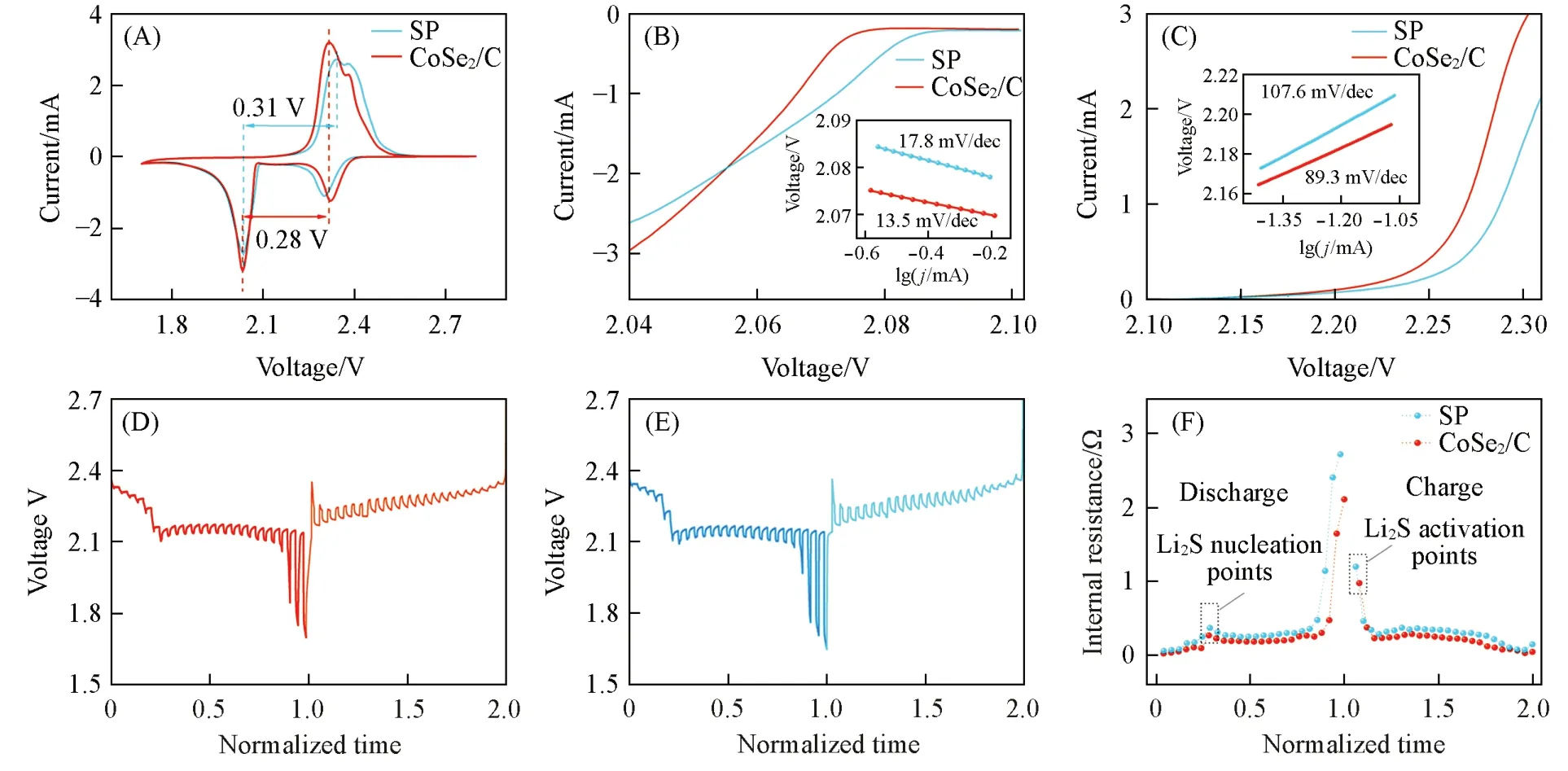
Fig.5 Cyclic voltammertry curves with CoSe2/C and SP modified separators(A),linear sweep voltammetry curves obtained from Fig.5(A)(B, C), GITT potential profiles of cells with CoSe2/C(D) and SP(E)modified separators, resistance of the cells as a function of normalized time of CoSe2/C and SP in lithium sulfur coin cells(F)(B,C)Insets are the corresponding Tafel plots.
为进一步探究CoSe2/C和SP两种电催化剂在电池中的效果,采用恒电流间歇滴定(GITT)技术进行了测量[图5(D)和(E)],可见,在放电至约2.1 V(放电深度约25%)时有固相Li2S形成,对应于Li2S的成核过程[43],此时电池内阻明显增加;在刚开始充电时,由于固相Li2S的存在,此时电池内阻也比后续充电过程要大[44]. 对比两种材料对电池内阻的影响,如图5(F)所示,无论在哪个状态下,CoSe2/C隔膜修饰的电池内阻均小于SP,这有利于电子和离子的传输. 由上述结果可知,CoSe2/C的引入不仅能够加快各类LiPSs相关的多相转化反应,还能够有效降低电池在各个状态下的内阻.

Fig.6 LiPSs permeation test with SP(top) and CoSe2/C(bottom) modified separators of 5 min(A),6 h(B),12 h(C),and 24 h(D)
作为修饰隔膜用的电催化材料,除了要求电催化剂具有优异的催化活性外,还要求其对LiPSs 的扩散具有一定抑制能力,降低穿梭效应的负面影响. 因此,通过渗透实验评价了CoSe2/C和SP修饰的隔膜抑制LiPSs穿梭的能力. 如图6(A)所示,U型管的一端为5 mmol/L Li2S6的DME/DOL(体积比1∶1)溶液,另一端为不含Li2S6的空白溶液,中间则用不同材料修饰的隔膜分开. 观察可知,静置6 h后,SP修饰的隔膜对LiPSs的阻隔能力已显著下降,空白溶液逐渐变色[图6(B)];CoSe2/C修饰的隔膜,即使经过24 h静置,空白溶液仍然没有明显的颜色变化[图6(D)],说明CoSe2/C对LiPSs有较强的阻隔能力和吸附作用. Zhang 等[32]通过对比吸附Li2S4前后CoSe2的XPS 谱图,证实CoSe2与LiPSs 会通过形成Co—S 和Se—S 键提高CoSe2对可溶性LiPSs 的吸附能力,故CoSe2/C 的引入能够有效缓解LiPSs 的穿梭效应,进一步提升电池的电化学性能.
2.3 CoSe2/C的电化学性能
由于CoSe2/C 对LiPSs 相关转化反应优异的催化能力,将其修饰在商用Celgard 2400 隔膜(PP)表面,并组装成扣式电池,通过恒流充放电对其电化学性能进行了评价,作为对比,也用未经修饰的和SP 修饰的隔膜进行了电池组装. 图7(A)给出了不同电池的倍率性能. 可见,在0.2C 的低倍率下,CoSe2/C修饰隔膜的电池展现出1548 mA·h/g的首次放电比容量,硫利用率高达92.5%,远高于商用隔膜(1061 mA·h/g)和SP隔膜修饰(1299 mA·h/g)的电池. 随着倍率的增大,CoSe2/C隔膜修饰的电池与另外两种隔膜的电池之间的性能差距更加明显. 在0.5C,1C,2C和4C的倍率下,CoSe2/C隔膜电池的比容量分别为1207,1068,923 和813 mA·h/g,均高于SP 隔膜(989,848,752 和649 mA·h/g)和PP 隔膜(720,636,585和512 mA·h/g). 当倍率重新回到0.2C 时,CoSe2/C 隔膜修饰的电池可逆比容量仍可达1180 mA·h/g,容量为首次比容量的76.2%. 图7(B)~(D)为不同倍率下不同隔膜电池的恒流充放电曲线,其中CoSe2/C 隔膜修饰的电池在不同倍率下,都显示出两个明显的放电平台,即使在4C 的高倍率下,其放电平台的特征也得到了很好的保持. 需要指出的是,隔膜修饰层的面载量约为0.15 mg/cm2,而其中CoSe2/C的质量分数仅为30%. 对比CoSe2/C和SP隔膜修饰电池的性能可知,少量CoSe2/C的加入即可对电池的倍率性能有明显的提升.
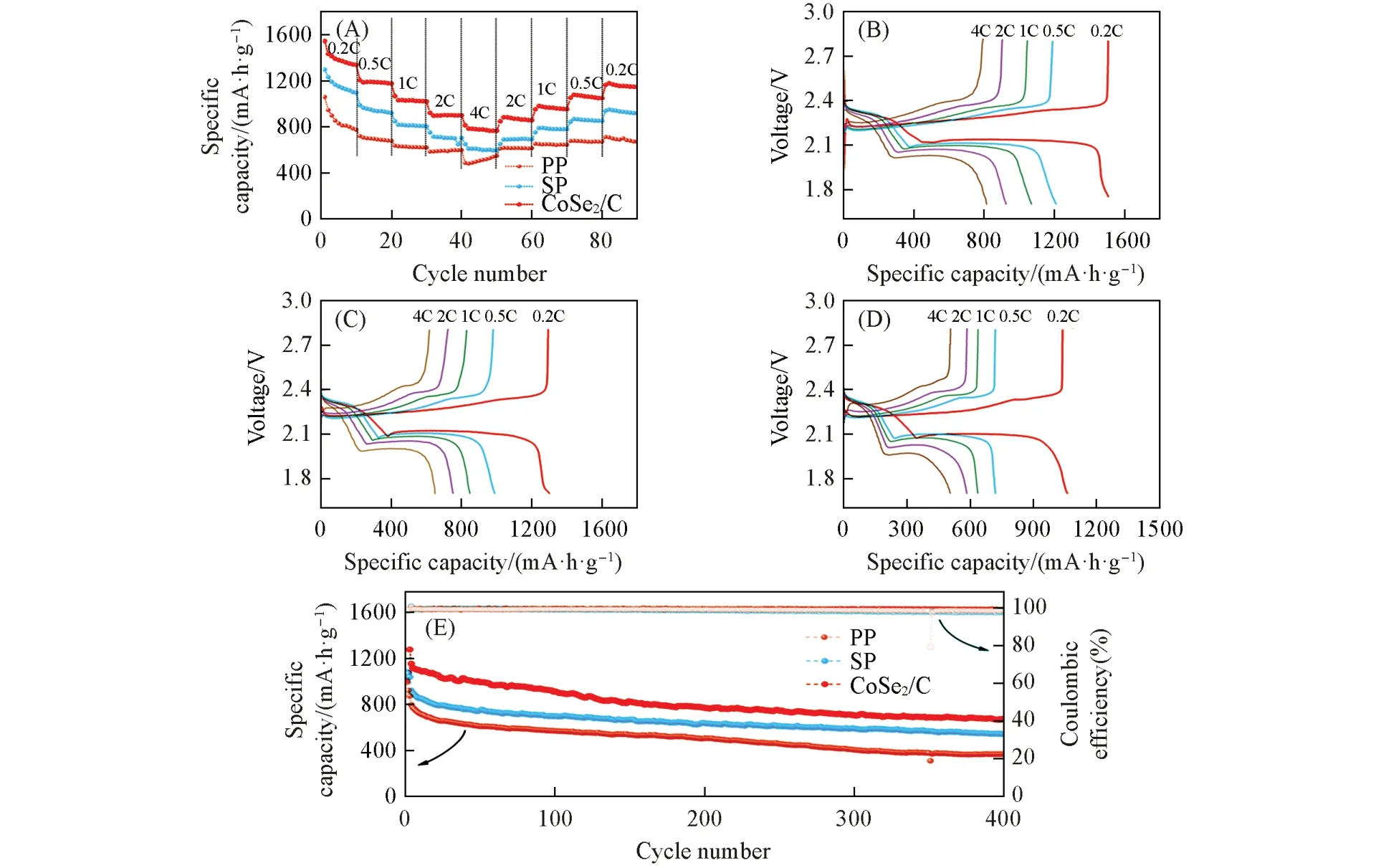
Fig.7 Rate performance of the cells with different separators(A), galvanostatic discharge/charge profiles from 0.2C to 4C for the cells with CoSe2/C modified separators(B),SP modified separators(C),and commercial separators(D)and cycle performance for the cells at 0.5C(E)of the cells with different separators
图7 (E)为不同电池在0.5C倍率下的循环性能,商用隔膜及SP隔膜修饰的电池首次放电比容量分别为872和919 mA·h/g,而CoSe2/C隔膜修饰的电池首次放电比容量可达1153 mA·h/g. 经过400次循环后,商用隔膜和SP 隔膜修饰电池的比容量分别衰减至367 和543 mA·h/g,而引入CoSe2/C 修饰层后,400 次循环后电池容量仍达670 mA·h/g,且库仑效率维持在99%以上,展现出优异的循环性能. 以上结果充分说明,由于CoSe2/C对LiPSs的固-液-固转化反应具有优异的催化能力,及其对LiPSs穿梭效应的阻隔作用,使得电池展现了出色的倍率性能和优异的电化学稳定性.
利用循环伏安法测算了不同隔膜修饰电池中的锂离子扩散系数,以揭示CoSe2/C对锂离子传输动力学的影响. 图S2(A)和(B)(见本文支持信息)分别为CoSe2/C和SP隔膜修饰电池在不同扫描速率下的CV曲线. 可见,随着扫描速率的不断增加,氧化峰和还原峰分别向两侧移动,表明电化学极化增大.将不同氧化还原峰的峰值电流(Ip)对扫描速率的平方根(v0.5)作图,根据经典Randles-Sevcik方程可以计算得到锂离子扩散系数[图S2(C)~(F)],计算结果列于表S1(见本文支持信息),可见,CoSe2/C隔膜修饰的电池在各氧化还原过程中的锂离子扩散系数均高于SP隔膜修饰的电池,进一步证实了CoSe2/C对各氧化还原反应的催化作用,促进了各反应的反应动力学,提高了锂离子的扩散能力.
为了进一步评估CoSe2/C 隔膜修饰后对电池性能的提升,对其进行了高倍率长程循环测试. 如图8(A)所示,在1C 倍率下,电池的首次放电比容量为1080 mA·h/g,经500 次循环后仍有60%的容量保持率,平均每次循环衰减率仅为0.08%. 为了提高电池整体的能量密度,对高硫载量电池进行了测试. 如图8(B)所示,在3.8 mg/cm2的硫载量下,电池首先在0.05C 的低倍率下进行活化,首次放电容量高达1195 mA·h/g,随着倍率的增加,在0.1C,0.2C 和0.5C 的倍率下,电池的比容量分别为1001,823 和613 mA·h/g,当 恢 复 到0.1C倍率时,电池的比容量可以稳定在936 mA·h/g,说明即使在较高的硫载量下,电池仍具有较好的倍率性能. 由图8(C)可见,进一步将硫载量提高至4.8 mg/cm2,在0.2C 倍率下,放电容量为756 mA·h/g,经过180 次循环后,容量依然能够维持在715 mA·h/g,衰减率为0.031%,库仑效率高于97%.
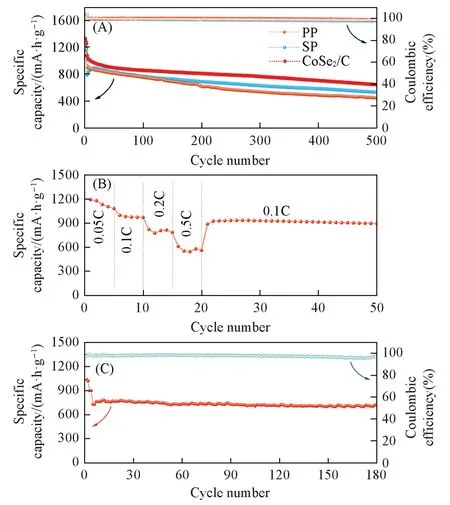
Fig.8 Cycle performance at high rate of 1C(A),rate performance of cells with a high sulfur loading of 3.8 mg/cm2(B),cycle perfor⁃mance of cells with a high sulfur loading of 4.8 mg/cm2 at 0.2C(C)of the cells with CoSe2/C modified separators
3 结论
以ZIF-67为前驱体,通过分步热处理方法,得到了分散在菱形十二面体碳骨架上的CoSe2纳米颗粒(CoSe2/C). 均匀分散的CoSe2纳米颗粒可以提供大量的催化活性位点,有利于其对LiPSs的吸附;电化学测试结果表明,CoSe2对LiPSs相关的各个氧化还原反应均具有优异的催化能力. 将CoSe2/C在较低面载量下,应用于隔膜修饰并组装为锂硫电池,其展示了优异的循环和倍率性能.
支持信息见http://www.cjcu.jlu.edu.cn/CN/10.7503/20220163.

