甲状腺影像检查的人工智能应用进展
邱永康,陈钊,杨琦,康磊
北京大学第一医院核医学科,北京 100034;*通信作者 康磊 kanglei@bjmu.edu.cn
甲状腺疾病的发病率近年不断升高。甲状腺功能异常已经成为第二常见的内分泌疾病,我国约4 000万人被诊断为甲状腺功能减退症,甲状腺功能亢进症患者超过1 000万人,甲状腺癌的发病率在过去几十年内也稳步上升。我国甲状腺癌占新发恶性肿瘤的4.8%,高于世界平均水平(3%)[1]。甲状腺疾病,尤其是甲状腺癌的诊断目前主要依赖超声、CT和核医学等影像检查以及病理学检查。然而,超声医师的诊断能力以及细胞病理学诊断的不确定性等因素制约着甲状腺疾病的诊断准确度和效率[2]。
人工智能是一门能够模拟与延伸人的智能、方法与技术的技术科学。常规影像学检查方法不易通过肉眼观察量化,而人工智能可以提取和量化关键的图像信息,从而使图像诊断从主观的定性任务转变为客观的定量分析。本文对近年基于影像学资料的人工智能技术辅助诊断甲状腺疾病的相关研究进行综述。
1 人工智能技术在医学影像中的应用
20世纪60年代,有学者尝试使用计算机分析医学图像[3]。随着技术的发展,计算机辅助诊断系统(computer aided diagnosis system,CAD)利用人工智能技术分析医学影像图像特征,从而检测病变或做出诊断,为临床医师提供第二诊断意见,以提高诊断效率和准确性[4]。人工智能包括传统的符号人工智能和以机器学习为核心的数字人工智能,目前的研究热点深度学习是机器学习的一个分支。
1.1 深度学习 深度学习是人工智能的重要方法,是随着人工神经网络的发展而兴起的一类新的机器学习方法,可以适用于图像分类、图像分割、病灶检测等多种任务。人工神经网络能够使用多层计算模拟人类大脑解释信息,并从信息中得出结论,而深度学习通过排列在层中的神经元,逐渐从输入数据(如甲状腺超声图像)中提取更高级别的特征。与基于人类专家提取特征的传统机器学习方法不同,深度学习能够自动学习输入信息的特征,并从原始数据中积累经验,自动从影像中提取并筛选出更多、更深层次、更适应研究任务的特征,在模拟非线性关系方面具有优越的性能[5-6]。得益于硬件设备、学习算法和大型数据库的快速发展,深度学习是目前最成功的人工智能方法之一。
1.2 卷积神经网络(convolutional neural networks,CNN)及常用模型 CNN是深度学习的一种结构,也是人工神经网络的一个子类别,能够保留二维数据中的空间关系,常应用于图像识别和计算机视觉应用,能够高效执行医学成像任务[7]。典型的CNN结构由一系列层组成,①卷积层:CNN的主要组成部分,由可训练的滤波器组成;②池化层:在卷积层之后,逐步缩小特征张量维度,并控制过拟合;③全连接层:将CNN在训练中获取的特征映射到样本标记空间,起到分类器的作用。CNN的多个处理层使其能够具有学习医学影像的层次和抽象特征的能力[8]。
自诞生以来,医学影像常用的CNN模型随临床需求不断改进发展。1994年,LeNet5模型的出现标志着CNN正式问世。但LeNet5模型深度较浅,网络结构较为简单,训练过程中容易出现过拟合显像,其图像特征提取能力和训练速度也较为一般。因此,目前的研究通常采用基于CNN的改进模型。
由LeNet5模型改进而来的AlexNet、VGGNet、GoogLeNet模型通过不同的技术方式使训练时间大幅度减少,并能够提取更多的复杂特征和这些特征的组合,增加了模型的稳定性和准确率。2015年提出的ResNet模型通过引入残差单元,简化了学习目标和难度,使训练误差会随着层数增大而减小,降低了信息传递时丢失和损耗对训练结果产生的影响,可用于训练上百乃至近千层的CNN,对于医学影像信息的深度挖掘具有重大意义[9]。
1.3 人工智能医学图像分析流程 人工智能医学图像分析流程包括以下步骤:首先对模型进行预训练,然后是图像输入和分割、特征提取与图像判别和输出预测结果(图1)。
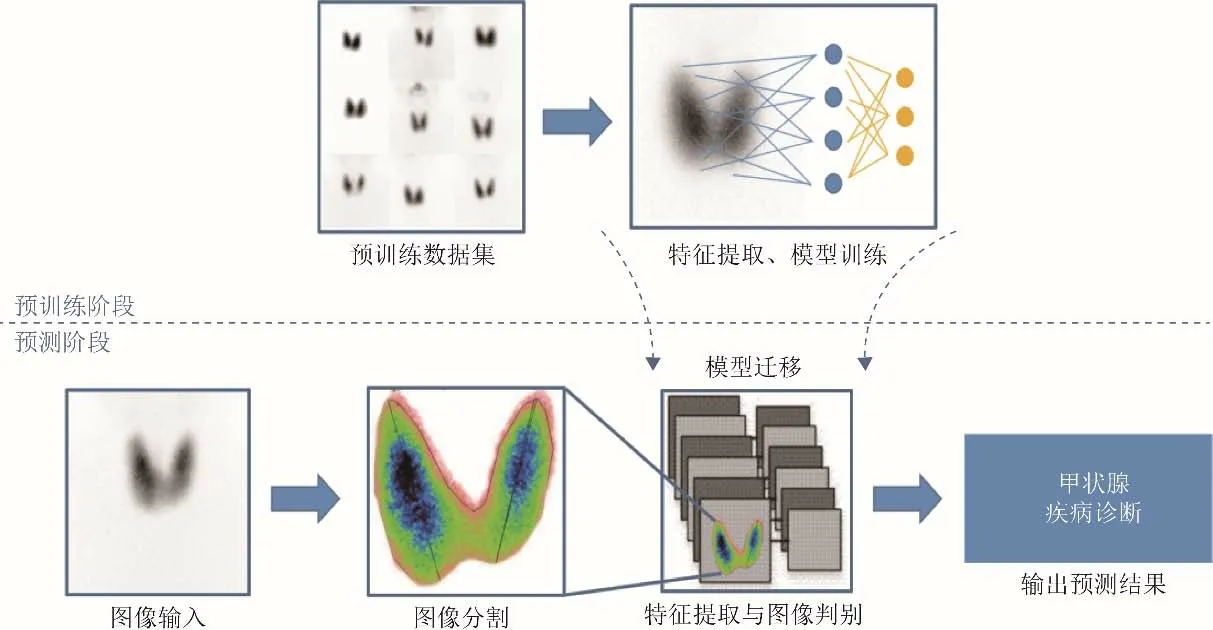
图1 人工智能医学图像分析流程
2 不同影像学方法联合人工智能技术
2.1 超声检查 超声具有价格低、无创和无辐射等特点,是对甲状腺疾病,尤其是甲状腺结节的一线检查手段[10]。然而,超声表现的描述依赖于超声医师的主观判断,对于医师的经验和水平提出了较高要求。人工智能可以提取和量化关键的图像信息,使图像诊断从主观的定性任务转变为客观的定量分析,从而提高诊断效率与准确度,并有望减少侵入性操作的应用。人工智能联合甲状腺超声检查的主要目的是区分结节的良恶性,而人工智能模型常用的分类特征均来自美国放射学会甲状腺影像报告和数据系统(ACR TIRADS),即成分、回声、形状、边缘和钙化。人工智能模型学习的重点特征仍是人类医师进行诊断所依赖的特征。
2.1.1 人工智能与医师的诊断效能对比 Park等[11]比较了基于深度学习的CAD系统、基于支持向量机的CAD系统与超声科医师对甲状腺小结节的诊断表现,结果显示基于深度学习的CAD系统显示出与超声医师大致相当的诊断性能,并在不损失敏感度的情况下比基于支持向量机的CAD系统能够更有效地评估甲状腺结节。Kim等[12]也得到类似的结果,CNN提供的诊断性能可与经验丰富的超声医师相当。而Buda等[13]的研究显示,9名平均具有17年诊断经验的超声科医师的平均敏感度和平均特异度均低于深度学习算法(87%比68%,52%比45%);Li等[14]构建的CNN模型识别甲状腺癌的诊断效能也高于熟练的超声科医师。这些研究预示着人工智能模型在一定层面上展现出超越人类医师的可能性。
2.1.2 人工智能应用的意义 精准识别出良性结节,减少不必要的穿刺活检是将人工智能模型应用于超声检查流程的重要意义之一。Buda等[13]开发的深度学习算法对甲状腺结节活检建议的敏感度和特异度与经验丰富的超声科专家相似。Zhao等[15]利用支持向量机,基于超声图像与剪切波弹性成像图像构建了诊断模型,应用该模型后,建议穿刺活检的比例由人类医师判断的37.7%降至4.7%。
将人工智能模型给出的诊断结果作为第二建议可以显著提升人类医师的诊断表现。Jin等[16]研究显示,在基于CNN的CAD系统的帮助下,初级超声医师的诊断表现可提升至中级水平。此外,TI-RADS 4类与5类结节一直是临床重点关注的问题,对此类结节的良恶性鉴别也是临床工作中的难点。Wu等[17]构建的深度学习模型,对于此类结节的诊断效能较人类医师得到一定提升(敏感度79.0%比68.0%,特异度77.9%比76.1%)。未来此类研究的进一步深入可能对临床诊疗流程产生积极影响。
2.2 CT检查 CT常用于甲状腺结节检查,可以对胸骨后甲状腺病变和超声难以探及的颈部淋巴结进行检查,对较大病变及其与周围结构的关系也能进行细微观察。CT检查对操作者的经验依赖性小,可重复性更强[18],但受制于分辨率,仅适用于最大径>5 mm的结节。此外,CT图像信息丰度相对较高,简单的视觉分析无法捕捉到病灶更深层次的信息,已无法满足精准医疗和个体化治疗的要求。人工智能方法能够对CT图像的像素与空间分布关系进行量化,充分挖掘图像中肉眼无法观察到的隐藏信息,定量且客观地将其呈现并用于指导临床诊断、治疗及预后。目前人工智能联合CT图像诊断甲状腺疾病主要用于甲状腺癌的术前精准分期分级,对于治疗方式的选择和预后评估具有重要意义。
2.2.1 甲状腺结节良恶性鉴别 Peng等[19]利用支持向量机模型对113例患者的284幅甲状腺CT图像进行分析;Wu等[20]对171例1 cm以下甲状腺病变的CT图像进行分析,两项研究的模型均展现出良好的诊断效能(敏感度与特异度约80%)。值得注意的是,Wu等[20]研究指出,对于最大直径<1.0 cm的甲状腺微小乳头状癌,基于CT图像的人工智能模型较基于超声图像的人工智能模型诊断效能更加稳定和出色,而美国甲状腺协会指南不建议对超声高度可疑甲状腺乳头状癌的1 cm以下病变进行活检,因此该研究可能用于指导1 cm以下甲状腺病变的临床诊疗决策。
2.2.2 甲状腺癌颈部淋巴结转移的预测 对淋巴结,尤其是通常最先出现转移的中央区颈部淋巴结状态的判断,是决策是否进行淋巴结清扫术与淋巴结清扫范围的核心因素。近年已有部分相关研究分别用以预测颈部淋巴结转移[21-22]和中央区颈部淋巴结转移[22-24]。这些研究的诊断效能虽然达不到对结节良恶性的鉴别水平,但是在同类研究中,基于CT图像的人工智能模型对于临床决策的指导作用已经显著高于术前超声(超声仅能改变约20%患者的手术方式)[25]。
2.2.3 甲状腺外侵犯的预测 出现甲状腺外侵犯的甲状腺癌发病率和死亡率增加,需要行全甲状腺切除术。因此,准确的评估可以帮助外科医师确定合适的外科治疗策略,以降低再次手术的风险。Chen等[26]构建了机器学习模型对624例甲状腺乳头状癌患者的CT图像进行分析,以预测是否存在甲状腺外侵犯。结合性别、年龄、结节大小、钙化等临床指标构建的放射组学诺模图具有比临床模型更好的表现(F1得分0.732比0.692)。
2.3 MRI MRI包含反映病变不同特征的多种成像模式,其除具有较高的软组织分辨率外,扩散加权成像及表观扩散系数还能反映病变组织的微观结构特性(如细胞密度和膜完整性),对于恶性肿瘤的诊断有显著优势[27]。利用人工智能技术综合分析MRI不同成像模式图像中的丰富信息,提取人眼无法直接识别的深层特征,是评估甲状腺疾病的新思路。
Sharafeldeen等[28]和Naglah等[29]分别基于神经网络和CNN构建模型,对甲状腺结节不同成像模式图像进行多参数分析,综合分析甲状腺结节的功能成像特征表观扩散系数与结构形态和纹理特征,并预测甲状腺结节的良恶性,取得了满意的结果(准确度0.87、0.93,特异度0.97、0.96)。此外,Wang等[30]采用相似的研究方式预测甲状腺病变的侵袭性,基于MRI图像多参数预测模型的诊断表现明显优于基于临床特征的预测模型(曲线下面积0.92比0.56)。
2.4 核医学检查 核医学检查是诊断甲状腺疾病功能的重要手段。甲状腺平面显像的一大优势是可以实现甲状腺毒症的功能诊断,进而指导临床制订治疗方案。甲状腺平面显像的影像特征明显,变异度小,是利用人工智能技术进行自动或辅助诊断的理想影像资料来源[31]。人工智能模型应用于核医学检查的主要目的是消除主观观测偏差,并将人类医师从重复而繁重的工作中解放出来。
根据甲状腺的功能状态,甲状腺毒症可以分为“生产性”甲状腺毒症(如Graves病、结节性毒性甲状腺肿和甲状腺自主高功能腺瘤等)与“破坏性”甲状腺毒症(如急性、亚急性甲状腺炎)。通过甲状腺平面显像准确判断甲状腺毒症图像对于指导临床治疗意义重大。Qiao等[32]对1 430例甲状腺平面显像图像进行分析,构建了深度学习模型,并通过迁移学习进行训练,以区分正常甲状腺、Graves病患者甲状腺和甲状腺功能亢进期亚急性甲状腺炎患者的甲状腺平面显像图像,模型的预测结果与临床诊断结果具有较高的一致性(Kappa>0.715)。值得注意的是,该研究还对比了模型与住院医师的诊断表现,3种模型的诊断效能均优于第一年住院医师,但较第三年住院医师低。
3 结语及展望
结合目前的甲状腺结节临床诊疗工作实际,超声检查凭借其无创和方便的特点,仍将是甲状腺结节的主要筛查及初步诊断手段。基于此,人工智能在鉴别甲状腺结节良恶性方面的应用不仅有利于提高医师的诊断准确率和诊断速度,更为超声检查提供了相对客观的第二意见,弥补了超声检查标准化程度较低、主观性强的缺点。但对于已经确诊的甲状腺癌病情分期,CT的诊断效能更好。利用人工智能技术分析CT图像中难以被人眼捕捉的丰富信息,在术前对甲状腺癌进行精准分期,将极大地促进甲状腺癌的精准和微创治疗。而人工智能技术联合MRI及核医学图像,综合分析病变形态和功能的影像表现,将会是诊断甲状腺疾病的有力补充手段。
尽管大量研究已经证实人工智能在甲状腺疾病诊断中的作用,但其进一步发展仍存在挑战。人工智能方法的“黑匣子”问题(结果的不可解释性)及其带来的相关法律、伦理问题仍需解决。此外,目前人工智能分析流程存在一定的方法学问题,如不同研究采用不同的图像分割及处理方法、不同的算法软件、样本容量的巨大差异和有无验证集等。以上问题均在一定程度上制约了人工智能模型向其他中心的推广应用。
纳入多种指标的综合诊断模型可能是人工智能在甲状腺疾病应用中的发展方向。此外,学科交融和医工结合也尤为重要,医师、技师和工程师等紧密合作,从而规范人工智能分析流程,提高模型的普适性。此外,最关键的问题是如何把成熟有效的人工智能模型与技术转化为切实的临床应用,在这一方面仍需付出大量努力。
利益冲突 所有作者均声明不存在利益冲突

