桑皮饮对糖尿病周围神经病变(阴虚燥热证)患者神经震动感觉阈值,血清IGF-1、TNF-α表达的影响*
高达,赵逸菲,孙宇轩,许华,邱帆,赵璐
1.河南中医药大学,河南 郑州 450046; 2.河南中医药大学第三附属医院,河南 郑州 450008; 3.黄河科技学院,河南 郑州 450063
糖尿病周围神经病变(diabetic peripheral neuropathy,DPN)为糖尿病常见慢性并发症之一,发生率为60.0%~90.0%,并随糖尿病病程延长呈上升趋势[1-2]。DPN发病机制较为复杂,临床多认为是由炎性反应、氧化应激及神经损伤等因素协同作用所致[3-4]。目前,临床治疗DPN多采用抗氧化剂、营养神经制剂等西药,但整体疗效不甚理想。为进一步改善DPN治疗效果,临床将治疗重点转向中西医结合。中医认为,根据麻木、疼痛等临床表现,DPN属“不仁”“痹证”“麻木”等范畴,阴虚燥热、痰瘀互结为主要病机,阴虚燥热证为DPN临床最常见证候之一,痰瘀互结贯穿始终,桑皮饮具有退热解郁、除烦止渴的功效。基于此,本研究在西药治疗基础上联合桑皮饮,重在活血祛瘀、化痰通络、滋阴降火[5],并探讨其对DPN(阴虚燥热证)患者证候及神经震动感觉阈值、神经传导速度的影响,现报道如下。
1 资料与方法
1.1 病例纳入、排除、剔除标准
1.1.1 纳入标准①西医标准:肌电图检查提示感觉、运动神经传导速度减慢;皮肤对称性感觉异常。②中医标准:均符合《糖尿病周围神经病变中医临床诊疗指南(2016年版)》[6]中DPN诊断标准,属阴虚燥热证,肢体麻木,腿足挛急,酸胀疼痛,或肢体灼热疼痛,夜间为甚,五心烦热,失眠多梦,皮肤干燥,口干咽燥,腰膝酸软,头晕耳鸣,便秘,舌质嫩红或暗红,脉细数或细涩。③患者及家属签署知情同意书。
1.1.2 排除标准(自拟)①感染性多发神经炎、中毒性末梢神经炎等疾病所致周围神经病变者;②肝肾等重要脏器器质性病变者;③既往有硫辛酸注射液、甲钴胺等药物过敏史者;④合并糖尿病肾病等严重并发症者;⑤近期有叶酸、维生素B12等药物服用史者;⑥凝血机制紊乱或活动性出血者;⑦认知功能障碍或精神行为异常者。
1.1.3 剔除标准(自拟)①出现严重药物不良反应;②治疗依从性差,中途终止治疗退出者;③未按照研究方案规定接受治疗者。剔除病例后,根据入选病例标准重新纳入病例,保证病例11配对。剔除病例数量应小于总病例数量的5.0%。
1.2 一般资料选取2019年6月至2020年10月在河南中医药大学第三附属医院就诊的60例DPN(阴虚燥热证)患者,随机分为观察组与对照组各30例。两组患者基本资料[性别、体质量指数(body mass index,BMI)、年龄、糖尿病病程、DPN病程、空腹血糖、糖化血红蛋白]比较,差异无统计学意义(P>0.05),具有可比性,见表1。
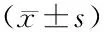
表1 两组患者一般资料比较
1.3 治疗方法两组均给予降糖、控制饮食、运动指导、营养神经及调节微循环等常规干预。
1.3.1 对照组给予静脉滴注硫辛酸注射液(南京新百药业有限公司,国药准字H20093235)600 mg+氯化钠注射液(9 g·L-1)250 mL,同时静脉推注甲钴胺(石家庄四药有限公司,国药准字H20066715)0.5 mg,每日1次。
1.3.2 观察组在对照组基础上给予桑皮饮,方药组成:桑白皮10 g,干葛5 g,柴胡5 g,黄芩5 g,地骨皮7.5 g,天冬7.5 g,麦冬7.5 g,甘草2 g,木通2 g。以上中药由河南中医药大学第三附属医院药房提供,并由药房统一煎制,早晚温服。两组均治疗1个月。
1.3.3 检测方法取空腹静脉血3 mL,采用酶联免疫吸附法检测血清胰岛素样生长因子-1(insulin like growth factor-1,IGF-1)、白细胞介素-6(interleukin-6,IL-6)、血清游离脂肪酸(free fatty acid,FFA)、人髓磷脂碱性蛋白(myelin basic protein,MBP)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)水平。
农业产业技术创新联盟合作系统运行分析——基于共生理论的视域……………………………………………………………………罗雪英(1):60
1.4 观察指标①临床疗效。②采用震动感觉阈值检测仪[型号:Sensiometer A100,购自美迪信达(北京)医疗器械有限公司]检测两组治疗前后左侧及右侧下肢神经震动感觉阈值(nerve vibration sensory threshold,VPT)。③采用肌电图仪(型号:SA7550,购自上海涵飞医疗器械有限公司)检测两组治疗前后腓总神经及正中神经感觉传导速度(sensory conduction velocity,SNCV)、运动传导速度(motor conduction velocity,MNCV)水平。④比较两组治疗前后血清FFA、MBP及IGF-1水平。⑤比较两组治疗前后血清IL-6、TNF-α水平。⑥统计两组不良反应(头晕、皮疹、呕吐恶心、面色潮红)发生率。
1.5 临床疗效判定标准显效:治疗后,肢体麻木、疼痛、烧灼感等临床症状基本消失,痛觉、运动觉、压力觉异常明显好转,肌电图检查显示神经传导速度恢复正常或提升≥5 m·s-1;有效:治疗后,上述症状有所缓解,痛觉、运动觉、压力觉有所改善,肌电图检查显示神经传导速度提升<5 m·s-1;无效:治疗后,未达到显效、有效标准[6]。
有效率=(显效+有效)/n×100%
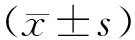
2 结果
2.1 两组患者临床疗效比较观察组有效率为93.33%(28/30),对照组为73.33%(22/30),两组比较,差异有统计学意义(P<0.05),见表2。

表2 两组患者临床疗效比较 例(%)
2.2 两组患者治疗前后VPT值比较治疗后,两组患者下肢VPT值均低于本组治疗前;观察组左侧下肢VPT值为(16.04±2.19)V,右侧下肢VPT值为(15.77±2.30)V,均低于同期对照组(P<0.05),见表3。

表3 两组患者治疗前后VPT值比较

表4 两组患者治疗前后神经传导速度比较
2.4 两组患者治疗前后血清FFA、MBP及IGF-1水平比较两组患者FFA、MBP水平显著低于治疗前,IGF-1水平显著高于治疗前;观察组血清FFA水平为(409.64±21.18) μmol·L-1、MBP水平为(1.69±0.38) ng·L-1,均低于同期对照组,血清IGF-1水平为(164.18±11.64) ng·L-1,高于同期对照组(P<0.05),见表5。
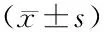
表5 两组患者治疗前后血清FFA、MBP及IGF-1水平比较
2.5 两组患者治疗前后血清IL-6、TNF-α水平比较治疗后,两组患者血清IL-6、TNF-α水平均显著低于治疗前,观察组血清IL-6水平为(29.31±15.53) ng·L-1、TNF-α水平为(26.40±11.39) ng·L-1,低于同期对照组(P<0.05),见表6。
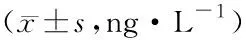
表6 两组患者治疗前后血清IL-6、TNF-α水平比较
2.6 两组患者不良反应比较两组患者不良反应比较,差异无统计学意义(P>0.05),见表7。

表7 两组患者不良反应比较 例(%)
3 讨论
研究认为,DPN发生机制为持续高糖状态损伤机体微血管,促使神经滋养血管、小动脉管壁增厚,从而聚集血小板,降低微血管神经功能,增加糖尿病足风险,甚至截肢风险[7-8]。促进损伤神经营养供应恢复,加快神经再生是现阶段治疗DPN的根本所在。
DPN属中医“痹证”“不仁”“痛证”“血痹”等范畴,主要病理机制为消渴日久不愈,气阴两虚,气虚不能帅血,血行不畅,脉络瘀阻,筋脉失养,累及脏腑功能受损,继而出现肢体麻木,刺痛或感觉异常[9-10]。因此,治疗DPN(阴虚燥热证)关键在于滋阴清热。本研究遵循“治病求本”的指导思想,以“滋阴清热”为治疗原则。由于阴虚燥热是本病的根本,肺乃娇脏,肺络灼伤,皮毛失养,故以桑白皮、地骨皮为君,即泻白散,清泻肺脏之燥热,同时因泻白散药性寒凉、沉降,可顺应肺气肃降,犹如天降甘霖。柴胡、黄芩为臣,取小柴胡汤之意,旨在舒畅三焦气机,清利肝胆郁热,亦可助君药畅达三焦、五脏。天冬、麦冬养阴生津以治本,滋阴清热缓消渴之急;葛根入阳明经,清泻胃肠之火,顾护阴液;木通暗含导赤散之意,一是清其郁热,二是给邪热以出路。生甘草坐使中州,调和诸药。《肘后备急方》记载桑白皮可治“消渴尿多”,具有活血化瘀、利水消肿之功。现代药理学研究表明,桑白皮具有降糖、修复受损组织细胞的功能,可用于糖尿病并发症的治疗[11]。《神农本草经》记载地骨皮治疗“热中消渴,周痹”,其功效为凉血除蒸,清肺降火,二者入肺经,配伍可清少阴之火,养阴生津。《神农本草经》记载葛根“主消渴”,天冬有滋阴润燥、清火止咳之功,麦冬有滋阴润肺、清心除烦之效,三者配伍共奏清热养阴润燥之功。药理学研究表明,葛根素可增强脂肪细胞对糖的吸收利用,起到降糖的作用[12]。柴胡、黄芩可疏肝泄热,木通有利尿通经、清心除烦之效,甘草可调和诸药。本研究结果表明,观察组有效率(93.33%)明显高于对照组(73.33%),有力佐证了二者联合能有效提高治疗效果。桑皮饮中富含麦冬多糖成分,具有良好抗菌、抗炎、降糖效果[13],与甲钴胺、硫辛酸注射液联合,能相得益彰、相辅相成、互增药效,从而抑制神经退变,加快神经髓鞘形成,改善神经细胞营养,促进神经损伤区域修复、再生。
持续性氧化应激、炎症反应会损伤DPN患者神经细胞,促进细胞内特异性物质分泌进入细胞外,减少神经营养物质[14]。IGF-1为神经生长因子,具有胰岛素样及促进神经生长、修复等功能,其水平下调一定程度会减慢周围神经传导速度[15]。MBP为营养神经髓鞘的重要营养物质。张丽等[16]认为,MBP是DPN发生的独立危险因素,能反映周围神经损害范围及严重程度。FFA可产生大量氧自由基,诱发胰岛素抵抗,参与DPN发生、发展[17]。IL-6、TNF-α水平过高会诱导神经纤维损伤。本研究显示,治疗后观察组血清FFA、MBP、IL-6、TNF-α水平低于对照组,血清IGF-1水平高于对照组。桑皮饮中柴胡、木通能清除过氧自由基,抑制脂质过氧化反应及炎症反应,减轻过氧化氢所致人皮肤成纤维细胞氧化应激损伤,与甲钴胺、硫辛酸注射液联合,能增强三磷酸腺苷酶活性,刺激机体抗氧化剂代谢,提高机体抗氧化能力,减轻高糖所致氧化应激状态,避免神经细胞被炎症因子损害,从而缓解DPN患者氧化应激反应、炎症反应。
胡雪剑等[18]认为,受高血糖及醛糖还原酶等影响,DPN患者果糖激酶匮乏,导致周围神经组织内山梨醇、果糖等成分堆积,从而引发神经水肿、脱髓鞘,甚至坏死,诱发周围神经感觉障碍。VPT是早期筛查DPN发生及评估死亡风险的重要指标,可为及早预防、预后改善提供量化参考[19]。本研究发现,治疗后观察组左侧及右侧下肢VPT值低于对照组。桑皮饮中地骨皮不仅能降低血糖,改善胰岛功能,缓解内皮损伤,炎症反应,还能促进血管扩张,调节末梢循环及血氧供给[20],联合硫辛酸注射液、甲钴胺,能有效改善神经电生理状况,降低神经震动感觉阈值。王靖清等[21]发现,DPN神经传导速度减慢的内在机制与高血糖有关,可造成神经磷酸肌醇代谢紊乱,引发周围神经轴索损伤。比较两组治疗前后神经传导速度发现,两组治疗后腓总神经及正中神经MNCV、SNCV均高于治疗前,提示西药单独治疗及联合桑皮饮均能提高神经传导速度,进一步分析可知,观察组治疗后腓总神经及正中神经MNCV、SNCV高于同期对照组,考虑可能为桑皮饮中富含黄芩素等化学成分,能抑制血小板聚集,防止凝血酶诱导的纤维蛋白原转化为纤维蛋白,与甲钴胺、硫辛酸注射液联合,能调节机体微循环,减轻微血管损伤所致神经系统低灌注,促进腱鞘形成及轴突生长,增加神经内膜血流量,修复神经传导系统,从而提高神经传导速度[22]。
综上可知,在西药治疗基础上联合桑皮饮治疗DPN疗效确切,能有效降低DPN(阴虚燥热证)患者下肢VPT,提高神经传导速度,减轻机体氧化应激反应,降低炎症因子水平,保证安全性。但本研究尚需进一步探讨桑皮饮联合西药对DPN(阴虚燥热证)患者血管内皮功能的影响,这也是下一步研究的重点。

