胚胎植入前染色体非整倍体检测试剂盒评价
曲守方 黄传峰 于婷 黄杰
胚胎植入前非整倍体筛查(preimplantation ge⁃netic testing for aneuploidy,PGT⁃A)是对体外受精的胚胎,进行染色体非整倍性及染色体拷贝数变异(Copy number variants,CNV)检测,筛选正常的胚胎植入子宫的一种早期筛查方法,能够提高种植率、妊娠率及活产率。1993年首次报道了经胚胎植入前遗传学筛查(Preimplantation genetic Screening,PGS)后获得成功妊娠的病例,这项技术的临床应用性逐渐拓展[1⁃2]。目前PGS 检测方法主要包括荧光原位杂交(fluorescence in situ hybrid⁃ization,FISH)、比较基因组杂交技术(comparative genomic hybridization,CGH)和高通量测序(next generation sequencing,NGS)等方法[3⁃4]。其中高通量测序技术已经成为临床上使用较多的胚胎染色体分析技术,多项临床对照试验均表现出胚胎经染色体筛查后妊娠率有所提高[5]。
目前国内已经有多家公司开发基于高通量测序技术的胚胎植入前染色体非整倍体检测试剂盒。中国食品药品检定研究院于2017年研制胚胎植入前染色体非整倍体国家参考品,用于胚胎植入前染色体非整倍体检测试剂盒上市前的注册检测。2019年国家药品监督管理局批准YY/T 1657⁃2019 胚胎植入前染色体非整倍体检测试剂盒(测序法)行业标准的发布,用于规范该类产品的标准。本研究使用胚胎植入前染色体非整倍体国家参考品,评价基于半导体测序法的胚胎植入前染色体非整倍体检测试剂盒的质量。
1 材料与方法
1.1 样本
胚胎植入前染色体非整倍体国家参考品,中国食品药品检定研究院提供。
1.2 试剂与仪器
胚胎植入前染色体非整倍体检测试剂盒(半导体测序法)和测序反应通用试剂盒(半导体法),购自东莞博奥木华基因科技有限公司;Qubit dsDNA HS Assay Kit 购自美国Invitrogen 公司;PCR 扩增仪,型号:Veriti,购自美国Thermo Fisher 公司;荧光定量仪,型号:Qubit 3.0,购自美国Life Technology 公司;荧光定量QPCR 仪,型号:StepOne Plus,购自美国ABI 公司;基因测序仪,型号BioelectronSeq 4000,购自东莞博奥木华基因科技有限公司。
1.3 方法
按照胚胎植入前染色体非整倍体检测试剂盒(半导体测序法)的说明书,取国家参考品置于Veriti 型PCR 扩增仪进行细胞裂解及片段化,并制备文库。将文库进行PCR 扩增和单细胞扩增后纯化。纯化的DNA 使用Qubit 3.0 荧光定量仪和Qubit dsDNA HS Assay Kit 进行定量,样本的浓度要求≥20 ng/μL,确定单细胞扩增是否成功。将纯化的单细胞扩增DNA 继续进行片段化和纯化后,进行末端修复、接头连接以及PCR 扩增等步骤,构建文库。将文库纯化后,使用StepOne Plus 荧光定量QPCR 仪和试剂盒的定量标准品进行文库定量。按照文库上机浓度的要求,混合各个文库。
按照测序反应通用试剂盒(半导体法)说明书,混合文库使用基因测序仪BioelectronSeq 4 000进行测序。使用试剂盒配套的全自动分析软件对测序数据进行生信分析,从而识别染色体拷贝数变异。计算比对到基因组中的测序读长数并归一化成拷贝数值;然后采用环状二元分割算法(Cir⁃cular Binary Segmentation,CBS)识别染色体拷贝数的断点位置,进而将染色体分段(segment)并计算每个分段的平均拷贝数值(CBS Ratio),最后统计各染色体分段的Z⁃score 和显著性水平。CBS Ratio 值的显著性水平(P⁃value)采用R 软件(版本3.4.1)进行统计分析,利用t⁃检验计算P⁃value。将Z⁃score 大于3 或小于⁃3、且P⁃value 小于0.0001 的染色体分段判断为染色体拷贝数变异阳性。
2 结果
2.1 阳性参考品结果
对于65 个异常片段大于4 Mb 的国家阳性参考品,试剂盒均能检出对应的染色体异常,检出率为100%。国家阳性参考品19⁃del(7)⁃25.3M 在7号染色体100.5 Mb⁃125.8 Mb 位置存在片段大小约25.3 Mb 的拷贝数缺失,其Z⁃score 为⁃28.6。见图1;其他国家阳性参考品的相应异常区域对应的染色体Z⁃score 均>3 或<⁃3。见图2。对于15 个异常片段小于等于4 Mb 的国家阳性参考品,对应的染色体异常检出率为86.7%(13/15)。国家阳性参考品22⁃del(7)⁃1.5 M 在7 号染色体72.1 Mb⁃73.6 Mb位置存在片段大小约1.5 Mb 的拷贝数缺失,其Z⁃score 为⁃8.1。见图3;国家阳性参考品30⁃dup(17)⁃1.9 M 的17 号染色体的Z⁃score 为2.0,未检测到相应异常区域,国家阳性参考品100⁃NC4⁃dup(Xq12)⁃1.4 M 的X 染色体的Z⁃score 为1.1,未检测到相应异常区域,其他13 个国家阳性参考品的相应异常区域对应的染色体Z⁃score均>3或<⁃3。见图4。
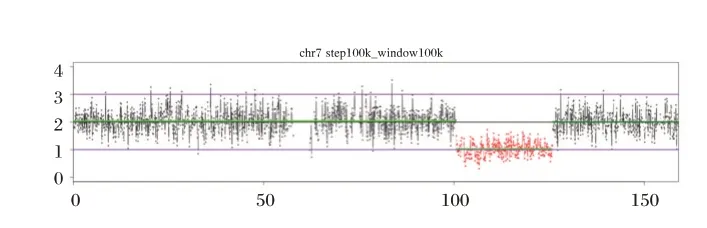
图1 国家阳性参考品19⁃del(7)⁃25.3M 的结果Figure 1 The result of nationalpositive reference for 19⁃del(7)⁃25.3M
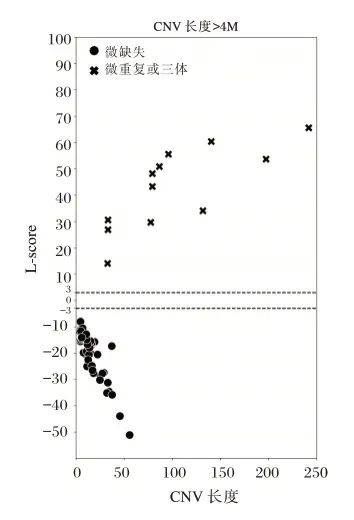
图2 国家阳性参考品(异常片段大于4Mb)结果Figure 2 The result of national positive reference materials(abnormal fragments>4 Mb)

图3 国家阳性参考品22⁃del(7)⁃1.5M 的结果Figure 3 The result of national positive reference for 22⁃del(7)⁃1.5M

图4 国家阳性参考品(异常片段小于等于4 Mb)结果Figure 4 The result of national positive reference materials(abnormal fragments ≤4 Mb)
2.2 阴性参考品结果
10 个国家阴性参考品均未检出试剂盒范围内的染色体异常,其Z⁃score 均小于3 且大于0,显著性水平P⁃value>0.0001,如国家阴性参考品97⁃NC1在1⁃22 号染色体和性染色体区域内均未检测出异常区域。见图5、图6。
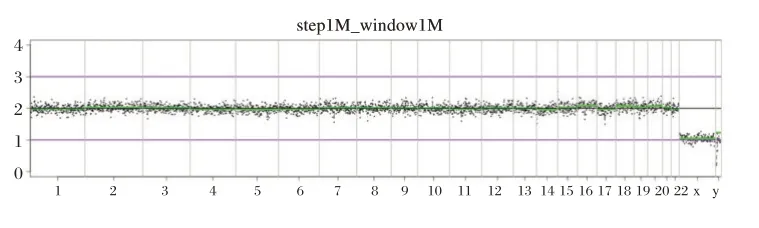
图5 国家阴性参考品97⁃NC1 结果Figure 5 The result of national negative reference material for 97⁃NC1

图6 国家阴性参考品结果Figure 6 The result of national negative reference materials
2.3 嵌合体参考品结果
对30%嵌合的嵌合体样本检出率为50%(3/6),相对应的70%嵌合体样本检出率为83.3%(5/6)。见图7。国家嵌合体参考品110⁃0.3⁃del(4)⁃37.7M是两种细胞不同比例的混合,30%嵌合比例细胞在4 号染色体153.1 Mb⁃190.8 Mb 位置存在大小约37.7 Mb 拷贝数缺失,其Z⁃score 为⁃16.5;70%嵌合比例细胞在15号染色体23.6 Mb⁃28.5 Mb位置存在大小约4.9 Mb 拷贝数缺失,其Z⁃score 为⁃10.5,结果显示30%嵌合和70%嵌合的细胞均正确检出。见图8。

图7 国家嵌合体参考品结果Figure 7 The result of national chimera reference materials

图8 国家嵌合体参考品110⁃0.3⁃del(4)⁃37.7M 结果Figure 8 The result of national chimera reference material for 110⁃0.3⁃del(4)⁃37.7 M
3 讨论
在体外受精形成的胚胎中,约50%存在染色体异常,可导致移植后早期胚胎丢失、自然流产和死产,是限制辅助生殖技术成功率和有效推广的重要原因之一。基于高通量测序的胚胎植入前染色体非整倍体检测,检测胚胎卵裂球细胞或者囊胚滋养层细胞的DNA,获得样本中23 对染色体数量的差异,对胚胎染色体非整倍体或部分染色体拷贝数变异进行植入前辅助诊断,选择正常胚胎植入子宫,从而提高辅助生殖的成功率。而单细胞全基因组扩增(whole genome amplification,WGA)技术的选择与评价,不同测序平台的数据量要求,分析算法的选择以及阴阳性预测的划分标准等,这些均是影响胚胎植入前染色体非整倍体检测结果的因素[6]。目前单细胞全基因组扩增包括多重置换扩增(multiple displacement amplifica⁃tion,MDA)、多次退火环状循环扩增(multiple annealing and looping⁃based amplification cycles,MALBAC)和简并寡核苷酸引物PCR(Degenerate oligonucleotide primerPCR,DOP⁃PCR)等技术方法,每种方法各有自己的优势[7⁃8]。为使胚胎植入前遗传学筛查更加规范并能够有效地实施,国内外发布不同的胚胎植入前遗传学诊断和筛查技术的指南性文件和专家共识[9⁃10]。传统的细胞遗传学核型分析一直被用作诊断染色体异常的金标准,然而它费时费力且很大程度上依赖于细胞培养,染色体分辨率很低,为5~10 M。高分辨率染色体微阵列分析(CMA)技术可以检测染色体数目异常、微缺失/重复、单亲二体,在人力资源有限的产前诊断实验室中,CMA 可以单独用于代替细胞遗传学核型分析。拷贝数变异测序(CNV⁃Seq)分辨率为0.2 Mb,用于检测具有临床意义的染色体异常[11]。2020年,美国医学遗传学和基因组学学会(ACMG)等发布对CNV 致病性评估的最新指南,对>100 kb 的CNV 进行分类,分为致病性CNV(patho⁃genic CNV,pCNV)、可能致病性CNV(1ikely patho⁃genic CNV,lpCNV)和良性CNV(benign CNV,bC⁃NV)等5 类[12]。CNV 是良性的或者是致病性的,取决于它们的位置和基因含量,致病性CNV 越来越多地与复杂疾病相关,尤其是一些结构性先天性异常[13]。参考临床上致病性CNV 的异常片段大小和检测方法的灵敏度,我们将染色体异常片段大小设置为4Mb,用于评价试剂盒CNV 检测能力。胚胎嵌合是指在胚胎的组成细胞中存在两种或以上不同染色体组成的细胞系,对于介于正常与异常之间的整倍体/非整倍体嵌合胚胎,需要设置嵌合报出的阈值[14]。对于嵌合胚胎的检测,不同研究报道对于诊断染色体嵌合推荐的阈值,国际胚胎植入前遗传学诊断协会(Preimplantation Genetic Diagnosis International Society,PGDIS)推荐的嵌合报出阈值是20%~80%[15⁃16]。
中国食品药品检定研究院研制了胚胎植入前染色体非整倍体国家参考品,用于试剂盒的注册检测和上市后监督抽验工作。为了评价试剂盒对囊胚筛选中染色体不同大小CNV 的检测能力,国家参考品设置了不同异常片段大小的国家阳性参考品,并规定异常片段大于4 Mb 的阳性参考品对应的染色体异常要求检出率达到100%,异常片段小于等于4 Mb 的阳性参考品对应的染色体异常要求检出率达到30%以上。研究结果显示胚胎植入前染色体非整倍体检测试剂盒(半导体测序法)对异常片段大于4 Mb 的国家阳性参考品均能够检出对应的染色体异常,对异常片段小于等于4 Mb 的国家阳性参考品的检出率为86.7%,符合要求。针对嵌合胚胎,国家参考品设置了30%嵌合的嵌合体样本,要求其检出率应达到30%以上,同时要求相对应的70%嵌合体样本的检出率应达到60%以上。研究结果显示试剂盒对30%嵌合比例国家嵌合体参考品的检出率为50%,对70%嵌合比例国家嵌合体参考品的检出率为83.3%,符合相应的要求。对于国家阴性参考品,试剂盒均未检出范围内的染色体异常。本研究表明胚胎植入前染色体非整倍体检测试剂盒(半导体测序法)能够符合国家参考品的阳性参考品符合率、阴性参考品符合率和嵌合体参考品符合率的要求,国家参考品能够对胚胎植入前染色体非整倍体检测试剂盒的质量进行有效评价,具有很好的适用性。

