稳定期COPD患者骨骼肌力量下降现状及膳食风险因素分析
裴华莲,乔婷婷,王 璐,张泽文,戴江红*
(1新疆医科大学公共卫生学院流行病学与统计学教研室,乌鲁木齐 830013;2新疆医科大学第一附属医院呼吸重症医学科;3新疆医科大学护理学院;*通讯作者,E-mail:epidjh@163.com)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是一种以气流受限为特征的呼吸道慢性炎症性疾病,发病率及死亡率高,临床表现为进行性呼吸困难及肺功能减退[1]。骨骼肌力量下降已成为COPD患者重要的肺外表现[2],握力是肌肉力量的主要测量指标[3-5],肌肉力量下降不仅出现在中重度疾病中,也出现于病程的早期[6,7],严重影响患者的生存质量及预后,并已被证明是COPD患者死亡的独立预测因子[8]。研究显示,营养状况、体力活动、慢性疾病等多因素均与肌肉力量密切相关[9,10],但缺乏针对性风险预测数据。本研究旨在通过调查COPD患者以握力为测量指标的骨骼肌力量降低的发病现状,进而分析其影响因素并建立风险诊断模型,对肌肉力量下降进行更准确风险评估,探索更有效预防、护理及康复的途径,提高患者健康水平。
1 资料与方法
1.1 一般资料
研究对象来源于国家重点研发计划“西北区域自然人群队列研究”子课题“新疆多民族自然人群队列建设及健康随访研究”乌鲁木齐现场(冶建及卡子湾社区)的基线人群,从中筛选COPD患者共计370人。纳入标准:①年龄35~74岁;②明确诊断为COPD,且咳嗽、咳痰、气短等症状得到明显控制者;③同意接受并能完成问卷调查和体格检查。排除标准:①合并有血压过高(收缩压≥170 mmHg)、肺大泡、肺结核、肺部感染患者;②近1年内脑出血、心肌梗死患者;③恶性肿瘤患者;④合并有心衰、2型糖尿病及严重骨质疏松患者;⑤残疾、精神障碍等无法配合运动测试者。本研究已通过新疆维吾尔自治区中医药研究所伦理委员会审查(2018XE0108),所有研究对象均已签署知情同意书。
1.2 问卷调查
采用《中国西北区域自然人群队列建设研究》统一制定的调查问卷,由培训合格的调查员采用面对面的方式进行调查,收集研究对象的基本信息(性别、年龄、民族、受教育程度等)及健康信息(吸烟、体力活动情况及慢性病的疾病史)。采用标准方法测量身高、体质量。体质指数(body mass index, BMI)计算公式为:BMI(kg/m2)=体质量/身高2。
1.3 膳食调查
通过膳食调查问卷了解研究对象过去一年中的食物摄入情况,对调查对象摄入食物的频率(每天、4~6次/周、1~3次/周、1~3次/月、不吃或极少吃)以及平均每次的摄入量进行询问。依据膳食平衡指数(DBI-16)的标准[11]进行赋值,计算每种食物组的摄入情况。DBI-16由8个指标构成,分别为:①谷类食物(米类、面类、粗粮);②蔬菜水果(深色蔬菜、浅色蔬菜、水果);③奶类及大豆类;④动物性食物(肉类、蛋类、鱼虾类);⑤纯能量食物(食用油和酒精);⑥调味品(添加糖、盐);⑦饮水;⑧食物种类。本次研究中未调查饮水的情况,故没有对水的摄入量进行评估。
1.4 食物组摄入情况界定
依据DBI-16标准[11],食物评分在-2~2分之间为摄入适宜,<-2为摄入不足,>2为摄入过量。而其中谷类适宜分值范围在-4~4,食物种类适宜分值范围在-4~0,即低于8种推荐食物种类(每种25 g,大豆为5 g)即为食物种类摄入不足。
1.5 体成分测量
采用TANITADC-430MA人体成分分析仪(多导生物电阻抗原理),测量内容包括体质量、体脂肪量、肌肉量、水分、蛋白质等多个指标,由经过统一培训并考核合格的调查员测量。本研究重点关注体脂肪量(fat mass,FM)及去脂含量(fat free mass, FFM),去脂含量指体质量扣除体脂肪量部分。体脂指数(fat mass index, FMI)=全身脂肪质量/身高2。去脂体质量指数(fat free mass index, FFMI, kg/m2)=全身非脂肪质量/身高2[12]。
1.6 握力测量
应用北京斯普特科技有限公司SPT-M276328型握力测试仪测量,调整两蹬间距使其符合测试者手掌大小,测试者保持直立,双足分开,待测试仪校零后左右手各测两次,两次间隔休息30 s,取其最大值。依据亚洲肌肉减少症工作组(AWGS)[5]诊断标准,握力≤26 kg以上(男性)或≤18 kg以上(女性)定义为骨骼肌力量下降。
1.7 实验室检测
被调查对象空腹10~12 h后,清晨由专业的护士使用真空采血装置采集研究对象血标本,实验室检测由医院检验科专业人员完成,本研究重点关注血红蛋白(HB)和血清白蛋白(ALB)测量指标。男性血红蛋白小于130 g/L,女性小于110 g/L为血红蛋白偏低;男女性白蛋白<20 g/L为白蛋白偏低[13]。
1.8 统计学分析

2 结果
2.1 骨骼肌力量下降情况调查结果
本研究共纳入COPD患者共370例,平均年龄(66.8±10.6)岁,骨骼肌力量下降者143例,占38.7%;超重及肥胖者(BMI≥24.0 kg/m2)197例,占53.2%。基线特征中不同年龄、教育程度、体力活动、COPD分级、体质指数、去脂体质量指数及不同血红蛋白含量的患者,以及膳食特征中奶类、蛋类、食用油及食物种类摄入量不同的患者,其骨骼肌力量下降情况的差异具有统计学意义(P<0.05,见表1,表2)。

表1 不同基线特征患者骨骼肌力量下降情况的分布
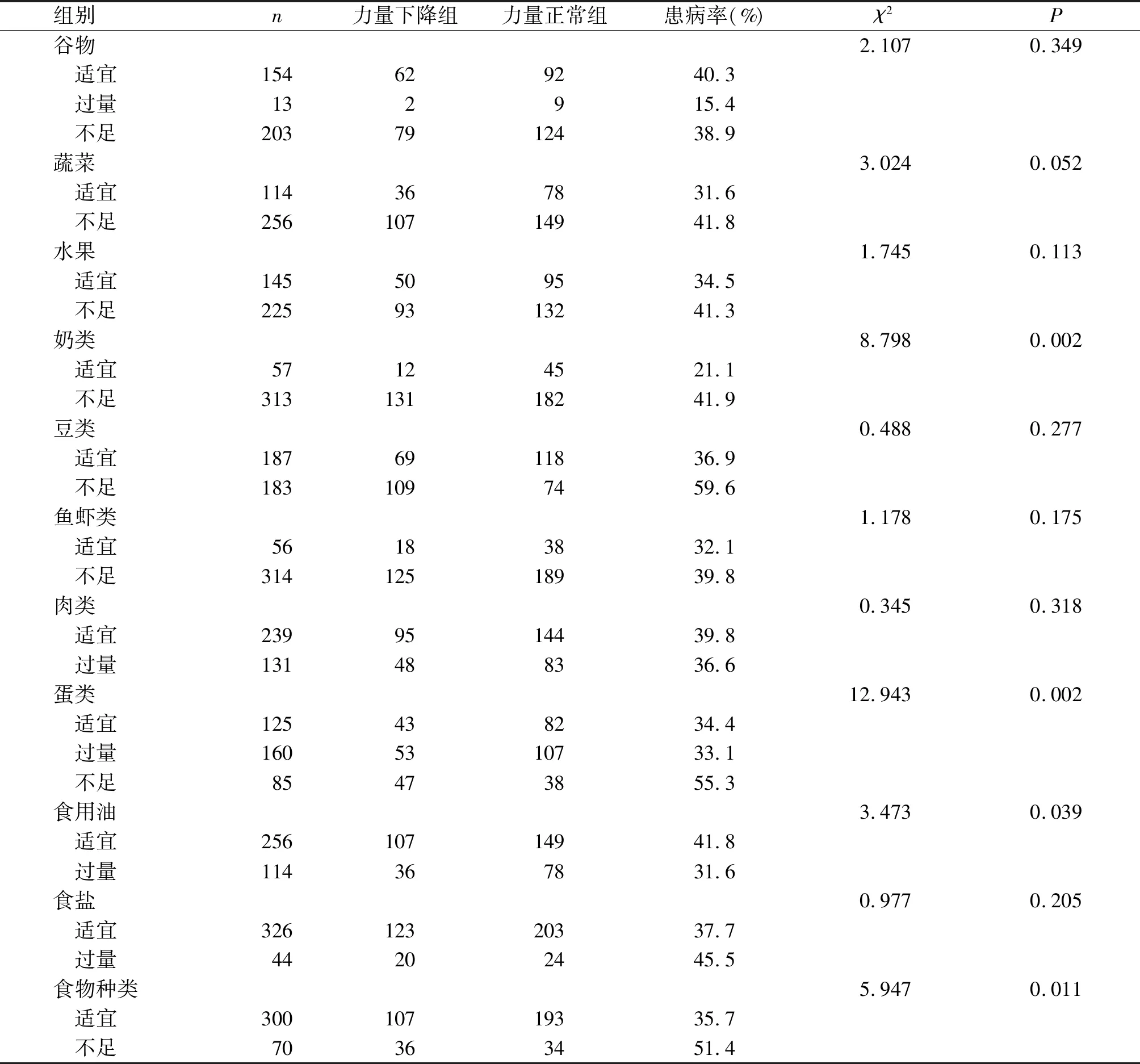
表2 不同食物组摄入特征患者骨骼肌力量下降情况的分布
2.2 Lasso方法筛选骨骼肌力量下降的影响因素
由表1、表2筛选出的变量(P<0.20),包括年龄、民族、教育程度、体力活动、COPD分级、BMI、FFMI、血红蛋白、白蛋白、蔬菜、水果、奶类、鱼虾、蛋类、食用油、食物种类共16个变量,进行多重共线性分析,计算方差膨胀因子(variance inflation factor, VIF)为42.441,即变量间存在明显的共线性,因此选用Lasso回归分析进行进一步变量筛选。
运用Lasso回归筛选变量时以赤池信息准则(AIC,Akaike Information Criterion)为标准选择平均误差在一个标准差以内的最大的正则化参数λ,使用Lasso方法从变量中选出5个具有非零系数的显著性指标,分别为食物种类、蛋类、年龄、FFMI和COPD分级。在Lasso模型中通过交叉验证的方法筛选参数λ最合适值的过程见图1。随着λ值逐渐增大,回归系数趋向于零;并且随着λ值逐渐增大,均方误差逐渐增大(见图1)。两条虚线之间为最优模型,当logλ为-5.05时,所选择参数为5个,此时Lasso模型为最优。筛出以上5个因素后再次进行共线性分析,VIF为4.830,此时适合进一步的Logistic回归分析。

图1 基于Lasso回归的特征性变量筛选Figure 1 Characteristic variable screening based on lasso regression
2.3 影响COPD患者骨骼肌力量下降的多因素Logistic回归分析
以骨骼肌力量下降为因变量,以Lasso方法筛选出的5个因素为自变量,变量赋值见表3,建立多因素Logistic回归风险诊断模型,得出有统计学意义的因素为食物种类、年龄、FFMI、COPD分级,其中食物种类不足、高龄、COPD高分级均与骨骼肌力量下降的高风险相关,而较高的FFMI为保护相关(见图2)。进一步应用列线图实现模型可视化,如患者年龄45岁,膳食种类不足,FFMI=14,COPDⅢ级,骨骼肌力量下降的发生概率约为0.52(见图3),应用ROC曲线下面积AUC分析列线图模型的区分度,AUC为0.958(见图4),表明模型的区分度较好。

表3 多因素Logistic回归变量赋值表

图2 COPD患者骨骼肌力量下降的多因素Logistic回归分析结果Figure 2 Results of multivariate logistic regression analysis of decreased skeletal muscle strength in patients with COPD
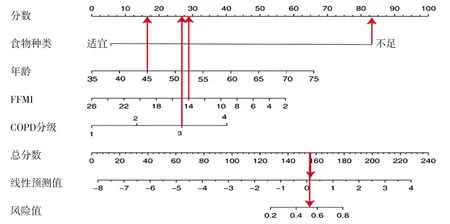
图3 COPD患者骨骼肌力量降低的多因素Logistic回归风险诊断模型列线图Figure 3 Nomogram of multivariate logistic regression risk diagnosis model for skeletal muscle strength reduction in COPD patients
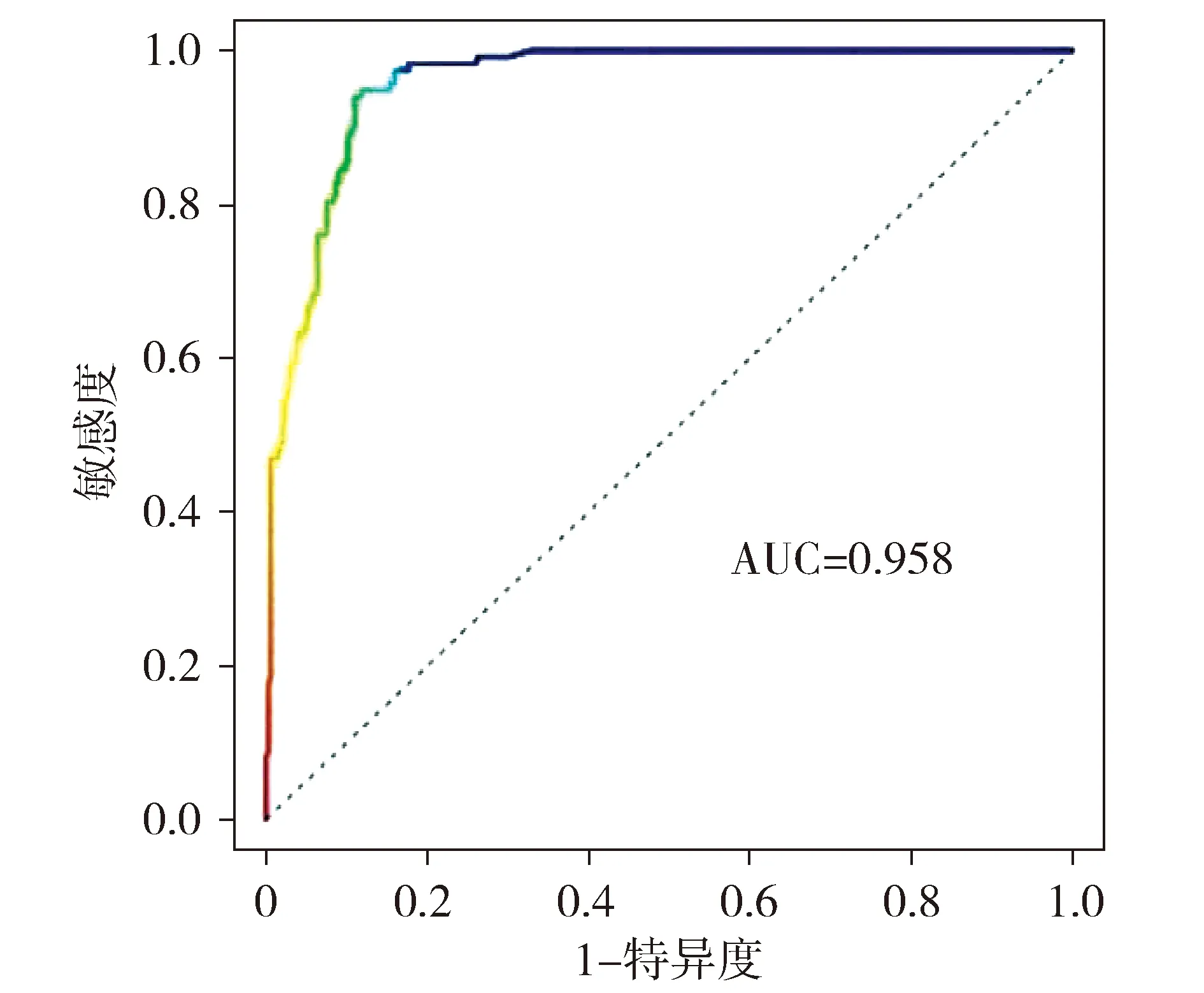
图4 COPD患者骨骼肌力量降低的多因素logistic回归模型ROC曲线Figure 4 ROC curve of multifactor logistic regression model of decreased skeletal muscle strength in patients with COPD
3 讨论
握力是全身肌肉力量及全因死亡率的重要预测因子[14],是一系列疾病和不同部位相互关联的肌力的潜在反映,握力的基线值和日常活动功能之间呈现明显的线性关系[15]。COPD患者由于活动减少、营养及能量失衡、缺氧、高碳酸血症、炎症、电解质紊乱等多种因素导致肌肉力量下降[16],且下降速度明显高于同龄健康人群。对于COPD患者骨骼肌力量下降的预防策略及针对性的干预治疗,已经成为目前COPD管理和研究的热点内容。Jaitovich等[17]研究发现约40%的COPD患者出现不同程度肌肉力量下降及功能障碍,并与疾病的不良结局有关。Seymour等[6]的报道显示,三分之一的COPD患者在疾病早期出现股四头肌功能障碍。另外,一项涉及9 637例COPD患者的荟萃分析显示,肌肉质量及力量下降总患病率为15.5%~34%[18]。本研究所调查COPD患者骨骼肌力量下降的检出率为38.65%,与以上研究结果基本一致。
骨骼肌力量下降的风险因素研究有助于探索其尽早预防、治疗及干预的有效途径,以改善患者的运动能力,提高其生活质量。首先,膳食作为疾病的重要外源性因素与机体的健康结局紧密相关,且整体膳食模式与疾病关联已成为膳食研究新的方向。Schols等[19]的研究证实,均衡、高质量的膳食对所有COPD患者机体功能都是有益的。Bloom等[20]的荟萃分析同样显示了均衡膳食与身体衰弱的负向关联性。本研究基于膳食平衡指数(DBI-16)对COPD患者进行膳食质量与肌肉力量下降的关联分析也得到了与之相似的结果,即摄入食物种类不足是骨骼肌力量下降的危险因素。食物多样性是均衡膳食的保证,多样性膳食可满足机体各种营养需求,补充单一膳食的不足,对于保护身体机能具有重要作用。另外,低FFMI同样是影响骨骼肌力量下降的重要因素,这与Chua等[21]团队的研究结果一致。FFMI是反映去脂含量的指标,体现肌肉骨骼等健康成分,代表健壮程度,COPD患者会出现肌肉质量和骨密度的同步下降[22,23],导致患者肌肉力量下降,甚至导致认知功能障碍[24],加之患者呼吸困难导致的气体交换受损,使患者处于被迫静息状态,最终加剧肌肉力量下降。
本研究中还进一步呈现了可视化模型及模型验证,列线图可以简单直观地看出COPD骨骼肌力量下降的诊断风险,AUC为0.958,较精准确定肌力下降的风险,并具有较高的灵敏度、可靠性及可推广性。虽然握力下降临床测量非常简单,但是提前风险评估更为重要。COPD患者机体处于高分解代谢状态,营养摄入量下降和活动减少加剧了营养不良的发生,导致骨骼肌质量损失和功能下降[25],甚至构成了肌肉衰减综合征,并进一步影响全身各器官系统的功能及疾病预后。因此,肌肉功能成为制约疾病进展与生存状态的重要因素,应从预防和管理与年龄、营养状况及疾病分级有关的肌肉力量和身体功能损失的策略出发,精准评估,采取防病治病及营养干预综合措施提高患者健康水平,延缓疾病进展。
综上所述,本研究在针对COPD患者骨骼肌力量下降基线调查的基础上,以膳食质量调查为切入点构建膳食相关的风险评估模型,对骨骼肌力量下降进行更精准风险评估,对今后探索更有效预防、护理及康复途径,提高患者运动能力及生活质量提供理论依据。但本研究存在局限性,样本量偏小且非随机抽样,可能存在选择偏倚。另外,仅局限于横断面的研究,因果关系的结论还需要今后更大规模的前瞻性研究进一步确定。

