[Co(II)Salen]配合物的制备及载氧实验装置的改进
郝俊生,于海英,邢隆飞,何迎春,梁琪,刘涛,常瑞雪
1山西大学化学化工学院,太原 030006
2山西大学应用化学研究所,太原 030006
自然界的生物体中含有多种过渡金属离子的蛋白,如血红蛋白等,在一定条件下能够吸收和放出氧气,以供有机体生命活动的需要[1]。研究者们常用一些人工合成的无机配合物[2–7]的吸氧、放氧作用来模拟研究生物体内金属蛋白的载氧机理。其中,[Co(II)Salen]配合物具有可逆载氧能力,是天然氧载体的模型化合物[8],[Co(II)Salen]配合物的制备及载氧实验[9–12]以其较强的综合性而被多所高校列为综合化学实验教学项目。在教学过程中,我们发现教材中所涉及的[Co(II)Salen]配合物的制备及载氧装置存在一些不足,因此对装置进行了创新设计与改进。
在[Co(II)Salen]配合物的制备过程中,为了防止空气中的氧气将Co(II)氧化到Co(III),导致反应失败,合成时必须使用氮气保护。在同时开展多组实验时,一般采用图1所示的三通联用的方法。但在多年来的教学过程中,我们发现该方法存在不足,如各装置的气密性不同、排气管插入液面的深度不一,均会导致各反应体系的压力存在差异,气体易从阻力小的装置中逸出,造成反应失败,学生实验的失败率高达30%以上(实验报告统计结果),为实验教学工作造成很大困扰。
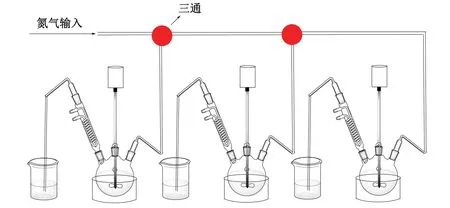
图1 现有装置通气示意图
[Co(II)Salen]配合物的载氧实验是测定溶剂与[Co(II)Salen]接触时,在一定压力、温度下,系统中氧气的体积变化,根据公式pV=nRT求得所吸收氧的物质的量n。研究者们根据该原理对载氧装置不断探索改进[9–12],得到如图2所示的装置[12],该装置也是现行教材中“[Co(II)Salen]配合物的制备及载氧实验”普遍使用的装置。该装置较为简单,具有操作方便、学生易上手等优点,但不足也是无法忽视的:
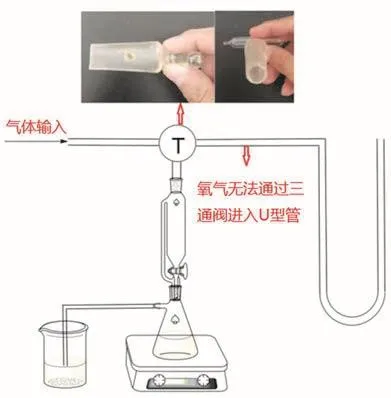
图2 现行教材中的载氧装置示意图
(1) 该载氧装置中U型管端的空气无法排出,直接影响载氧数据的准确性;
(2) 载氧装置中关键构件,如三通阀、导气管等均为玻璃制品(图3),使用过程中容易损坏。

图3 现行教材中载氧装置实物图
鉴于以上原因,本文对该实验的通气装置以及载氧装置进行了进一步的研究和改进,较好地解决了上述问题。本文采用了气体稳压稳流装置,可以提供稳定的气体流量,不受反应装置阻力和气密性的影响,可实现气体在多组实验中的稳定分配,同时又避免了浪费,学生实验成功率显著提升;载氧装置中三通阀与二通阀并联,实现了对U型管的氧气吹扫,使得反应装置完全充满氧气,吸氧体积测量更为准确、科学,数据准确性得以进一步提高;载氧装置全部固定在面板上,关键构件(三通阀、二通阀以及导气管道)全部采用钢制结构,不仅显著提升了仪器的气密性,而且很大程度上增加了仪器的使用寿命。
1 实验原理
1.1 [Co(II)Salen]配合物的制备装置
[Co(II)Salen]配合物通过如图4所示的实验路线合成。
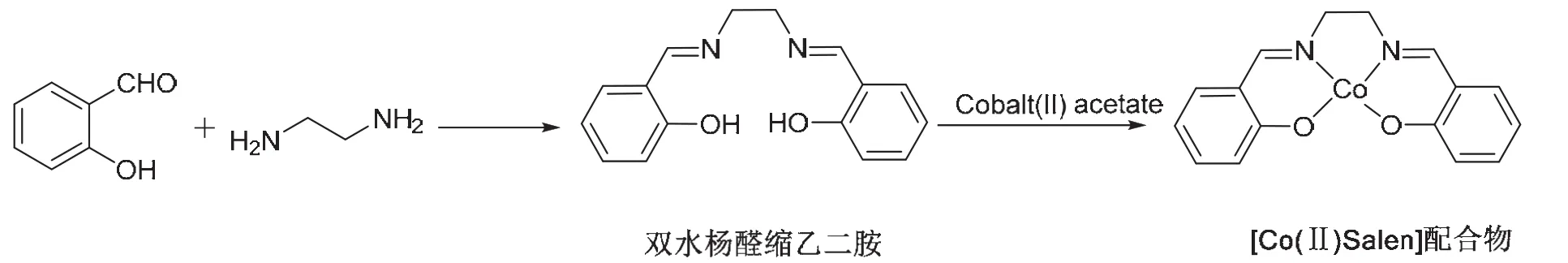
图4 [Co(II)Salen]配合物的实验合成路线
该实验首先以水杨醛与乙二胺为原料制备双水杨缩乙二胺,然后在氮气保护下加入四水合乙酸钴合成[Co(II)Salen]配合物。针对图1所示的三通联用方法所存在的不足,本文采用了如图5所示的装置连接方法,在高压氮气瓶与各反应装置之间安装了如图6所示的气体稳压稳流装置。该装置主要由稳压阀和稳流阀构成,高压氮气瓶通过该装置输出的各路气体流量稳定,不受反应装置阻力和气密性的影响,可实现气体在多组实验中的稳定分配,同时又避免了浪费,尤其适用于多组学生同时开展实验,实验成功率几乎可达100% (实验报告统计结果)。

图5 [Co(II)Salen]配合物的制备装置连接图

图6 稳压稳流装置流程图(左)和实物图(右)
(1) 稳压阀。
稳压阀的结构如图7所示。稳压阀为后面的针形阀提供稳定的气压,或为后面的稳流阀提供恒定的参考压力。旋转调节手柄,即可通过弹簧4将针阀2旋到一定的开度,当压力达到一定值时就处于平衡状态,当气体进口压力P1稍有增加时,P2处的压力也增加,波纹管就向右移动,并带动三根连动阀杆也向右移动,使阀开度变小,使出口压力P3维持不变,反之亦然。

图7 稳压阀示意图
(2) 稳流阀。
稳流阀的结构如图8所示。其工作原理是:针阀在输入压力保持不变的情况下旋到一定的开度,使流量维持不变。当进口压力P1稳定,两端的压力差ΔP=P3-P2,当ΔP等于弹簧压力时,膜片两边达到平衡。当出口压力P4增加时,流量降低。因为P1是恒定的,所以P1-P2小于弹簧压力,这时弹簧向上压动膜片,球阀开度增大,流量增加,P2也相应下降,直至P1-P2等于弹簧压力时,膜片又处于平衡,使气体流量维持不变。
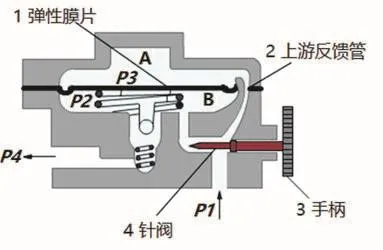
图8 稳流阀示意图
1.2 配合物载氧实验装置
[Co(II)Salen]配合物的载氧实验是基于非活性型的[Co(II)Salen]配合物在室温下不吸氧,而在某些极性溶剂中(如二甲基亚砜、二甲基甲酰胺、吡啶等)可与溶剂(L)配位转化为活性型配合物,进而能迅速吸氧形成1 : 2的氧加合物([Co(II)Salen]2L2O2)。载氧实验测定的是一定压力、温度下,当溶剂与[Co(II)Salen]接触时,体系中氧气的体积变化,然后根据公式pV=nRT求得所吸收氧的物质的量n。本文新设计的配合物载氧装置如图9所示,该装置是基于这一原理,在现行教材中的载氧装置(图2)的基础上进行的改进。

图9 本文改进的载氧装置流程图
该装置的主要特点有:
(1) 本装置中三通阀(吹扫阀)与二通阀(反应阀)并联,实现了对U型管的氧气吹扫,解决了传统装置U型管与反应器连接端不能完全排除空气的缺陷,使得装置完全充满氧气,测定的载氧数据更为科学准确。
(2) 本装置全部固定在面板上,且关键构件(三通阀、二通阀以及导气管)全部采用钢制结构,不仅仪器的气密性显著提高,而且很大程度上增加了仪器的使用寿命(图10)。

图10 本文改进的载氧装置
2 实验试剂与仪器
2.1 实验试剂
乙二胺、水杨醛、95%乙醇、四水合乙酸钴、N,N-二甲基甲酰胺(DMF)、三氯甲烷。均为分析纯。
2.2 实验仪器
三颈瓶、冷凝管、滴液漏斗、带支管三角烧瓶、布氏漏斗、抽滤瓶、U型管、电热套、电动搅拌器、气体稳压稳流装置、N2钢瓶、O2钢瓶、数字压力温度计。
3 实验步骤
3.1 [Co(II)Salen]配合物的制备
按图5所示仪器连接方法,将电热套、三颈瓶、电动搅拌器、冷凝管、滴液漏斗、气体稳压稳流装置及氮气钢瓶正确安装。
(1) 在三颈瓶中依次加入水杨醛(1.6 mL)、95%乙醇(80 mL)及乙二胺(0.5 mL),混合物室温搅拌4–5 min,此时生成亮黄色的双水杨缩乙二胺片状晶体。
(2) 溶解四水合乙酸钴(1.9 g)于热水(15 mL)中,将该溶液转移到滴液漏斗中。随后,打开氮气钢瓶,调节气体稳压稳流装置,向烧瓶中通入氮气3–5 min,赶尽其中的空气。接着,开回流水,加热使溶液微沸。
(3) 待亮黄色片状晶体全部溶解后,把乙酸钴溶液加入烧瓶中,立即生成棕色的胶状沉淀,在微沸下搅拌40–50 min。在这段时间内棕色沉淀慢慢转为暗红色晶体。
(4) 上述溶液依次冷却,抽滤,洗涤,干燥。最后称重并计算产率,测定产品红外光谱。
3.2 [Co(II)Salen]配合物的吸氧测定
(1) 装置气密性检查。关闭吹扫阀和集液阀,封住反应器上的放空口,打开反应阀,使反应器与U形管相通,向U形管敞口的一边加入少量水,使其左右有一液面差。如果U形管中的液面仅在开始时稍有下移,以后即维持恒定,这表明装置不漏气。
(2) 在三角瓶中加入[Co(II)Salen]配合物(0.05–0.1 g),滴液漏斗中加入DMF (5–8 mL)。关闭反应阀,旋转吹扫阀,使气体管路与U形管相通,打开氧气钢瓶,调节气体稳压稳流装置,通O2约3–5 min后,从U型管开口的一端加水封口。继续旋转吹扫阀,使气体管路与反应器相通,约3–5 min后,打开反应阀,封住反应器上的放空口,同时关闭吹扫阀,调节集液阀使U型管中两液面在同一水平,这时装置内的压力与大气压力相等,读取和体系相连一端U形管中液面的刻度。
(3) 将DMF从滴液漏斗中放出,并同时开启磁力搅拌器,一直到U形管中液面不再明显变化为止,这时给U型管中加水,使两液面相平,读取读数,此读数与第一次读数之差即为吸氧体积,读取此时的温度和大气压。重复上述操作,记录3组数据。由理想气体方程pV=n1RT,就可以求出氧气的物质的量n1。通过公式n2=W/M计算[Co(II)Salen]的物质的量n2,由n1和n2即可求得O2与[Co(II)Salen]的物质的量之比。
(4) 把上述氧加合物溶液转移到两个离心管中,然后在离心机上离心分离使沉淀沉积在离心管底部,小心除去上层溶液,得到暗褐色的加合物固体,沿管壁慢慢注入3 mL三氯甲烷,细心观察管内所发生的现象。
4 结果与讨论
4.1 [Co(II)Salen]配合物产率计算
乙二胺(99%)密度ρ:0.8995 g·cm-3;相对分子质量M:60 g·mol-1;体积V:0.5 mL。
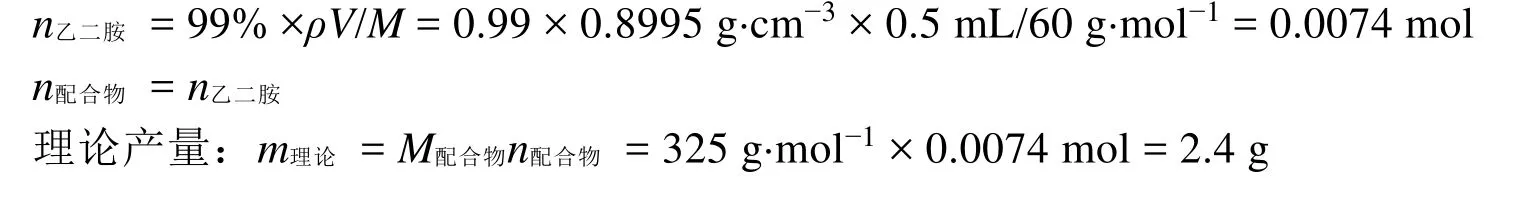
A组:

B组:
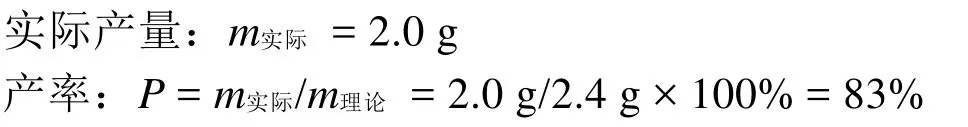
[Co(II)Salen]配合物的制备实验采用了气体稳压稳流装置,同时开展了两组合成实验(A组,B组),在实验过程中氮气可以稳定分配,两组实验能够独立进行,全部一次完成,且均具有较高的合成产率。通过红外光谱分析确定了[Co(II)Salen]配合物的主要官能团。由此可知,气体稳压稳流装置非常适于多组反应同时独立开展。
4.2 载氧量测定结果
室温:25.2 °C,大气压:93.13 kPa,室温时饱和水蒸汽压:3.278 kPa。
由理想气体方程pV=n1RT,测得一定温度和压力下吸收氧气的体积(表1),就可以求出O2的物质的量n1:
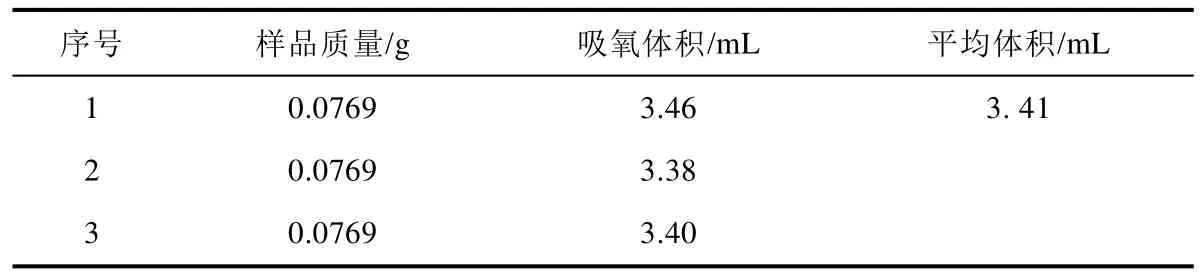
表1 载氧量测定结果
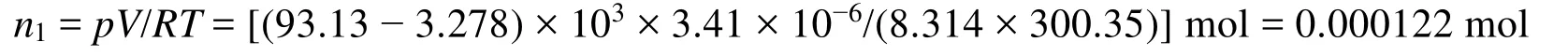
[Co(II)Salen]的物质的量n2:
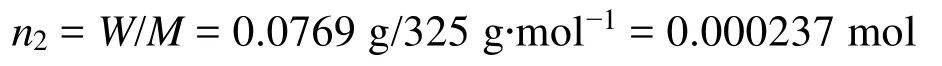
式中,W为[Co(II)Salen]配合物的质量,M为[Co(II)Salen]的摩尔质量(325 g·mol-1)。
O2: [Co(II)Salen]物质的量之比的计算:
n1:n2= 1 : 1.94
通过改进的载氧装置测定的O2: [Co(II)Salen]物质的量之比为1 : 1.94,而该载氧实验理论值为n1:n2= 1 : 2,相比于使用教材中的载氧装置所测定的实验值(n1:n2= 1 : 2.3–2.5),所得的实验数据重复性好且与理论值具有较高的吻合度。该载氧装置实现了在实验过程中操作简单、仪器使用寿命延长、数据准确度高等目标。
5 结语
本文对[Co(II)Salen]配合物的制备和载氧作用实验进行了创新设计,在气体钢瓶与[Co(II)Salen]配合物的制备实验装置间采用了气体稳压稳流装置,该设计保证了实验过程中气体的稳定分配,避免了多组学生同时开展实验过程中因采用常规三通连接而引起的气体供应不稳定而导致反应失败的情况。载氧装置的设计方式保证了实验过程中反应装置为纯氧气体系,所得的实验数据重复性好并与理论值具有较高的吻合度,实现了在实验过程中操作简单、仪器使用寿命延长、数据准确度高等目标。该实验使学生对[Co(II)Salen]配合物的制备过程、物化特性以及载氧机理有了更加深入的了解,显著提高了学生的知识综合运用能力。我们也希望通过这个改进实验,培育学生的创新意识,进而提高他们的创新能力。

