基于HPLC法测定三种不同剂型贞芪扶正产品中黄芪甲苷、毛蕊异黄酮葡萄糖苷、特女贞苷的含量
倪 琳,王 娟
(1.甘肃省药品检验研究院,甘肃 兰州 730030;2.甘肃兰药药业有限公司,甘肃 兰州 730046)
贞芪扶正系列产品(片剂、胶囊剂、颗粒剂)是由黄芪、女贞子2味中药组成的制剂,具有补气养阴的功效,具有提高人体免疫功能、保护骨髓和肾上腺皮质功能的功效,常用于各种疾病引起的虚损,可配合手术、放射线、化学治疗,促进正常功能的恢复[1-4]。贞芪扶正系列产品原有质量控制标准中,三个剂型原标准鉴别项、含量测定项中样品前处理繁琐,且采用的是薄层色谱扫描法测黄芪甲苷的含量,其样品斑点分离不好,测定数据不准确,误差较大。通过查阅文献[5-12],贞芪扶正系列产品一般采用LC-MS、HPLC法测定贞芪扶正胶囊中毛蕊异黄酮葡萄糖苷、黄芪甲苷、红景天苷等成分的含量,采用近红外光谱法对贞茂扶正颗粒进行快速鉴别等,但有关统一贞芪扶正片、贞芪扶正胶囊、贞芪扶正颗粒质量标准的研究,国内相关文献报道较少。本研究旨在建立简单的样品前处理HPLC法,统一贞芪扶正系列产品(片剂、胶囊剂、颗粒剂)中黄芪甲苷、毛蕊异黄酮葡萄糖苷、特女贞苷的含量测定方法,为贞芪扶正系列产品(片剂、胶囊剂、颗粒剂)的质量控制提供依据。
1 材料
1.1 仪器
电热恒温水浴锅(北京科伟永兴仪器有限公司);METTLER AE240型电子天平(瑞士梅特勒公司);薄层加热板(瑞士CAMAG公司);Waters ACQUITY ARC型高效液相色谱仪(美国Waters);硅胶G薄层板(青岛海洋化工厂)。
1.2 试药
1.2.1 对照品 黄芪甲苷对照品(批号110781-201717,以96.9%计),毛蕊异黄酮葡萄糖苷对照品(批号111920-201606,以97.6%计),特女贞苷对照品(111926-201605,以93.3%计),以上对照品均由中国食品药品检定研究院提供。
1.2.2 供试品 由甘肃兰药药业有限公司提供30批贞芪扶正系列产品(片剂、胶囊剂、颗粒剂);试剂:甲醇、乙腈均为色谱纯;其他试剂均为分析纯,水为纯化水。
2 方法与结果
2.1 黄芪甲苷的含量测定
2.1.1 色谱条件 色谱柱选用CAPCELL PAK C18(4.6 mm×250 mm,5 μm);流动相:乙腈-水(32∶68),蒸发光散射检测器检测;进样量:对照品溶液10 μL、25 μL,供试品溶液20 μL;柱温:30 ℃。理论板数按黄芪甲苷峰计算>4 000[13]。
2.1.2 对照品溶液的制备 精密称取黄芪甲苷对照11.60 mg至25 mL容量瓶中,加甲醇适量使溶解,定容,即得(此浓度适用于贞芪扶正片和贞芪扶正胶囊含量的计算)。再精密吸取2 mL至10 mL容量瓶中,加甲醇稀释至刻度,摇匀,即得(此浓度适用于贞芪扶正颗粒的含量计算)。
2.1.3 供试品溶液的制备 取贞芪扶正片样品20片,精密称定,研细,取约1.5 g,精密称定;取贞芪扶正胶囊样品10粒,精密称定,研细,取约1 g,精密称定;取贞芪扶正颗粒(无糖型)样品10袋,精密称定,研细,取约2 g,精密称定;分别置具塞锥形瓶中,精密加入含4%浓氨试液的80%甲醇溶液(取浓氨试液4 mL,加80%甲醇至100 mL,摇匀)50 mL,密塞,称定重量,加热回流1 h,放冷,再称定重量,用含4%浓氨溶液的80%甲醇溶液补足减失的重量,摇匀,滤过。精密量取续滤液25 mL,蒸干,残渣用80%甲醇溶解,转移至10 mL量瓶中,加80%甲醇至刻度,摇匀,滤过,取续滤液,即得。
取贞芪扶正颗粒(含糖型)样品10袋,精密称定,研细,取约5 g,精密称定,置具塞锥形瓶中,精密加入含4%浓氨试液的80%甲醇溶液(取浓氨试液4 mL,加80%甲醇至100 mL,摇匀)50 mL,密塞,称定重量,加热回流1 h,放冷,再称定重量,用含4%浓氨溶液的80%甲醇溶液补足减失的重量,摇匀,滤过。精密量取续滤液25 mL,蒸干,残渣加水10 mL,微热使溶解,用水饱和的正丁醇液提取4次,每次50 mL,合并正丁醇液,蒸干,转移至10 mL容量瓶,取上清液,用微孔滤膜过滤,即得。
2.1.4 阴性对照溶液的制备 按处方比例及工艺,取不含黄芪的阴性样品按上述供试品溶液的制备方法制成阴性对照溶液。
2.1.5 系统适应性试验 分别精密吸取对照品溶液、供试品溶液及阴性溶液各10 μL,按照“2.1.1”项下的色谱条件进行测定,见图1。结果样品中黄芪甲苷达到基线分离,且阴性无干扰。

注:A.对照品;B.供试品(贞芪扶正片);C.供试品(贞芪扶正胶囊);D.供试品(贞芪扶正颗粒无糖型);E.供试品(贞芪扶正颗粒含糖型);F.阴性对照(1.黄芪甲苷)。图1 黄芪HPLC图谱
2.1.6 线性关系考察 (1)贞芪扶正片和贞芪扶正胶囊线性关系考察:精密吸取黄芪甲苷对照品(0.449 6 mg/mL)1 mL、3 mL、4 mL分别置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(黄芪甲苷的浓度为0.044 96 mg/mL、0.134 88 mg/mL、0.179 85 mg/mL),各浓度进样体积为20 μL。精密吸取黄芪甲苷对照品(0.449 6 mg/mL)5 mL置10 mL
量瓶中,加甲醇稀释至刻度,摇匀,即得(黄芪甲苷的浓度为0.224 8 mg/mL),进样体积为30 μL。精密吸取黄芪甲苷对照品(0.449 6 mg/mL)1 mL置5 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(黄芪甲苷的浓度为0.089 92 mg/mL),进样体积为20 μL。以上得到系列进样量的黄芪甲苷对照品,测得峰面积的积分值,以峰面积的积分值的对数为纵坐标(logA),以对照品溶液的进样量(μg) 的对数为横坐标(logc),作图,得到经过原点的一条直线,回归方程:logA=2.149 8logc+3.846 6,r=0.996 5。结果表明,黄芪甲苷在0.899 2~6.744 2 μg范围内呈良好的线性关系。
(2)贞芪扶正颗粒线性关系考察:精密吸取黄芪甲苷对照品(0.089 9 mg/mL)2.5 mL、4 mL、5 mL分别置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(黄芪甲苷的浓度为0.022 5 mg/mL、0.035 97 mg/mL、0.044 96 mg/mL),各浓度进样体积为20 μL。精密吸取黄芪甲苷对照品(0.089 92 mg/mL)5 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(黄芪甲苷的浓度为0.044 96 mg/mL),进样体积为30 μL。精密吸取黄芪甲苷对照品(0.089 92 mg/mL)5 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(黄芪甲苷的浓度为0.044 96 mg/mL),进样体积为50 μL。以上得到系列进样量的黄芪甲苷对照品,测得峰面积的积分值,以峰面积的积分值的对数为纵坐标(logA),以对照品溶液的进样量(μg) 的对数为横坐标(logc),作图,得到经过原点的一条直线,回归方程:logA=1.183 0logc+4.462 0,r=0.998 6。结果表明,贞芪扶正颗粒中黄芪甲苷在0.449 6~2.248 1 μg范围内呈良好的线性关系。
2.1.7 精密度试验 精密吸取同一浓度对照品溶液20 μL,按照“2.1.1”项下的色谱条件连续进样6次,测定黄芪甲苷峰面积,RSD为1.39%,表明此方法精密度良好。
2.1.8 稳定性试验 精密吸取同一批号供试品溶液20 μL,每隔2 h进样测定1次,结果在12 h内,供试品(贞芪扶正片、贞芪扶正胶囊、贞芪扶正颗粒无糖型、贞芪扶正颗粒含糖型)溶液中黄芪甲苷峰面积稳定,RSD分别为3.03%、3.62%、1.03%、2.29%。
2.1.9 重复性试验 取同一批号(贞芪扶正片批号:20190405;贞芪扶正胶囊批号:J20170309;贞芪扶正颗粒(无糖型)批号:K20191129;贞芪扶正颗粒(含糖型)批号:K20200201)供试品按拟定的含量测定方法依法测定黄芪甲苷含量,独立测定6次,RSD分别为2.07%、1.27%、1.56%、1.94%。
2.1.10 加样回收率试验 精密称取已知含量[贞芪扶正片含黄芪甲苷1.213 3 mg/g、贞芪扶正胶囊含黄芪甲苷 2.414 4 mg/g、贞芪扶正颗粒(无糖型)含黄芪甲苷 0.546 5 mg/g、贞芪扶正颗粒(含糖型)含黄芪甲苷0.277 6 mg/g]的供试品适量[贞芪扶正片约0.75 g、贞芪扶正胶囊约0.5 g、贞芪扶正颗粒(无糖型)约1 g、贞芪扶正颗粒(含糖型)约2~3 g]6份,分别精密加入一定量的黄芪甲苷对照品溶液(浓度0.089 9 mg/mL、0.443 8 mg/mL、0.395 7 mg/mL、0.277 6 mg/mL),按供试品含量测定方法依次测定,结果测得黄芪甲苷的平均回收率分别为99.08%、97.06%、98.92%、97.06%,RSD分别为2.76%、2.74%、2.55%、2.74%(n=6)。见表1。

表1 贞芪扶正系列产品(片剂、胶囊剂、颗粒剂)片中黄芪甲苷的加样回收率试验 (n=6)
2.2 毛蕊异黄酮葡萄糖苷的含量测定
2.2.1 色谱条件 色谱柱选用CAPCELL PAK C18(4.6 mm×250 mm 5 μm);检测波长:260 nm;进样量:10 μL;柱温:30 ℃;流动相以乙腈-0.2%甲酸溶液(17∶83)为流动相;理论板数按毛蕊异黄酮葡萄糖苷峰计算>3 000[13]。
2.2.2 对照品溶液的制备 精密称取毛蕊异黄酮葡萄糖苷对照品11.00 mg(含量以97.6%计)置100 mL容量瓶中,加甲醇适量使溶解,定容至刻度。[此浓度适用于贞芪扶正片、贞芪扶正胶囊、贞芪扶正颗粒(无糖型)]。再精密吸取3 mL至10 mL容量瓶中,加甲醇至刻度摇匀,作为对照品溶液[此浓度适用于贞芪扶正颗粒(含糖型)],即得。
2.2.3 供试品溶液的制备 取贞芪扶正片样品20片,精密称定,研细,取约1.5 g,精密称定;取贞芪扶正胶囊样品10粒,精密称定,研细,取约1 g,精密称定;取贞芪扶正颗粒(无糖型) 样品10袋,精密称定,研细,取约2 g,精密称定;取贞芪扶正颗粒(含糖型)样品10袋,精密称定,研细,取约5 g,精密称定;置具塞锥形瓶中,精密加入甲醇25 mL,称定重量,加热回流4 h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,即得。
2.2.4 阴性对照溶液的制备 按处方比例及工艺,取不含黄芪的阴性样品按上述供试品溶液的制备方法制成阴性对照溶液。
2.2.5 系统适应性试验 分别精密吸取混合对照品溶液、供试品溶液及阴性溶液各10 μL,按照“2.2.1”项下的色谱条件进行测定,见图2。结果样品中毛蕊异黄酮葡萄糖苷达到基线分离,且阴性无干扰。

注:A.对照品;B.供试品(贞芪扶正片);C.供试品(贞芪扶正胶囊);.供试品(贞芪扶正颗粒无糖型);E.供试品(贞芪扶正颗粒含糖型);F.阴性对照(1.毛蕊异黄酮葡萄萄苷)。图2 黄芪HPLC图谱
2.2.6 线性关系考察 (1)贞芪扶正片、贞芪扶正胶囊、贞芪扶正颗粒(无糖型)线性关系考察:精密吸取毛蕊异黄酮葡萄糖苷对照品(0.107 4 mg/mL)2 mL、4 mL、6 mL、8 mL分别置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(毛蕊异黄酮葡萄糖苷的浓度为0.010 7 mg/mL、0.021 5 mg/mL、0.042 9 mg/mL、0.064 4 mg/mL、0.085 9 mg/mL、0.107 4 mg/mL),各浓度进样体积为10 μL。精密吸取毛蕊异黄酮葡萄糖苷对照品(0.107 4 mg/mL)6 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(毛蕊异黄酮葡萄糖苷的浓度为0.064 416 mg/mL),进样体积为20 μL。以上得到系列进样量的毛蕊异黄酮葡萄糖苷对照品,测得峰面积的积分值,以峰面积的积分值为纵坐标(A),以对照品溶液的进样量(μg)为
横坐标(C),作图,得到经过原点的一条直线,回归方程:A=3.430 4×106C+5.322 0×104,r=0.999 7。结果表明,贞芪扶正片、贞芪扶正胶囊、贞芪扶正颗粒(无糖型)中含毛蕊异黄酮葡萄糖苷在0.214 7~1.288 3 μg范围内呈良好的线性关系。
(2)贞芪扶正颗粒(含糖型)线性关系考察:精密吸取毛蕊异黄酮葡萄糖苷对照品(0.032 2 mg/mL)2 mL、4 mL、6 mL、8 mL分别置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(毛蕊异黄酮葡萄糖苷的浓度为0.006 4 mg/mL、0.012 9 mg/mL、0.019 3 mg/mL、0.025 8 mg/mL、0.322 1 mg/mL),各浓度进样体积为10 μL。精密吸取毛蕊异黄酮葡萄糖苷对照品(0.032 2 mg/mL)6 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(黄芪甲苷的浓度为0.019 32 mg/mL),进样体积为20 μL。以上得到系列进样量的毛蕊异黄酮葡萄糖苷对照品,测得峰面积的积分值,以峰面积的积分值为纵坐标(A),以对照品溶液的进样量(μg)为横坐标(C),作图,得到经过原点的一条直线,回归方程:A=3.424 2×106C+1.875 4×104,r=0.999 7。结果表明,贞芪扶正颗粒(含糖型)中毛蕊异黄酮葡萄糖苷在0.064 4~0.386 5 μg范围内呈良好的线性关系。
2.2.7 精密度试验 取同一浓度毛蕊异黄酮葡萄糖苷对照品溶液(浓度为0.042 9 mg/mL),进样量:10 μL,注入液相色谱仪,连续进样6次,测定毛蕊异黄酮葡萄糖苷峰面积,RSD为0.21%,表明此方法精密度良好。
2.2.8 稳定性试验 取同一供试品溶液(贞芪扶正片批号:20190405;贞芪扶正胶囊批号:J20191004;贞芪扶正颗粒(无糖型)批号:K20191129;贞芪扶正颗粒(含糖型)批号:K20170311),每隔2h进样1次,结果在12 h内,供试品溶液中毛蕊异黄酮葡萄糖苷峰面积稳定,RSD分别为0.33%、0.26%、0.61%、0.54%。
2.2.9 重复性试验 取同一批号[贞芪扶正片批号:20190405;贞芪扶正胶囊批号:J20191004;贞芪扶正颗粒(无糖型)批号:K20191129;贞芪扶正颗粒(含糖型)批号:K20170311]供试品按拟定的含量测定方法依法测定毛蕊异黄酮葡萄糖苷含量,独立测定6次,RSD分别为0.76%、1.30%、0.78%、0.87%。
2.2.10 加样回收率试验 精密称取已知含量的供试品适量[贞芪扶正片约0.5 g、贞芪扶正胶囊约0.2~0.3 g、贞芪扶正颗粒(无糖型)约0.4 g、贞芪扶正颗粒(含糖型)约0.4~0.6 g]6份,分别精密加入一定量的毛蕊异黄酮葡萄糖苷对照品溶液(浓度0.107 4 mg/mL),按供试品含量测定方法依次测定,结果测得毛蕊异黄酮葡萄糖苷的平均回收率为97.83%、98.27%、98.78%、98.71%;RSD为3.08%、2.74%、2.12%、2.57%(n=6)。见表2。

表2 贞芪扶正系列产品(片剂、胶囊剂、颗粒剂)片中毛蕊异黄酮葡萄糖苷的加样回收率试验 (n=6)
2.3 特女贞苷的含量测定
2.3.1 色谱条件 色谱柱选用CAPCELL PAK C18(4.6 mm×250 mm 5 μm);进样量:5 μL;柱温:30 ℃。流动相:以甲醇-水(40∶60)为流动相,检测波长为224 nm。理论板数按特女贞苷峰计算>4 000[13]。
2.3.2 对照品溶液的制备 取特女贞苷对照品适量,精密称定,加甲醇制成每1 mL含0.079 9 mg的溶液,即得。
2.3.3 供试品溶液的制备 贞芪扶正片:取20片,精密称定,研细,取约1 g;贞芪扶正胶囊:取本品10粒,精密称定,研细,取约1 g;贞芪扶正颗粒(无糖型)取本品10袋,精密称定,研细,取约2 g,贞芪扶正颗粒(含糖型)取约5 g,精密称定,分别置具塞锥形瓶中,精密加入稀乙醇25 mL,称定重量,加热回流1 h,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,即得。
2.3.4 阴性对照溶液的制备 按处方比例及工艺,取不含女贞子的阴性样品按上述供试品溶液的制备方法制成阴性对照溶液。
2.3.5 系统适应性试验 分别精密吸取混合对照品溶液、供试品溶液及阴性溶液各10 μL,按照“2.3.1”项下的色谱条件进行测定,见图3。结果样品中特女贞苷达到基线分离,且阴性无干扰。

注:A.对照品;B.供试品(贞芪扶正片);C.供试品(贞芪扶正胶囊);D.供试品(贞芪扶正颗粒无糖型);E.供试品(贞芪扶正颗粒含糖型);F.阴性对照(1.特女贞苷)。图3 女贞子 HPLC图谱
2.3.6 线性关系考察 精密吸取特女贞苷对照品(0.082 8 mg/mL)2 mL、4 mL、6 mL、8 mL分别置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(特女贞苷的浓度为0.016 556 mg/mL、0.033 1 mg/mL、0.049 7 mg/mL、0.066 2 mg/mL、0.082 8 mg/mL),各浓度进样体积为10 μL。精密吸取特女贞苷对照品(0.082 8 mg/mL)6 mL置10 mL量瓶中,加甲醇稀释至刻度,摇匀,即得(特女贞苷的浓度为0.049 7 mg/mL),进样体积为20 μL。以上得到系列进样量的特女贞苷对照品,测得峰面积的积分值,以峰面积的积分值为纵坐标(A),以对照品溶液的进样量(μg)为横坐标(C),作图,得到经过原点的一条直线,回归方程:A=1.323 2×106C+1.403×103,r=0.999 8。结果表明,贞芪扶正系列产品中含特女贞苷在0.165 5~0.993 3 μg范围内呈良好的线性关系。
2.3.7 精密度试验 取同一浓度特女贞苷对照品溶液(浓度为0.082 8 mg/mL),进样量:5 μL,注入液相色谱仪,连续进样6次,测定特女贞苷峰面积,RSD为0.25%,表明此方法精密度良好。
2.3.8 稳定性试验 取同一供试品溶液[贞芪扶正片批号:20190405;贞芪扶正胶囊批号:J20190619;贞芪扶正颗粒(无糖型)批号:K20170222;贞芪扶正颗粒(含糖型)批号:K20170355],每隔2 h进样1次,结果在12 h内,供试品溶液中特女贞苷峰面积稳定,RSD分别为0.35%、1.81%、0.26%、0.35%。
2.3.9 重复性试验 取同一批号[贞芪扶正片批号:20190405;贞芪扶正胶囊批号:J20191004;贞芪扶正颗粒(无糖型)批号:K20191129;贞芪扶正颗粒(含糖型)批号:K20170311]供试品按拟定的含量测定方法依法测定特女贞苷含量,独立测定6次,RSD分别为0.48%、1.55%、1.16%、1.03%。
2.3.10 加样回收率试验 精密称取已知含量的供试品适量[贞芪扶正片约0.1~0.2 g、贞芪扶正胶囊约0.1 g、贞芪扶正颗粒(无糖型)约0.2~0.4 g、贞芪扶正颗粒(含糖型)约0.5~0.7 g]6份,分别精密加入一定量的特女贞苷对照品溶液,按供试品含量测定方法依次测定,结果测得特女贞苷的平均回收率分别为99.62%、98.28%、97.01%、101.37%,RSD分别为2.13%、2.61%、1.67%、3.03%(n=6)。见表3。
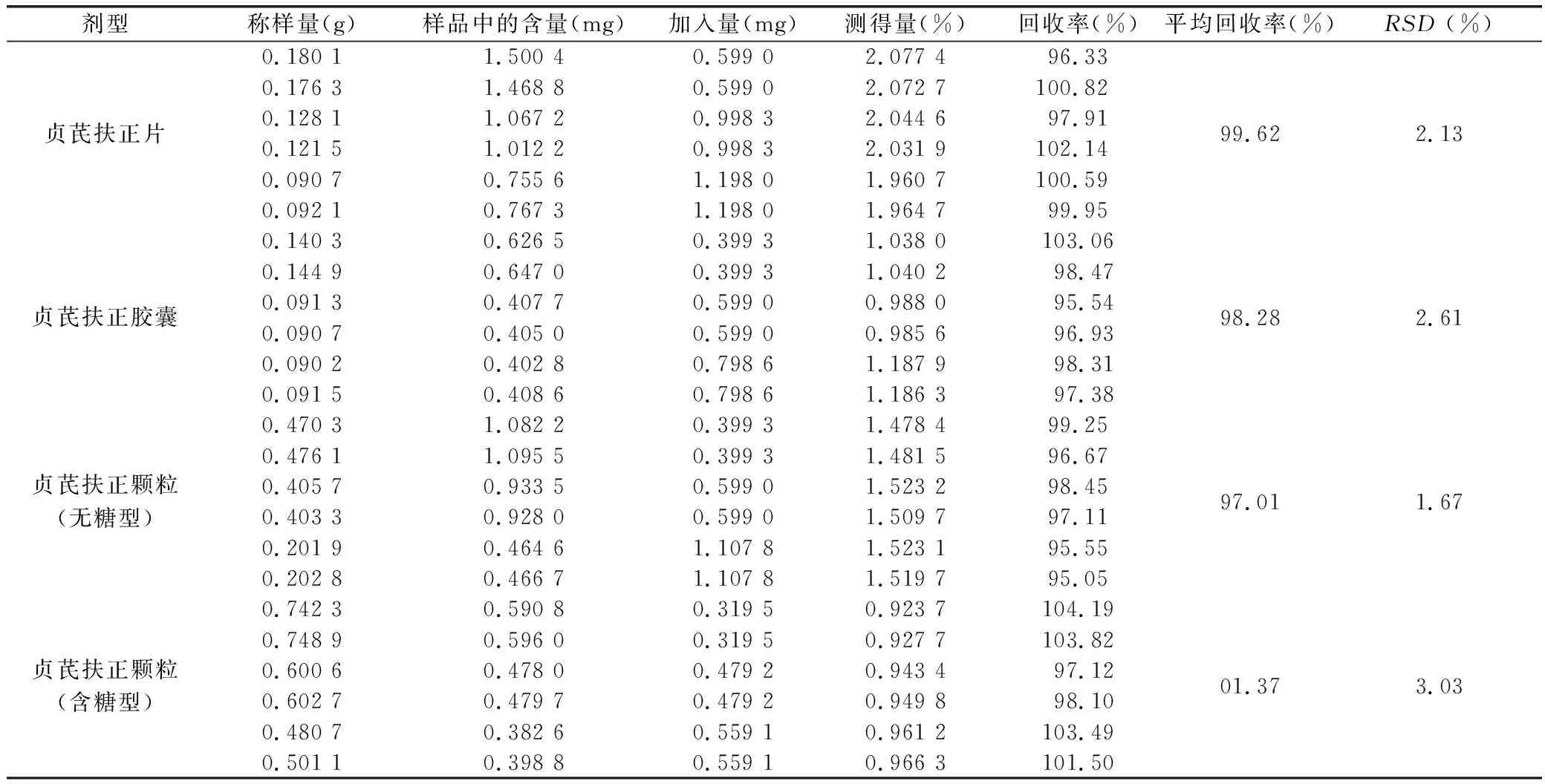
表3 贞芪扶正系列产品中特女贞苷的加样回收率试验 (n=6)
2.3.11 样品的测定 按“2.1.3”“2.2.3”“2.3.3”项下方法制备供试品溶液,分别进样,测定峰面积,计算贞芪扶正系列产品中黄芪甲苷、毛蕊异黄酮葡萄糖苷、特女贞苷的含量。见表4。

表4 贞芪扶正系列产品中黄芪甲苷、毛蕊异黄酮葡萄糖苷、特女贞苷的含量测定结果
3 讨论
(1)样品中毛蕊异黄酮葡萄糖苷的提取方法的选择。采用甲醇超声和加热回流提取样品、稀乙醇加热回流和甲醇加热回流提取样品,采用甲醇分别测定不同提取时间:超声1 h、1.5 h以及加热回流1 h、2 h、4 h、5 h样品中毛蕊异黄酮葡萄糖苷的含量,结果采用甲醇加热回流4 h提取样品中毛蕊异黄酮葡萄糖苷的含量较高。采用稀乙醇和甲醇分别加热回流4 h提取样品中毛蕊异黄酮葡萄糖苷,结果采用甲醇加热回流4 h提取样品中毛蕊异黄酮葡萄糖苷的含量较高,故本研究采用甲醇溶液加热回流4 h的提取方法。
(2)样品中黄芪甲苷的提取时间的确定。采用含4%氨试液的80%甲醇溶液超声和加热回流提取样品,分别测定不同提取时间:超声30 min、40 min、60 min、90 min以及加热回流1 h、2 h样品中黄芪甲苷的含量,结果加热回流1 h样品中黄芪甲苷的含量较高,故本研究采用含4%氨试液的80%甲醇溶液加热回流1 h的提取方法。
(3)色谱柱的选择。选用Capcell pak C18色谱柱、Diamonsil C18色谱柱、Phenomenex C18色谱柱3 个不同品牌色谱柱测定样品中黄芪甲苷、毛蕊异黄酮葡萄糖苷、特女贞苷的含量基本一致,结果3个品牌色谱柱均能使样品中3种成分达到基线分离,且重现性较好,能够满足系统适用性试验要求。

