甘青青兰质量标准的研究
范莹莹马青青杨凤梅张炜骆桂法
(青海省药品检验检测院,青海省中藏药现代化研究重点实验室,国家药品监督管理局中药藏药质量控制重点实验室,青海 西宁810016)
甘青青兰又名“唐古特青兰”“陇塞青兰”,是藏医习用药,常用于治疗肝炎、胃炎、黄水类病,为唇形科植物甘青青兰Dracocephalum tanguticumMaxim 的干燥地上部分,始载于《四部医典》,生长在海拔3 000~4 600 m 的河谷阶地、荒坡草滩、灌丛林缘,产于西藏东部、青海和甘肃西南部,四川西部[1-3],主要有黄酮、萜类、多糖、无机元素、挥发油等成分[4-6],具有抗缺氧、抗菌、抗病毒、降血糖等作用[7-12],作为藏族民间常用药大多入丸、散剂,常用相关品种有大月晶丸、秘诀清凉散、二十六味通经胶囊等,临床上还用其花季鲜全草提取的精油外涂加穴位按摩,用于亚健康的赤巴症调理。但现行标准(《卫生部药品标准》 1995 年版藏药第一册)中甘青青兰项下仅有基原、性状、鉴别项,专属性不强,缺乏必要的定量控制指标,无法有效控制药材质量,目前也鲜有相关报道。因此,在参考甘青青兰及其近似种研究的基础上,本实验建立了该药材定性鉴别和定量测定方法,可为其整体质量控制提供科学依据。
1 材料
Linomat 5 半自动薄层点样仪(瑞士卡玛公司);LC-20A 高效液相色谱仪,配置PDA 检测器(日本岛津公司);E2695 型高效液相色谱仪,配置2998PDA 检测器(美 国 Waters公司);PURELAB Ultra Mk2 型纯水仪(威立雅水处理技术有限公司);AR5120 型电子天平(美国奥豪斯公司);AUW220D 型电子天平(日本岛津公司);DT1028 CH 超声波提取器(德国Bandelin 公司)。聚酰胺薄膜(浙江台州四甲生化塑料厂);Silica gel 60 型高效硅胶薄层层析板(德国Merck 公司);硅胶G 薄层板(青岛海洋化工厂或自制)。甘青青兰对照药材(批号121529-201102)、齐墩果酸对照品(批号110709-201607)、绿原酸对照品(批号110753-201817,纯度96.8%)均购自中国食品药品检定研究院;胡麻素-6-O-葡萄糖苷对照品(纯度≥98%)由中国科学院西北高原生物研究所研制并提供。本实验从青海、甘肃、西藏、四川各地采集甘青青兰共18批,经西北高原生物研究所卢学峰教授鉴定为正品。乙腈为色谱纯;其余试剂均为分析纯;水为超纯水。
2 方法与结果
2.1 TLC 定性鉴别
2.1.1 齐墩果酸 取甘青青兰药粉约1 g,加入10 mL 无水乙醇,超声处理30 min,滤过,滤液通过活性炭小柱,浓缩至约2 mL,作为供试品溶液;取甘青青兰对照药材1 g,同法制备对照药材溶液;取齐墩果酸对照品约5 mg,精密称定,无水乙醇制成每1 mL 含1 mg 该成分的溶液,作为对照品溶液。吸取以上3 种溶液各5 μL,点样于gel 60 型高效硅胶薄层色谱板上,以甲苯-乙酸乙酯-冰醋酸(14∶4∶0.5)为展开剂,展开,取出,晾干,10%硫酸乙醇溶液显色,加热至斑点清晰后在紫外灯(365 nm)下检查,结果见图1。由此可知,在甘青青兰对照药材、齐墩果酸对照品相应位置上,各批样品均显示相同的橙红色荧光斑点。

图1 齐墩果酸TLC 色谱图Fig.1 TLC chromatogram of oleanolic acid
2.1.2 绿原酸 取甘青青兰药粉约0.5 g,加入20 mL 甲醇,超声处理30 min,滤过,蒸干滤液,加2 mL 甲醇溶解残渣,作为供试品溶液;再取0.5 g 甘青青兰对照药材,同法制备对照药材溶液;取绿原酸对照品约5 mg,精密称定,甲醇制成每1 mL含1 mg 该成分的溶液,作为对照品溶液。吸取上述3 种溶液各1 μL,点样于同一聚酰胺薄膜上,以甲苯-甲酸乙酯-丙酮-甲醇-甲酸(30∶5∶5∶20∶1)为展开剂,展开,取出,晾干,在紫外灯(365 nm)下检视,结果见图2。由此可知,在与甘青青兰对照药材、绿原酸对照品相应位置上,各批样品均显示相同的蓝色荧光斑点。

图2 绿原酸TLC 色谱图Fig.2 TLC chromatogram of chlorogenic acid
2.2 HPLC 定量测定
2.2.1 色谱条件与系统适用性试验 Waters XBridge C18色谱柱(250 mm×4.6 mm,5 μm);流动相乙腈(A)-0.1% 甲酸(B),梯度洗脱(0~20 min,95%~85% B;20~25 min,85%~82% B;25~50 min,82%B);体积流量1.0 mL/min;柱温30 ℃;检测波长325 nm,色谱图见图3。理论塔板数按绿原酸峰计,不低于3 000。

图3 各成分HPLC 色谱图Fig.3 HPLC chromatograms of various constituents
2.2.2 对照品溶液制备 精密称取绿原酸、胡麻素-6-O-葡萄糖苷对照品适量,50% 甲醇制成每1 mL分别含两者233.3、207.7 μg 的贮备液,取适量,50% 甲醇制成每1 mL 分别含两者116.6、83.1 μg的溶液,即得。
2.2.3 供试品溶液制备 取甘青青兰粉末(过3号筛)约0.5 g,精密称定,置于具塞三角瓶中,精密加入50 mL50%甲醇,超声(功率200 W、频率40 kHz)处理30 min,50% 甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.2.4 线性关系考察 精密吸取“2.2.2”项下对照品溶液 2、4、10、12、16、20 μL,在“2.2.1”项色谱条件下进样测定。以峰面积积分值(Y)对进样量(X)进行回归,得绿原酸、胡麻素-6-O-葡萄糖苷方程分别为Y=3.067×106X+5.962×103(r=0.999 9)、Y=1.976×106X-3.669×104(r=0.999 9),分别在0.23~2.33、0.17~1.67 μg 范围内线性关系良好。
2.2.5 精密度试验 精密吸取“2.2.2”项下对照品溶液10 μL,在“2.2.1”项色谱条件下进样测定6次,测得绿原酸、胡麻素-6-O-葡萄糖苷峰面积RSD 分别为0.2%、0.1%,表明仪器精密度良好。
2.2.6 稳定性试验 精密吸取同一份供试品溶液(1 号)10 μL,于0、2、4、8、16、24 h 在“2.2.1”项色谱条件下进样测定,测得绿原酸、胡麻素-6-O-葡萄糖苷峰面积RSD 分别为0.2%、0.3%,表明溶液在24 h 内稳定性良好。
2.2.7 重复性试验 取同一批本品(1 号)6份,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定,测得绿原酸、胡麻素-6-O-葡萄糖苷含量RSD 分别为0.6%、0.4%,表明该方法重复性良好。
2.2.8 耐用性试验 选择沃特世e2695 高效液相色谱 仪(Agilent Extend C18色谱柱,4.6 mm ×250 mm,5 μm)、安捷伦高效液相色谱仪(Agilent ECLIPSE XDB C18色谱柱,4.6 mm × 250 mm,5 μm)、岛津LC20AT 高效液相色谱仪(Waters XBridge C18色谱柱,4.6 mm×250 mm,5 μm),在“2.2.1”项色谱条件下进样测定。结果,供试品溶液中各成分色谱峰的峰形对称,分离度良好,可满足实验要求。
2.2.9 加样回收率试验 取各成分含量已知(绿原酸8.92 mg/g、胡麻素-6-O-葡萄糖苷8.30 mg/g)的甘青青兰粉末6份,每份约0.25 g,精密称定,置于具塞三角瓶中,精密加入含绿原酸、胡麻素-6-O-葡萄糖苷0.045 48、0.041 02 mg/mL 的50%甲醇50 mL,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下各进样10 μL 测定,计算回收率,结果见表1。
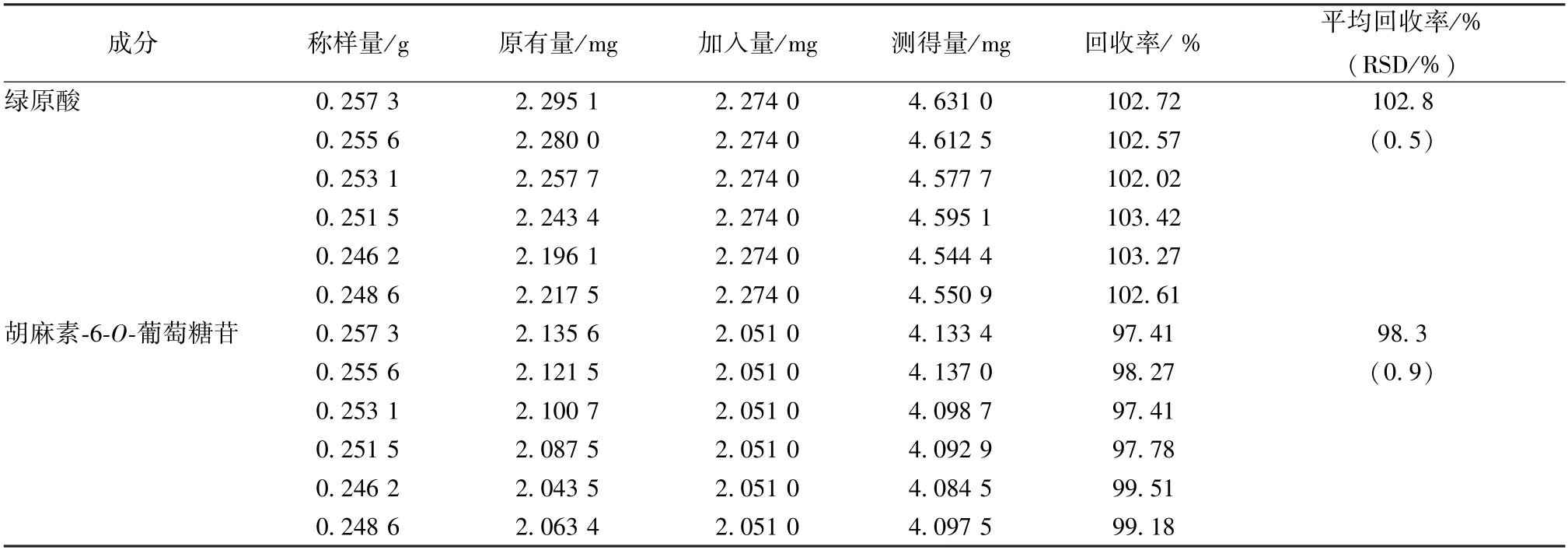
表1 各成分加样回收率试验结果(n=6)Tab.1 Results of recovery tests for various constituents(n=6)
2.2.10 样品含量测定 取18 批甘青青兰,每批2份,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下各进样10 μL 测定,外标法计算含量,结果见表2。
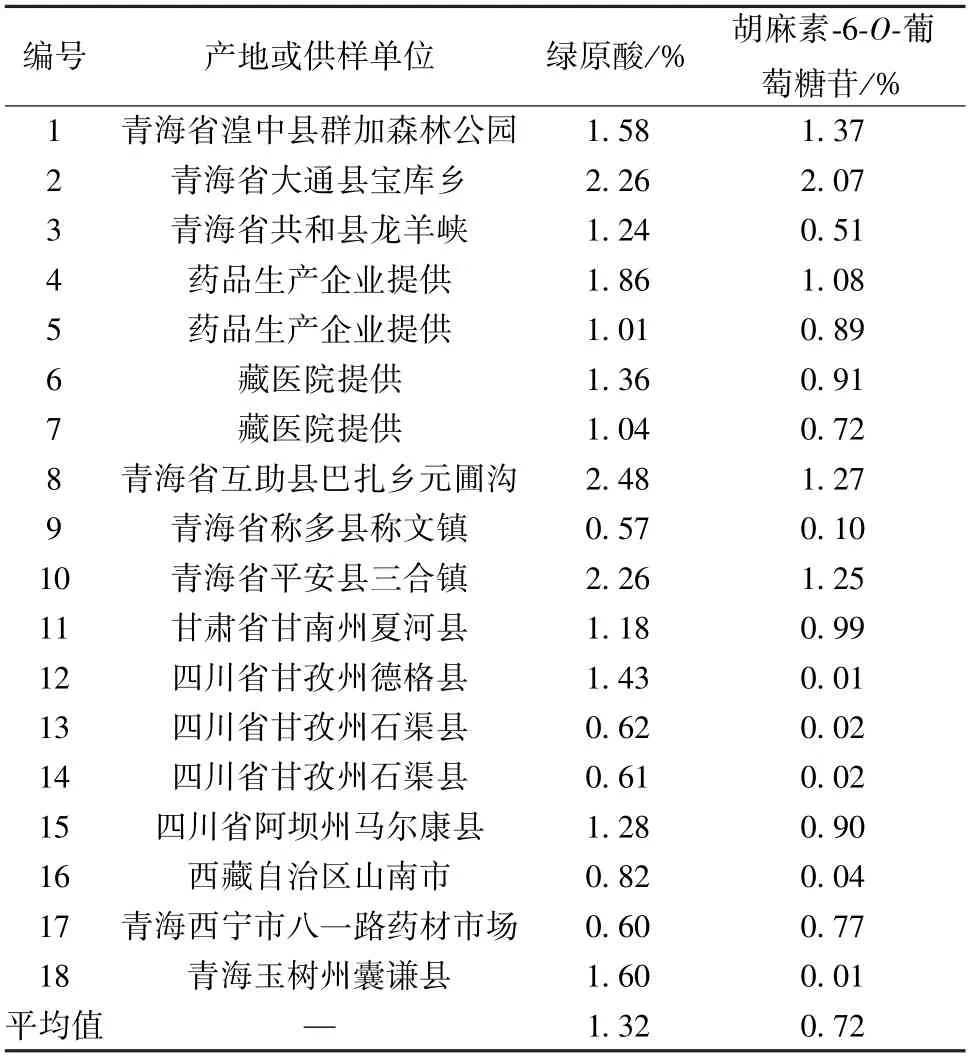
表2 各成分含量测定结果(n=2)Tab.2 Results of content determination of various constituents(n=2)
3 讨论
3.1 TLC 定性鉴别 本实验选择甘青青兰中的萜类化合物齐墩果酸、苯丙素类化合物绿原酸作为指标成分,固定相分别采用硅胶G 薄层板、聚酰胺薄膜,还增加了对照药材,可提高TLC 法专属性。同时,分别采用不同厂家生产的硅胶G 薄层板、聚酰胺薄膜,在不同温度、相对湿度下进行耐用性实验,发现不同条件下上述2 种成分均得到较好的分离,主斑点清晰,Rf值适中。
3.2 HPLC 定量测定 本实验选择绿原酸、胡麻素-6-O-葡萄糖苷作为指标成分,其中前者具有抗菌、抗病毒、降脂、降糖、保护心血管等作用[13-16],与甘青青兰药效相关,是药材有效成分,而后者相关文献报道较少。结果,绿原酸含量在0.57%~2.48%范围内,平均1.32%;胡麻素-6-O-葡萄糖苷含量在0.01%~2.07% 范围内,平均0.72%,由于后者地域差异明显,药理作用不明确,故不建议列入甘青青兰质量标准草案。另外,由于梯度洗脱耗时、不环保,故采用等度洗脱对绿原酸含量进行测定,并规定其限度为按干燥品计算,不得低于1.0 %。
——基于CMS 模型的实证分析

