骨桥蛋白在不同病理分期原发性胆汁性胆管炎的表达特点分析
王彦坤 马俊骥
原发性胆汁性胆管炎(primary biliary cholangitis, PBC)是一种慢性胆汁淤积性肝病,其病因尚不清楚,以免疫介导的胆道损伤和慢性胆汁淤积为特征[1]。肝脏组织标本中出现肝内胆管损伤及纤维化等改变是PBC病理分期的重要依据,据此可以将PBC分为4期[2]。由PBC引起的肝硬化在肝组织病理分期中为第4期,此时可能会伴有多种并发症,终末期甚至需要肝移植治疗。
骨桥蛋白(osteopontin,OPN)是一种糖蛋白,又称为分泌型磷蛋白1(secreted phosphoprotein 1,SPP1),由人类SPP1基因编码。SPP1基因位于染色体4的4q13.22位点,经过转录后OPN被选择性剪接,可以形成OPN-a、OPN-b、OPN-c、OPN-4和OPN-5五种异构体,其中OPN-a被认为是典型的转录本[3-5]。Fam20C介导的骨桥蛋白磷酸化是骨桥蛋白分泌的关键,肝硬化患者肝硬度与血清OPN表达密切相关[6-7]。研究显示肝脏炎症可以通过OPN促成巨噬细胞活化,OPN参与了内源性调控肝脏摄取过多的脂质以保护肝脏免受脂质毒性、细胞凋亡及相关的肝纤维化发生,从而保证肝细胞的存活,但也可能会导致分化型肝癌[8-9]。在PBC引起的肝硬化肝组织中检测发现,OPN在肉芽肿和损伤的胆管周围单核细胞胞质为强表达[10]。本研究通过免疫组织化学方法检测不同PBC病理分期肝组织OPN的表达情况,探讨OPN在PBC疾病进展过程中的作用。
资料与方法
一、研究对象
收集2013年12月至2020年1月首都医科大学附属北京佑安医院70例PBC患者的病理资料。PBC诊断需满足以下条件中的至少2条:①ALP>150 U/L;②抗线粒体抗体(anti-mitochondrial antibody, AMA )阳性,或其他 PBC特异性自身抗体如抗gP210抗体、抗spl00抗体中任意一项呈阳性(血清AMA阴性时);③肝组织病理检查提示非化脓性胆管炎和小叶间胆管破坏[2]。患者肝组织病理检查均签署知情同意书,研究符合伦理要求。
二、方法
评估PBC肝脏不同病理分期组织病变和纤维化选用HE、Masson和Gomori银染方法。CK19、CK7和OPN抗体用来研究PBC肝组织胆管损伤情况和OPN表达特点,免疫组织化学染色步骤参照文献[11-13]。OPN抗体购自abcam公司,CK7和CK19免疫组织化学染色抗体购自北京金桥雅图生物技术有限公司,OPN、CK7和CK19阳性部位均位于细胞质。根据OPN阳性细胞数百分比和细胞平均染色强度进行综合评分[14]。阳性细胞比例得分:0=无,1=<1%,2=1%~1/10,3=1/10至1/3,4=1/3~2/3,5=>2/3。阳性细胞平均染色强度得分:0=无,1=弱,2=中,3=强。综合评分计算分析后1~3分的OPN被认为是低表达,4~6分的OPN被认为是中度表达,7~8分的OPN被认为是高表达。
三、 统计学处理
结 果
一、一般资料
70例患者血清AMA均阳性,其中男性10例,年龄为(53±9)岁,女性60例,年龄为(51±11)岁,男性和女性患者年龄差异无统计学意义(P=0.594)。
PBC病理1期患者18例,男性4例,女性14例,年龄(48±12)岁;2期17例,男性3例,女性14例,年龄(48±12)岁;3期18例,男性2例,女性16例,年龄(53±9)岁;4期17例,男性1例,女性16例,年龄(56±7)岁,与1期PBC患者年龄相比,年龄较大,差异有统计学意义(P=0.026)。
二、随着PBC病程进展,肝纤维化和胆管损伤逐渐加重
肝脏穿刺病理标本是进行PBC病理分期的重要依据。通过HE、Masson和Gomori银染方法可以初步判断汇管区和肝小叶损伤情况,并评估肝纤维化进展程度(图1)。PBC病理1期可以看到汇管区炎症,部分可见汇管区肉芽肿,肝小叶基本完整、无明显纤维化形成。随着PBC病程进展,病理分期会逐步增加。在病理2期可以看到汇管区局灶性界板炎以及纤维化组织深入肝实质。在病理3期可以看到明显的肝纤维化和肝脏胆汁淤积。到第4期可以看到明显的肝硬化病理改变,以及毛细胆管胆栓形成。
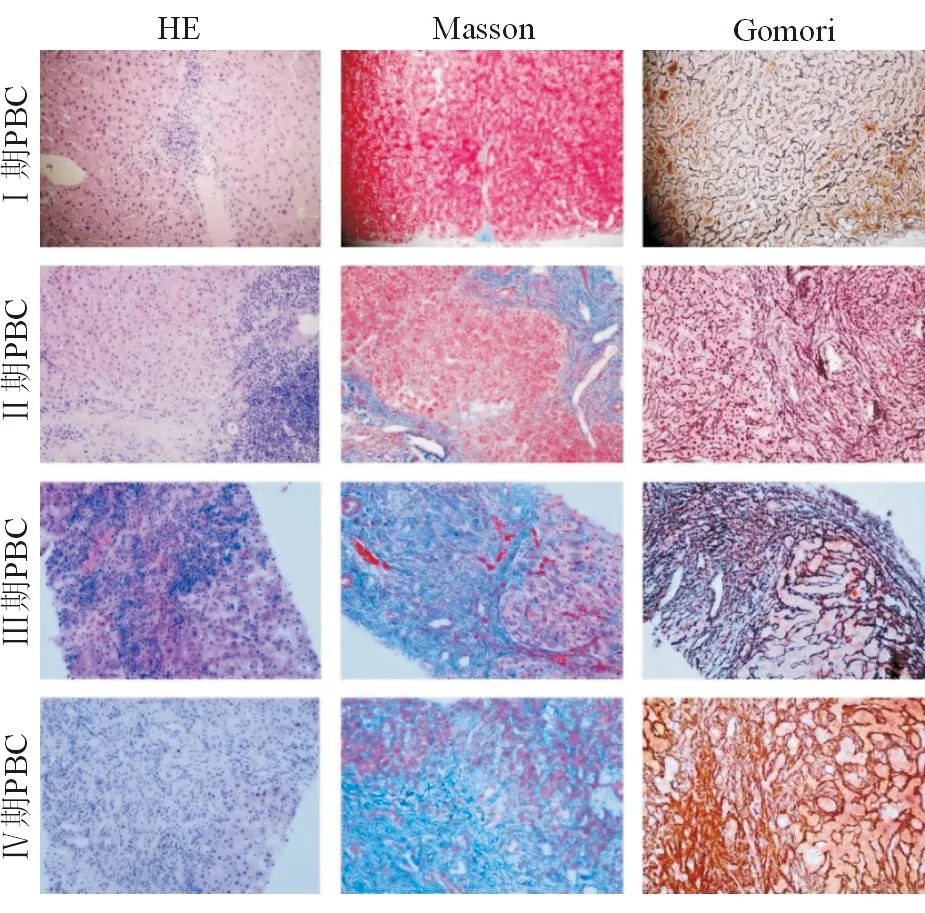
图1 采用HE、Masson和Gomori银染方法判断汇管区和肝小叶损伤情况,并评估肝纤维化进展程度(200×)
非化脓性胆管炎和小叶间胆管破坏是PBC典型的病理改变。本研究采用CK7和CK19抗体进行肝组织免疫组织化学染色结合评估导管反应(DR)和具有胆管化生倾向的中间肝细胞,以帮助判断不同PBC病理分期胆管损伤、肝组织胆汁淤积情况(图2)。在PBC病理1期肝组织切片汇管区看到受损的胆管,周围可见炎症细胞浸润,胆汁淤积相对较轻。在病理2期可以看到汇管区大量的胆管反应性增生的情况发生,周围新生肝细胞。病理3期汇管区胆管消失情况很常见。在第4期肝硬化阶段,汇管区胆管缺少情况更加严重,周围大量新生CK7阳性的肝细胞,同样提示胆汁淤积很严重。
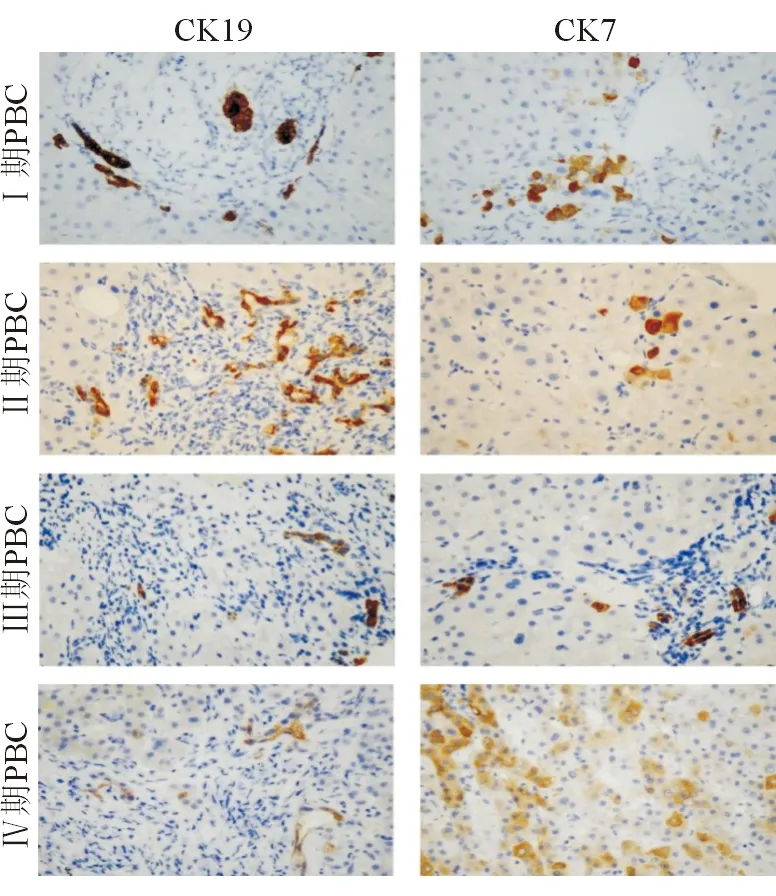
图2 肝穿刺组织CK7和CK19免疫组织化学染色结果(400×)
三、在PBC病程进展后OPN表达增多,在不同病理分期存在不一样的分布特点
免疫组织化学分析发现,OPN在男性患者中的强表达比率为20.00%,而在女性患者中OPN的强表达比率为41.67%,差异无统计学意义(χ2=0.907,P=0.341),见表1。
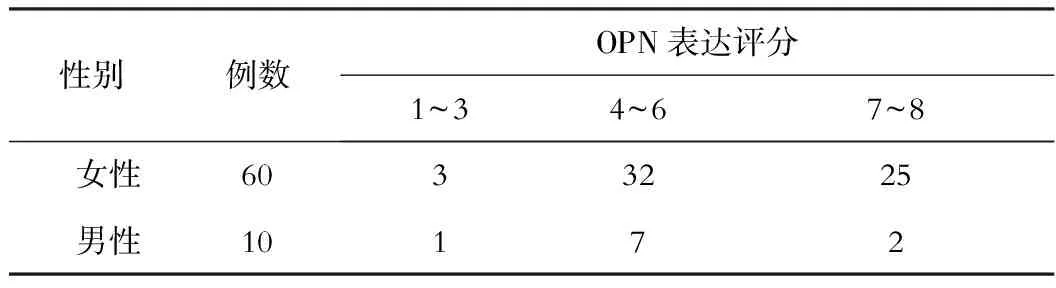
表1 肝组织OPN表达评分在PBC患者中的性别差异
在1期PBC和2期PBC肝组织,OPN以中度表达为主,分别为72.22%和76.47%,也存在一部分低表达病例(分别为11.11%和5.88%)。PBC 1至3期OPN免疫组化评分强表达的比率分别为11.11%、17.65%和83.33%;1期和2期比较差异无统计学意义(χ2=0.005,P=0.945),3期比1期明显增加(χ2=12.586,P<0.01),3期比2期也明显增加(χ2=21.394,P<0.01)。OPN在4期PBC中的强表达比率为41.18%,中度表达比率为58.82%。OPN在4期PBC中的强表达与1期(χ2=0.907,P=0.341)和2期(χ2=0.907,P=0.341)相比差异无统计学意义,与3期相比则明显下降(χ2=4.972,P=0.026)。见表2。

表2 肝组织OPN表达评分在PBC不同病理分期中的表达分布情况
OPN阳性细胞在1期PBC汇管区偶尔可以看到。与1期PBC不同,在PBC第2期至第4期肝组织汇管区中的OPN阳性细胞数均明显增多(图3)。
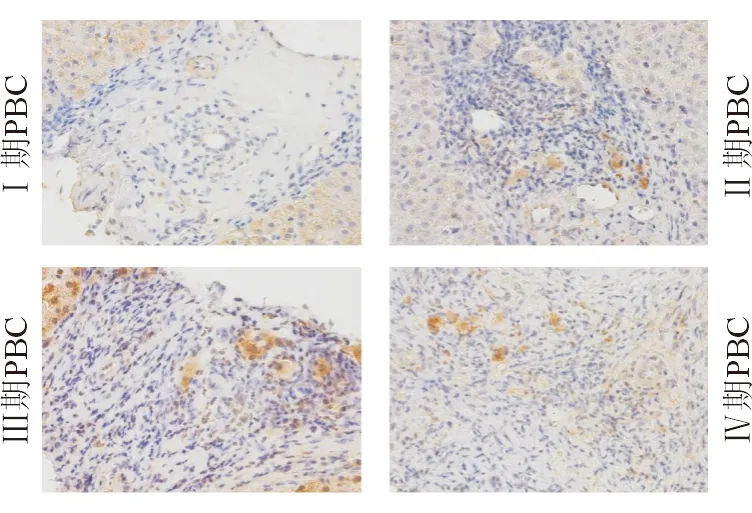
图3 不同病理分期肝组织OPN免疫组织化学染色结果(400X)
采用非参数Spearman相关分析发现,PBC病理分期与OPN病理评分具有一定的相关性(r=0.396,P=0.001)。
讨 论
PBC是导致肝硬化的一个重要病因,早期以小胆管内皮细胞损伤为主要特征,通过生物化学指标ALP和AMA抗体等可以做出临床诊断,肝活组织检查对于PBC治疗应答和预后都有重要指导价值[2, 11]。OPN在肝硬化发病过程中具有重要作用[3-4],但是OPN在PBC不同病理分期中的表达情况未见详细阐述。因此,本研究重点探讨了OPN在肝组织的表达情况与PBC病理分期之间的关系。
美国的研究资料显示,每百万人口就有293例PBC患者,其中女性PBC患者为每百万人口428例,男性为每百万人口107例,女性和男性比例为4∶1[2, 15]。欧洲的流行病学分析发现,每百万人口就有222.7例PBC患者,其中女性患者为每百万人口380.7例,男性患者为每百万人口76.6例,女性和男性比例为5∶1[16]。本研究中PBC女性患者比例很高,OPN强表达在女性患者的比率为42%,而男性患者OPN强表达比率为20%,这可能与女性患者在病理分期3和4期中所占比重较大有关。
OPN作为细胞连接蛋白,在正常肝脏细胞、肝星状细胞和巨噬细胞常规低表达[3, 10]。本研究中在1期PBC病理分期中3例患者肝组织OPN呈低表达状态,2期中有1例患者肝组织OPN呈低表达状态,但是在PBC病理分期3期和4期患者,肝组织中未见OPN低表达状态。对肝组织OPN高表达病例进行分析发现,随着病理分期从1期进展至3期的过程中,OPN高表达比例逐渐增高,提示OPN高表达与PBC进展过程密切相关。PBC病理分期第3期也称为肝纤维化期,OPN高表达比例在第3期最高,说明OPN可能与肝组织纤维化相关。尽管在第4期无OPN低表达状态患者,但是OPN高表达比例与第3期相比较低,这可能与肝硬化期PBC肝组织再生能力下降有关系。
本研究采用CK7和CK19来标记胆管细胞,可以区分正常胆管结构、肝组织再生过程中反应性增生的胆管细胞和具有双向分化潜能的部分肝细胞[11-12]。PBC病理1期汇管区胆管消失很少见,常见的是胆管细胞损伤,并伴随周围炎细胞浸润形成肉芽肿,因此在PBC病理1期肝组织偶尔可以OPN阳性表达的巨噬细胞,而在汇管区周围肝细胞表达以低表达或者中度表达为主。PBC病理2期汇管区导管反应常见,损伤的胆管细胞周围明显肉芽肿,常伴随界面性肝炎,CK7阳性肝细胞增多,在PBC病理2期扩大的汇管区常可以看到OPN阳性表达的巨噬细胞。PBC病理3期汇管区胆管缺失常见,胆汁淤积加重,Masson染色和Gomori银染可以看到来自汇管区大量纤维组织延伸至肝小叶内,汇管区内可见大量OPN阳性表达的巨噬细胞和淋巴细胞,汇管区周围肝细胞OPN通常高表达。在PBC病理4期成纤维细胞明显增多,形成巨大的纤维瘢痕分割肝组织,形成假小叶,OPN阳性表达的巨噬细胞和淋巴细胞所占比率与第3期相比有所下降,毛细胆管中可见胆栓形成。通过OPN在PBC病理4个分期汇管区的表达分布特点分析可以发现,OPN高表达与引起胆管细胞免疫损伤的炎症细胞有关,同时也与肝组织损伤修复过程中的再生肝细胞有关。
综上所述,PBC发展到肝纤维化后,OPN在肝组织中的表达量明显增加,肝硬化后OPN高表达比率降低。OPN高表达提示胆管免疫损伤负荷加重,同时也预示肝组织增生能力较强。OPN与PBC病理分期密切结合对于病情严重程度评估及患者预后预测有重要的临床价值。

