雷珠单抗联合曲安奈德在息肉状脉络膜血管病变患者治疗中的临床疗效分析
刘庆言 薛敏 姜丽丽 李晶 史春生
息肉状脉络膜血管病变(polypoid choroidal angiopathy,PCV)是一种在亚洲人群中常见的脉络膜血管病变,发病机制尚未完全阐明,临床特征是眼底结节状橙红色血管病变和视网膜色素上皮(retinal pigment epithelium, RPE)和神经感觉层的复发性浆血性脱离[1]。玻璃体内注射抗血管内皮生长因子(vascular endothelial growth factor, VEGF)是目前PCV的临床一线治疗方式[2],联合光动力治疗(photodynamic therapy, PDT)更有助于息肉的消退[3],但临床中存在很多PCV的患者对抗VEGF治疗反应不佳,视力改善不佳或需反复多次注射的现象,加之国内目前维替泊芬缺药的现状,故寻找PCV新的有效治疗方案一直是眼科工作者努力的课题,曾有研究发现[4],在新生血管性年龄相关性黄斑变性(neovascular age-related macular degeneration,nAMD)患者中0.7 mg地塞米松玻璃体植入物和抗VEGF药物联合使用的患者其无注射间隔时间明显长于接受安慰剂和抗VEGF单药治疗的患者。也有在PCV患者中应用抗VEGF药物+PDT联合Tennon囊下注射曲安奈德(triamcinolone acetonide,TA)的三联治疗的3年临床观察证实其临床效果明显优于抗VEGF药物+PDT的两联治疗,患者治疗间隔延长,视力明显提升(P<0.05)[5]。但国内相关的随机对照研究较少。
本研究将雷珠单抗+TA联合注射与雷珠单抗单药注射做对比,观察两组不同治疗方式在PCV患者中的临床疗效,以期对临床有一定的指导意义。报告如下。
资料与方法
一、研究对象
前瞻性随机对照研究。选取2019年8月至2020年12月在安徽省第二人民医院未经治疗的拟行玻璃体腔药物注射的PCV患者30例(30只眼),随机选取其中15例患者行0.5 mg雷珠单抗联合0.5 ml TA玻璃体腔注射,另外15例患者作为对照组,行0.5 mg雷珠单抗单药注射,两组患者随访观察1年,评估最佳矫正视力(best corrected visual acuity,BCVA)、中心视网膜厚度(central retinal thickness ,CRT)和注射频次的变化。纳入标准为:(1)经吲哚青绿血管造影(indocyanine green angiography,ICGA)临床诊断明确为PCV;(2)能配合治疗且保证至少1年的随访。排除标准:(1)在治疗和随访期间出现由非PCV导致的视力或眼底异常;(2)不能控制的系统性疾病:如高血压、Ⅱ型糖尿病等及各种肿瘤、免疫性疾病;(3)在治疗和随访期间出现眼部外伤、因晶状体混浊明显加重行白内障手术或因患者个人意愿更改注射药物种类的患者;(4)不能保证一年随访的患者。所有患者均自愿参与研究,在注射前均详细告知手术风险并签署手术知情同意书。本研究遵循《赫尔辛基宣言》关于涉及人体受试者的研究的原则。
二、 检查设备和药物资料
所有参与者都进行了全面的眼部检查,包括BCVA测试、使用裂隙灯显微镜进行的散瞳眼底检查、相干光层析成像术(optical coherence tomography,OCT)(Topcon,日本)、荧光素眼底血管造影(fluorescein fundus angiography,FFA)和ICGA(德国海德堡)检查。患者在随后的随访中接受了常规散瞳眼底检查和OCT检查,以OCT下CRT和团块状息肉形态变化作为是否追加注射的临床依据。所有患者注药前3 d开始滴用加替沙星滴眼液(0.3%,5 ml,安徽双科药业),4次/d,术后2 h后取下敷料,测术眼眼压,并开始滴用加替沙星滴眼液至术后1周,4次/d。玻璃体腔注射药物为雷珠单抗注射液(诺华公司,瑞士)和TA(5 ml:50 mg,上海通用药业)。TA以10 ml注射用水配置成混悬液,抽取0.5 ml,浓度约为5 mg/ml。
三、玻璃体腔注药操作流程
玻璃体腔药物注射在手术室无菌环境中进行,爱尔凯因滴眼液局部麻醉和5%聚维酮碘结膜囊消毒后,距角膜缘后3.5~4.0 mm处梯形进针注药,注射后局部按压30 s,所有患者均在角膜缘处行5号针头穿刺前房放液至眼压Tn,以防止出现术后的急性高眼压。所有入组患者的注药操作均由我院同一位眼底病组副主任医师完成。
四、统计学分析方法
采用SPSS 25.0软件进行分析,对分类数据(性别、眼别)使用卡方检验,对连续数据(年龄)使用两独立样本t检验进行比较,用标准对数视力表测量BCVA,转换为最小分辨率角的对数(logMAR),CRT被定义为中心凹处视网膜内界膜至色素上皮层之间的距离,此次实验结果为定量数据资料,两组数据之间应用Wilcoxon Mann-Whitney秩和检验分析,(P<0.05)具有统计学意义。
结 果
一、基本资料
本次研究共纳入30例(30只眼)患者,其中联合组15例(男性8例,女性7例,右眼9例,左眼6例),平均年龄为(64.8±6.75)岁,单药组15例,(男性9例,女性6例,右眼11例,左眼4例),平均年龄为(66.60±5.60)岁,两组间在性别(P=0.948)、眼别(P=0.439)、年龄(P=0.896)方面差异无统计学意义。见表1。
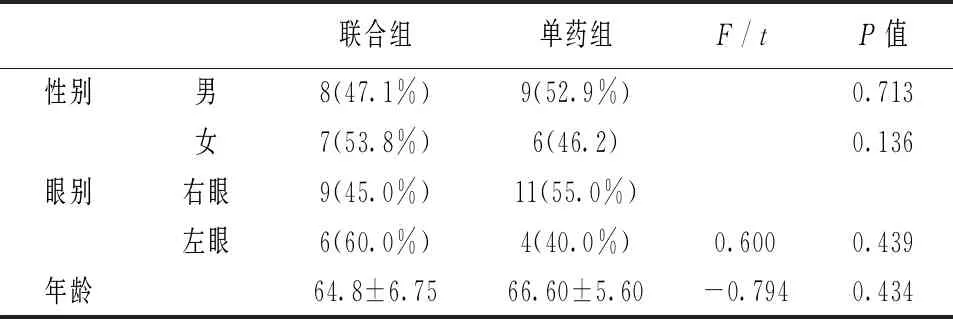
表1 两组患者的基本资料
二、1年内随访的结果
以初次检查的BCVA和CRT数值为基线,记录1年内(治疗后1、3、6、12个月)复查的结果,并将1年后的结果与基线值做比较,将差值:BCVA提升和CRT降低做分析,联合组BCVA提升中位数为0.24(0.16,0.32),CRT降低中位数为122.00(93.00,165.00)μm,单药组BCVA提升中位数为0.22(0.14,0.26),CRT降低中位数为133.00 (108.00,170.00)μm,两组间在BCVA提升(Z=-0.934,P=0.350)和CRT降低(Z=-0.415,P=0.678)方面差异无统计学意义,联合组1年随访内注射针数中位数为4.00 (4.00,5.00)次,单药组1年随访内注射针数中位数为5.00 (4.00,5.00)次,两组间差异有统计学意义(Z=-2.100,P=0.036)。见表2。
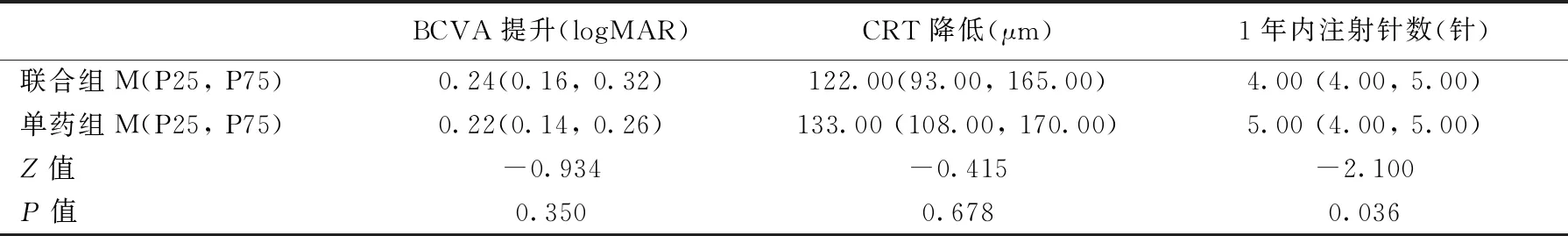
表2 两组患者在BCVA提升、CRT降低和1年内注射针数的比较
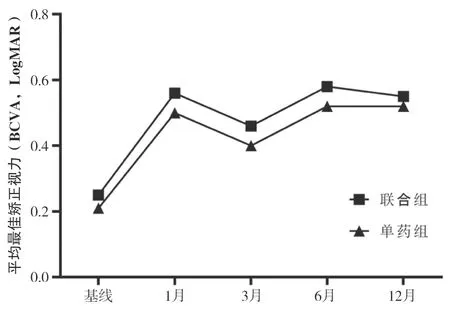
图1 两组患者在不同时间点的平均BCVA
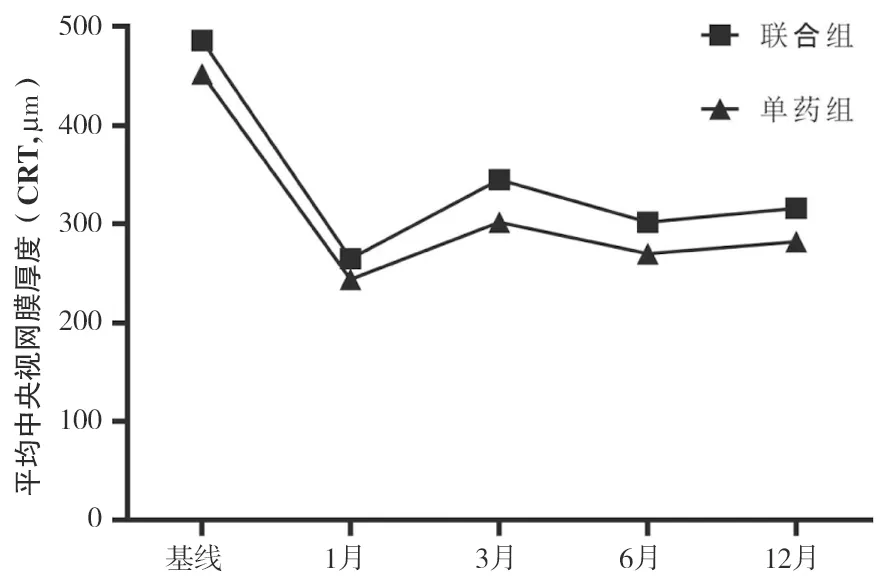
图2 两组患者在不同时间点的平均CRT
三、术后并发症和随诊情况
所有患者均在注药操作后常规行前房穿刺放液,故未出现术后高眼压患者,1例患者第2次注射隔日复查时白内障明显加重,考虑为操作不当引起,在与患者沟通后,行白内障超声乳化吸除联合人工晶状体植入术后视力改善,2例患者因高血压和糖尿病出现眼底黄斑区外出血,给予对症治疗,此3例患者给予出组,并纳入新的患者入组。因为疫情、交通等原因,部分农村地区或外地患者存在失访问题,短期失访的患者我们将其作为缺失值处理,长时间失访的患者需给予出组,并纳入新的患者入组,所有入组患者在1年随访时间内未出现严重眼内炎或感染、玻璃体出血、视网膜脱离或黄斑裂孔等严重并发症。
讨 论
目前的观点认为PCV是nAMD的一种亚型/动脉瘤样1型新生血管形成(AT1)[6],标准治疗是抗VEGF单一疗法或抗VEGF联合PDT治疗[7],EVEREST Ⅱ和PLANET研究证实抗VEGF单一疗法治疗PCV是有效的[8],但也有研究[9]发现PCV患眼中的VEGF水平低于典型的nAMD眼,抗VEGF单一疗法虽可以稳定视力,减少视网膜下液渗出,但对息肉样病变的影响有限,因VEGF因子和多种炎症因子可能共同参与了PCV的进展,因此,抗VEGF联合抗炎治疗对于PCV的治疗可能获得良好的临床结果。
临床中很多PCV患者面临需多次注射抗VEGF药物或停止注射后色素上皮脱离与息肉样病变会复发的问题,但反复多次注射抗VEGF药物也会有增加全身或眼睛局部不良反应的风险[10]。因 PCV的发病机制可能包括脉络膜增厚和渗透性过高,Yanagi等[11]指出脉络膜增厚和脉络膜血管渗透性过高是PCV抗VEGF治疗后预后欠佳的主要因素,而光动力疗法和激素类药物均有降低血管高渗透性作用,但临床效果也存在争议。
TA是一种氟原子位于第九位的皮质类固醇,在玻璃体中的存留时间比其他皮质类固醇长,易并被制成玻璃体内植入物,是首批评估用于治疗继发于nAMD的脉络膜新生血管的药物化合物之一[12],TA通过阻断包括类花生酸生物合成在内的级联炎症机制、降低各种细胞因子、趋化蛋白和基质金属蛋白酶的释放和活性来发挥抗炎作用;通过抑制磷脂酶A2调节细胞粘附,并抑制血管扩张、白细胞迁移和降低血管渗透性;同时可以稳定和重建血-视网膜屏障,通过毛细血管收缩和VEGF下调对Starling平衡产生积极影响来发挥拮抗新生血管形成的作用[13]。过去十余年内,玻璃体内注射TA已成为治疗葡萄膜炎、继发于视网膜脉管系统疾病的黄斑水肿、新生血管形成和玻璃体视网膜病变等多种眼部疾病的有效方法[14]。
Jonas等[15]认为单次玻璃体内注射4 mg TA可能具有相当好的耐受性,并有助于治疗渗出性AMD,在67例(71只眼)的nAMD患者给与1次或多次玻璃体内注射25 mg TA,平均随访时间为7.46个月的时间内,患者平均视力增加0.23(P<0.05),注射后1~3个月术后视力提高最显著,眼压从基线的平均15.1 mmHg 增加至最大值 23.0 mmHg,经药物的短暂使用后均可控制正常。作者得出结论,玻璃体腔内注射TA可以改善nAMD患者的视力。Okubo等[16]发现经Tennon囊注射12 mg TA德(40 mg/ml)后可提高PCV患者视力,降低脉络膜血管的渗漏,且在注射后的15个月的随访内没有眼压升高,没有眼内炎,视力稳定良好。Sakai等[17]研究发现玻璃体腔注射抗VEGF药物+PDT+Tennon囊下注射TA的三联疗法可使PCV患者在1年后的BCVA、CRT和PED高度分别有69.2%、84.6%和100%的眼睛得到改善,在转换后的12个月内,平均每年需要注射3次抗VEGF药物注射,息肉样病变和色素上皮脱离迅速减少。
但TA在眼部的使用,尤其是在玻璃体腔注射后有引起眼内压升高、白内障、视网膜血管阻塞等风险[18],故TA在眼部的使用有其一定的局限性,但考虑到其价格便宜,注射小剂量TA并定期随访观察可有效的控制风险。本研究中使用0.5 ml小剂量TA,严格遵循玻璃体腔注药标准操作流程,常规在注药后行前房放液,术后定期随访,故所有患者均未出现高眼压,TA的使用安全性有保障。
本研究中抗VEGF药物联合TA的观察组在1年内的平均注射针数为4.27针,雷珠单抗的单药组在1年内的平均注射针数为5.00针,联合组的针数明显低于单药组(P<0.05),虽然在1年随访的时间内,两组间在BCVA提升和CRT降低方面对比无明显差异,但对PCV这种临床易复发的眼底疾病来说,能减少注射频次同样可使患者获益,值得在临床中进一步研究,目前临床中已经有地塞米松玻璃体缓释剂,但鉴于目前尚未在黄斑新生血管疾病中纳入医保范围,患者使用仍需承担经济压力,小剂量TA仍是现阶段临床的选择之一。
综上所述,雷珠单抗联合TA玻璃体腔注射较雷珠单抗单药注射在PCV患者1年随访内是安全有效的,可降低注射频次,减轻患者的就医负担和医疗成本,但本研究存在样本量较少,失访率较高,随访时间有限等问题,我们会后期继续扩大样本量,增加随访时间来进一步研究此治疗方案在PCV患者中应用的临床前景。

