经导管主动脉瓣置换术和外科主动脉瓣置换术治疗老年重度主动脉瓣狭窄的临床疗效
程 帅,冯胜东,冯晔子,张申伟
主动脉瓣狭窄是常见的瓣膜性心脏病,主要发生在60岁以上的人群中[1]。年龄>75岁的人群中主动脉瓣狭窄患病率约为3.4%[2-3]。主动脉瓣狭窄的自然进展缓慢,长达数年甚至数十年,之后快速恶化且死亡率较高[4]。症状严重的主动脉瓣狭窄病人伴有心力衰竭,未置换主动脉瓣情况下,2年病人死亡率接近50%[5]。主动脉置换可有效降低左室后负荷和室壁厚度,且可逆转心室重构,降低死亡率[6]。经导管主动脉瓣置换术(TAVR)认为是有外科主动脉瓣置换术(SAVR)禁忌或高风险的严重主动脉瓣狭窄病人的治疗方法,中危主动脉瓣狭窄病人可替代SAVR[7]。本研究通过收集接受TAVR和SAVR治疗的老年重度主动脉瓣狭窄病人的临床资料,比较术后1个月心功能改善、血流动力学、心室逆重构和早期不良心血管事件发生情况,为老年重度主动脉瓣狭窄治疗方案的选择提供依据。
1 资料与方法
1.1 一般资料 选取2017年1月—2020年10月在我院接受治疗的老年重症主动脉瓣狭窄病人77例,其中TAVR治疗45例,SAVR治疗32例。纳入标准:年龄≥60岁;重度主动脉瓣狭窄;纽约心脏病协会(New York Heart Association,NYHA)心功能分级≥Ⅲ级。排除标准:有手术禁忌证(如严重感染或血栓等);左室流出道梗阻;伴有二尖瓣、三尖瓣或主动脉瓣的重度反流;伴有严重的心功能不全;伴有其他严重疾病,生存时间短。本研究经医院伦理委员会批准,病人或家属签署知情同意书。
1.2 观察指标 收集病人临床资料,包括年龄、性别、体质指数(BMI)、NYHA心功能分级、合并症[高血压、糖尿病、冠心病、慢性阻塞性肺疾病(COPD)、陈旧性心肌梗死、心房颤动和外周血管病]、既往经皮冠状动脉介入(PCI)史、胸外科医师协会(STS)评分、总住院时间和监护时间。
1.3 心脏超声数据收集 术前和术后1个月采用彩色多普勒超声仪测量心脏个各切面指标,左心两腔切面和心尖四腔切面下测量左室舒张末期内径(left ventricular end diastolic diameter,LVEDD)、左室后壁厚度(left ventricular posterior wall thickness,LVPWT)、室间隔厚度(interventricular septum thickness,IVST),3个心搏下测量取平均值。根据公式计算左室质量指数(left ventricular mass index,LVMI)和室壁相对厚度(relative wall thickness,RWT)。在心尖五腔切面测量主动脉瓣平均跨瓣压差(mean pressure gradient,mPG)、主动脉瓣瓣口面积(aortic valve area,AVA)和主动脉峰值流速(Vmax)、左室射血分数(left ventricular ejection fraction,LVEF)。
1.4 NYHA分级改善评定标准 心功能改善未达到Ⅰ级、无变化或恶化为无效;心功能改善1级为有效;心功能改善≥2级为显效。总有效为有效与显效之和。
1.5 终点事件 主要终点事件为全因死亡;次要终点事件主要包括脑卒中、心包填塞、心肌梗死、恶性心律失常和重度房室传导阻滞。

2 结 果
2.1 两组临床资料比较 TAVR组年龄和STS评分高于SAVR组,总住院时间和监护时间少于SAVR组,差异有统计学意义(P<0.001)。详见表1。
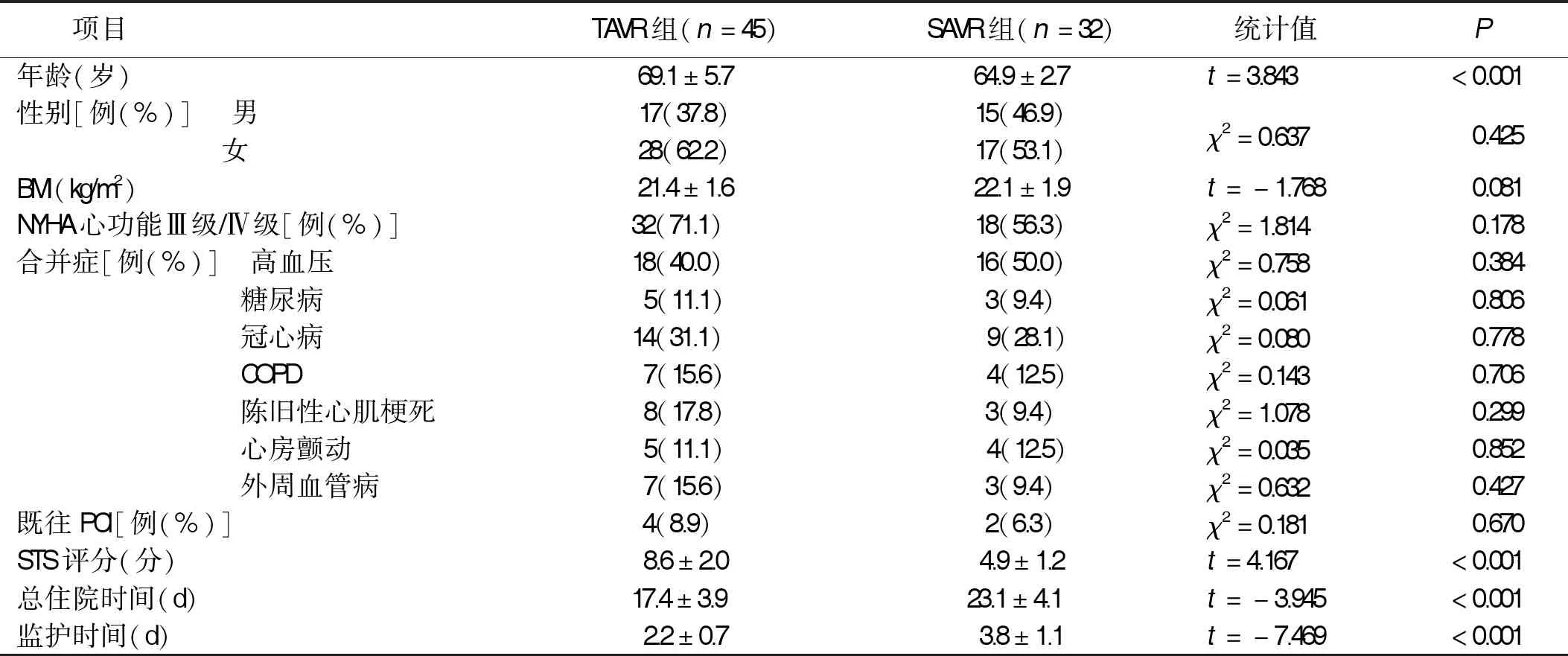
表1 两组临床资料比较
2.2 两组术前与术后1个月超声指标比较 TAVR组术后1个月RWT、LVEF和AVA高于术前,LVMI、mPG和Vmax低于术前,差异均有统计学意义(P<0.05)。SAVR组术后1个月LVEF和AVA高于术前,LVEDD、LVMI、mPG和Vmax低于术前,差异均有统计学意义(P<0.05)。术后1个月,SAVR组RWT和Vmax高于TAVR组,LVEDD、LVMI、LVEF、mPG和AVA低于TAVR组,差异均有统计学意义(P<0.05)。详见表2。

表2 两组术前与术后1个月超声指标比较(±s)
2.3 两组术后1个月NYHA分级改善比较 术后1个月,TAVR组NYHA分级显效18例(40.0%),有效22例(48.9%),无效5例(11.1%);SAVR组显效14例(43.8%),有效15例(46.8%),无效3例(9.4%)。TAVR组总有效率为88.9%,SAVR组总有效率为90.6%,两组比较差异无统计学意义(χ2=0.061,P=0.806)。
2.4 两组术后1个月主要终点事件和次要终点事件发生率比较 TAVR组与SAVR组术后1个月内全因死亡率及次要终点事件发生率比较,差异无统计学意义(P>0.05)。详见表3。

表3 两组术后1个月主要终点事件和次要终点事件发生率比较 单位:例(%)
3 讨 论
随着年龄增加,主动脉瓣狭窄发病率逐渐增加,我国人口老龄化剧增,导致主动脉瓣狭窄患病人数增多。主动脉瓣狭窄早期症状轻微,发展至重度时中位生存时间为23个月,出现心力衰竭症状的病人中位生存期仅为11个月[8]。目前尚无药物可改善主动脉瓣狭窄病人预后,动脉瓣置换是改善生存的治疗方法[9]。采用SAVR治疗虽然可提高病人生存率但创伤较大,部分病人有手术禁忌证。对有禁忌证的病人仅采用药物治疗,对延缓病情进展效果不理想。尽管2014年美国心脏病学会/美国心脏协会已将主动脉瓣置换术列为严重症状性主动脉瓣狭窄的治疗首选[10],但约33.3%的严重症状性主动脉瓣狭窄病人未接受主动脉瓣置换术,原因是多种合并症、高龄、左室功能障碍或身体虚弱等。左室功能障碍病人SAVR的手术死亡风险高达10%[11]。患有慢性肾脏疾病和高龄的SAVR病人中也发现了类似风险增加。TAVR为主动脉瓣置换的治疗提供了新方法,具有创伤小和恢复快的优势,应用于高风险不能耐受外科手术治疗的病人。
一项使用Sapien球囊瓣膜的TAVR与SAVR研究中,两组术后1年死亡率比较,差异无统计学意义(P>0.05)[12]。TAVR最初应用于具有高风险对外科手术不能耐受的主动脉瓣狭窄病人,随着手术技术和医疗器械的改进,中低度危险病人可接受TAVR的治疗。相关指南指出,对存在外科手术禁忌证的重度主动脉瓣狭窄病人,Ⅰ级推荐为TAVR,对无外科手术禁忌证的高危病人TAVR和SAVR均为Ⅰ级推荐,对中度外科手术风险的病人将TAVR升级为Ⅱa类推荐,对低危病人仅推荐SAVR[13]。
本研究选取重度主动脉瓣狭窄病人,TAVR组与SAVR组术后1个月NYHA分级改善情况比较差异无统计学意义。TAVR组年龄和STS评分高于SAVR组,总住院时间和监护时间较SAVR组缩短。多项研究显示,SAVR术后LVMI明显降低,术后2年达到稳定状态,并表现为左心室逆重构[14-15]。本研究中,TAVR组术后1个月RWT降低,而LVEDD无明显变化,且TAVR组RWT低于SAVR组,说明TAVR术后心室逆重构由室壁相对厚度降低引起。SAVR组术后1个月RWT和LVEDD与术前相比均降低,说明SAVR术后左心室逆重构由室壁相对厚度和LVEDD降低引起。SAVR组术后1个月LVMI低于TAVR组,Hahn等[16]研究显示,SAVR组术后LVMI下降速度快于TAVR,但术后1年和术后2年LVMI下降程度相近。TAVR组与SAVR组术后1个月相比mPG和AVA增加更显著,说明接受TAVR治疗的病人发生左心室逆重构更快。TAVR组术后1个月LVEF高于SAVR组。TAVR组与SAVR组术后1个月内全因死亡率及次要终点事件比较,差异无统计学意义(P>0.05)。
综上所述,接受TAVR治疗的病人年龄大、STS评分高、住院时间缩短,血流动力学和心室逆转重构改善,且未增加全因死亡率及次要终点事件发生率,TAVR为治疗老年重度主动脉瓣狭窄的有效方法之一。

