绿脓杆菌内毒素蛋白微胶囊的制备及免疫效果
曲晓军,胡基华,潘 钰
(1. 黑龙江省科学院微生物研究所,黑龙江 哈尔滨 150010;2. 中国医学细菌保藏管理中心铜绿假单胞菌专业实验室,黑龙江 哈尔滨 150010)
近年来雏鸡急性败血症(Acute Septicemia)在我国不断增多,给养鸡业造成了较大的危害,其主要病原为铜绿假单胞菌(Pseudomonas Aeruginosa,简称绿脓杆菌)。本病多发于10日龄以内的雏鸡,主要表现为发热、精神萎靡、食欲减退、出现下痢便,最后因衰竭而死亡,死亡率可高达80%。
绿脓杆菌是一种人畜共患病的机会性病原体,寄主范围非常广泛,涵盖了水生和陆生植物、动物和人类,在畜禽养殖场动物和工作人员体内、土壤、饮用水中均有该菌被发现的报道,其在动物免疫力低下时可引发感染。绿脓杆菌对很多种类的抗生素具有固有的耐药性,还可以通过突变或水平基因转移扩大其抗生素耐药性和耐药谱,从而导致药物治疗失败。绿脓杆菌内毒素蛋白是一种免疫原性强、副作用低的良好抗原,可激发动物体液免疫和细胞免疫。因此,研制安全有效的绿脓杆菌内毒素蛋白微胶囊(Microcapsule),评价微胶囊的免疫效果和保护效果,为我国流行的雏鸡急性败血症的防控提供有效手段。
1 材 料
1.1 试验动物7日龄白羽肉鸡购自哈尔滨江北养鸡场,未经绿脓杆菌疫苗免疫,预饲期间饲喂不含抗生素饲料,自由采食和饮水。
1.2 菌 株绿脓杆菌PA-526 株(血清型III型)、PA-1537 株(血清型VIII)和PA-261 株(血清型X 型)由本实验室鉴定保存。
1.3 试 剂绿脓杆菌内毒素蛋白、兔抗绿脓杆菌内毒素蛋白抗体(一抗)由本实验室制备;明胶、司班80 购自天津科密欧化学试剂有限公司;阿拉伯树胶粉购自上海化学试剂站分装厂;冰乙酸购自天津光复科技发展有限公司;37 %甲醛购自辽宁泉瑞试剂有限公司;液体石蜡购自天津富宇精细化工有限公司;无水乙醇购自天津北辰方正试剂有限公司;氢氧化钠购自天津欧博凯化工有限公司;羊抗兔二抗购自武汉博士德生物工程有限公司。
1.4 主要仪器生物安全柜(型号为CLASS II TYPE A2),购自北京东联哈尔仪器制造有限公司;恒温培养振荡器(型号为ZHWY-211C),购自上海智成分析仪器制造有限公司;细菌浊度计(型号为TA-2XJ),购自北京天安联合科技有限公司;独立送风隔离笼具(型号为IVC- II),购自苏州冯氏实验动物设备有限公司;高速台式离心机(型号为TGL-16G),购自上海安亭科学仪器厂;倒置式生物显微镜(型号为DIAPHOTTMD),购自尼康英士特株式会社;多功能酶标仪(型号为Infinite M200 PRO),购自瑞士Tecan 公司。
2 方 法
2.1 微胶囊制备条件的优化
2.1.1 微胶囊制备方法 在50℃明胶溶液(5%)中,缓慢滴加10%冰乙酸溶液,调节pH,范围在3.8~4.8;称取20g 内毒素蛋白加入到20mL 阿拉伯胶溶液(5%)中,混合均匀,缓慢滴加10%冰乙酸溶液,调节pH,3.8~4.8;量取100mL 液体石蜡于250mL 三口瓶中,加入适量司班80,将三口瓶置于50℃水浴中,搅拌条件下,将加有内毒素蛋白的阿拉伯胶溶液缓慢滴入三口瓶中,乳化30min;向三口瓶中缓慢加入5% 明胶溶液20mL,乳化30min 后,缓慢加入10%冰乙酸溶液,调节pH,3.8~4.8,凝聚反应120min,降温到10℃;用10%氢氧化钠调节反应体系pH 为9.0,降低搅拌速度,用适量37%甲醛固化交联40~70min;反应结束后,离心加过滤洗涤(蒸馏水和无水乙醇),得到微胶囊;将抽滤得到的微胶囊和滤纸置于表面皿中,50℃烘箱干燥24h。
2.1.2 最佳搅拌速度 在交联反应时,保持其他条件不变,分别以700、750、800、850、900、950、1000 r/min 的搅拌速度,制备内毒素蛋白微胶囊,监测内毒素蛋白微胶囊的成囊效果。
2.1.3 最佳pH 在反应体系中,保持其他条件不变,分别以pH 为3.8、4.0、4.2、4.4、4.6、4.8 的条件下制备内毒素蛋白微胶囊,研究在不同pH 条件下制备的微胶囊粒径和形态。
2.1.4 最佳固化时间 在制备过程中,保持其他条件不变,分别以40、45、50、55、60、65、70min 的固化时间,制备微胶囊,研究不同固化时间对内毒素蛋白微胶囊厚度的影响。
2.1.5 最佳甲醛用量 在实验过程中,保持其他条件不变,改变固化剂甲醛的用量,分别以6.0、6.5、7.0、7.5、8.0、8.5、9.0mL 的甲醛加入量进行固化交联反应,研究不同甲醛用量对内毒素蛋白微胶囊形态的影响。
2.2 微胶囊免疫抗体水平的监测60只7日龄白羽肉鸡分为4组,每组15只,第1~3组为微胶囊低、中、高剂量免疫组,第4组为空白对照组。第1组每只免疫含0.3mg 内毒素蛋白的微胶囊;第2组每只免疫含0.6mg 内毒素蛋白的微胶囊;第3组每只免疫含0.9mg 内毒素蛋白的微胶囊;第4组正常喂食饲料。免疫组均采取口服方式免疫,共免疫3次,每次间隔3d。免疫前及免疫后7、14、21、28、35、42、56d 颈静脉采血分离血清,ELISA 法监测血清中免疫抗体水平,确定雏鸡最佳免疫剂量。
2.3 攻毒菌株最小致死量测定取绿脓杆菌PA-526 株(血清型III 型)、PA-1537 株(血清型VIII)和PA-261 株(血清型X 型),营养琼脂培养基37℃培养12~16h,用无菌生理盐水洗下菌体,稀释,充分混匀,用细菌浊度计稀释成含菌5.00×107,7.50×107,1.00×108,1.25×108,1.50×108CFU/mL 等浓度的菌悬液,用每一稀释度的菌悬液,腹腔注射5只雏鸡,注射量为1.0mL,观察7d,使雏鸡全部死亡的最小剂量为1个最小致死量(mLD)。
2.4 免疫攻毒保护试验120只7日龄的白羽肉鸡随机分为4组,每组30只,1~3组为免疫攻毒组,采用口服内毒素蛋白微胶囊最佳免疫剂量免疫,共免疫3次,每次间隔3d;第4组为空白对照组。免疫后第35 d,免疫攻毒组分别用PA-526 株、PA-1537 株、PA-261 株腹腔注射攻毒1mLD(表1)。同时应用同批饲养的雏鸡45只作攻毒菌株mLD 验证试验,分成3个大组,每个大组15只,每个大组再分成2mLD、1mLD 及1/2mLD 3个小组,每个小组各5只;分别于腹腔注射2mLD、1mLD 及1/2mLD 的PA-526 株、PA-1537 株和PA-261 株的新鲜菌悬液,观察7d,进行结果判定:mLD 验证组感染2mLD及1mLD 者应全部死亡,感染1/2mLD 者应有部分死亡,计算免疫攻毒组雏鸡保护率(见表1)。
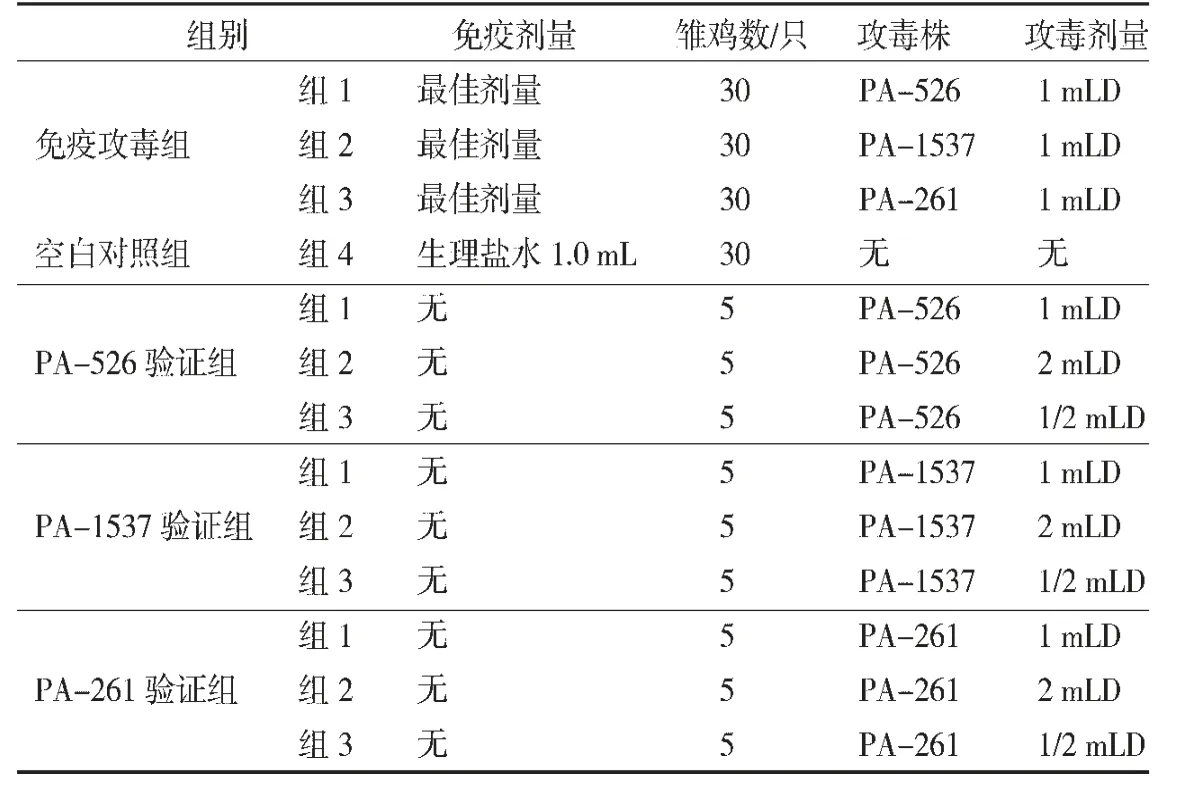
表1 分组免疫及攻毒情况表
3 结果与分析
3.1 最佳搅拌速度搅拌速度小,液滴形成不均匀;搅拌速度过大,容易使微胶囊破碎。在本研究中,当搅拌速度在800 r/min 时,成囊率最高,粒径大小适中,因此,800 r/min 的搅拌速度适合制备内毒素蛋白微胶囊。
3.2 最佳pHpH 过低时,凝聚反应较难,微胶囊易黏连;pH 过高时,也不利于凝聚反应和微胶囊成形。在本研究中,当pH4.2 时,成囊率高,粒径均匀,因此,pH4.2 条件下适合制备内毒素蛋白微胶囊。
3.3 最佳固化时间固化时间过短,微胶囊形态不稳定;固化时间过长,微胶囊囊壁变厚,蛋白包裹率下降。在本研究中,当固化时间为55min 时,微胶囊形态稳定,囊壁厚度适中,因此,55min 的固化时间适合制备内毒素蛋白微胶囊。
3.4 最佳甲醛用量甲醛用量少时,微胶囊易黏连;甲醛用量多时,微胶囊囊壁过厚,蛋白包裹率下降。在本研究中,当甲醛用量为7.5mL 时,微胶囊形态均匀,不黏连,囊壁厚度适中,因此,甲醛用量7.5 mL 适合制备内毒素蛋白微胶囊。
3.5 内毒素蛋白微胶囊最佳制备工艺在搅拌速度800r/min,pH4.2,固化时间55min,固化剂甲醛用量7.5mL 时,制备的微胶囊颗粒均匀,不黏连,囊壁厚度适中,蛋白包裹率较高,成囊率高,以此作为内毒素蛋白微胶囊的最佳制备工艺。
3.6 微胶囊免疫抗体水平监测结果免疫后7d,免疫组抗体水平逐渐升高,在第35d 达到峰值,然后抗体水平开始缓慢降低,至免疫后56d 时依然维持在较高水平。从14d 开始,免疫组与空白对照组的抗体水平存在显著性统计学差异(P<0.01);免疫组1 和免疫组2、3 在免疫后的14~56d 抗体水平存在统计学差异(P<0.05),免疫组2,3 免疫后的抗体水平未见统计学差异(图1),因此,内毒素蛋白免疫雏鸡的最佳剂量为0.6mg/次。
3.7 攻毒菌株最小致死量测定结果PA-526菌株对雏鸡最小致死量为1.00×108CFU/mL,PA-1537菌株对雏鸡最小致死量为1.25×108CFU/mL,PA-261 菌株对雏鸡最小致死量为7.50×107CFU/mL(见表2)。
3.8 免疫攻毒保护试验结果观察雏鸡临床表现,3个免疫攻毒组的绝大多数雏鸡在攻毒后2d 左右出现精神萎靡、食欲降低症状,从第4d 起开始恢复正常,少数雏鸡死亡;空白对照组雏鸡无异常表现;PA-526、PA-1537 和PA-261 菌株验证组雏鸡,攻毒1mLD 和2mLD组均全部死亡,攻毒1/2mLD组有部分死亡。计算免疫攻毒组的保护率,分别为86.7%、90.0%和83.3%(见表3)。
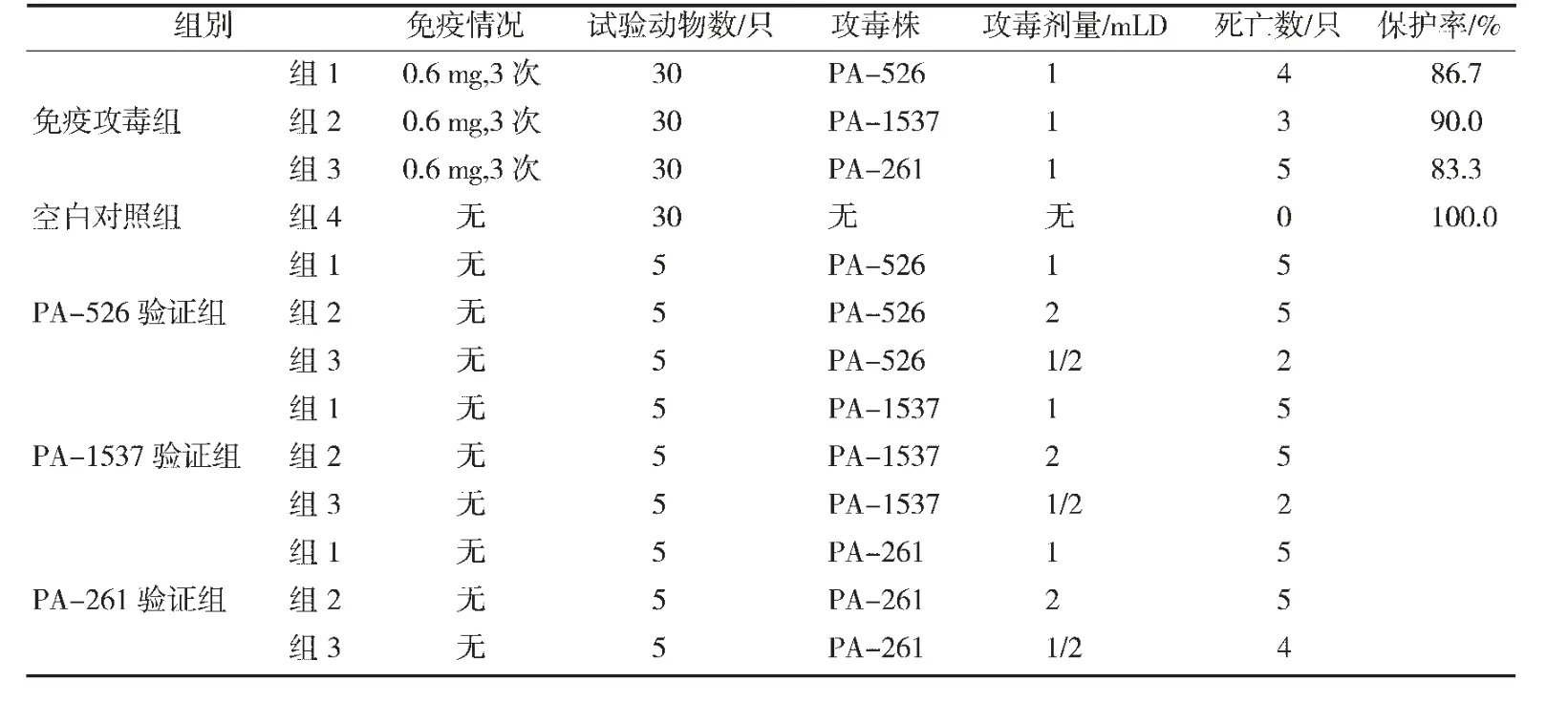
表3 免疫攻毒保护试验结果
4 讨 论
由绿脓杆菌引起的雏鸡急性败血症发病快、死亡率高,且该菌耐药机制复杂、对抗生素耐药严重,导致了抗生素治疗效果不佳。疫苗免疫防治疾病是一种经典、效果很好的方法,但由于疫苗申请临床试验之前的实验室研究工作繁琐、耗时长,临床试验中又往往存在疫苗对不同血清型病原菌保护效果不一致等问题,目前国内未见可用于预防和治疗雏鸡急性败血症的商品化疫苗。
本实验室制备的绿脓杆菌内毒素蛋白,经动物试验(小鼠、家兔)和人体试验研究证实,是一种免疫原性强、副作用低的良好抗原,可激发机体体液免疫和细胞免疫,且针对绿脓杆菌不同血清型菌株具有很好的交叉保护效果,因此,本研究将内毒素蛋白作为一种新型的、具有免疫功能的饲料添加剂应用于雏鸡急性败血症的防治研究,是一种很新颖的思路和尝试。
蛋白经口服给药,通过动物胃肠道时,容易受酸性环境和蛋白酶的作用而失活。微胶囊技术在最近几年发展越来越快,在医药行业应用较多,可利用该技术的靶向特性,将药物送到体内特定部位发挥作用,可避免胃肠道低pH 和蛋白酶对药物的破坏。
本研究采用复凝聚法+乳化- 化学交联法,以阿拉伯胶、明胶为壁材,内毒素蛋白为芯材制备微胶囊,研究了搅拌速度、pH、固化时间、固化剂用量等因素对微胶囊的影响作用,确定了最佳制备工艺,制备的微胶囊颗粒均匀、成囊率高、囊壁厚度适中、蛋白包裹率较高,适合作为饲料添加剂给雏鸡口服。
本研究制备的绿脓杆菌内毒素蛋白微胶囊能很好的诱导雏鸡产生较高的免疫抗体水平。从抗体变化趋势可以看出,低、中、高3个剂量免疫组,在免疫后7d 抗体水平逐渐升高,在第35d 达到峰值,至免疫后56d 时依然维持在较高水平。对低、中、高3个剂量免疫组数据分析可以看出,中剂量免疫组和高剂量免疫组无差别,说明过多的抗原不能使雏鸡产生更多的抗体,而是被鸡体分解代谢掉。本研究制备的微胶囊能使雏鸡产生体液免疫,但是否能使雏鸡产生细胞免疫还需进一步研究证实。
免疫攻毒保护试验结果显示,该内毒素蛋白微胶囊能够有效抵抗绿脓杆菌菌株的攻击,对3个血清型菌株(III 型、VIII 型和X 型)的保护率在83.3%以上。研究表明,该内毒素蛋白微胶囊能够提供对多种血清型绿脓杆菌菌株的交叉保护作用。目前绿脓杆菌已确定的血清型有14种,血清型比较复杂,该内毒素蛋白微胶囊对其他血清型菌株的防治效果还需进一步的研究验证。

