醋酸钠林格注射液与包材中抗氧剂的相容性研究
邹宇,刘杨,刘亚威,张迪,孙苓苓(辽宁省检验检测认证中心,辽宁省药品检验检测院,沈阳 110036)
醋酸钠林格注射液是一种新型的电解质平衡液,组成接近细胞外液生理比例,其含有的醋酸钠盐代谢速率快,可迅速改善微循环,纠正酸中毒[1-2]。临床上广泛用于围术期液体治疗,在安全性、有效性方面优势明显[3-5]。醋酸钠林格注射液为五层共挤输液用袋包装,直接接触药品的包材有五层共挤输液用袋、聚丙烯接口、聚丙烯组合盖,均为塑料制品。塑料药包材在生产过程中会加入抗氧剂来抑制或延缓老化降解,注射液在生产、流通、储存及使用过程中长时间与药包材接触,抗氧剂可能溶出、迁移至药液中,影响药物的理化性质和药理作用,甚至对人体具有一定的毒性[6-8]。2012年9月,我国药审中心发布了《化学药品注射剂与塑料包装材料相容性研究技术指导原则(试行)》[9],指出包装系统应与药品具有良好的相容性,即不能引入可引发安全性风险的浸出物,或引入浸出物的水平应符合安全性要求。欧洲药典中对各种塑料材料中添加剂的添加量进行了限定,并给出了检验方法[10]。有文献对不同塑料材料中的抗氧剂含量、不同注射液包材相容性进行了研究[11-20],但未见醋酸钠林格注射液包材相容性的相关报道。
醋酸钠林格注射液的药包材中使用了抗氧剂1010、抗氧剂330、抗氧剂1076、抗氧剂168,本研究参考欧洲药典方法[10]和相关文献[11-20],建立了4种抗氧剂的测定方法,并对包材和注射液进行提取、迁移试验,现报道如下。
1 材料
1.1 仪器
Waters 2695高效液相色谱仪(美国Waters公司),Tomy SX-700型高压灭菌锅(日本Tomy公司),BUCHI旋转蒸发仪(瑞士BUCHI公司),TechMate C18-STII色谱柱(250 mm×4.6 mm,5 μm,北京泰克美公司),Cleanert S C18-SPE固相萃取柱(600 mg/6 mL,天津Agela公司)。
1.2 试药
抗氧剂1010[四(3,5-二叔丁基-4-羟基)苯丙酸季戊四醇酯,批号:195014-201601,纯度:98.2%]、抗氧剂330 [2,2',2'',6,6',6''-己 烷-叔丁基-4,4',4''-(2,4,6-三甲基-1,3,5-苯基)三亚甲基]三苯酚,批号:195007-201601,纯度:99.6%]、抗氧剂1076[β-(3,5-二叔丁基-4-羟基苯基)丙酸十八碳醇酯,批号:195009-201601,纯度:99.5%](中国食品药品检定研究院);抗氧剂168[三(2,4-二叔丁基)亚磷酸苯酯,批号:172881,纯度:98.5%,LGC];四氢呋喃、甲醇(色谱纯,Fisher);乙腈(色谱纯,Tedia);二氯甲烷和甲苯(分析纯,国药集团)。
醋酸钠林格注射液(规格:500 mL,批号:B19041901,B19041902,B19041903,A公司),五层共挤输液用袋(批号:2001680853,2001680898,2001680930,B公司),聚丙烯接口(批号:1809151)、聚丙烯组合盖(批号:1811012)(C公司)。
2 方法与结果
2.1 色谱条件
采用TechMate C18-STII(250 mm×4.6 mm,5 μm)色谱柱,流动相为水-四氢呋喃-乙腈(1∶3∶6),流速为1.5 mL·min-1,检测波长为280 nm,柱温为40℃,进样量为20 μL。
2.2 对照品溶液的制备
称取抗氧剂1010、抗氧剂330、抗氧剂168、抗氧剂1076对照品适量,加入少量二氯甲烷溶解,以二氯甲烷-甲醇(3∶7)稀释至含抗氧剂1010、抗氧剂330、抗氧剂168、抗氧剂1076各约0.24 mg· mL-1的混合对照品溶液。
2.3 供试品溶液的制备
2.3.1 包材提取试验供试品溶液的制备 取包材样品约2.0 g,精密称量,置于烧瓶中,加入甲苯80 mL,持续搅拌,加热回流1.5 h,冷却至60℃,在搅拌下加入甲醇120 mL,烧结玻璃过滤器滤过。用甲苯-甲醇(4∶6)混合液25 mL清洗烧瓶和滤渣,将清洗液与滤液合并,并用相同的混合溶剂稀释至250 mL。取50 mL在45℃真空蒸干,残渣用二氯甲烷-甲醇(3∶7)溶解残留物并定容至5 mL,0.45 μm有机膜过滤,即为包材提取试验供试品溶液。同法制备空白溶液。
2.3.2 相容性提取试验供试品溶液的制备 模拟并适当加强灭菌工艺条件,考察目标物的浸出情况。取五层共挤输液用袋,剪切成0.5 cm×2 cm条状,按表面积6 cm2· mL-1比例加入醋酸钠林格注射液100 mL;分别取聚丙烯接口、组合盖,剪成小块,按0.2 g·mL-1比例加入醋酸钠林格注射液100 mL,置高压蒸汽灭菌器中,121℃浸提1 h,取出放冷至室温,作为提取试验供试品溶液。固相萃取柱使用前分别用3 mL甲醇和3 mL水依次活化。量取提取试验供试品溶液100 mL,以约1.5 mL·min-1的流速通过固相萃取柱,用6 mL水淋洗,再分别用5 mL甲醇、3 mL二氯甲烷依次洗脱,收集洗脱液,用甲醇稀释至10 mL,0.45 μm有机膜过滤后进样测定。同法配制空白溶液。
2.3.3 相容性迁移试验供试品溶液的制备 固相萃取柱使用前分别用3 mL甲醇和3 mL水依次活化。量取醋酸钠林格注射液100 mL,以约1.5 mL·min-1的流速通过固相萃取柱,用6 mL水淋洗,再分别用5 mL甲醇、3 mL二氯甲烷依次洗脱,收集洗脱液,用甲醇稀释至10 mL,0.45 μm有机膜过滤后进样测定。同法配制空白溶液。
2.4 测定方法
将对照品溶液、供试品溶液与空白溶液分别注入高效液相色谱仪,采用外标法定量。要求抗氧剂对应峰之间的分离度均不小于2.0,空白溶液在抗氧剂的出峰位置不得有干扰。
2.5 方法学考察
2.5.1 专属性试验 取制备好的抗氧剂对照品溶液、空白溶液、供试品溶液,在“2.1”项色谱条件下进行测定,抗氧剂1010的保留时间为5.3 min;抗氧剂330的保留时间为6.5 min;抗氧剂1076的保留时间为11.2 min;抗氧剂168的保留时间为12.8 min,各峰分离良好,醋酸钠林格注射液及空白溶液无干扰,典型色谱图见图1。
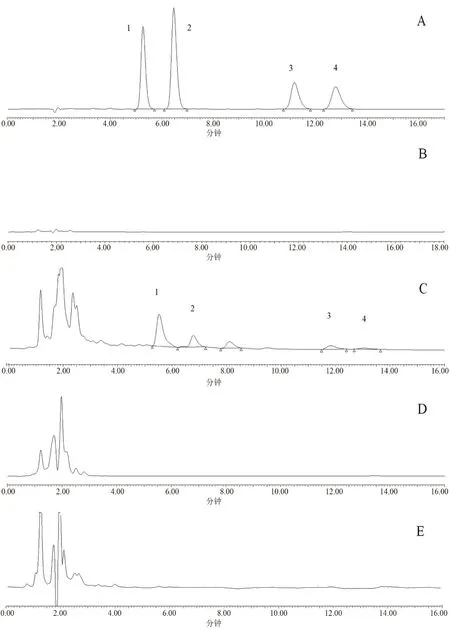
图1 典型HPLC色谱图Fig 1 Typical HPLC chromatogram
2.5.2 线性关系考察 以二氯甲烷-甲醇(3∶7)溶液稀释抗氧剂对照品,制得含抗氧剂1010质量浓度为0.4596、1.149、2.298、4.596、22.98、45.96、229.8、459.6 μg· mL-1,含抗氧剂330质量浓度为0.4594、1.148、2.297、4.594、22.97、45.94、229.7、459.4 μg· mL-1,含抗氧剂1076质量浓度为1.173、2.346、4.692、23.46、46.92、234.6、469.2 μg· mL-1,含抗氧剂168质量浓度为1.152、2.305、4.610、23.05、46.10、230.5、461.0 μg· mL-1的系列混合对照品溶液,依法测定,以质量浓度为横坐标,响应值为纵坐标,进行线性回归,结果见表1,表明4种抗氧剂在各自质量浓度范围内与峰面积线性关系良好。

表1 线性关系结果 Tab 1 Linearity
2.5.3 精密度试验 取质量浓度均为0.24 μg·mL-1的4种抗氧剂混合对照品溶液,连续进样6次,以峰面积计算RSD值,结果抗氧剂1100、抗氧剂330、抗氧剂1076、抗氧剂168的峰面积RSD分别为0.32%、0.16%、0.21%、0.25%,表明仪器精密度良好。
2.5.4 包材提取试验回收率 取五层共挤输液用袋,聚丙烯接口、组合盖,剪成小块混合,精密称定(约2.0 g),按“2.3.1”项下方法制备回收率本底供试品溶液;同法加入低、中、高浓度的抗氧剂对照溶液,制备回收率加标供试品溶液,进样测定,计算回收率,结果见表2,表明包材提取试验准确度良好。
2.5.5 相容性提取试验和迁移试验回收率 固相萃取柱使用前分别用3 mL甲醇和3 mL水依次活化。分别取24 μg·mL-1、46 μg·mL-1、240 μg·mL-1的低、中、高质量浓度对照溶液1 mL,加入醋酸钠林格注射液至100 mL,混匀。溶液以约1.5 mL·min-1的流速通过固相萃取柱,用6 mL水淋洗,分别用5 mL甲醇、3 mL二氯甲烷依次洗脱,收集洗脱液,用甲醇稀释至10 mL,0.45 μm有机膜过滤后进样测定,结果见表2,表明提取迁移试验准确度良好。

表2 回收试验考察结果 Tab 2 Recovery
2.5.6 检测限和定量限 取抗氧剂对照品溶液用二氯甲烷-甲醇(3∶7)逐步稀释测定,以各抗氧剂峰信噪比S/N为3的质量浓度作为检测限,以S/N为10的质量浓度作为定量限,结果见表3。

表3 抗氧剂的检测限与定量限 Tab 3 LOD and LOQ of different antioxidants
2.5.7 稳定性试验 将混合对照品溶液分别于0、16、24、48、96 h进样测定,结果抗氧剂1100、抗氧剂330、抗氧剂1076、抗氧剂168的峰面积RSD值分别为1.4%、1.4%、1.1%、0.90%,表明抗氧剂对照品在二氯甲烷-甲醇(3∶7)溶剂中稳定性良好。
2.6 样品测定
2.6.1 包材提取试验测定结果 取包材样品,照“2.3.1”项下方法进行制备,按外标法计算五层共挤输液用袋、聚丙烯接口、聚丙烯组合盖中各抗氧剂的含量,结果见表4。

表4 包材中抗氧剂含量(%) Tab 4 Content of antioxidants in packaging materials (%)
2.6.2 相容性提取试验测定结果 取醋酸钠林格注射液及包材样品,按“2.3.2”项下方法进行制备,按外标法计算抗氧剂在提取液中的浸出量,提取液中的抗氧剂含量均低于检测限。
2.6.3 相容性迁移试验测定结果 取醋酸钠林格注射液3批样品,照“2.3.3”项下方法进行制备,按外标法计算抗氧剂在注射液中的迁移量,注射液中的抗氧剂含量均低于检测限。
3 讨论
3.1 溶剂的选择
欧洲药典方法中使用四氢呋喃-乙腈(1∶1)作为溶剂[10]。笔者在试验中发现,抗氧剂168在使用该溶剂配制对照品溶液时不稳定,连续进样6次,峰面积呈连续下降趋势,1.5 h峰面积下降了22%。经过条件优化,最终选择二氯甲烷-甲醇(3∶7)溶液作为溶剂,4种抗氧剂峰形良好,溶液稳定性良好,96 h内峰面积没有明显变化。
3.2 固相萃取小柱的选择
抗氧剂在注射液中的迁移量很小,且不溶于水,本试验采用Cleanert S C18固相萃取柱进行富集。该固相萃取柱为高纯球型硅胶基质的反相C18萃取柱,既通过强疏水作用保留非极性化合物,又避免了普通C18对碱性与极性物质的过度吸附,更适合用于萃取低浓度分析物。
3.3 分析评价阈值(AET)与方法检测限比较
根据《化学药品注射剂与塑料包装材料相容性研究技术指导原则(试行)》[9]要求,分析测试方法应满足待测物AET的测定要求,选择可达到其能灵敏检出的分析方法。AET计算方法为各抗氧剂最大日暴露量(PDE)与最大剂量的比值,醋酸钠林格注射液的最大日剂量为1000 mL,即AET=PDE/1000。由文献[21]可知,PDE值有两种计算方法,可采用口服途径PDE数据的10%计算注射途径的PDE值,则抗氧剂1010、抗氧剂330、抗氧剂1076、抗氧剂168的PDE值分别为15、5、0.5、5 mg·d-1,其对应的AET值分别为15、5、0.5、5 μg·mL-1;也可按动物NOEL数据计算注射途径的PDE值,抗氧剂1010、抗氧剂330、抗氧剂1076、抗氧剂168的PDE值分别为10、200、0.3、2.5 mg·d-1,则其对应的AET值分别为10、200、0.3、2.5 μg·mL-1。本方法抗氧剂1010、抗氧剂330、抗氧剂1076、抗氧剂168的提取迁移试验检测限分别为0.011、0.011、0.023、0.046 μg·mL-1,远低于两种方法对应的AET值,灵敏度高,方法可行。
3.4 安全性评估
五层共挤输液袋、聚丙烯接口及聚丙烯组合盖中的抗氧剂单个含量和总含量均小于0.3%,符合欧洲药典[10]和《化学药品注射剂与塑料包装材料相容性研究技术指导原则(试行)》[9]规定的单个抗氧剂含量不得过0.3%,总量不得过0.3%的限度要求。五层共挤输液袋、聚丙烯接口及聚丙烯组合盖在醋酸钠林格注射液高压121℃浸提1 h的提取试验及迁移试验中检出量均低于检测限,试验结果可为其安全性提供数据参考。

