755例质子泵抑制剂致新的和严重的药品不良反应报告分析
周秀丽,刘宝生,宫凯凯,纪强(.阳光融和医院药学部,山东 潍坊 26000;2.潍坊市中医院临床药学科,山东 潍坊 26000;.滨州医学院附属医院肿瘤研究实验室,山东 滨州 25660)
质子泵抑制剂(PPIs)具有强大而持久的抑酸作用,广泛用于治疗急、慢性消化系统相关性疾病,例如胃食管反流病(GERD)、卓-艾综合征、消化性溃疡、上消化道出血及相关疾病、根除幽门螺杆菌(Helicobacter pylori,H.pylori)感染以及预防和治疗应激性胃黏膜病变等[1-2],这类药物主要包括奥美拉唑、兰索拉唑、泮托拉唑、雷贝拉唑、艾司奥美拉唑以及艾普拉唑等。随着该类药物的普遍应用,逐渐显现出超适应证、超剂量、超疗程用药以及药物联合使用不当等不合理用药现象,这可能会增加患者用药的风险以及经济负担[3-4]。为了解山东省PPIs致ADR发生的情况及特点,笔者对2018年1月—2020年9月山东省ADR监测中心收集到的PPIs致新的/严重的ADR病例报告进行统计和分析,为进一步促进临床安全合理使用PPIs提供参考。
1 资料与方法
1.1 资料来源
2018年1月—2020年9月山东省医疗机构、药品生产企业、经营企业、个人向山东省ADR监测中心自愿上报,经评估认定有效的所有PPIs致ADR病例报告,并根据《药品不良反应报告和监测管理办法》[5]筛选出符合标准要求的新的和严重的ADR病例报告。
1.2 统计方法
对新的和严重的ADR报告进行信息提取,包括患者的性别、年龄、原患疾病、有无既往史或家族ADR史、ADR的发生对原患疾病的影响及ADR转归情况、药品种类、给药途径、用法用量、用药原因、ADR发生时间分布、ADR累及的系统/器官及临床表现等,采用Excel电子表格和手工检索对数据进行回顾性分析与描述。
2 结果
2.1 ADR基本情况
PPIs致ADR共计3925例,其中新的和严重的ADR 755例(19.24%),包括严重的288例(7.34%),新的严重的71例(1.81%)以及新的一般的396例(10.09%)。在755例新的和严重的ADR报告中,关联性评价为可能的362例(47.95%),为很可能的365例(48.34%),为肯定的28例(3.71%)。上报单位中医疗机构上报745例(98.68%),生产企业上报8例(1.06%),经营企业上报2例(0.265%)。
2.2 患者性别、年龄基本情况
在755例新的和严重的ADR报告中,男性378例(50.06%),女性375例(49.67%),不详2例,男女比例为1∶1.01。≥65岁的患者ADR发生例次最多,其次为45~64岁,见表1。
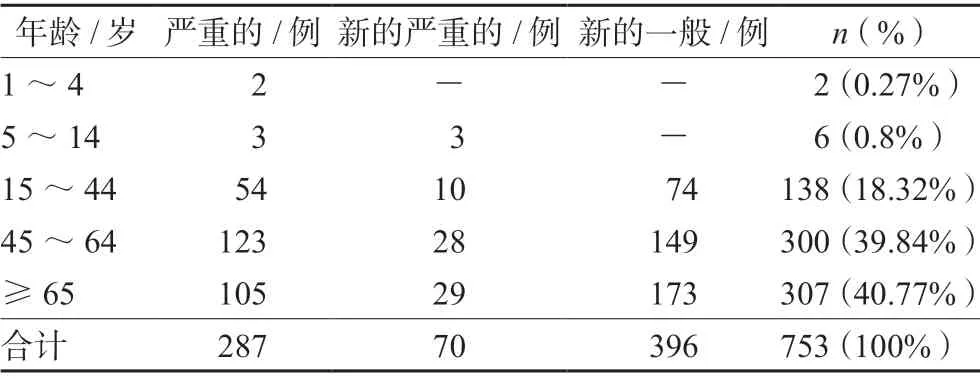
表1 发生ADR患者的年龄分布 Tab 1 Age distribution of patients in ADR cases
2.3 患者原患疾病、既往ADR史、家族ADR史
在755例新的和严重的ADR报告中,原患疾病以消化系统疾病为主,共438例(58.01%);其次为心脑血管系统,共127例(16.82%),见表2。既往出现过ADR史患者有31例(4.11%),其中14例患者为药物过敏史,包括奥美拉唑2例,卡马西平1例、磺胺类2例、利伐沙班1例、热毒宁1例、丹参注射液1例、左氧氟沙星1例、头孢类1例、青霉素3例以及具体药物不详1例,其余17例未记录具体ADR原因;无既往ADR史患者511例(67.68%),既往ADR史记录不详的患者201例(26.62%),未记录既往ADR史患者12例(1.59%)。无家族ADR史患者478例(63.32%),家族ADR史记录为不详患者263例(34.83%),家族ADR史未记录患者14例(1.85%)。
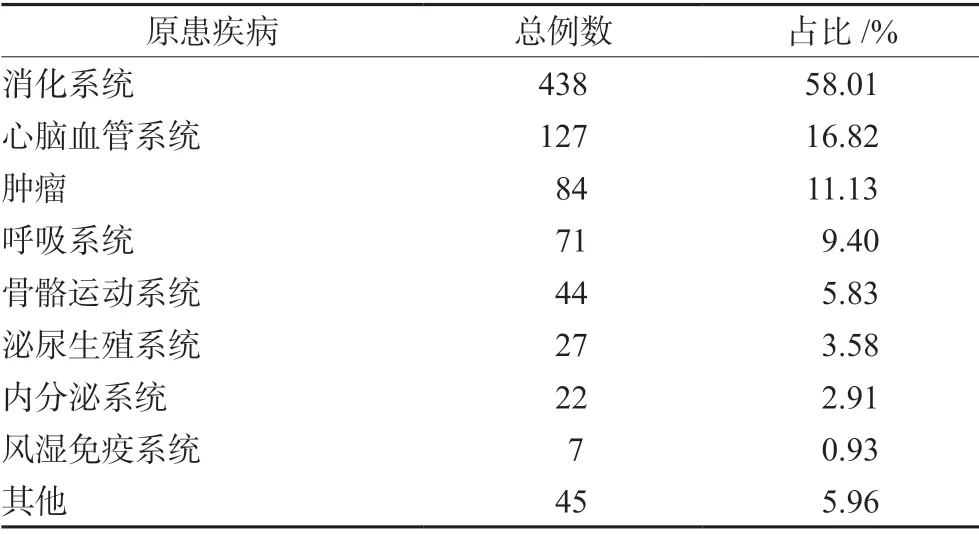
表2 患者原患疾病分布 Tab 2 Distribution of primary diseases
2.4 ADR对原患疾病的影响及ADR转归情况分析
在755例新的和严重的ADR报告中,ADR的发生对原患疾病病程影响不明显的698例(92.45%),致使患者病程延长的50例(6.62%),导致患者病情加重的7例(0.93%)。所有患者经过停药或救治处理后,痊愈368例(48.74%),病情好转373例(49.40%),病情未好转4例(0.53%),转归不详10例(1.32%)。
2.5 可疑药品的品种及给药途径
ADR涉及的可疑药品主要包括6种PPIs,剂型为注射剂型和口服剂型。其中奥美拉唑引起的新的和严重的ADR数量最多(47.15%),其次为泮托拉唑(31.52%)。静脉给药是引发ADR的主要给药途径,静脉滴注共554例(73.38%),其次为口服给药123例(16.29%),见表3。

表3 ADR涉及的药品品种及给药途径 Tab 3 Drug types and administration routes involved in ADRs
2.6 质子泵抑制剂用药原因
在755例ADR报告中,用药原因排名前五的有胃炎(包括急、慢性胃炎)、胃酸分泌过多、保护胃黏膜、预防应激性溃疡以及消化性溃疡,此外,其他用药原因的占比(14.05%)也较大,见表4。
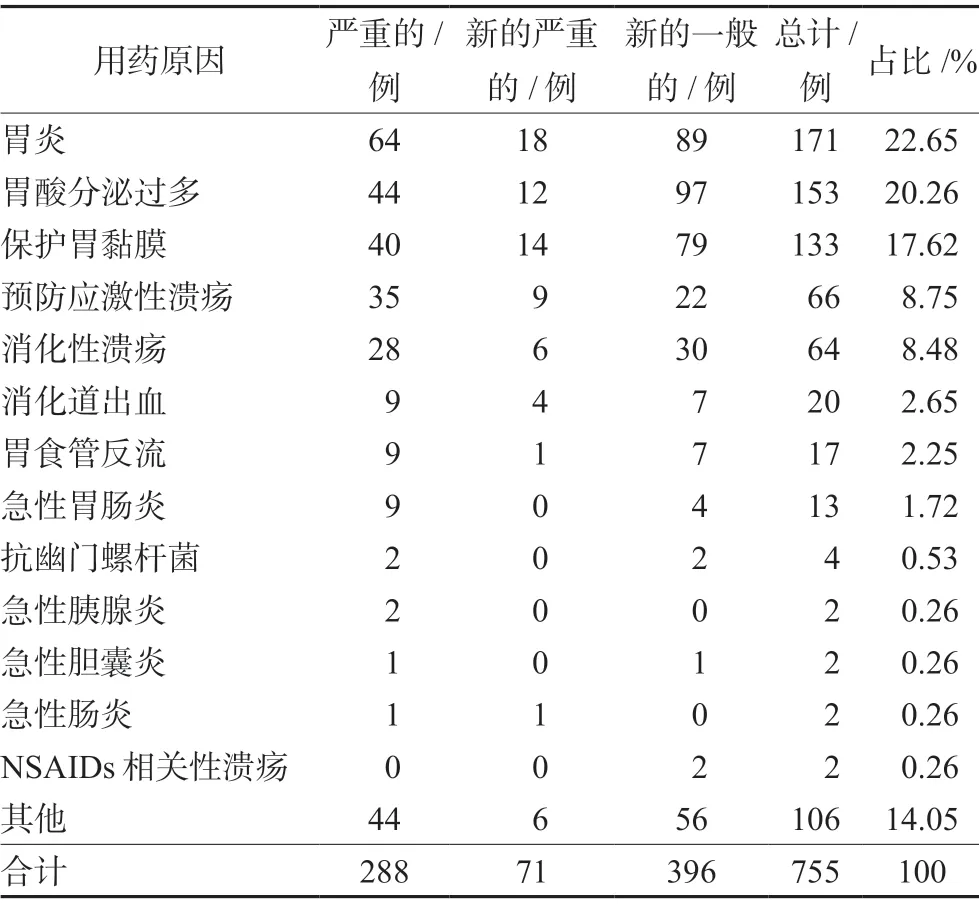
表4 质子泵抑制剂用药原因 Tab 4 Reasons for medication of proton pump inhibitors
2.7 质子泵抑制剂的用量分布
在PPIs用量分布中,奥美拉唑、泮托拉唑以及艾司奥美拉唑用量为40 mg qd所致的ADR数量最多,分别为198例、120例及14例。兰索拉唑所致ADR数量最多的用量为30 mg qd,共涉及48例。雷贝拉唑致ADR数量最多的为20 mg qd,共涉及27例,见表5。
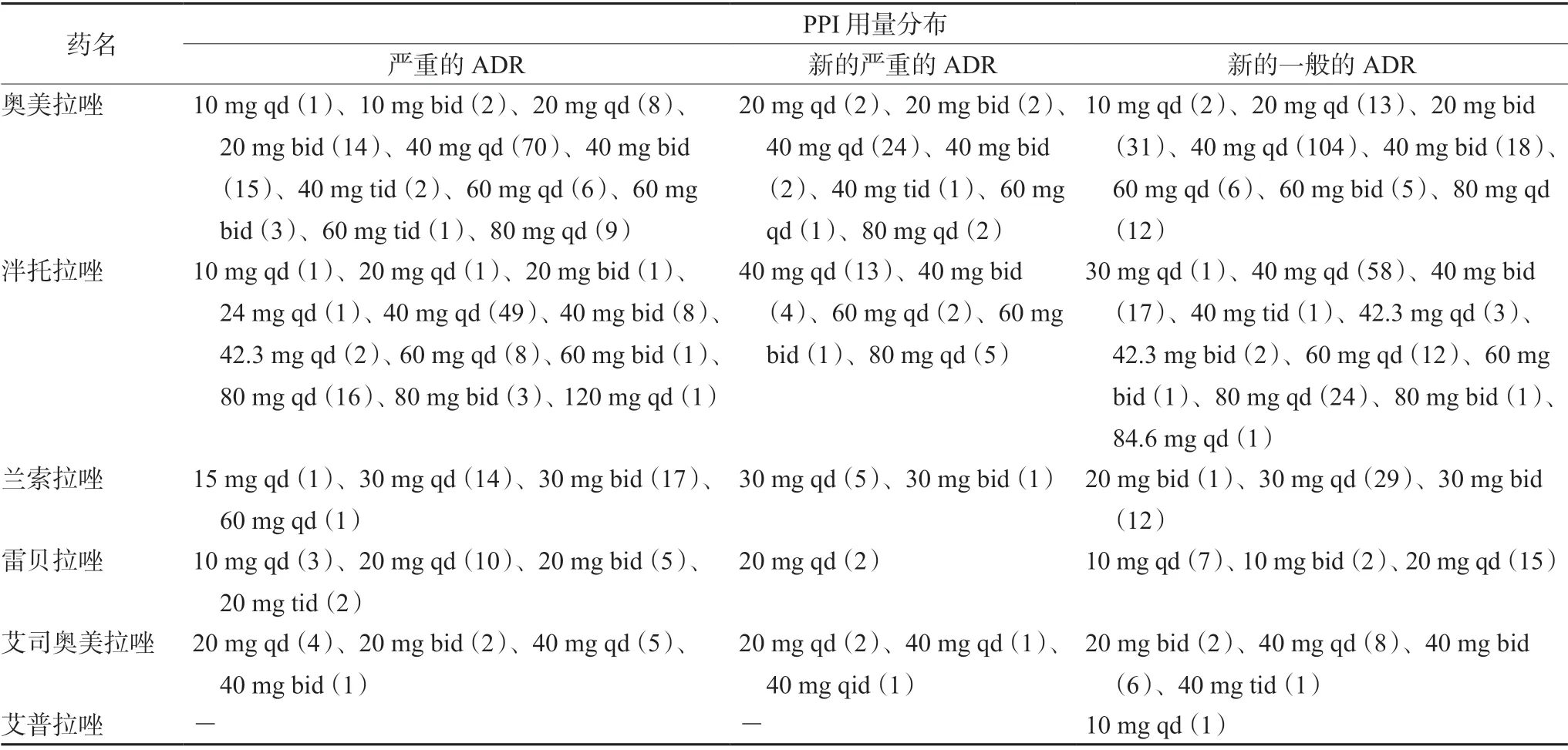
表5 质子泵抑制剂用量 Tab 5 Usage for proton pump inhibitors
2.8 ADR发生时间
从发生时间来看(除去未记录的),主要集中在10~25 min内,其次是2~5 d,最短发生于0~5 min,最长可在用药7 d后发生,见表6。
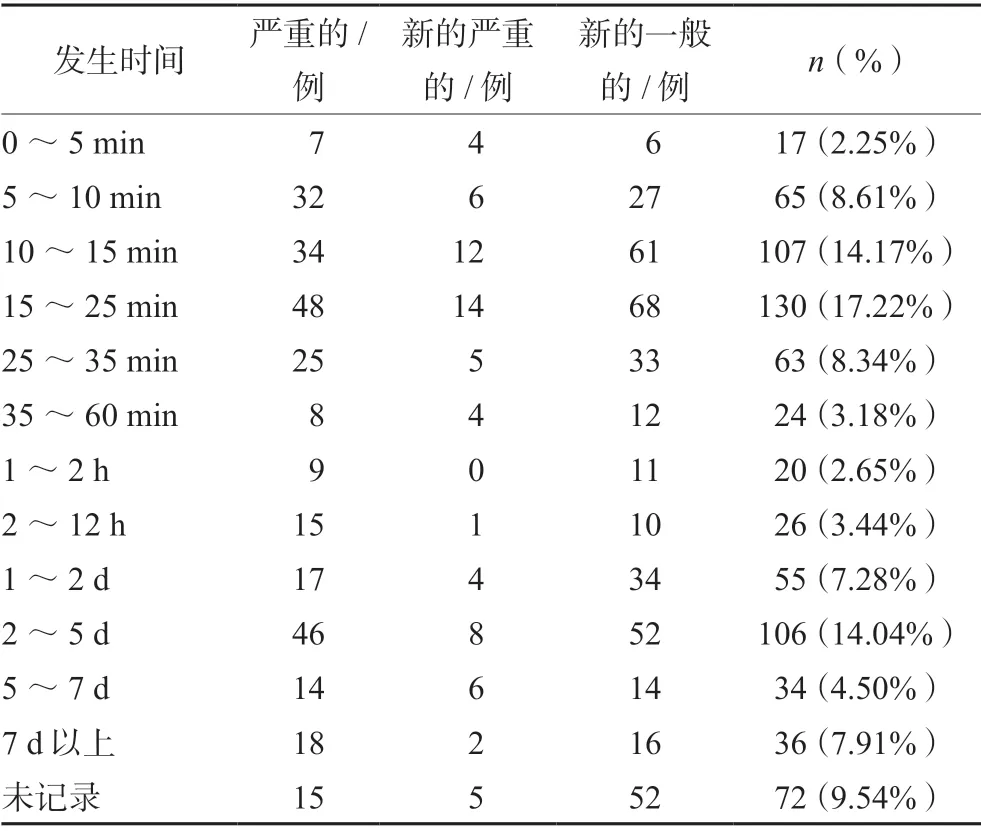
表6 ADR发生时间与例次 Tab 6 Onset times and numbers of ADRs
2.9 ADR累及的系统/器官及临床表现
在755例ADR报告中发现PPIs 导致的ADR可同时累及多个系统/器官,其临床表现共涉及1357例次,主要累及全身系统损害,表现为寒战、多汗、发热、过敏性休克等;其次累及皮肤及其附件损害,表现为瘙痒、皮疹、皮肤潮红等,见表7。

表7 ADR累及的系统/器官情况 Tab 7 Involved organs and systems of ADRs
3 讨论
3.1 基本情况分析
在755份新的和严重的ADR报告中,部分ADR会导致患者病程延长或病情加重,对于基础疾病较多的老年患者或病情较重的患者来说,可能会增加用药风险。既往有ADR史的患者发生严重的ADR的风险较高,临床对患者既往ADR史和家族ADR史知晓率不高。针对以上问题,临床药师建议在患者用药前应详细询问患者ADR史,同时用药过程中应加强观察与监测,及时与患者沟通用药反应,避免发生严重的ADR。总体来看,各年龄段均有新的和严重的ADR的发生,且无性别差异,65岁以上老年人发生最多,老年人PPIs药动学与青年人相似,一般无需调整剂量[6-7],但老年人生理机能逐渐出现下降且多合并其他基础疾病,较青年人易发生ADR[8-9],故对于老年患者应严格掌握适应证,从低剂量开始,考虑短疗程用药。此外,笔者发现有8例儿童患者发生严重的ADR,值得注意的是该类药物暂未在中国获批儿童适应证,因此临床药师建议原则上儿童不使用此类药物,如需使用应向医疗机构备案超说明书用药,并在患者知情同意下使用。
3.2 ADR与用药原因的分析
该类药物应用涉及多种疾病,以消化系统疾病为主,如急、慢性胃炎,消化性溃疡,出血等,但急、慢性胃炎并非药品说明书中明确适应证,提示超说明书用药的现象比较普遍,但对于由黏膜糜烂或酸相关症状的慢性胃炎患者,可酌情选用PPIs[10-11],由于报告描述有限,无法进一步判断应用是否合理。其次为心脑血管系统,如脑梗死、脑出血、高血压、冠心病等,这类疾病用药目的多为预防,指南提出当患者存在某些危险因素时或者出现化疗后上消化道等不适症状时可预防应用[2,11],这进一步增加了该类药物超说明书用药的数量。另外,不同PPIs用于治疗各种酸相关性胃肠道疾病的适应证有所差异,相较其他5种PPIs,奥美拉唑注射剂适应证说明书规定最广,因此应用数量最多,可能为其发生ADR数量最多的主要原因。笔者还发现实际用药中存在泮托拉唑、雷贝拉唑、兰索拉唑注射剂型用于预防应激性溃疡的现象,这已超出说明书适应证范围并可能增加ADR发生率。以上提示实际用药中存在一定盲目扩大适应证的情况,因此,临床药师建议应根据疾病的治疗目标、药物的效应及患者的意愿,选择适宜的药物,避免盲目扩大适应证,以减少ADR的发生。
3.3 ADR与用法用量分析
雷贝拉唑注射剂型相较于口服剂型其适应证仅限于上消化道出血,应用范围相对较小,因此口服给药导致新的和严重的ADR例数多。其他类PPIs的两种剂型均存在2~3种相同适应证,对于住院患者使用静脉给药的人数较多。该类药物发生ADR频率较高的用量均为常规给药剂量[1-2],这与常规用量患者基数较大有一定关系。有文献提出若患者存在难治性GERD、非静脉曲张性上消化道出血等较严重病情时,往往需加大剂量或增加给药频率[12-13],这势必会增加ADR发生的风险。笔者发现超出常规剂量时发生ADR的例数也相对较多(237例,占比31.39%),因此,临床药师建议对于轻、中度疾病的患者,首选口服给药,在治疗卓-艾综合征等须增加给药剂量或频率的情况时,应增加对患者的用药监护,及时评估治疗效果,一旦达到治疗目标应及时改口服或逐渐停药,以避免严重ADR的发生。
3.4 ADR发生时间分析
该类药物新的和严重的ADR主要为速发型ADR,而用药2~5 d后,发生ADR的例次相对也较高,一方面可能是该类药物用药疗程大多在这个时间范围内;另一方面也可能在多次给药后体内药物浓度逐渐趋于稳定,当再次给药时更易诱发ADR的发生。因此建议临床医疗工作者持续密切观察用药反应,一旦发现严重ADR,立即停药并采用积极措施救治患者。
3.5 ADR的临床表现分析
PPIs具有基本相同的作用机制,故发生ADR所累及的系统/器官基本相似[14],全身系统损害中过敏性休克最快发生于用药2 min后,最晚发生于用药4 h后,但主要集中在用药后30 min内,主要涉及奥美拉唑、泮托拉唑以及雷贝拉唑,注射剂较口服剂发生迅速,因此在给药后30 min内应严密监测患者的用药反应,一旦发生过敏性休克,应及时停药并给予抢救。值得注意的是,奥美拉唑、泮托拉唑、雷贝拉唑以及兰索拉唑均可引起罕见的血液系统损害,且大多发生在用药后的4~14 d,主要表现为白细胞、中性粒细胞、血小板以及血红蛋白减少,除有1例患者导致病情延长未好转外,其他8例经停药和对症治疗后均好转。对于该类药物引起白细胞以及粒细胞减少的机制目前暂无确切研究,有人认为是免疫抑制机制或者骨髓抑制机制,或者两者混合机制[15]。对于血小板减少,有研究认为PPIs与血小板表面糖蛋白 GPⅡb/Ⅲa、GPⅠb/Ⅸ 特异性表位结合,引起机体免疫反应,直接或间接破坏血小板、使血小板生成减少,但当药物清除后,血小板可逐渐恢复正常[16-17]。另有研究提出,由于PPIs抑制胃酸分泌,胃内pH升高,长期服用后可导致铁吸收减少,从而诱发血红蛋白合成降低[18]。近年来有关PPIs致肝胆损害的报道逐渐增多[19-21],本研究中PPIs导致肝胆损害的有27例,最短的在用药2 d后发生,最长的在用药29 d后发生,有研究认为可能是由于PPIs经过P450 酶代谢,与P450酶的基因多态性相关或可能与特异性反应相关[22],但雷贝拉唑、泮托拉唑的代谢并不完全依赖于P450酶,因此可能存在其他机制,也可能与患者的特异质有关[23]。PPIs致肝损害以肝细胞损伤型为主,其恢复时间相对较短,且一般预后良好[24]。笔者还发现部分PPIs还可引起患者痛风,主要为艾司奥美拉唑(2例)和泮托拉唑(2例)用药后6~9 d引起,有研究指出PPIs可能对肾小管H+/K+-ATP酶产生抑制作用,致机体肾小管酸碱平衡紊乱和/或尿酸代谢障碍,进而导致痛风复发或加重,但具体机制仍待研究[25-26]。血液系统损害、肝胆系统损害以及痛风均为相对罕见的不良反应,虽发生率低,但严重程度较高,临床应重视,在用药过程中进行监测。
此外,笔者通过查阅药物说明书发现不良反应项下对循环系统以及呼吸系统相关ADR的临床表现缺少相关描述,这类不良反应通常伴发于其他不良反应的过程中,往往不易引起临床重视,因此实际应用中应加强对该类ADR的分辨,以便及时采取应对措施。
综上所述,临床在应用PPIs时存在一定超适应证、超用法用量等现象,建议临床应严格把握适应证,按照药品说明书和指南规范用药,同时对儿童患者应谨慎用药,若必须使用应做好超说明书用药备案和相关知情同意;对老年患者用药应遵循低剂量、短疗程原则,必要时加强用药监护。该类药物致血液系统损害、肝胆系统损害以及痛风等相对罕见的严重ADR数量较多,循环系统损害和呼吸系统损害等新的ADR也时有发生,因此临床药师应加强用药监护,增强与临床医师的沟通与交流,同时呼吁各生产厂家及时补充说明书中ADR内容,保障患者安全用药。

