冬枣粉吸湿的色泽、热力学特性及糖物质基础分析
夏晓霞,薛艾莲,寇福兵,赵吉春,温 靖,肖更生,曾凯芳,明 建,*
(1.西南大学食品科学学院,食品贮藏与物流研究中心,重庆 400715;2.广东省农业科学院蚕业与农产品加工研究所,农业农村部功能食品重点实验室,广东省农产品加工重点实验室,广东 广州 510610)
枣(Mill.)是一种重要的果品和常用的中药,其含有大量的生物活性物质。研究表明,枣是维生素、多糖、环磷酸腺苷、多酚类物质、矿物质的良好来源,这些生物活性物质具有抗氧化、抗炎、抗癌、抗心血管疾病、保肝等功能,在预防和抑制不同疾病中发挥着重要作用。目前,枣除鲜食外,已广泛应用于制作枣汁、枣酱、枣粉、枣蜜等产品。
食品粉末通常易从周围环境中吸收水分,是吸湿性材料,这也正是枣粉加工中的一个瓶颈。由于枣粉中含有大量处于无定形态的糖类、有机酸等物质,极易吸湿结块,严重影响了枣粉的品质,最直观的现象就是色泽的变化。吸附等温线可反映平衡水分含量与水分活度()之间的关系,能了解物料与水分子之间的吸附机理,已被广泛应用于预测食品的货架期和储存稳定性。目前,有较多数学模型可以用于吸附等温线的拟合,如Peleg、GAB(Guggenheim-Anderson-de Boer)、BET(Brunauer-Emmett-Teller)、Halsey模型等。Rosa等研究发现番木瓜种子的吸附等温线呈II型,Peleg模型可较好地拟合(>0.99)。Oh等研究发现红薯的吸附等温线呈II型,GAB模型较好地解释干红薯的吸湿特性。此外,可通过吸附等温线计算出水分吸附过程中的净等量吸附热()及微分熵(Δ),进而解释其吸附机理和能量需求。如菠萝粉表现出两个吸附区:在低水分含量下,水分吸附由熵机制控制;在高水分含量下,由焓机制驱动。干制‘储良’龙眼的水分吸附过程为焓驱动,且是自发性的。目前,关于枣粉的吸湿结块研究大多是通过添加抗结剂来改善枣粉吸湿性,而对枣粉吸湿过程的水分吸附特性以及粒径对枣粉吸湿性的影响鲜有研究。了解枣粉吸湿过程中的水分吸附特性对于干燥终点的判断、预测其在贮存期间的稳定性及选择合适的包装材料非常重要。此外,了解枣粉中引起枣粉吸湿的主要糖类物质可为枣粉吸湿改善提供参考。因此,本研究采用静态称量法来探究枣粉的吸附特性,观察其吸湿前后的色泽变化,研究超微粉碎前后的吸附等温线及热力学性质的变化,确定枣粉吸湿的糖物质基础,以期为枣粉贮藏条件的选择提供理论参考。
1 材料与方法
1.1 材料与试剂
山东沾化冬枣,购自农贸市场,挑选大小均匀、成熟度一致、无明显病斑果实清洗干净并去核,置于-40 ℃冰箱待用。
LiCl、CHCOOH、MgCl、KCO、Mg(NO)、CuCl、NaCl、KCl、KNO、PO、麝香草酚、葡萄糖、蔗糖(分析纯) 成都科龙化工试剂有限公司;果糖(分析纯) 上海阿拉丁生化科技股份有限公司。
1.2 仪器与设备
SCIENTZ-20F真空冷冻干燥机 宁波新芝生物科技股份有限公司;UltraScanPro测色仪 美国HunterLab公司;高速万能粉碎机 永康市兆申电器公司;CJM-SY-B高能纳米冲击磨 秦皇岛太极环纳米制品有限公司;ZXGP-B2080隔水恒温培养箱 上海智城分析仪器制造有限公司;DHG-9140A电热恒温鼓风干燥箱上海齐欣科学仪器有限公司。
1.3 方法
1.3.1 样品制备
参照文献[7]的方法并略作修改。将冬枣去核后切成大小均一的12个小块,在-40 ℃预冷24 h后采用真空冷冻干燥法干燥,干燥程序为:-40 ℃,3 h;-30 ℃,2 h;-20 ℃,2 h;-10 ℃,6 h;0 ℃,5 h;10 ℃,6 h;20 ℃,5 h;30 ℃,7 h(真空度<10 Pa,冷阱温度-60 ℃)。冻干枣在高速万能粉碎机中粉碎10 s,重复3 次,每次间隔3 min,过60 目筛后得到普通粉碎枣粉(普通粉)。将普通粉投入CJM-SY-B高能纳米冲击磨中,粉碎6 h(转速380 r/min,粉碎腔温度≤20 ℃),制得超微粉碎枣粉(超微粉)。制备完成后的普通粉及超微粉即为对照组。将制得的枣粉置于底部含有PO的干燥器中备用。
1.3.2 枣粉色泽和吸附等温线的测定
配制100 mL不同盐的饱和溶液并分别置于内径为120 mm干燥器底部,不同温度下干燥器内的水分活度(0.112~0.946)如表1所示。准确称量1.000 0 g枣粉于35 mm培养皿(已干燥至恒质量),将培养皿分别置于盛有不同饱和盐溶液的干燥器上部,将干燥器分别置于20、30、40 ℃的恒温培养箱中进行吸湿平衡。定期称量样品的质量,直至连续两次的质量差小于1 mg,即为吸湿平衡。采用UltraScanPro测色仪测定枣粉吸湿前后的CIELab指标(*、*、*值)并计算出其变化量(Δ、Δ、Δ),并按照式(1)~(3)分别计算其总色差(∆)、色相角()、色度()。将吸湿后的枣粉在105 ℃下干燥至恒质量并按照式(4)计算枣粉的平衡干基水分含量。NaCl、KCl、KNO饱和溶液的干燥器中需分别放置0.2 g左右麝香草酚,以抑制霉菌的生长。
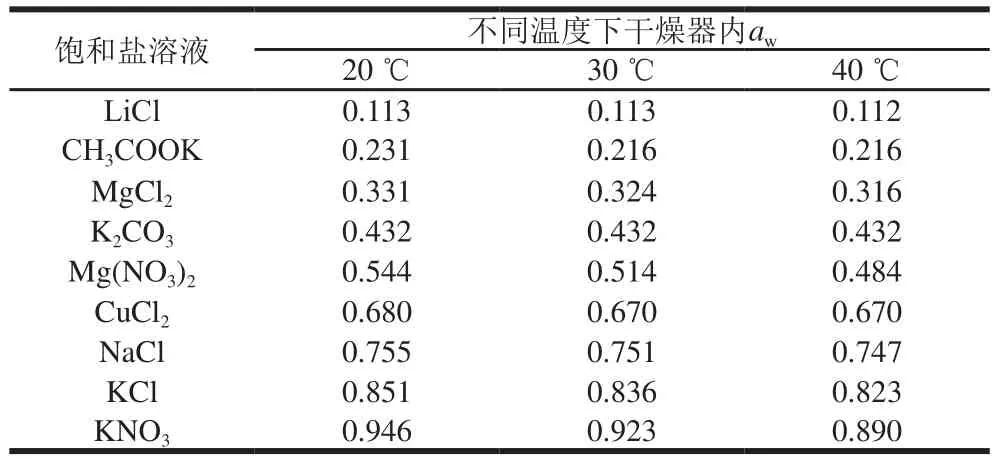
表1 不同温度下干燥器内饱和盐溶液的awTable 1 aw of saturated salt solutions at different temperatures
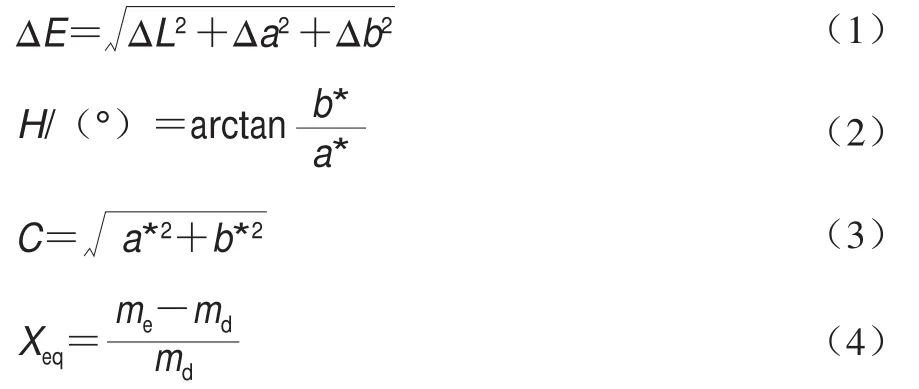
式中:是平衡干基水分含量/(g/g);是平衡质量/g;是干燥后的质量/g。
1.3.3 临界相对湿度的测定
分别作吸附等温线两端的曲线点切线,得到切线的方程式,参考文献[8]计算枣粉的临界相对湿度(critical relative humidity,CRH)。
1.3.4 吸附等温线模型拟合
本研究选用8种模型对枣粉的吸附等温线进行模型拟合(表2)。
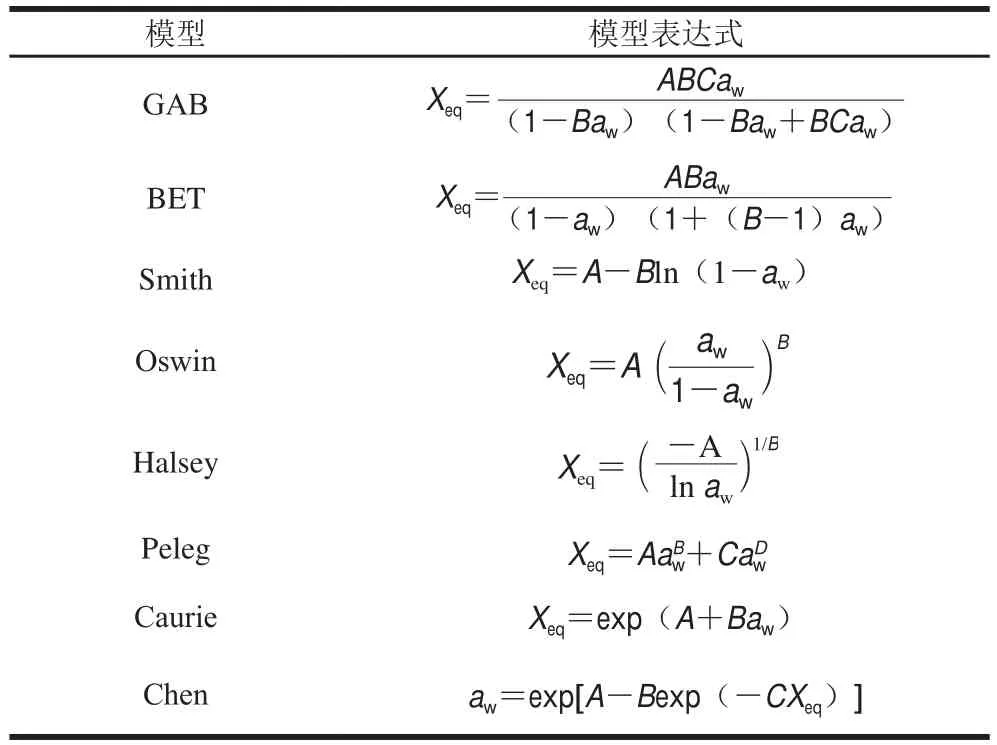
表2 吸附等温线的拟合数学模型Table 2 Mathematical models for fitting adsorption isotherm
分别用决定系数()、平均相对预测误差()、卡方误差()和均方根误差(root mean square error,RMSE)来评价所选模型的拟合优度。RMSE、、的计算分别见公式(5)~(7)。
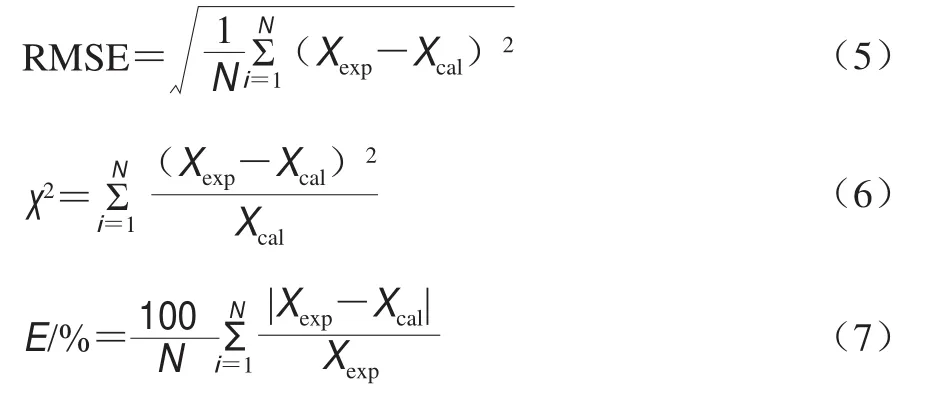
式中:是实验测得水分含量(干基)/(g/g);是模型预测水分含量(干基)/(g/g)。
1.3.5 热力学性质测定
1.3.5.1 净等量吸附热及微分熵
净等量吸附热()是向吸湿材料中除去或添加一定量水所需的最小能量,对于给定的平衡水分含量,可通过Clausius-Clapeyron方程(式(8))来确定。微分熵(Δ)与水分子和物料组分之间的引力或排斥力有关,并与物料的空间排列有关,其计算方法见式(9)。按式(10)计算吉布斯自由能(Δ)。

式中:为净等量吸附热/(kJ/mol);Δ为微分熵/(kJ/(molgK));为气体常数/(8.314h10kJ/(molgK));Δ为吉布斯自由能/(kJ/mol);为绝对温度/K;为水分活度。
整合式(8)~(10),可得到与Δ的关系式(式(11))。

1.3.5.2 熵焓互补理论
利用熵焓补偿理论可将与Δ结合(式(12)),评估促进水分吸附的熵焓驱动情况。该式表明与Δ存在线性关系,通过线性回归方程可计算与Δ,当Δ<0表明该反应是自发的,当Δ>0表明该反应是非自发的。

式中:为等速温度/K,即该温度下吸附过程中所有反应以同一速率进行;Δ为当温度为时的吉布斯自由能/(kJ/mol)。
此外,为了验证熵焓互补理论,参考Krug等提出将与(平均调和温度)相比较的方法(式(13)),当≠时,熵焓补偿理论才适用。当<时,该吸附过程为熵驱动;当>时,该吸附过程为焓驱动。

式中:为等温线条数。
1.3.6 枣粉中糖物质基础分析
1.3.6.1 枣粉中糖的组成与含量
样品的处理及测定参照文献[12]的方法并略作修改。样品处理:准确称量2.000 0 g枣粉样品,加20 mL超纯水混匀,设置超声功率150 W、温度50 ℃,进行超声提取30 min,离心取滤液(8 000 r/min、15 min),沉淀重复操作,混合两次滤液定容得到50 mL提取液,提取液过0.45 μm滤膜待测。
标准曲线绘制:称取葡萄糖、果糖、蔗糖(精确至0.1 mg)并用超纯水定容,制得质量浓度为4 mg/mL的混标溶液,过0.45 μm滤膜待用。再分别配制不同质量浓度梯度的单标溶液待测,以糖溶液质量浓度为横坐标,峰面积为纵坐标,绘制标准曲线。
色谱条件:ZORBAX-NH色谱柱(4.6 mmh250 mm,5 μm);流动相:(乙腈)∶(水)=85∶15;检测温度40 ℃;柱温30 ℃;流速1 mL/min;进样体积20 μL;示差检测器。
样品中糖的组成与质量分数测定:取枣粉提取液代替上述标准糖溶液进行测定。
1.3.6.2 枣粉及不同糖的吸湿率
参照文献[6]的方法并略作修改。准确称量1.000 0 g超微粉(/g)于35 mm的培养皿中,将其置于分别含有LiCl、MgCl、Mg(NO)、NaCl、KNO饱和溶液的干燥器上部,其水分活度如表1所示(相对湿度为水分活度值h100%)。将干燥器置于30 ℃培养箱中7 d,每隔24 h称量枣粉质量(/g)。在干燥器中放置约0.2 g麝香草酚以抑制霉菌的生长。同时设置葡萄糖、果糖、蔗糖及混合糖(按照超微粉中3种糖的相对含量配制)进行同一吸湿性的研究。吸湿率按下式计算。

1.4 数据处理与分析
每组实验平行测定3 次,实验结果以平均值±标准差表示。采用SPSS Statistics 18.0软件进行单因素方差分析,通过邓肯检验进行显著性分析,<0.05表示差异显著。采用Origin 2018软件进行相关统计分析并作图。
2 结果与分析
2.1 湿度对不同颗粒枣粉色泽的影响
如图1所示,枣粉的亮度(*值)与色相角()的变化趋势相似,随着增加,呈逐渐降低的趋势,且在相同下,普通粉大于超微粉;随着温度升高,*值、降低。枣粉的红绿度(*值)、黄蓝度(*值)与色度()均随增加而呈现先增加后降低的趋势,普通粉分别在为0.7、0.4、0.4左右时达到最大值,超微粉分别在为0.5、0.2、0.2左右时达到最大值,温度对其影响无明显规律。枣粉的色差(∆)随着增加而增加,除>0.75之外,超微粉的∆均大于普通粉。结合图2可以看出,在高下,枣粉的颜色变化较大,且超微粉大于普通粉。枣粉吸湿后颜色由淡黄色逐渐变成黄色、褐色,褐变现象较严重,可能是因为氧化和美拉德反应的存在导致的颜色变化。枣粉从环境中吸收水分后,逐渐从玻璃态转变为橡胶态,研究表明,橡胶态的褐变反应速率明显高于玻璃态,这在南瓜粉中可观察到相似的结果。同样地,通过增加也会使甜菜根提取物粉末由紫色逐渐变成褐色再变成黑色。
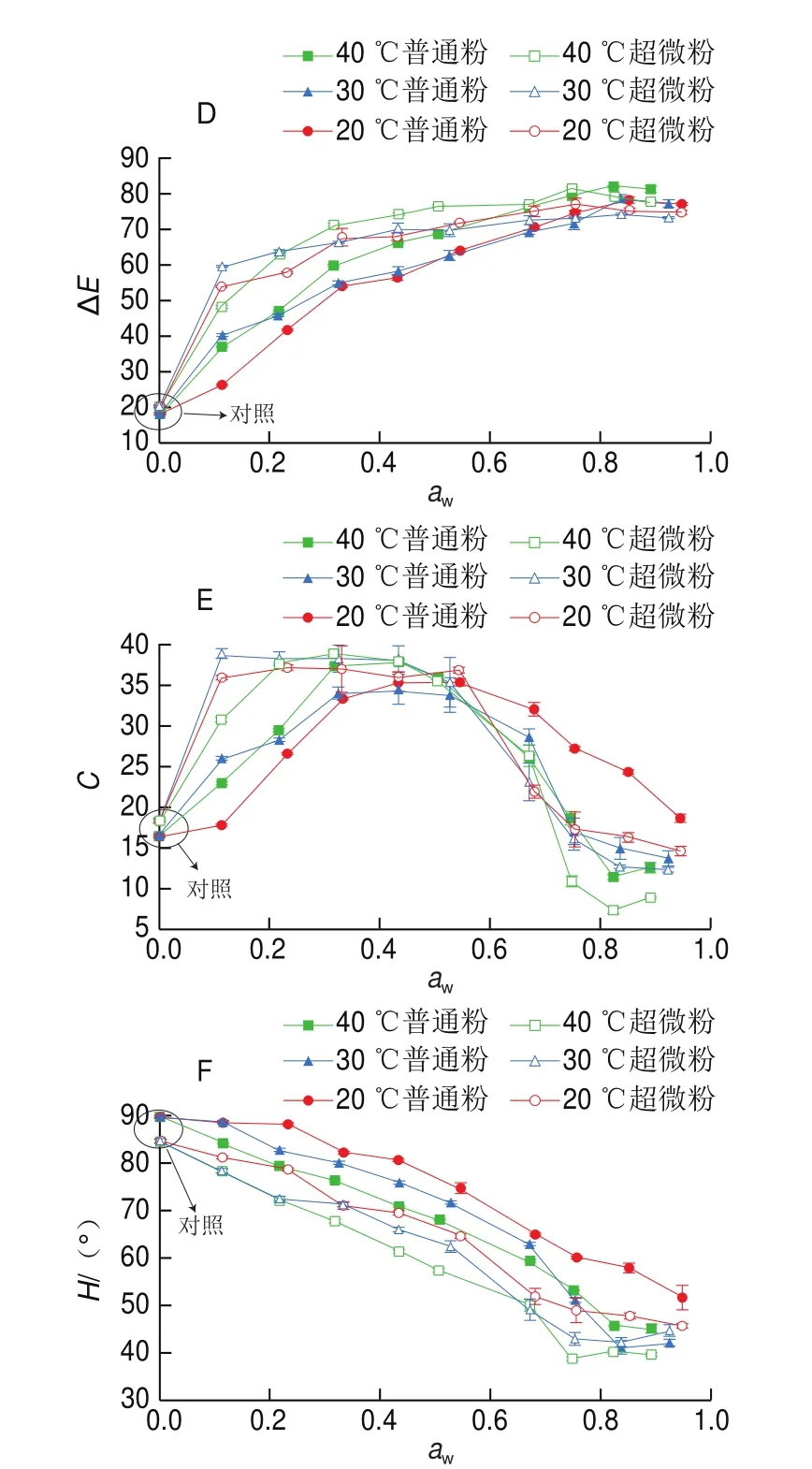
图1 不同aw条件下枣粉的色泽变化Fig.1 Color parameters of jujube powder as a function of water activity at different aw
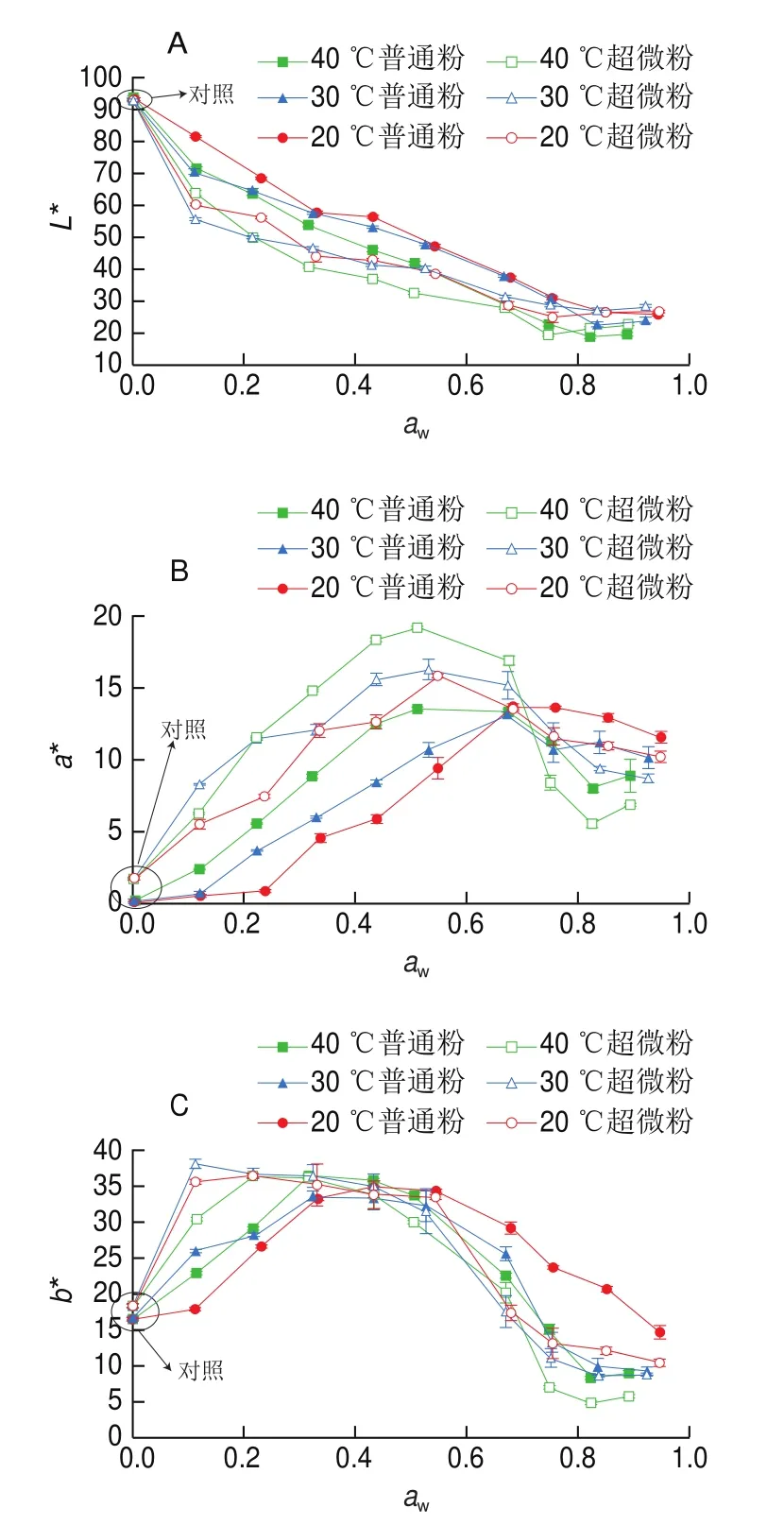

图2 枣粉在30℃、不同aw条件下吸湿平衡后色泽对比Fig.2 Color changes of jujube powder at 30 ℃ under different aw
2.2 温度对不同颗粒枣粉吸附等温线的影响
如图3所示,随着的增加,枣粉的平衡干基水分含量呈增加趋势,且在低水分活度下(<0.70)缓慢增加,高水分活度下迅速增加,可归因于物料在空气相对湿度降低时其水分的蒸气压也降低,这与芒果的水分吸附等温线趋势相似。在恒定的下,<0.70时,枣粉的平衡干基水分含量随温度的升高而降低,可能是因为随着温度的升高,分子处于增强的激发态,增加了分子间距离,降低了分子间的吸引力,从而导致吸水率降低;>0.70时,出现相反的趋势,分析原因是枣粉中含有的大量诸如糖类等可溶性物质溶解,其溶解性随着温度的升高而增大,以及晶体结构的崩溃增加了吸附位点,从而导致随温度升高枣粉的水分吸附能力也增强,这在杏片中有相似的结果。如图3所示,枣粉的吸附等温线呈“J”型(第III型等温线),该类型与糖溶解相关的溶质-溶剂相互作用相关,是典型的高含糖量物质的吸附等温线类型。就吸附现象而言,这一分类表明较弱的吸附剂(枣粉)-吸附质(水分)作用力将导致低水分活度下有限的吸湿率;然而,一旦一个水分子被吸附,吸附质-吸附质的作用力将促进更多水分子的吸附,这与枸杞粉、鳄梨等吸附等温线相似。比较两种枣粉的吸附等温线可以发现(图4),在<0.70时普通粉的吸湿能力显著优于超微粉(<0.05),>0.70时两种粉体的吸湿能力无显著性差异,表明在低水分活度下,超微粉碎有利于枣粉的贮藏。
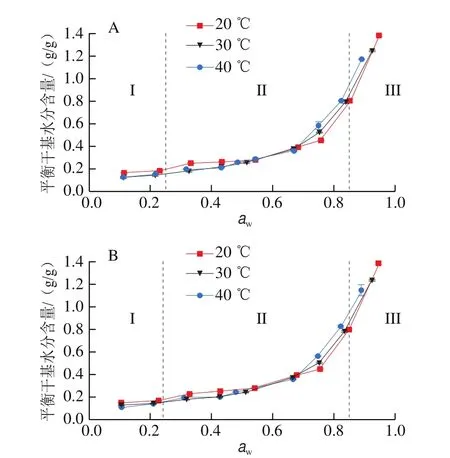
图3 温度对枣普通粉(A)、超微粉(B)吸附等温线的影响Fig.3 Effect of temperature on moisture adsorption isotherms of ordinary (A) and superfine (B) jujube powder
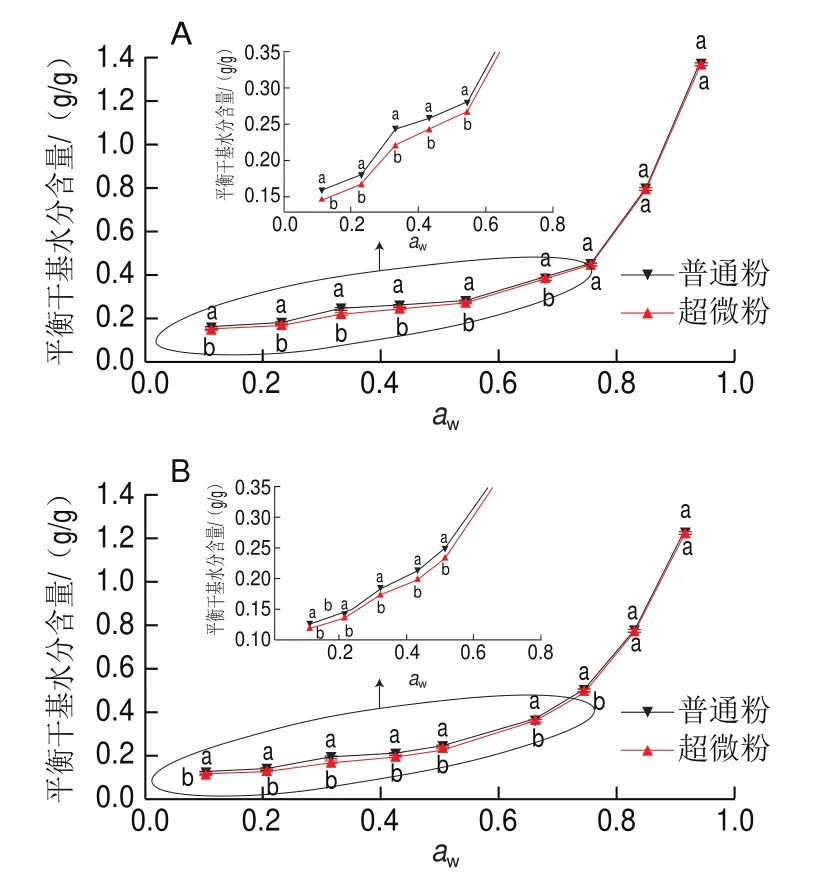
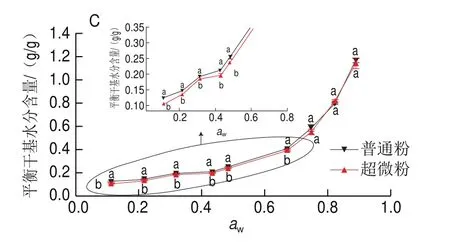
图4 超微粉碎对枣粉吸附等温线的影响Fig.4 Effect of superfine grinding on moisture adsorption isotherms of jujube powder
CRH对枣粉的贮藏有重要的指导意义,贮藏环境的相对湿度应低于枣粉的CRH,超过CRH时,枣粉的吸湿将迅速增加。如表3所示,普通粉在20、30、40 ℃的CRH分别为76.36%、72.93%、72.47%;超微粉在20、30、40 ℃的CRH分别为76.59%、72.83%、71.00%。由此可见,温度会影响枣粉的CRH,随着温度升高,枣粉的CRH呈下降趋势。因此,为保证枣粉贮藏稳定,需严格控制环境相对湿度,避免超过其CRH。
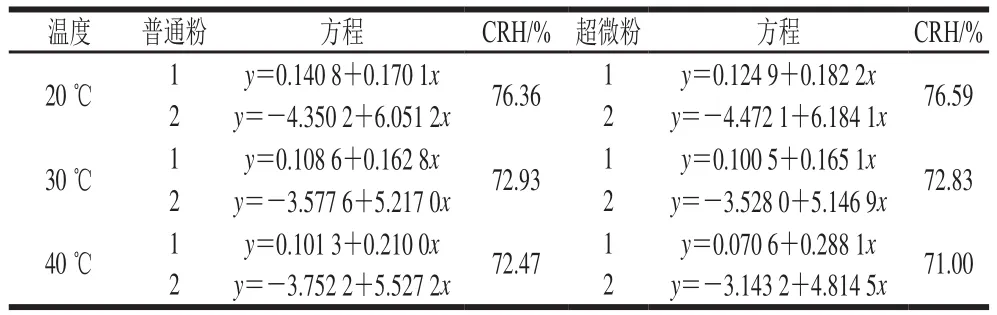
表3 枣粉吸附等温线切线方程及CRHTable 3 Critical relative humidity values of jujube powder and equations for their calculation
2.3 不同颗粒枣粉吸附等温线的模型拟合
表4列出了吸附等温线模型拟合相关参数及统计学参数,一般情况下越大,、RMSE、值越小,拟合越好;<10%时拟合效果良好,<5%时,拟合效果极好。结果显示,这几种模型拟合效果从优到次的顺序为:Peleg>GAB>Halsey>Oswin>BET>Smith>Caurie>Chen。Peleg模型拟合效果极好(<5%),其为0.995 0~0.999 6;RMSE为0.005 3~0.018 8;χ为0.001 3~0.008 6;为2.077 6%~4.763 7%。Peleg模型也同样适用于菊花粉、冬瓜粉、无花果块等的吸附等温线拟合,目前还没有一个模型能够在整个水分活度范围内准确预测所有类型的食品水分吸附等温线。图5显示了实验所测得的平衡干基水分含量与Peleg模型预测值的比较,可以观察到实测值与预测值都均匀分布在=线上或附近,实测值与预测值具有较高的相关性(为0.996 4~0.999 6)。因此,Peleg模型用于描述枣粉的水分吸附特性较佳。
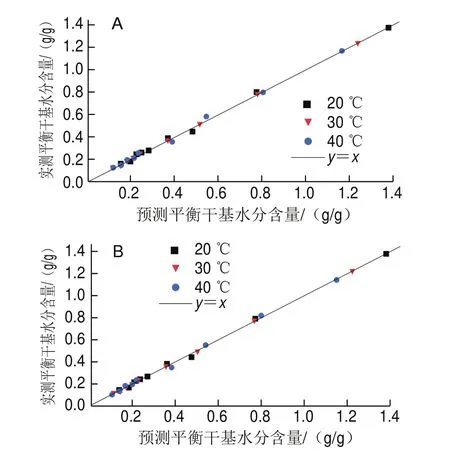
图5 普通粉(A)、超微粉(B)平衡干基水分含量的Peleg模型预测值与实测值的关系Fig.5 Relationship between Peleg model predicted and measured equilibrium moisture contents of ordinary powder (A) and superfine powder (B)
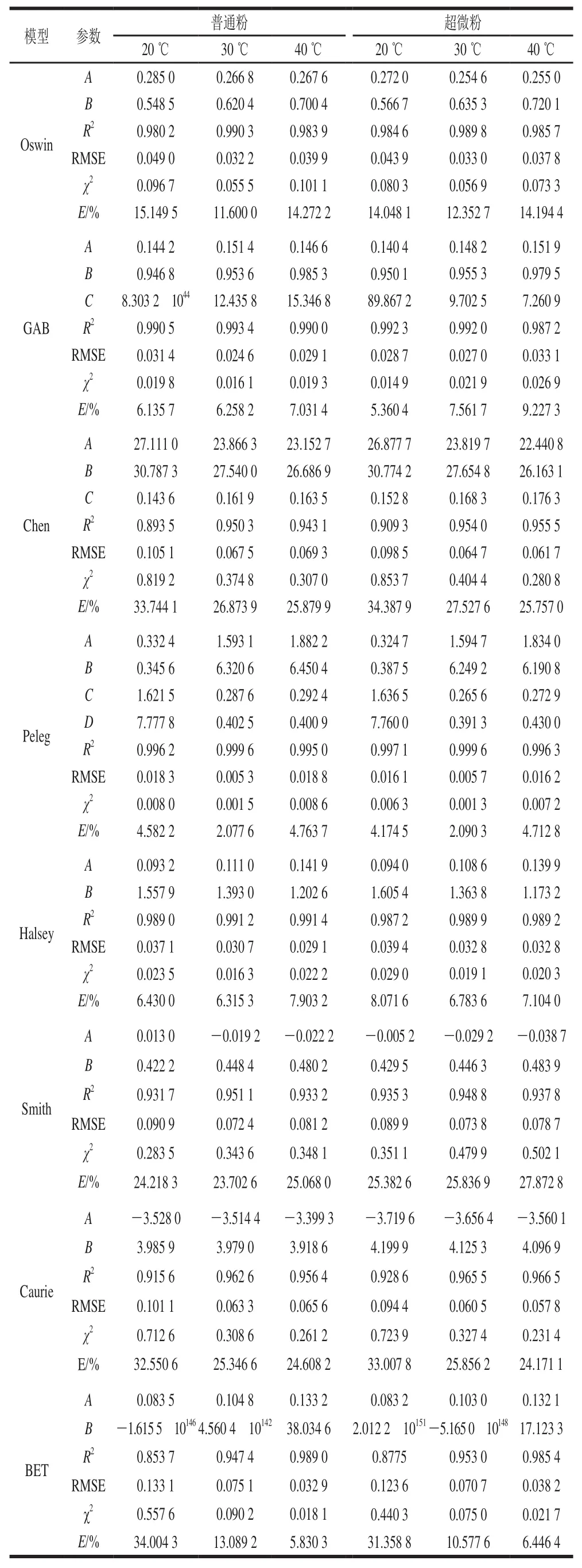
表4 枣粉吸附等温线模型拟合的统计学参数与模型参数Table 4 Estimated coefficients for isotherm models of jujube powder
为了深入理解吸附等温线上不同水分活度下枣粉的水分特性,可将吸附等温线分为:I区(<0.25)、II区(0.25<<0.85)、III区(>0.85)(图3)。I区对应的水是食品中吸附得最牢固,回潮时最先被吸入的水,这部分水在-40 ℃下不结冰,对食品的固形物不会产生增塑效应;II区是多层水区,当食品中的水分含量逐渐趋近该区间的最大值时,会引发非水物质的轻微溶解,加快化学反应速率,导致干燥食品出现轻微溶胀;III区的水是自由水,这部分水可以结冰,可作为溶剂,还可供微生物生长,有利于化学发应的进行。因此,基于Peleg模型可计算出枣粉在特定温度下每个区间临界点的水分含量,为枣粉的贮藏提供参考。以30 ℃为例,在=0.25时,普通粉和超微粉的平衡水分含量(干基,下同)分别为0.164 9、0.154 7 g/g;在=0.85时,普通粉和超微粉的平衡干基水分含量分别为0.839 7、0.826 8 g/g。
控制食品的水分含量可有效抑制微生物的生长繁殖。目前,普遍认为食品中的<0.70时,可显著抑制酵母菌、霉菌及细菌的生长;当<0.50时,几乎所有微生物无法生长繁殖。因此,枣粉=0.70时的水分含量是相对安全的;=0.50时的水分含量是绝对安全的。由Peleg模型回归方程可计算出普通粉和超微粉的相对安全及绝对安全的水分含量。以30 ℃为例,普通粉和超微粉的相对安全水分含量分别是0.416 3、0.402 7 g/g;绝对安全水分含量分别为0.237 5、0.223 5 g/g,枣粉在加工时有效控制其水分含量在绝对安全水分含量以下,有利于枣粉的贮藏。
2.4 不同颗粒枣粉水分吸附的净等量吸附热及微分熵
根据Peleg模型拟合的数据来计算枣粉的和Δ。由式(11)可知,以1/为横坐标,-ln为纵坐标作图,由曲线斜率可推算出、由曲线截距可推算出Δ。如图6所示,每条曲线确定了在特定水分含量的情况下蒸发吸湿区域中的水所需的净热量。由图7可知,随着平衡水分含量的增加呈指数下降,表明在低水分含量下去除枣粉中存在的水分需要更高的能量。当0.05 g/g<<0.30 g/g时,普通粉和超微粉的分别从38.50、34.77 kJ/mol下降至0.59、0.07 kJ/mol;当>0.30 g/g时,两种粉的均趋于稳定。分析原因是由于水和吸附剂表面(枣)之间结合强度的变化,如图8所示,在吸附初始(低水分含量),吸附剂(枣粉)表面有许多具有高相互作用能的高活性极性吸附位点,这些位点通过较强静电相互作用被水分子逐渐覆盖,形成单分子层;由于水分子之间存在较强的分子间作用力,当有单分子层水分吸附后,便会由内向外吸附更多层水分子,即吸附开始发生在相互作用能较低的较不活跃的位置(高水分含量)。是吸附热与水蒸发潜热之间的差值,当>0.30 g/g时,趋近于0,表明吸附热接近汽化热,在这种状态下被枣粉吸附的水分大部分都是自由水,且逐渐趋于稳定。因此,随着水分含量的增加,水分由单分子层吸附变成多分子层吸附,吸附剂表面的作用力逐渐减弱,相应地逐渐降低,这在杨梅粉、干制甜瓜种子中出现类似的结果。Δ的变化趋势与相似,当<0.35 g/g时,Δ迅速下降;当>0.35 g/g时,Δ逐渐趋近于0,意味着在吸附过程中物料表面的吸附位点逐渐减少,最终趋近于0。在高水分含量下,物料的活性位点趋于饱和,物料的结构特征使得其对吸水性影响较小,从而微分熵趋于接近纯水的值(Δ=0)。
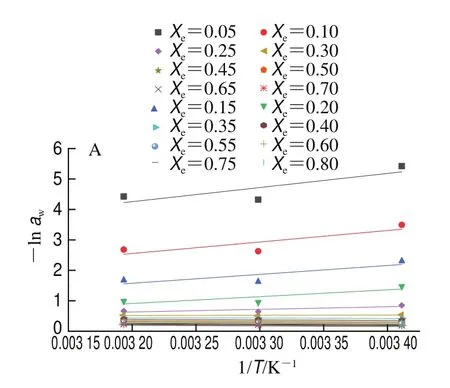
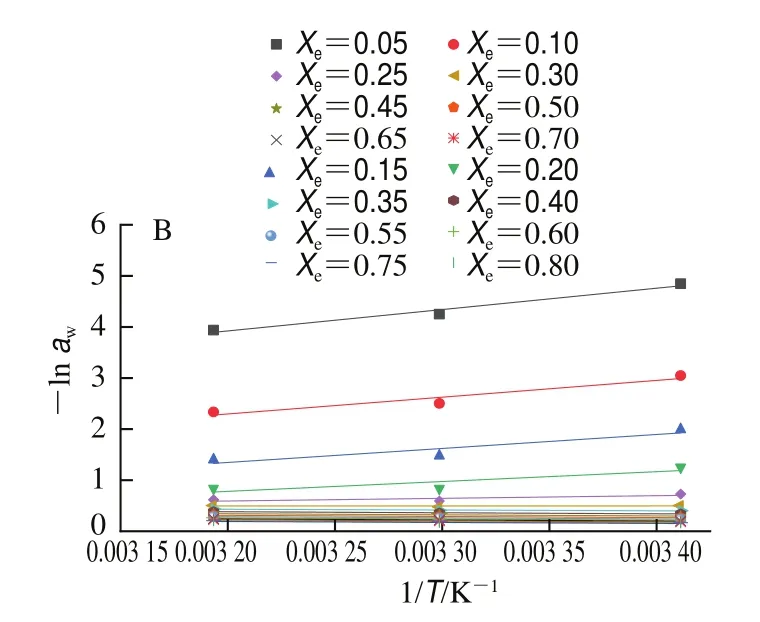
图6 普通粉(A)、超微粉(B)水分吸附过程中1/T与-ln aw关系Fig.6 Relationship between 1/T and (−ln aw) for water adsorption of ordinary powder (A) and superfine powder (B)
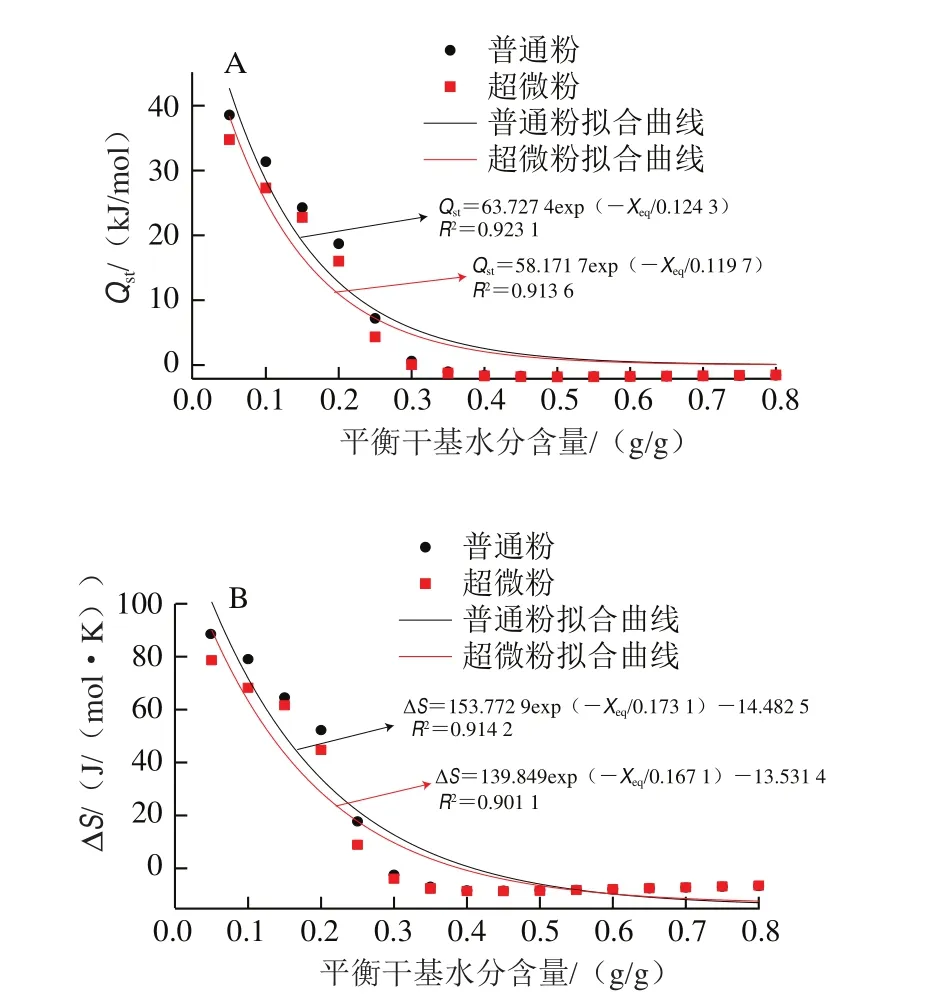
图7 枣粉Qst(A)和ΔS(B)与平衡干基水分含量的关系Fig.7 Relationship between Qst (A) and ΔS (B) of jujube powder and its equilibrium moisture content
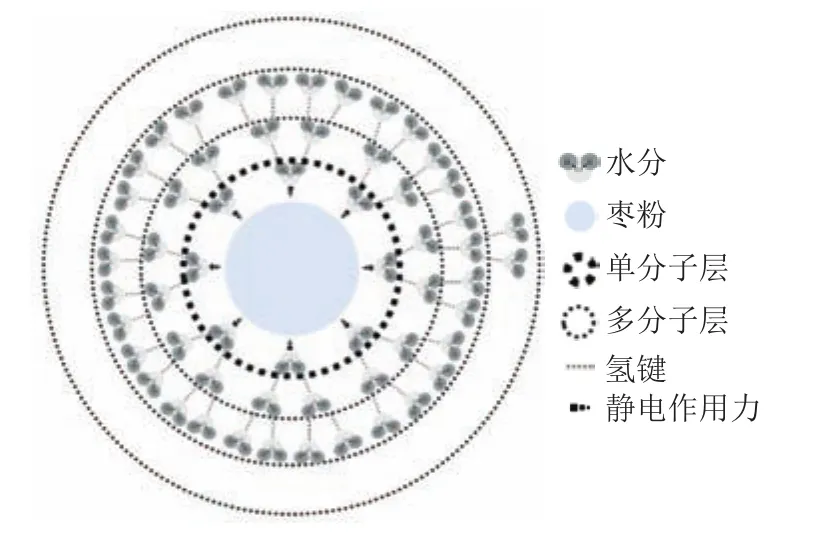
图8 枣粉颗粒水分吸附模拟图Fig.8 Simulation diagram of water adsorption of jujube powder particles
相较于两种粉体,在低水分含量下,普通粉的和Δ始终高于超微粉,表明在水分吸附过程中普通粉对传热、传质有较大的阻碍作用,水分子的吸附需要消耗更多的活化能,同时普通粉的吸附位点比超微粉多,吸附的水分更多;高水分含量时两种粉体的和Δ几乎相同,此结果与吸附等温线结果保持一致。
2.5 不同颗粒枣粉水分吸附的熵焓补偿理论
如图9所示,两种枣粉的和Δ均呈线性关系,且线性关系较好。普通粉和超微粉的分别为385.69、384.63 K,显著大于平均调和温度(302.93 K),因此证实了枣粉样品吸附现象的补偿理论,且枣粉的吸附机制是焓驱动,这表明枣粉的微观结构是稳定的,在吸湿过程中不会发生任何变化,这与无花果块、米粉等的吸附机制类似。从热力学的角度来看,一定温度下的吉布斯自由能(Δ)可以作为吸附剂对水的亲和力的指示,并进一步提供关于水分吸附是自发(Δ<0)还是非自发(Δ>0)的过程。普通粉和超微粉的Δ分别是1 152.80、1 184.22 J/mol,表明枣粉的水分吸附过程是非自发的。因此,可以通过控制环境的水分条件来实现枣粉的良好贮藏。
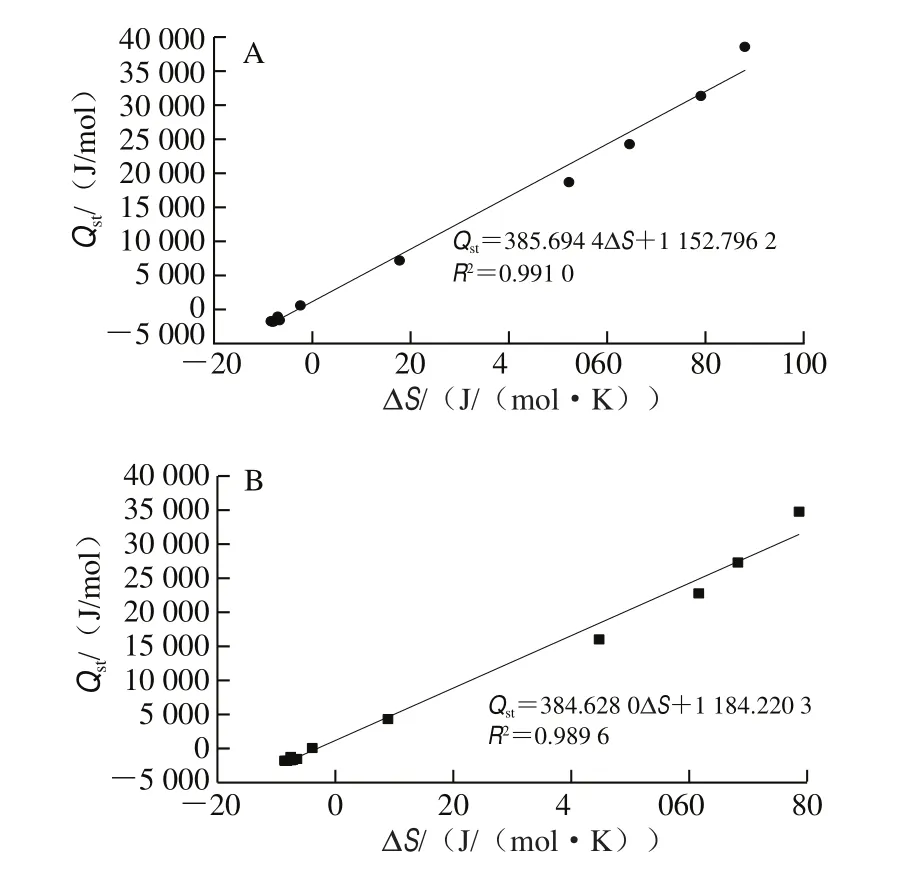
图9 普通粉(A)、超微粉(B)水分吸附过程Qst和ΔS的关系Fig.9 Relationship between Qst and ΔS for water adsorption of ordinary powder (A) and superfine powder (B)
2.6 枣粉中糖的组成及吸湿率
为了更好地解释枣粉的吸湿结块,本实验选用超微粉来探究枣粉吸湿的糖物质基础,经测定,超微粉中果糖、葡萄糖、蔗糖的质量分数分别为21.65%、17.38%、20.42%,3种糖的相对含量为36.42%、29.23%、34.35%。预实验测得在相对湿度为11.3%、32.4%、51.4%时葡萄糖、果糖、蔗糖几乎不吸湿(数据未显示),因此,本实验选择对水分活度0.751、0.923(即相对湿度为75.1%、92.3%)条件下的吸湿率进行分析。如表5所示,3种糖的吸湿率由大到小依次为果糖>葡萄糖>蔗糖,蔗糖几乎不吸湿。果糖、葡萄糖、蔗糖的玻璃化转变温度()分别为5、31、62 ℃,表明果糖在常温下极易发生玻璃化转化变成橡胶态,从而导致产品变黏。低分子质量聚合物(如蔗糖)和单体(如果糖、葡萄糖)具有较低的,其对降低富含糖类食品的有显著的影响。混合糖按照果糖、葡萄糖、蔗糖分别占比36.42%、29.23%、34.35%混合而成,其吸湿率较大,推测原因是果糖吸湿后溶解,由于水的增塑效应以及协同吸湿导致葡萄糖和蔗糖也部分溶解,从而导致吸湿率增加。枣粉的吸湿率明显大于3种单糖及混合糖,可归因于当物料存在多种结晶成分时,相互潮解进一步增加了混合物对水分的敏感度,随着共混物的复杂性增加,对水分的敏感度也增加,共混物的物理稳定性降低。因此,可推测枣粉中吸湿的糖类物质主要是果糖。
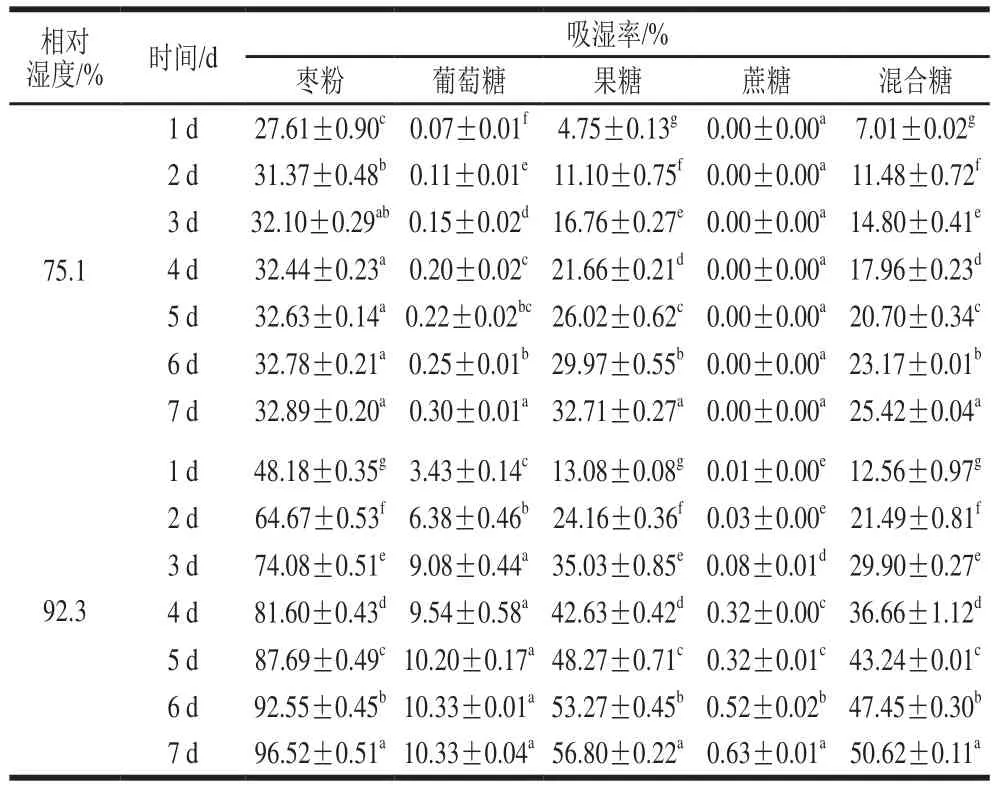
表5 枣粉、葡萄糖、果糖、蔗糖及混合糖的吸湿率Table 5 Moisture adsorption rates of jujube powder, glucose, fructose,sucrose and a mixture of the three sugars
3 结 论
本研究测定了普通粉碎及超微粉碎冬枣粉在20、30、40 ℃下吸湿后色泽的变化、吸附等温线及吸附过程的热力学性质。此外,还探究了枣粉吸湿的糖物质基础。枣粉吸湿后,褐变现象严重,由最初的淡黄色逐渐变成黄色、褐色。枣粉的吸附等温线属于III型等温线,Peleg模型可较好地对其进行拟合(=0.995 0~0.999 6,=2.077 6%~4.763 7%)。在低水分活度下(<0.70),枣粉的平衡水分含量随的增加而缓慢增加,且超微粉显著低于普通粉;高水分活度下迅速增加,因而在枣粉贮藏时环境应尽量控制在0.70以下可延缓枣粉的吸湿结块,且超微粉碎有利于枣粉的贮藏。两种枣粉水分吸附过程的净等量吸附热()及微分熵(Δ)均随着平衡水分含量的增加呈指数降低,且普通粉大于超微粉。当>0.30 g/g时,两种粉的与Δ均趋近于0。普通粉和超微粉的相对安全水分含量分别约为0.416 3、0.402 7 g/g;绝对安全水分含量分别约为0.237 5、0.223 5 g/g,枣粉在加工时有效控制其水分含量在绝对安全水分含量以下,可有效抑制微生物的生长繁殖,有利于枣粉的贮藏。焓熵补偿理论存在于枣粉水分吸附过程中,并且表明该过程是焓驱动的非自发反应。最后,推测果糖是枣粉中吸湿的主要糖类物质。

