湿法消解-火焰原子吸收光谱法测定刺梨果汁中锌含量的不确定度评定
陈 露, 游元丁, 李跃红, 赵 阳, 徐孟怀, 焦彦朝
(1.六盘水市口岸服务中心,贵州 六盘水 553000;2.贵阳海关综合技术中心果蔬实验室(六盘水),贵州 六盘水 553000;3.贵阳海关综合技术中心,贵州 贵阳 550081)
刺梨为蔷薇科蔷薇属多年生落叶小灌木,多见于云贵地区[1],富含维生素C、超氧化物岐化酶和10 余种对人体有益的微量元素[2-3]。传统的刺梨鲜果味道酸涩,大众接受度低。因此市场上多见以果脯形式为主的果肉和榨汁后的果汁等刺梨制品[4]。刺梨鲜果制成的果汁中含有锌元素,锌有助于维持人体正常的生命活动,在人体生长发育、免疫、内分泌等生理过程中起着关键作用[5-7]。因此,锌一直是食品、饲料、环境、药物等的重要检测项目之一[8]。在锌的检测过程中,由于受仪器设备、标准物质、技术水平等多种因素影响,分析结果必定存在误差,需要进行不确定度分析[9-11]。测量不确定度是指根据所用到的信息,表征赋予被测量值分散性的非负参数。其能反映出检测过程中各影响因素对结果不确定度的影响程度,也用来科学有效地评价检测数据的质量[12-14]。因此测量不确定度成为实验室检测过程及判定测量结果准确度的重要参考指标[15-16]。依据《测量不确定度评定与表示》(JJF 1059.1—2012)[12]和《测量不确定度评定与表示》(GB/T 27418—2017)[13]的要求和规定,采用湿法消解-火焰原子吸收光谱法对刺梨果汁中锌含量进行不确定度评定,分析测量不确定度来源的贡献,以期为实验室认可、质量控制提供科学严谨、准确的理论依据,同时为果汁饮料中其他微量元素的不确定度分析提供借鉴,确保实验室检测结果的公正性与权威性。
1 材料与方法
1.1 材料
1.1.1 试验原料 高原魔梨金刺梨汁(贵州安顺)。
1.1.2 试验试剂 高氯酸、硝酸(优级纯,国药集团化学试剂有限公司);锌标准溶液(GSB 04-1761-2004,1 000 mg/L,有色金属及电子材料分析测试中心);乙炔(99.99%)。
1.1.3 试验仪器 原子吸收光谱仪(岛津AA-7000,配火焰原子化器,日本岛津公司);可调式电热板(莱伯泰科EG35A PLUS,莱伯泰科北京有限公司);超纯水系统(热电UV/UF,美国Thermo Fisher 公司);移液管和容量瓶等所有玻璃器皿均为A级。
1.2 试验方法
1.2.1 标准溶液的配制 准确吸取锌标准溶液(1 000 mg/L)1.00 mL 于100 mL 容量瓶中,用5%硝酸溶液定容,混匀,即得到锌标准中间液(10 mg/L)。再分别向100 mL 容量瓶中准确吸取10 mg/L 的锌标准中间液0.00 mL、1.00 mL、2.00 mL、4.00 mL、8.00 mL 和10.00 mL,用5%硝酸溶液定容至刻度,混匀。即得到质量浓度分别为0.000 mg/L、0.100 mg/L、0.200 mg/L、0.400 mg/L、0.800 mg/L 和1.00 mg/L 的锌标准系列溶液。
1.2.2 样品前处理 依据《食品安全国家标准食品中锌的测定火焰原子吸收光谱法》(GB 5009.14—2017),准确移取5 mL 高原魔梨金刺梨汁液体试样于锥形瓶中,加入硝酸20 mL、高氯酸1 mL,在可调式电热板上消解至冒白烟,消化液若呈无色透明或稍带黄色,取下锥形瓶,冷却后用超纯水定容至50 mL,摇匀待上机检测。同时做样品空白试验。
1.2.3 仪器条件 火焰原子吸收光谱仪仪器条件:波长213.9 nm,狭缝宽0.7 nm,灯电流8.0 mA,燃烧头高度7 mm,助燃气压力0.35 MPa,乙炔压力0.09 MPa。
1.2.4 锌浓度计算 根据GB 5009.14—2017,采用湿法消解对刺梨汁进行前处理,原子吸收光谱仪进行测定;用最小二乘法线性拟合得到标准曲线,待测样品中锌的浓度由标准曲线计算得出,计算公式:

式中,X 为样品中锌的含量,mg/L;C 为样品溶液中锌的浓度,mg/L;C0为空白溶液中锌的浓度,mg/L;Vd为样品消化液的定容体积,mL;V为样品移取体积,mL。
设Cx为扣除空白后刺梨汁中锌的实际浓度,即Cx=C-C0,则式(1)可简化为式(2):

1.2.5 不确定度来源识别 根据建立的数学模型,测定刺梨果汁中锌含量的不确定度来源主要包括2 部分:样品前处理和样品测定。样品前处理包括样品量取、样品定容;样品测定包括仪器测量、回收率、标准曲线拟合和重复性。不确定度来源分析如图1。
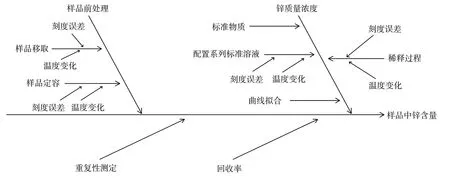
图1 刺梨果汁中锌含量测定不确定度因素来源
2 结果与分析
2.1 不确定度来源的量化
2.1.1 样品前处理引入的不确定度u(C1)
用5 mL 移液管量取5 mL 样品,样品经湿法消解后定容至50 mL,所用玻璃器皿为5 mL 移液管和50 mL 的容量瓶,玻璃器皿引入的不确定度包括刻度误差与温度变化引入的不确定度组成,参照《常用玻璃仪器》(JJG 196—2006),假设按均匀分布,样品前处理过程中引入的不确定度见表1。 则合成样品前处理过程引入的相对不确定度:
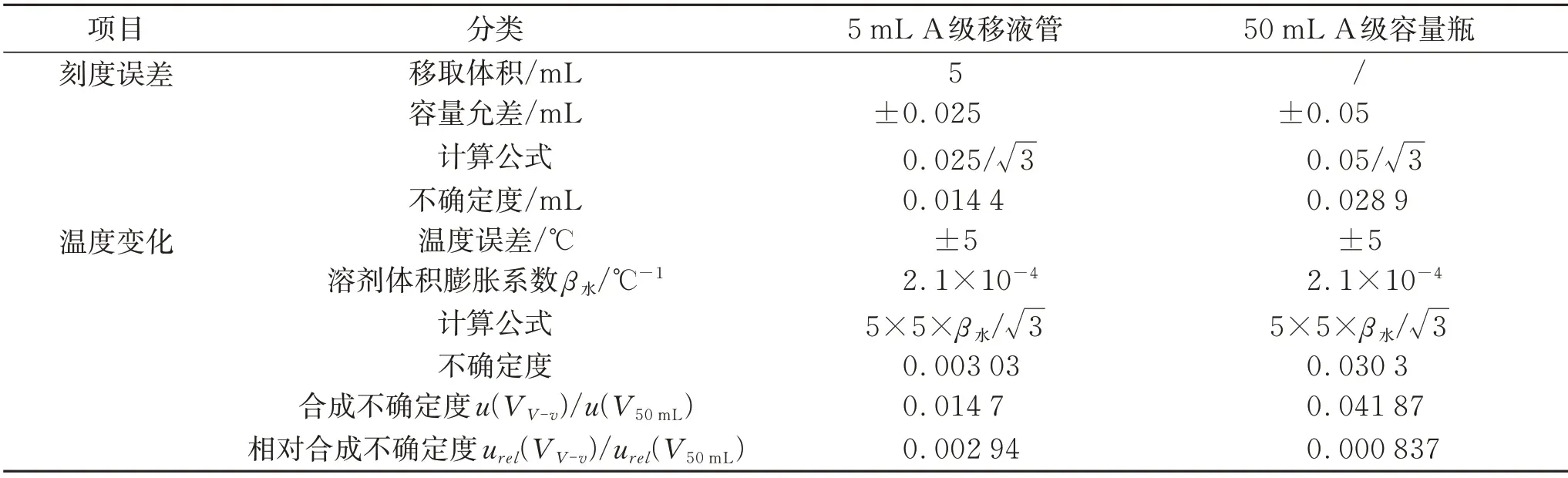
表1 样品前处理过程引入的不确定度
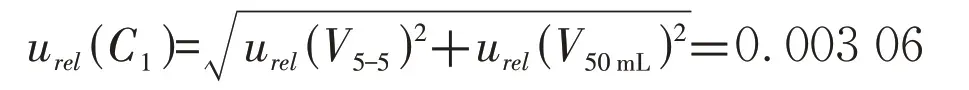
2.1.2 锌质量浓度引入的不确定度u(C2)
1)标准物质的不确定度u(C2-1)。测量使用有证标准物质,锌的质量浓度为1 000 mg/L,根据锌标准物质证书得锌浓度的相对标准不确度urel(C2-1)=0.007,包含因子k=2。
2)稀释锌标准物质溶液引入的不确定度u(C2-2)。用1 mL 移液管移取1 000 mg/L 的锌标准溶液1 mL 于100 mL 容量瓶中,定容得到10 mg/L 锌标准中间液。按均匀分布,计算结果见表2。由稀释过程引入的相对标准标准不确定度:
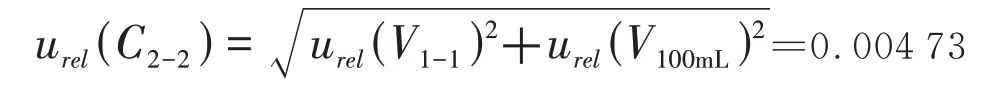
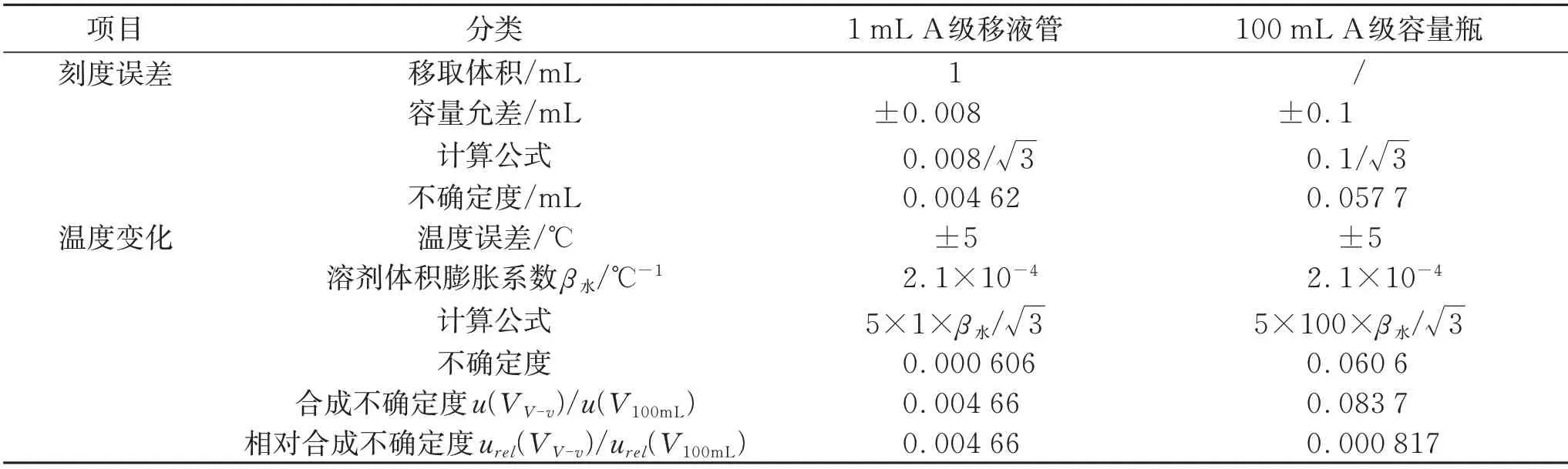
表2 稀释过程引入的不确定度
3)配置系列标准溶液引入的不确定度u(C2-3)。用10 mL 移液管分别移取10 mg/L锌标准中间液0 mL、1 mL、2 mL、4 mL、8 mL、10 mL 于100 mL 中容量瓶中,定容得到锌标准系列溶液,按均匀分布,该过程引入的不确定见表3,计算100 mL 容量瓶引入的不确定度。由表计算稀释锌标准物质溶液引入的相对标准不确定度:
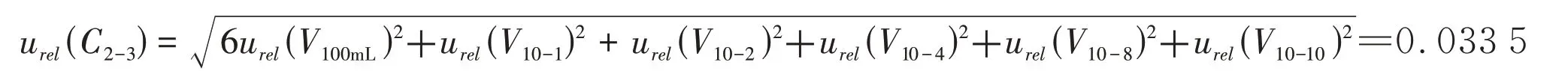
4)拟合标准曲线引入的不确定度u(C2-4)。在测定不同质量浓度的标准溶液之前,原子吸收光谱仪使用空白标准溶液进行吸光度调零,将配制的6个不同质量浓度的锌标准溶液上机测定,分别重复测定3 次,采用最小二乘法拟合标准曲线各标准点的浓度和吸光度值(表4)。

表4 标准曲线拟合结果
线性拟合得到校准曲线方程:A=0.163 83C+7.216 5×10-5(R2=0.999 9),测得刺梨汁样品中锌的平均质量浓度为Cx=0.44 mg/L。拟合标准曲线引入的不确定度由式(3)~(5)[17]计算,结果见表5。

表5 拟合标准曲线引入的不确定度
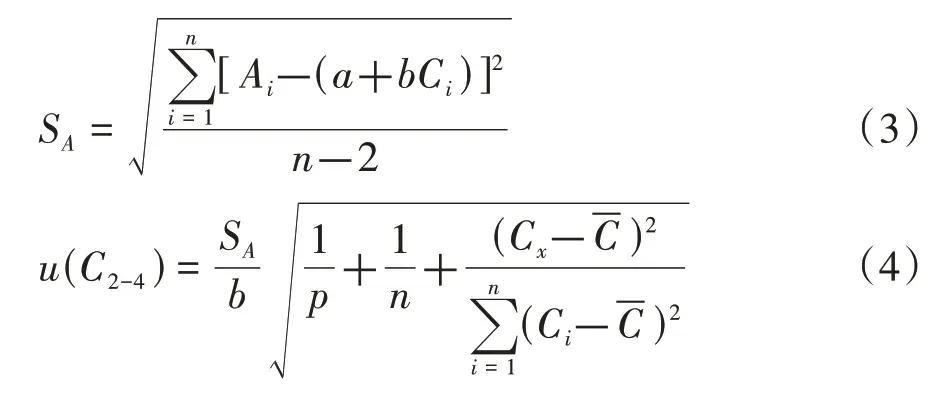

式中,SA为校准溶液的残余标准偏差;Ai为各标准溶液单次测量的吸光度值;a 为校准曲线的截距;b 为校准曲线的斜率;Ci为各标准溶液中锌的浓度;为各标准溶液中锌的平均质量浓度;n 为标准溶液的测量总次数,n=18;p 为样液的测量次数,p=3。由锌质量浓度产生的相对不确定度:urel(C2)=0.044 5
2.1.3 重复性测定引入的不确定度u(C3) 重复测定6次刺梨汁样液后进行定量,考察其重复性产生的不确定度,定量结果见表6。重复性测定引入的不确定度按式(7)和式(8)计算。


表6 样液中锌含量测量结果
2.1.4 回收率引入的不确定度u(C4) 对刺梨汁样品添加水平为0.1 mg/L 的标准溶液,按照前处理方法处理后,进行6次加标回收率测定试验,测定结果见表7。

表7 刺梨汁中锌加标回收率试验测定结果
加标回收率引入的标准不确定度,按式(9)进行计算。
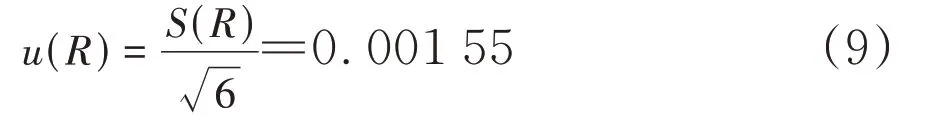
设k 为在计算测量结果扩展不确定度时所使用的包含因子,假设测量结果服从正态分布,在95%置信概率下k=1.96。设t =存在显著性差异,必须考虑由回收率引起的不确定度,则回收率相对不确定度按式(10)计算。

2.2 合成标准不确定度的计算
不确定度的各分量及数值见表8。将各不确定度的分量进行合成:=0.048
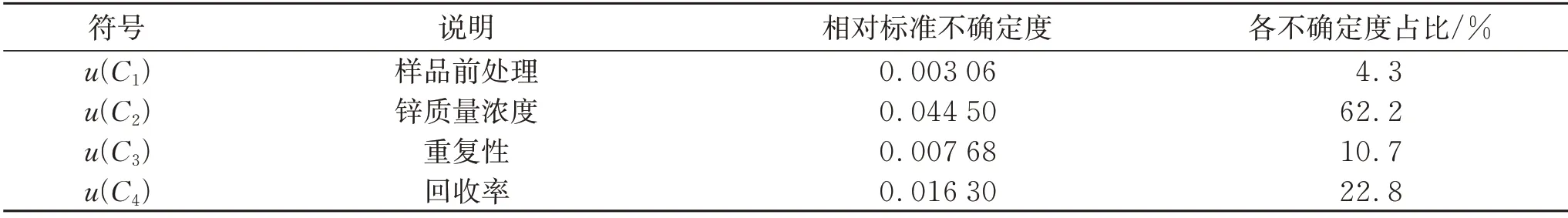
表8 各分量的相对不确定度
2.3 扩展不确定度的计算
刺梨汁样品中锌含量的最终检测结果:X=Cxv/m=0.044×50/5=0.44mg/L。因此,uc(X)=X×urel(X)=0.44×0.048=0.021 mg/L,则在置信概率P=95%,k=2时,扩展不确定度为U=kuc(X)=2×0.021=0.042。
由此可知,高原魔梨金刺梨汁样品中的锌含量为(0.44±0.042)mg/L,k=2。
3 小结
湿法消解-火焰原子吸收光谱法测定高原魔梨金刺梨果汁中锌含量为(0.44±0.042)mg/L,k=2。通过不确定度评估过程可知,该法测定刺梨果汁中锌含量过程中,样品前处理过程、标准物质配置过程及标准曲线拟合、测量的重复性及回收率等每一环节均会引入不确定度,由分析结果可知,锌质量浓度及回收率对测量不确定度的贡献较大,分别占比62.2%和22.8%。其中在分析锌质量浓度引入的不确定度过程中,配置系列标准溶液过程对不确定度的贡献最大,因此试验过程中应规范标准溶液的配制;其次加标回收率对不确定度的贡献比重较大,在试验过程中应注重这一环节。试验过程中每个步骤均会引入测量不确定度,因此应加强标准操作训练,提高检测人员检测能力,定期对标准物质和仪器进行期间核查,做好仪器的日常维护保养均可减少不确定度的影响。

