超声诊断技术在乳腺癌早期诊断中的应用及准确性分析
吴丽伟
(北京市通州区张家湾社区卫生服务中心超声科 北京 101113)
乳腺癌是全球范围内女性发病率最高的恶性肿瘤之一,全世界每年约有数百万的新发病例,死亡人数也高达数十万,而在我国,乳腺癌每年约有30 万~40 万的新发病例,死亡人数近10 万[1]。乳腺癌虽然对女性的健康和生命有着极大的危害,但早发现、早治疗有助于改善患者的预后。目前,临床诊断乳腺癌的方法主要有组织活检、分子标志物检验、影像学检查,而在影像学检查中又包括钼靶X 线、CT、PET-CT、超声、MRI 等,其中钼靶X 线存在辐射性,分辨率较为一般,诊断准确性一般;CT、PET-CT 虽然分辨率高,诊断准确性也比较高,但同样具有辐射性,无法在短时间内重复进行;MRI 诊断准确性高、安全性也比较高,但耗时长、价格贵[2-4]。相比之下,超声的诊断准确性和安全性高、耗时短、价格较低,在乳腺癌的诊断上具有非常显著的临床价值,受到广大医患的青睐。本文选择2019 年1 月—2021 年12 月期间收治的48 例乳腺癌高危患者,试探究超声技术对乳腺癌早期的应用价值及诊断准确性。
1 资料与方法
1.1 一般资料
选择2019 年1 月—2021 年12 月期间于通州区张家湾社区卫生服务中心进行乳腺癌筛查(乳腺超声检查)的乳腺病变患者4 894 例,其中阳性病例(发现乳腺结节)283 例。为283 例阳性患者进行二次超声检查,共筛查出48 例乳腺癌高危患者,对48 例乳腺癌高危患者的临床资料进行回顾性分析。患者全部为女性,年龄35~64 岁,平均(41.74±8.11)岁;结节位置:左侧23 例,右侧25 例。
纳入标准:①所有患者经手术病理检查和影像学检查均确诊存在乳腺结节,符合乳腺癌或乳腺良性疾病的诊断标准[5];确诊为乳腺癌者分期为Ⅰ~Ⅱ期[6];②所有患者均不存在超声检查的禁忌证;③所有患者近期均未接受治疗;④临床资料齐全者;⑤患者已经阅读知情协议并签字。
排除标准:①合并全身免疫性疾病、血液系统疾病、严重内外科疾病、其他恶性肿瘤等疾病者;②妊娠哺乳期女性;③分期为中晚期者;④因精神障碍、视听觉障碍、依从差等原因难以配合完成研究的患者;⑤中途退出研究者;⑥同时参与其他研究者。
1.2 方法
所有初筛患者使用Aloka α6 超声诊断仪进行初筛,二次超声用飞利浦EPIQ7 超声诊断仪进行检查,探头频率调节为7.5 MHz,患者保持仰卧体位,双手上举,将双侧的乳腺和腋窝全部暴露出来。将探头置于患者胸部,对乳腺四象限进行二维超声扫描,扫描的切面包括斜切面、横切面、纵切面。在发现结节后,对结节的边界、形态、大小、钙化情况、腋窝淋巴结等进行观察。随后,给予多普勒扫描,获取病灶内外血流情况的超声信号,以判断结节内外血流信号是否异常。以BI-RADS 分级筛查出乳腺癌高危患者,分级标准如下,0 级:有临床体征但超声无征象;1 级:未见异常;2 级:良性病变;3 级:良性可能性大,恶性率不足2%;4 级:可疑恶性,需穿刺活检,3%~94%的恶性可能;5 级:高度可疑恶性,恶性可能超过95%;6 级:病理证实为恶性。3 级以上者可认为是高危乳腺癌患者。
1.3 观察指标
①观察超声检查结果与声像特征;②与金标准—手术病理结果进行对比,计算超声对乳腺癌的诊断准确率。
1.4 统计学方法
采用SPSS 23.0 软件进行数据分析,以(±s)表示计量资料,行t检验;以频数、百分比(%)表示计数资料,行χ2检验。P<0.05 则差异有统计学意义。
2 结果
2.1 超声检查结果
首次超声检查筛查出283 例阳性患者,二次超声检查发现48 例乳腺癌高危患者及235 例乳腺良性病变患者。对于48 例乳腺癌高危患者,手术病理结果显示乳腺癌患者有45 例,其中40 例早期乳腺癌,故超声对早期乳腺癌的诊断准确率为88.89%。
2.2 超声声像特征
乳腺癌患者与乳腺良性病变患者各超声声像特征的检出率相比差异均有统计学意义(P<0.05)。乳腺癌患者呈沙砾样钙化、形态不规则、后方回声弱、边界模糊等超声表现;乳腺良性病变患者呈边界清晰、形态规则、后方回声强、无钙化灶等超声表现。见表1。

表1 超声声像特征的对比[n(%)]
2.3 血流信号等级
乳腺癌患者与乳腺良性病变患者的血流信号等级对比差异均有统计学意义(P<0.05)。乳腺癌患者血流信号多为2 级或3 级,0 级和1 级较为少见;乳腺良性病变患者血流信号多为0 级或1 级。见表2。
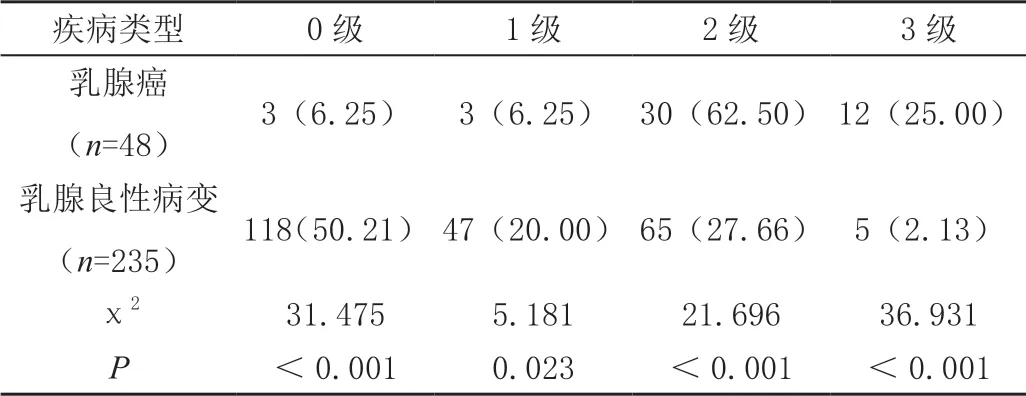
表2 血流信号等级的对比[n(%)]
3 讨论
乳腺癌作为女性最为常见的恶性肿瘤,不仅治疗方法繁多,诊断方法也是多种多样,这些诊断方式各有其优缺点。组织活检是乳腺癌临床诊断使用的“金标准”,其可以分为细针穿刺抽吸活检、空芯针活检、真空辅助活检等,这种方法虽然诊断准确性较高,但会给患者带来创伤,且细针穿刺抽吸活检、空芯针活检存在针道,容易导致针道种植,虽然真空辅助可以减少标本与针道的接触,但患者依然可能在活检后发生局部血肿、出血、感染等并发症,且组织活检会给患者带来疼痛,不适合重复进行,这些都限制了组织活检的临床应用。与组织活检相比,影像学检查可谓是目前临床诊断乳腺癌最常用的方法,诸如CT、MRI、超声等影像学技术对早期乳腺癌也有较高的诊断准确率,并且其操作是无创的,不会导致种植转移等问题,不易引发局部血肿、出血、感染等并发症,因此更受到临床的青睐[9]。这其中,CT 分辨率较高,不仅可以消除重叠,还能进行图像的三维重建,医生可以更加立体地观察结节的大小、形态规则性、边界清晰度、有无钙化灶等,并且CT 还能用于观察病灶周边组织情况,评估患者是否术后发生转移,但需要注意的是,部分容积效应给CT 带来了局限性,一些微小的钙化病灶只能局限性地限制高密度,对于脂肪型乳腺癌的小结节则发现能力有限,且与钼靶X 线等基础性方法相比,辐射量高、价格贵,重复性差,很难作为早期乳腺癌的常规筛查手段[10-11]。PET-CT 结合了结构成像与功能成像的特点,可以基于氟18-脱氧葡萄糖的摄取来了解病变特征,对病灶的解剖结构和代谢状况进行更加清晰的了解,这种方法多用于评估乳腺癌腋窝淋巴结转移或远处转移,对于直径不足1 cm 的结节则容易因为氟18-脱氧葡萄糖摄取不足而漏诊,而早期乳腺癌患者的恶性结节大多直径较小,因此该方法不适用于诊断早期乳腺癌,并且该方法价格昂贵,限制了该方法的临床价值[12]。乳腺钼靶X 线是基层医院诊断乳腺癌的主要方法,其对乳腺结节有较高的对比度及分辨率,对簇状的微小钙化灶有95%的敏感度、94%的特异度,但需要注意的是,钼靶X 线不适用于腺体致密或有植入物的女性,且贴近胸壁和腋前线的微小病灶容易漏诊,对于乳腺导管内存在非钙化灶的患者,也容易漏诊,因此在早期乳腺癌的诊断上价值有限,且乳腺钼靶具有一定的辐射性,短时间内不适合重复进行[13]。MRI 可以从多个方位成像,扫描序列非常丰富,即使是位于腺体深部的病变,或是多灶性病变,也有较高的诊断准确率,其不仅可以通过三维成像对结节的体积进行准确的判断,还能展现出结节的血流灌注情况和新生血管分布,临床除了将其用于乳腺癌的术前评估和术后新辅助化疗的疗效评价,还将其用于原发性隐匿性乳腺癌的诊断,但需要注意的是,有细微钙化的导管原位癌病灶MRI 难以检出,且MRI 检查时间长、价格昂贵,难以用于早期乳腺癌的常规筛查[14]。而超声不仅价格相对较低、检查时间短,更是具有清晰度和对比度高,诊断准确性强的优点,并且其不具有辐射性,因此安全性也非常高,综合对比是临床诊断早期乳腺癌最适合的方法[15]。超声不仅可以在二维模式下对结节的大小、位置、数量、形态规则性、边界清晰度、回声高低、有无钙化灶进行观察,还能利用基于多普勒技术对结节内外的血流丰富程度进行观察,进而实现对乳腺癌的准确诊断[16]。纵观既有的研究成果,可以发现乳腺癌有如下超声特征:①形态不规则、纵横比>1,这与肿瘤向周围组织浸润性生长、脱出正常组织平面有关;②边缘模糊,有毛刺征,这与病灶包膜受到破坏,肿瘤出现分化及侵袭性行为有关;③内部低回声,后方回声衰减,这与乳腺癌组织中有较多的胶原纤维,能够吸收大量声能,使得病灶后方回声衰减有关;④微小钙化,随着肿瘤的侵袭,乳腺组织将会变形坏死,钙盐逐渐沉积,形成微小钙化灶;⑤血供丰富:肿瘤为了更好地发育,会形成较多的血管,以获得足够的营养,因此肿瘤内外会出现较为丰富的血流信号[17]。本文结果中超声显示乳腺癌患者有沙砾样钙化、形态不规则、后方回声弱、边界模糊等超声表现,血流信号多为2 级或3 级,0 级和1 级较为少见,正符合以上列举的乳腺癌超声特点,临床可以基于以上特点进行早期乳腺癌的准确判断;此外结果显示超声对早期乳腺癌诊断准确率为88.89%,与杜娟娟[18]研究中超声对乳腺癌89.37%的诊断准确率相近,正可以体现超声对早期乳腺癌的显著诊断准确性。
超声诊断技术在乳腺癌早期诊断中有显著应用价值,准确性非常高,临床应将其作为早期乳腺癌的常规筛查手段。

