109例B淋巴系统恶性肿瘤患儿融合基因和免疫表型分析*
朱丽娟 苏晓霁 卓佳佳
急性B淋巴细胞白血病约占儿童急性淋巴细胞白血病的80%。该类白血病进展迅速,早期诊疗依赖于MICM综合分型(骨髓细胞形态学、免疫表型分析、细胞遗传学以及分子生物学)[1]。骨髓细胞形态学通过组织化学染色给出系别判断;免疫学方面,肿瘤细胞表面抗原存在高度的异质性,依赖流式细胞术可以很好地做出免疫表型分析;细胞遗传学与分子生物学,从染色体数目和结构上判断肿瘤细胞的类型[2]。随着儿童B淋巴系统恶性肿瘤的危险度分层日渐精细化以及个性化靶向治疗的广泛应用,不同的融合基因对临床的诊断、治疗和预后都有着重要的意义。当肿瘤细胞形态和免疫表型不一致时,融合基因的检出无疑给早期诊断提供了不可或缺的指示作用。如今国际主流观点是对成人急性B淋巴细胞白血病不再细分亚型,但对于儿童来说,不同的肿瘤亚型关乎不同的治疗方案和预后。本研究意在探讨急性B淋巴细胞白血病不同亚型的患儿的融合基因和免疫表型的关系,给临床个性化治疗方案提供一定的帮助。
材料与方法
1 研究对象 选取复旦大学附属儿科医院安徽医院收治的109名B淋巴系统恶性肿瘤患儿,男57例,女52例,平均年龄5.6岁(6个月~13岁),所有患儿均依据MICM分型明确诊断,其中108名为急性B淋巴细胞白血病( acute B-lymphoblastic leukemia,B-ALL),1名为B细胞淋巴瘤(B cell lymphoma,Bcl)。发病初期,抽取骨髓标本用于免疫分型和融合基因的检测。患儿自2018年1月随访至2021年9月,中位数随访时间20.6个月(1~44个月)。入选条件:(1)年龄<14岁;(2)符合急性淋巴细胞白血病的临床表现,MICM诊断分型确诊为急性B-ALL或Bcl;(3)初诊白血病患儿就诊前未进行白血病相关化疗;(4)观察诱导缓解期末的骨髓MRD。
2 研究方法 应用BD FACSCantoⅡ流式细胞仪进行骨髓细胞免疫表型分析,采用ABI QuantStudio Dx 荧光定量PCR仪检测融合基因的表达。回顾性分析白血病患儿的融合基因和免疫分型的结果。采用SPSS19.0统计软件分析数据,计数资料以例数(%)表示,采用χ2检验,P<0.05表示差异有统计学意义。
结 果
1 患儿融合基因阳性分布 109例患儿融合基因检测阳性者共42例,阳性检出率为38.5%(42/109)。其中,TEL/AML127例占64.3%(27/42);E2A/PBX19例,占21.4%(9/42);BCR/ABL5例均为P190亚型,占11.9%(5/42);MLL重排1例为MLL-AF4,占2.4%(1/42)。TEL/AML1、E2A/PBX1及BCR/ABL这3种类型融合基因在1~10岁患儿中占比最高,分别为:96.3%、100%和100%,1例MLL是1岁以下的儿童。整体分布情况如表1所示。

表1 109例患儿融合基因阳性分布情况
2 不同免疫表型的B-ALL和Bcl中融合基因表达情况 免疫表型中CD19+100%(109/109)、TDT+90.8%(99/109)、CD34+77.1%(84/109)、CD22+80.2%(87/109)、CD79a+92.7%(101/109)、CD10+96.3%(105/109)、CD20+20.2%(22/109)、cIgM 29.4%(32/109),根据CD34和CD10是否表达将109例患儿进行分型,如图1所示典型的免疫表型,Ⅰ(Pro-B-ALL):CD34+CD10-,共3例占2.8%(3/109),其中1例MLL基因重排阳性;Ⅱ(common-B-ALL):CD34+CD10+,共81例占74.3%(81/109),其中BCR/ABL5例以及TEL/AML127例;Ⅲ(Pre-BALL):CD34-CD10+,共24例占22.0%(24/109),其中E2A/PBX19例;Ⅳ(Bcl):CD34-CD10-,共1例,此型中无融合基因阳性患儿,见表2。

表2 109例患儿不同亚型及各亚型中融合基因表达情况

图1 不同亚型的B-ALL典型免疫表型分析
3 不同亚型B-ALL伴髓系抗原CD13/CD33表达 109例患儿中伴髓系抗原CD13/CD33表达的共38例,占整体总数的34.9%(38/109),在各亚型中的比例分别为33.3%、39.5%、20.8%和0,Ⅱ型(common-BALL)伴髓系抗原表达比例最高,见表3。
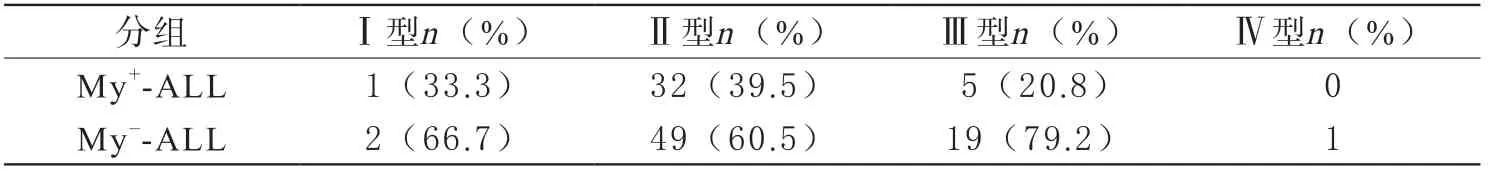
表3 伴髓系抗原CD13/CD33表达的情况分析
4 融合基因阳性病例的伴髓系抗原CD13/CD33表达情况 109例患儿中共有23例融合基因阳性的患儿伴髓系抗原CD13/CD33表达,占融合基因阳性例数的54.8%(23/42),各类型中比例如表4所示:在TEL/AML1、E2A/PBX1、BCR/ABL以及MLL中分别为66.7%、40%、33.3%和0,其中TEL/AML1融合基因阳性的患儿伴髓系抗原CD13/CD33表达的比例最高。

表4 伴髓系抗原CD13/CD33表达的融合基因情况分析
5 融合基因阳性患儿的临床特征及疗效的比较 经比较发现BCR/ABL融合基因阳性患儿在初诊时外周血白细胞总数明显高于其他组,1例MLL重排的婴儿白细胞总数>50×109/L;诱导缓解期末MRD阳性率TEL/AML1阳性组最低为7.4%,同样复发率最低为0,见表5。

表5 融合基因阳性患儿的临床特征及疗效的比较
讨 论
儿童白血病是最常见的儿童血液系统恶性肿瘤,通常在无任何诱因的情况下发病。现如今通过多种方法学检测对白血病的诊断已较为成熟,但较好的预后取决于精准的分型和早期的治疗,故白血病初发时的早期诊断显得尤为重要,MICM综合分型已普遍应用于白血病的诊疗,不同融合基因和不同免疫表型的白血病在临床上有着不同的意义,预后不同以及个性化诊疗方案不同[3-4]。
儿童中B-ALL明显比T-ALL高发,B-ALL的预后较T-ALL好[5],本研究针对109例B淋巴系统恶性肿瘤患者进行白血病融合基因42种筛查,共检出TEL/AML1、E2A/PBX1、BCR/ABL以及MLL重排,阳性检出率为38.5%,与张霞等研究报道的37.5%的阳性检出率相符[6]。TEL/AML1、E2A/PBX1以及BCR/ABL这3种类型融合基因集中在1~10岁患儿中,与吴崇军等以及王颖超等的研究相符[7-8]。不仅仅是融合基因阳性患儿,同时我们注意到融合基因阴性患儿也集中出现在1~10岁的年龄段,可能是因为此年龄段是B淋巴系统恶性肿瘤症状集中显现的阶段。根据CD34和CD10是否表达将109例患儿进行分型,其中Ⅱ型(common-B-ALL):CD34+CD10+共81例占74.3%,比例最高,与其他学者的研究结果相符[9]。109例患儿均表达CD19和HLA-DR。
Ⅰ型(Pro-B-ALL)表达早期干/祖细胞表面标志物CD34,在正常的B系祖细胞中CD10强阳性表达,但在此型白血病中CD10阴性。本研究中有3例患儿属此型,2例为小于1岁的婴幼儿,其中1名婴幼儿MLL-AF4融合基因阳性,这种累及MLL基因的婴幼儿白血病预后较差[10]。Ⅱ型(common-B-ALL)表达干/祖细胞表面标志物CD34和不成熟标志物CD10,儿童common-B-ALL患者最多,本研究中占74.3%。TEL/AML1融合基因阳性患儿均在此型中,这类患儿预后很好[11],TEL/AML1融合基因又叫ETV6-RUNX1,基础研究成果显示该融合基因的表达可抑制耐药基因的表达,从而降低了化疗药物的耐药性,且此类融合基因阳性的患者合并预后不良因素少,在早期治疗时即有不错的疗效,预后佳。BCR/ABL融合基因阳性患儿也在此型,有研究说明此类患儿比BCR/ABL融合基因阴性的生存期明显缩短,BCR/ABL基因融合后导致酪氨酸激酶活性持续增高,患儿在早期表现为外周血白细胞计数高,多数病例淋巴结及脾肿大,常规化疗剂量效果差,缓解期短,故此型患儿应采取更积极的治疗如骨髓移植[12]。Ⅲ型(Pre-B-ALL)不表达干/祖细胞表面标志物CD34,临床上普遍认为Pre-B-ALL预后比common-B-ALL差[13],近期研究发现这种差的预后与E2A/PBX1融合基因表达有关[14],PBX1蛋白的功能是参与细胞分化,E2A和PBX1基因融合后,降低其参与细胞分化的功能,导致B细胞停滞在发育早期,本研究中9例E2A/PBX1融合基因阳性患儿属于此型白血病。Ⅳ型(Bcl)比较少发,一般不表达CD34和CD10,但表达B系抗原CD19以及CD79a等,本研究中发现1例。
在对是否伴髓系抗原表达分析的时候发现,109例患儿中伴髓系抗原CD13/CD33表达的共38例,占整体总数的34.9%,共有23例融合基因阳性的患儿伴髓系抗原CD13/CD33表达,占融合基因阳性例数的54.8%。既往的研究对B-ALL伴髓系抗原表达的意义是有争论的,部分学者认为伴髓系抗原表达就伴随着较差的预后,大部分学者认为与预后无关[15]。本研究比较了融合基因阳性患儿的临床特征及疗效,经比较发现BCR/ABL融合基因阳性患儿在初诊时外周血白细胞总数明显高于其他组,诱导缓解期末MRD阳性率TEL/AML1阳性组最低为7.4%,同样复发率最低为0,各融合基因阳性组整体与阴性对照组间存在差异,但经仔细划分,将伴髓系抗原表达的融合基因阳性患儿重新挑出统计发现,各组间并不存在缓解和复发的差异,不排除样本量较小的原因,故本研究根据几种融合基因阳性的预后分析,推断髓系抗原的表达应该与预后无关。
综上所述,儿童急性B-ALL的发病年龄、融合基因以及免疫表型具有一定的分布特点,特定的免疫标志物的改变可用于发病初期融合基因表达的预测,特征性的融合基因阳性也有利于更精准的诊疗。本研究不足之处在于白血病融合基因42种试剂盒已应用于临床多年,能检测的融合基因类型有限,现如今已有更多的融合基因被发现与白血病有关,有待于后期的提高。
利益冲突所有作者均声明不存在利益冲突

