盐酸林可霉素硫酸大观霉素预混剂质量一致性评价研究
赵春蕊,张素卿,吉利伟,董玲玲
(山东鲁抗舍里乐药业有限公司,山东 济宁 272000)
0 引言
盐酸林可霉素硫酸大观霉素预混剂(商品名:利高)是硕腾公司开发的猪用复方预混剂,用于防治猪赤痢、沙门氏菌病、大肠杆菌性肠炎及支原体肺炎,具有广谱、高效、安全、低耐药等优点,临床应用前景广阔[1-2]。目前,农业农村部将其列为参比制剂,收入《兽药比对试验目录》(农业农村部公告第192号),国内仿制药申报需要进行比对研究。
肠炎与肺炎是养猪业中危害严重的常见疾病[3-4],为了防控上述疾病,依据《兽用化学药物制剂研究基本技术指导原则》《兽用化学药物稳定性技术指导原则》《兽药比对试验产品药学研究等资料要求》的通知要求,开发了盐酸林可霉素硫酸大观霉素预混剂,文中对研制的仿制药与利高的各项质量指标(如性状、粒度、干燥失重、有关物质、含量)及样品稳定性进行了全面的比对研究,以确定仿制药与利高质量的一致性。
1 仪器与试药
1.1 仪器
岛津液相色谱仪LC-20A(包括DGU-20A5R脱气机、LC-20AT四元泵、SLA-20AXR自动进样器、CTO-20A柱温箱、SPD-20A检测器、Labsolution色谱工作站);ZY-300IV 多功能微生物自动测量分析仪:北京先驱威锋技术开发公司;SPX-250 B型生化培养箱:上海佳胜实验设备有限公司;HPP260型药品稳定性试验箱,德国美墨尔特有限公司。
1.2 试药
盐酸林可霉素硫酸大观霉素预混剂(规格:100 g,林可霉素2.2 g与大观霉素2.2 g,山东鲁抗舍里乐药业有限公司高新区分公司,批号1808001、1808002、1808003;利高,硕腾(苏州)动物保健品公司,批号18070493A;林可霉素对照品:中国兽药监察所,批号K0101503,纯度84.6%;大观霉素对照品:中国兽药监察所,批号K0261705,每1 mg相当于644 IU大观霉素。甲醇为色谱纯;硼砂、磷酸为分析纯;水为双蒸水。
2 试验方法与结果
2.1 林可霉素含量测定
采用高效液相色谱法测定。色谱条件:色谱柱为YMC-Triart C18(250×4.6 mm,5 μm);流动相为0.05 mol/L硼砂溶液(用85%磷酸溶液调节pH值至6.1)-甲醇(1:1);流速为0.9 mL/min;柱温为40℃;检测波长为214 nm;进样浓度0.8 mg/mL,进样量为10 μL。
2.1.1 干扰试验
分别将稀释液、林可霉素对照品溶液、空白辅料溶液、供试品溶液过滤,取10 μL进样,记录色谱图(见图1),结果表明,稀释液、空白辅料均不干扰林可霉素的含量测定。

图1 稀释液(A)、空白辅料溶液(B)、对照品溶液(C)、供试品溶液(D)色谱图
2.1.2 线性和范围考察
分别配制浓度为0.603 mg/mL(75%)、0.724 mg/mL(90%)、0.804 mg/mL(100%)、0.885 mg/mL(110%)、1.005 mg/mL(125%)的林可霉素对照品溶液,过滤,取10 μL进样,每个浓度重复3次,记录色谱图。以林可霉素峰面积对浓度线性回归,得其回归方程Y=2E+06X+9 187.7(R2=0.999 4),表明林可霉素浓度在0.603~1.005 mg/mL与峰面积的线性关系良好。
2.1.3 精密度测定
依法配制6份供试品溶液(批号1808001),同时制备2份对照品溶液,分别进样,以外标法计算含量,得平均含量为104.11%,RSD为0.40%(n=6)。由不同分析人员在不同日期制备6份供试品溶液及2份对照品溶液进样测定,平均含量为104.03%,RSD为0.29%(n=6),重复性与中间精密度12次检测中,平均含量为104.07%,RSD为0.33%(n=12),表明此法精密度高,符合定量分析的要求。
2.1.4 准确度测定
分别称取林可霉素对照品约76 mg(相当于80%)、95 mg(相当于100%)、113 mg(相当于120%)与一定量的空白辅料,配制成混粉,每个重量3份并测定含量计算回收率。平均回收率为100.42%,回收率在99.0%~101.0%,RSD为0.46%,表明该方法回收率稳定,变异系数小,符合试验要求。
2.2 大观霉素含量测定
照抗生素微生物测定法测定[5-6]。1 000 IU大观霉素相当于1mgC14H24N2O7。
2.2.1 线性和范围考察
制备浓度约为49 IU/mL、70 IU/mL、100 IU/mL、142.86 IU/mL、204.08 IU/mL、291.55 IU/mL的大观霉素标准品溶液,采用一剂量法测定,以抑菌圈直径为横坐标,以浓度的对数LgC为纵坐标进行线性回归,得线性回归方程为:Y=2.077 5+0.133 5(X-18.031 4)(r=0.999 1),表明大观霉素含量测定方法在49~291.55 IU/mL浓度范围内线性关系良好。
2.2.2 精密度测定
依法配制6份供试品溶液(批号1808001),按抗生素微生物检定法测定,计算样品效价,得平均含量为103.76%,RSD为0.20%(n=6)。由不同分析人员在不同日期制备6份供试品溶液进行测定,得平均含量为102.49%,RSD为0.29%(n=6),重复性与中间精密度12次检测中,平均含量为103.12%,RSD为0.67%(n=12),表明此法精密度高,符合定量分析的要求。
2.2.3 准确度测定
取供试品(1808001,大观霉素测定效价22.9 IU/mg)约1 091 mg,精密称定,分别加入大观霉素标准品约23 mg、39 mg、54 mg,每个重量3份,配制成浓度为(80、160)IU/mL、(100、200)IU/mL、(120、240)IU/mL的溶液,按抗生素微生物检定法测定,计算样品效价及回收率。平均回收率为98.44%,其RSD为2.00%,表明此法准确度符合方法学验证的要求。
2.3 样品质量比对及稳定性考察
按照盐酸林可霉素硫酸大观霉素预混剂质量标准结合《中国兽药典》对原研药与仿制药样品含量、性状、干燥失重等项目进行检测,对比考察。结果(见表1)表明,原研药与仿制药的各项质控指标均无明显差异。
将仿制药及原研样品,按市售包装,进行加速试验(40℃±2℃、相对湿度75%±5%)、长期试验(25℃±2℃、相对湿度60%±10%),分别于不同时间点取样,考察样品的稳定性。考察项目包括性状、干燥失重、有关物质、林可霉素含量、大观霉素含量。结果显示(见表1):两者均为淡褐色粉末,自研样品林可霉素B在3.2%~3.5%,林可霉素含量下降不高于1.59%,大观霉素含量下降不高于1.08%,变化不显著;原研样品林可霉素在2.5%左右,林可霉素含量下降2.02%,大观霉素含量下降1.02%,变化不显著。仿制药与原研药在各考察时间点上均无明显变化,说明两者在不同试验条件下的样品稳定性一致。
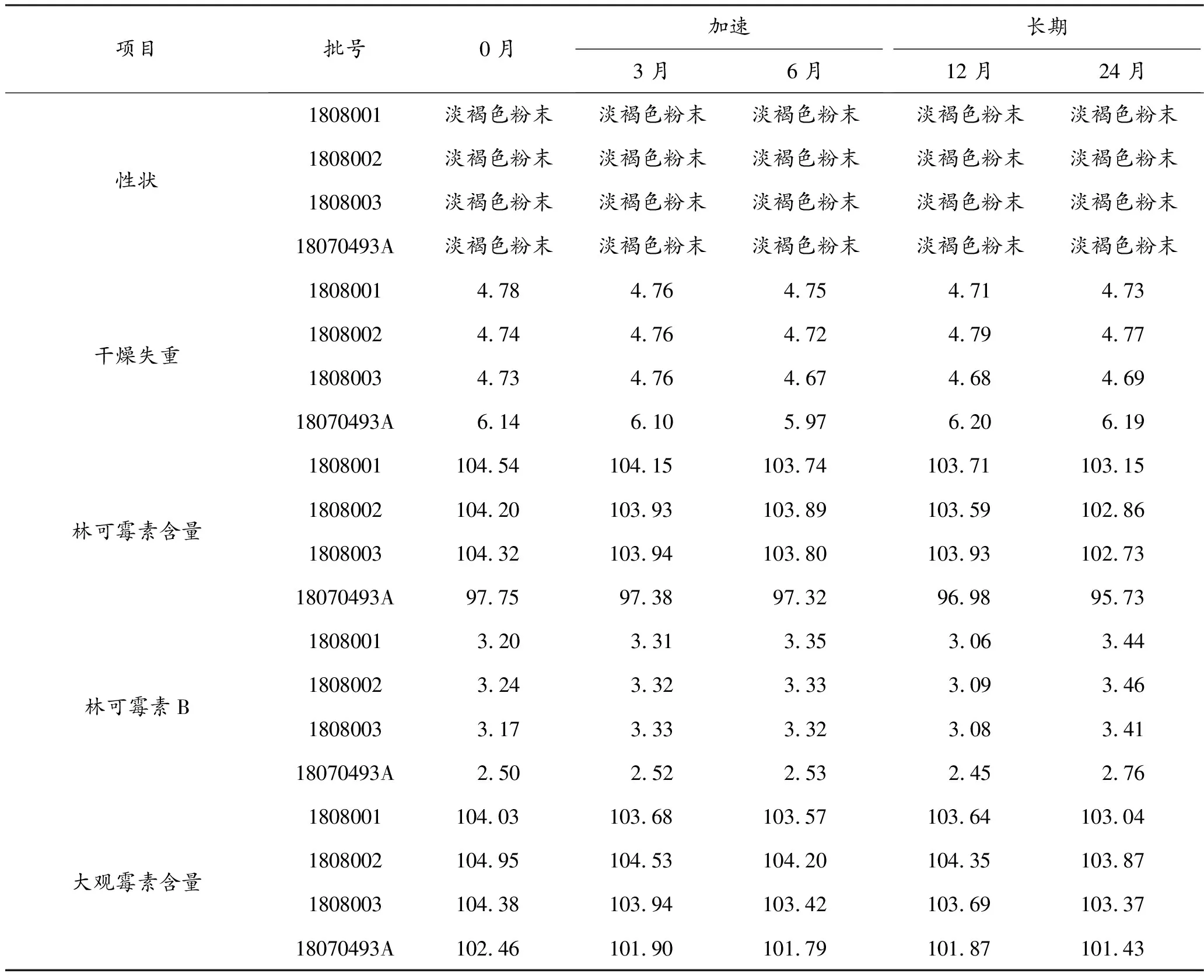
表1 盐酸林可霉素硫酸大观霉素预混剂质量稳定性考察 单位:%
3 结论
文中对盐酸林可霉素硫酸大观霉素预混剂原研药与仿制药进行了质量一致性评价,结果二者在各对比条件下,质量无明显差异,稳定性均良好,初步说明仿制药与原研药的质量具有一致性。文中结果为盐酸林可霉素硫酸大观霉素预混剂及类似剂型药物质量一致性评价工作的开展提供了依据。

